Симптом пробойника при подагре: Характерные рентгенологические признаки подагры – КСС. Подагра. + | Портал радиологов
Симптом пробойника подагра –
Содержание статьи
Подагра — болезнь любителей хорошей жизни?
Ни одно воспалительное заболевание суставов не привязано так тесно к нашему образу жизни, как подагра. Мало того — у этой болезни самое простое и одновременно сложное лечение. Если б не огромное количество врачебных ошибок, причина которых в игнорировании некоторых важных компонентов биохимического анализа крови, то лечение подагрического артрита не составило бы никакого труда. В прошлые века подагра считалась знаком избранности, так как поесть хорошо тогда могли лишь знатные вельможи.
Подагрический артрит: лечение и симптомы
Кто подвержен опасности заболеть
Сегодня подагру называют болезнью тучных людей и любителей хорошо покушать. Болеют ею в основном мужчины, и это неспроста:
Именно мужчины чаше предпочитают в питании красное мясо, копченную рыбу, алкоголь, в особенности пиво, содержащее в себе ксантин и гуанозин — продуктами распада этих соединений являются те самые злосчастные пурины, в результате обмена которых и образуется мочевая кислота.
Повышенное содержание мочевой кислоты в крови — это гиперурикемия
Однако это не значит, что женщины не болеют подагрой: пожилой возраст женщины сопровождается, как правило, гормональными нарушениями, которые могут спровоцировать подагрический артрит.
К этому приплюсовывается гиподинамия, резко замедляющая обмен веществ — и вот в крови происходит накопление мочевой кислоты
Факторы, способствующие развитию подагры
Провоцирующими факторами подагры могут также стать:
- Прием диуретиков в лечении гипертонии
- Противоопухолевая терапия
- Аутоиммунные заболевания
- Почечная недостаточность
- Гликогеноз
- Генетическая предрасположенность
- Стрессы
Наличие предков по прямой линии больных подагрой не означает неизбежность заболевания — всего на всего нужно следить за своим образом жизни:
- не допускать переедания и наличия в меню вредных продуктов
- не злоупотреблять алкоголем
- избегать стрессы и заниматься спортом
Как развивается подагрический артрит
Плохо то, что мочевая кислота нерастворима ни в воде, ни спирте, ни эфире. Она подвержена растворению в щелочных растворах, серной горячей кислоте и глицерине
То, что постоянно находится в крови, неизбежно кристаллизуется, и далее процесс протекает по стадиям:
Первые признаки заболевания
- Острый подагрический артрит начинается внезапно с приступа сильной, порой невыносимой боли: малейшее прикосновение к месту поражения, попытки двигаться доставляют страдания
- Обычно приступ начинается ночью
- Пораженный сустав распухает, кожа над ним становится багрово-красной и на ощупь горячей
- В 90% случаев поражается один сустав большого пальца стопы, но также могут воспалиться и другие сустава
На фото — пример подагры пальцев стопы: - Реже поражаются суставы кистей рук, голеностопа, коленные, локтевые, лучезапястные суставы
- Через три-четыре дня обострение бесследно проходит
- Спустя какое-то время приступ вновь повторяется
Чередование внезапных приступов с временным облегчением, удлинение каждого последующего приступа и сокращение интервалов между фазами обострения — все это признаки развития подагры
Симптомы хронического подагрического артрита
В заключительной стадии боль практически уже не отступает — констатируется хронический подагрический артрит.
Симптомы хронической подагры проявляются:
- В полном разрушении гиалинового хряща
- Кожных околосуставных разрастаниях (тофусах)
На фото — подагрические тофусы: - Образовании так называемых пробойников — полостей в костных эпифизах
- И пробойники, и подкожные тофусы заполнены солями уратов — этим и объясняется беловатый цвет кожи над узлами. При вскрытии или прорыве тофуса внутри него обнаруживается белая кашеобразная масса
На фото — подагра со вскрытием тофуса:
Узелки-тофусы образуются не только под кожей над больным суставом, но и на ушных раковинах.
Развитие мочекаменной болезни и пиелонефрита — это признаки того, что подагра уже сильно запущена
Симптомы женской подагры проявляются более мягко:
- Острые приступы редки
- Хроническая ноющая боль чаще всего в колене или голеностопе
- Реже происходит образование тофусов и пробойников
Причина врачебных ошибок
Симптомы подагры очень часто принимают за артроз, особенно при диагностике заболевания у женщин:
Полбеды, если проводится неправильное консервативное лечение с последующими неверными рекомендациями «коллагенового» питания — диеты со студнями и наваристыми мясными бульонами, убийственными при подагре.
Гораздо хуже, когда, констатировав полное разрушение сустава, горе-врачи предлагают дорогостоящее и абсолютно бесполезное эндопротезирование: ураты мочевой кислоты после этой операции с удовольствием принимаются за оставшиеся здоровые суставы.
Подагру большого пальца стопы хирурги могут, не задумываясь, принять за гангрену и, отчекрыжив палец, позже с удивлением цокают языком: Эка быстро идет процесс! — вот и на другой палец пошло…
А всего-то надо было — проверить уровень мочевой кислоты в крови.
Самое удивительное, что даже имеющийся анализ с зашкаливающим в два раза показателем по содержанию мочевой кислоты не очень отягощает разум некоторых «специалистов».
Другая сложность диагностики подагрической болезни — взятие биохимического анализа во время острого приступа:
- В период обострения подагры концентрация кристаллов уратов повышается именно в больном суставе, а в крови уровень мочевой кислоты может быть в пределах нормы
- Для исключения врачебной ошибки нужно повторно сдавать анализ в интервалах между приступами
Как лечить подагрический артрит
Если лечение ведется правильно, то подагрическую болезнь можно полностью вылечить.
Медикаментозное лечение
Медикаментозное лечение ведется при помощи следующих препаратов:
- Во время острого приступа в течение трех — семи дней применяются колхицин — препарат, используемый конкретно для лечения подагры
- Допустим также прием обычных НПВС: ибупрофена, индометацина, мовалиса, нимесила и т. д.
- На протяжении нескольких месяцев или даже лет проводится терапия с целью уменьшения содержания мочевой кислоты в крови — в этих целях применяется аллопуринол или зелорик
- Для выведения солей уратов вместе с мочой используют пробенецид, этебенецид, сулфинпиразон
- В целях разрушения имеющихся кристаллов моноуратов назначается препарат урикозим
Для препаратов группы пробенецида и урикозима имеются серьезные противопоказания:
- Нефропатии
- Почечная недостаточность
- Серьезные патологии почек
Поэтому данные препараты не считаются основными в лечения подагры.
Диета — важное условие излечения подагры
Любое медикаментозное лечение не принесет свои плоды, если больной не проявит волю и не умерит (в прямом смысле) свой аппетит
К сожалению, есть рабы желудка, которые даже под страхом смерти неспособны отказаться от своих пристрастий. Для таких лечение подагры очень тяжело: они беспрестанно (от приступа к приступу) вынуждены принимать аллопуринол, который умудряются заедать сочными бифштексами и запивать пивом.
Иным же аскетам в плане питания для излечения болезни достаточно одного курса приема лекарств.
Вот почему лечение подагры и легко, и тяжело — все зависит от привязки к конкретному человеку.
На рисунке ниже — таблица с разрешенными и нерекомендуемыми продуктами:
Специальные диеты при подагре — в конце статьи.
Лечение подагры народными средствами
Вылечить подагру можно, выводя из организма мочевую кислоту и обязательно используя диету. Если этого не делать, то не помогут никакие народные средства.
Местное лечение в виде всевозможных примочек и компрессов, возможно, снимет воспаление и боль, но не исключит возможность следующих приступов, поэтому мы его не будем даже и рассматривать.
Исключение составляют отвары и настойки, принимаемые внутрь для выведения солей.
Интерес могут вызвать следующие народные средства:
- Свежевыжатый сок из черной редьки:
- Начинать пить по одной чайной ложке, постепенно доведя дозу до столовой ложки, а затем до половины стакана
- Пить нужно с осторожностью, так как сок может вызвать печеночную колику и повышенное желчеотделение:
- при болях справа уменьшить дозировку
- избегать острых и кислых продуктов во время лечения
- Настой корней марены красной:
- Чайную ложку корней залить стаканом кипятка и кипятить 10 минут на водяной бане
- Принимать по половине стакана утром и вечером
- Отвар из лаврового листа:
Лавровый лист всегда считался прекрасным народным средством для очищения суставов от солей- Пять грамм листьев залить 300 г кипятка и кипятить в открытом виде пять минут
- Закутать посуду с отваром полотенцем и оставить на три часа
- Выпить отвар в течение дня
- Отварной рис:
- Две столовых ложки риса промыть и залить водой на ночь в пол-литровой банке
- Утром еще раз промыть и поставить на огонь
- Довести до кипения, опять промыть и вновь поставить варить — и так повторить четыре раза
- Напоследок еще раз промыть и съесть без всяких специй, масла и соли
- После такого рисового завтрака пищу не принимать четыре часа — за это время освобожденный от крахмала рис очистит кишечник от шлаков
- На вечер опять залить рис водой
- Проводить очищение рисом 45 дней
Видео: Как лечить подагрический артрит:
Использованные источники:zaspiny.ru
Диагностика подагры — методы исследований, какие анализы нужно сдать?
Болезни суставов – одни из самых распространенных в мире. А подагра – еще и самое болезненное из них. Недуг поражает и молодых, и пожилых пациентов. И связано это с неправильным питанием и злоупотреблением фаст-фудом.
Главной причиной развития заболевания является нарушение обменных процессов в организме. Повышенное содержание мочевой кислоты и ее солей приводит к образованию кристаллов, которые разрушают хрящевую ткань сустава и приводят к образованию тофусов.
Спровоцировать подагрический артрит могут патологии ЦНС (центральной нервной системы), щитовидки и головного мозга.
Неправильная или несвоевременная диагностика подагры и отсутствие адекватного лечения увеличивает риск осложнений.
Доктор Бубновский — Вылечить спину и суставы после 40 лет реально средством.
Читать далее >>>
Специальный Корреспондент: Лечение суставов дорогими пустышками — ревматологи 12 лет обманывали пациентов по всей стране.
Узнать подробности >>>
Диагностика подагры
Выявить подагру самостоятельно довольно сложно. Только опытный специалист может исключить другие заболевания с подобной симптоматикой и поставить диагноз подагра. Диагностика начинается в визуального осмотра больного и сбора анамнеза.
Опрос больного
Во время опроса пациента врач выясняет, какие симптомы его беспокоят, как они проявляются. На начальной стадии недуга происходит поражение мелких суставов на ногах и руках, затем болезнь распространяется на крупные сочленения.
Диагностическим критерием подагры является наличие генетической детерминированности. Если у близких родственников пациента диагностировали подагру, то риск развития именно этого недуга возрастает.
Также врач выясняет ранее перенесенные заболевания, которые могут спровоцировать подагрический артрит. К ним относятся:
- Хирургические операции;
- Нарушения функционирования почек;
- Продолжительный прием антибиотиков или стероидов.
Также выясняется наличие у пациента вредных привычек, пищевые пристрастия.
Клинические исследования
Опытный врач может определить подагру без анализов. Однако окончательно поставить диагноз, определить острую или хроническую форму протекания недуга можно только на основании результатов анализов. Для проведения дифференциальной диагностики назначают следующие обследования:
- Биохимический анализ крови при подагре на мочевую кислоту, сиаловые кислоты, фибрин и наличие белка (с С-реактивностью). Такая автодиагностика используется для определения количественных показателей уратов и их присутствие в кровотоке. Для мужчин норма мочевой кислоты составляет 460 мкМ/л, у женщин нормальные показатели ниже – 330мкМ/л. Руководствуясь одним биохимическим анализом диагностировать подагру суставов невозможно. Но повышенный уровень уратов свидетельствует о дисфункции мочевыводящих путей и нарушении работы почек. На патологию почек указывает и снижение уровня креатинина (в норме он составляет 115 ммоль/л). Дополнительно анализ на биохимию показывает количество азота, аммиака, глюкозы, липидов и билирубина. Резкое повышение их показателей свидетельствует о нарушении функционирования различных систем организма;
При развитии подагры результаты анализа на биохимию выглядят так: количество белка во время приступа значительно превышает норму, у некоторых заметно увеличение глюкозы и креатинина. Также завышенными будут показатели кальция, липидов, липопротеинов.
- Общее исследование крови. Количественные показатели нейтрофилов в анализе крови при подагре помогают выявить воспаление в суставе. Такой метод исследования эффективен при дисфункции почек. Показателем подагры по общему анализу крови служит присутствие кристаллических уратов в полученном осадке;
Высокая концентрация уратов в крови свидетельствует о развитии подагры суставов.
- Анализ мочи при подагре позволяет уточнить причину патологии. Результаты анализа показывают количество мочевой кислоты и общий уровень кислотности. Сдается моча в течение суток. Это помогает исследовать изменение результатов кислотности в течение дня.
Повышение показателей свидетельствуют о развитии мочекаменной болезни.
- Пункция синовиальной жидкости. Это метод позволяет диагностировать подагру суставов. У здорового человека синовиальная жидкость не имеет цвета, а по консистенции напоминает воду. Изменение цвета и снижение текучести свидетельствует о повышении кислотности, нарушении метаболизма. Также анализ показывает уровень нейтрофильных лимфоцитов;
- Рентген применяется для диагностирования подагры суставов нижних конечностей, а также пальцев. На снимке заметно развитие патологического процесса в суставе, отложение солей. К рентгенологическим признакам подагры относятся белые пятна, диаметром от 0,5 миллиметра до 3 сантиметров. Они обусловлены наличием тофусов, возникающих вследствие отложения солей мочевой кислоты в околосуставных тканях. Образование тофусов занимает около пяти лет. Ускорить их формирование может обострение подагры. Иногда рентгенографический снимок фиксирует полное или частичное разрушение железы внутренней секреции, а ее клетки заменяются кристаллами мочевой кислоты. Результативным рентгенографическое исследование будет для всех суставов. Оно помогает определить вид подагры, зафиксировать переход недуга на околосуставную сумку или сухожилия и возникновение в них воспаления. В таком случае назначается дополнительный анализ на биопсию;
Симптом пробойника при подагре – известен, как феномен поздней стадии заболевания. Это «косточка», на которую опирается сустав в основании или головке фаланги. Такой дефект может составлять в диаметре до 5 миллиметров. В большинстве случаев располагается в первом плюснефаланговом суставе стопы.
- УЗИ и томография – такая методика применяется только во время обострения подагры. Во время приступа заметно увеличивается межсуставная щель, наблюдается отечность, уплотнение и воспаление мягких тканей возле пораженного сустава. Такую клиническую картину можно наблюдать через неделю после острого приступа подагры. А вот во время ремиссии УЗИ не зафиксирует изменений. При хронической подагре при помощи УЗИ удается заметить деформацию сустава, а также присутствие воспалительного процесса. Также анализ позволяет определить отложение солей в почках и мочеточнике;
- Биопсия – высокоточный анализ, позволяющий выявить количественные показатели отложений мочевой кислоты в суставах. Для анализа производится забор внутрисуставной жидкости. Такая методика позволяет уточнить причину развития подагры.
Какие анализы нужно сдать при подагре, подскажет лечащий врач. Он составит схему проведения исследований, позволяющих уточнить диагноз, особенно при вторичной подагре.
Правила подготовки к анализам
Анализы при подагрическом артрите сдаются комплексно. В противном случае их результаты могут быть недостоверными. Что приведет к постановке ошибочного диагноза и нерезультативному лечению. Чтобы анализы оказались наиболее информативными, следует соблюдать такие правила:
- Исключить употребление алкоголя как минимум на сутки перед сдачей анализов;
- Снизить употребление пищи, содержащей высокие дозы витамина С, в противном случае отклонения от нормы могут быть завышены;
- Кофеин также способен повлиять на результаты анализов. Поэтому рекомендуется отказаться от кофе и чая за 8-10 часов до их сдачи;
- Аспирин повышает уровень кислотности, поэтому стоит от него отказаться;
- Мочегонные средства снижают уровни показателей анализов;
- Все анализы при подагре следует сдавать на голодный желудок. Последний прием пищи должен быть не раньше, чем за 8-10 часов до сдачи;
- Соблюдение диеты в течение 2-3 дней до сдачи анализов минимизирует искажение результатов анализов. Рекомендовано употребление растительных и молочнокислых продуктов;
- Также следует отказаться от чрезмерных занятий спортом перед проведением исследований.
Соблюдение правил подготовки к анализам – гарантия достоверности результатов, правильной постановки диагноза и назначения адекватного лечения.
Неправдивые результаты
Несоблюдение правил подготовки к сдаче анализов может привести к изменению их результатов:
- Показатели мочевой кислоты завышаются;
- Рентген или УЗИ перед сдачей анализов могут повлиять на их результаты;
- Злоупотребление жирной пищей, употребление алкоголя провоцируют искажение результатов исследований;
- Во время терапии подагры анализы не будут результативными.
Пациент должен знать, что хроническую подагру суставов полностью излечить невозможно. Но при помощи терапевтических методов можно снизить количество острых приступов, уменьшить болевой синдром.
Самолечение при подагрическом артрите суставов недопустимо. Это может стать причиной прогрессирования недуга и развития осложнений. Бесконтрольный прием препаратов может исказить результаты анализов, искусственно занизив их показатели.
Назначение адекватной терапии при подагре возможно только специалистом, на основании результатов проведенных анализов и инструментальных исследований. Подагрический артрит не всегда имеет визуальные проявления, поэтому диагностировать ее только при врачебном осмотре очень сложно. Комплексное обследование позволяет диагностировать заболевание, выявить его стадию, наличие сопутствующих болезней.
Использованные источники:nogivnorme.ru
Подагра и рентген
Подагра — системное заболевание связанное с нарушением пуринового обмена, которое проявляется отложением солей в организме. Поражает чаще мужчин, нежели женщин, и встречается у 1% населения земли. В диагностике заболевания очень важную роль играют лабораторные исследования и проведения рентгеновских процедур пораженных областей.
Признаки заболевания
Подагрический артрит сложно диагностировать на ранних стадиях течения болезни, ее симптомы часто бывают схожи с характерными признаками других заболеваний. Начальная стадия протекает бессимптомно, рентгеновские исследования будут малоинформативны. При появлении болевых ощущений в суставах назначается ряд анализов. Для определения подагры используют такие обследования:
- общий анализ мочи;
- исследование концентрации мочевой кислоты;
- общее и биохимическое изучение крови;
- пункция воспаленного сустава;
- изучение содержимого тофусов;
- УЗИ сочленений;
- КТ, МРТ и сцинтиграфия при смазанной клинической картине.
Вернуться к оглавлению
Рентгенологическое исследование подагры
Метод диагностики заключается в поглощении лучей пораженной областью и дальнейшем проецировании на пленках или мониторе ПК. Далее информацию обрабатывает врач и дает рекомендации. Для уточнения степени разрушения скелета при подагрическом артрите, назначают рентгеновские снимки пораженных суставов. Очень известен такой рентгеновский феномен, как симптом «пробойника», который характерен для поздних сроков болезни. Это дефект кости размером от 5 мм, который чаще всего локализуется у первого плюснефалангового сустава.
На рентгеновских снимках при подагре на ранних стадиях можно обнаружить преходящий остеопороз.
Рентгенологические признаки подагры
Проявлением начальных стадий подагры может служить диффузное уплотнение мягких тканей (отечность). Иногда находят воспалительный процесс костного вещества — транзиторный артрит. Во время болезни зачастую возникает деструкция кости пациента. Эрозия и разрушение могут происходить внутри и вне сустава. Рентгенологические проявления сперва проявляются по краю костей в виде раковины или скорлупки. Различают несколько рентген признаков, которые представлены в таблице:
Использованные источники:osteokeen.ru
Рентгенограмма при подагрическом полиартрите 3 стадии
therapy.odmu.edu.ua
На снимке отчетливо виден «симптом пробойника» — округлые пустоты в дистальной трети I плюсневой кости слева (показаны красной стрелкой). Суставные поверхности плюсне-фаланговых суставов (ПФС) уплотнены и склерозированы, сужение суставных щелей, особенно выраженное в I плюсне-фаланговых суставах с обеих сторон.
Определяется деструкция костной ткани в области 1 плюсне-фаланговых суставов с обеих сторон, краевые эрозии там же (желтая стрелка), деформация и подвывих I ПФС справа, а также выраженый отек и уплотнение мягких тканей в области голеностопных суставов (зеленые стрелки).
Заключение: Рентгенологические признаки подаргического полиартрита 3 стадии, для подтверждения диагноза определить уровень мочевой кислоты в крови, наличие уратов (кристаллы МУН) в суставной жидкости, выполнить биопсию тофусов.
Подагра – это хроническая суставная патология, протекающая с периодами обострения и ремиссии, основными причинами которой является гиперурикемия и реакция организма на нее. Частота данной патологии в среднем составляет 25 случаев на каждую 1000 населения, мужчины страдают чаще в 5-6 раз.
Тактика ведения пациента с подагрическим артритом включает следующие мероприятия:
- Коррекция образа жизни, строгая диета с исключением продуктов с большим содержанием пуринов, снижение веса.
- Достижение компенсации хронических заболеваний, влияющих на частоту обострений (ИБС, гипертоническая болезнь, дислипидемия, сахарный диабет).
- Назначение НПВС, глюкортикостероидов (внутрисуставные инъекции), колхицина в острый период;
Прием препаратов, снижающих уровень мочевой кислоты – аллопуринол, фебуксостат, пробенецид, сульфинпиразон, бензбромарон, бензиодарон.
Использованные источники:legsgo.ru
анализы, побочные эффекты, проявления, у взрослых
Многие годы пытаетесь вылечить СУСТАВЫ?
Глава Института лечения суставов: «Вы будете поражены, насколько просто можно вылечить суставы принимая каждый день…Читать далее »
Когда болят большие пальцы на ногах, человек не может нормально передвигаться, ведь именно на стопы приходится большая нагрузка. Боль в большом пальце стопы чаще всего возникает при заболеваниях суставов, а если происходит смещение 1-го пальца от своей оси и образуется шишка на большом пальце, то виною такого состояния становится плоскостопие. Бывают ситуации, когда болит большой палец по причине ношения неудобной обуви или при долгой нагрузке на ноги, в таких случаях симптоматика проходит в состоянии покоя. Но если болезненность не проходит или, наоборот, усиливается, то нужно посетить врача-ортопеда, который проведет необходимые исследования и расскажет, как лечить выявленную патологию.
Вообще, существуют три основных заболевания, при которых чаще всего болит сустав большого пальца, – это артроз, артрит и плоскостопие. Другое дело, что эти заболевания могут вызывать многочисленные причины, которые, на первый взгляд, не несут опасности. К ним относят ношение обуви на высоком каблуке или с узким носком, использование старой обуви со стоптанной подошвой, а также чрезмерные нагрузки на стопы. Нередко бывают ситуации, когда заболевания сочетаются между собой, кстати, поэтому нельзя шутить с диагнозом «плоскостопие», так как из-за него увеличивается нагрузка на передний отдел подошвы и пальцы. Большинство людей не предполагает, что поставленный диагноз «плоскостопие» может сильно повлиять на работоспособность и активность стоп человека в будущем, поэтому рассмотрим подробнее это заболевание и другие патологии, вызывающие боль в пальце.
Плоскостопие
При боли в больших пальцах ног нас больше интересует поперечное плоскостопие, возникающее при уплощении свода в переднем отделе стопы. Как известно, стопа выполняет амортизирующую функцию, чтобы гасить вибрации и не передавать их силу на другие суставы. От этого у человека в нормальном состоянии не болят колени, позвоночник при ходьбе, беге или просто стоянии. Но под действием негативных факторов происходит опущение свода и, как следствие, увеличение нагрузок на пальцы.
Возникает вопрос – почему болят большие пальцы сильнее, а ответ на него таков. В норме стопа опирается в переднем отделе на две точки – головки 1-й и 5-й плюсневой кости, естественно, головка 1-й плюсневой кости и есть начало большого пальца ноги. Вот когда большой палец начинает искривляться и образуется шишка, тогда и возникает состояние вальгусной деформации 1-го пальца. Может наблюдаться искривление пальца как левой ноги, так и правой ноги.
Вызывают вальгусную деформацию те же причины, что и плоскостопие. Это ношение неудобной обуви, особенно на высоком каблуке, получение травм стопы, работа, при которой нужно много ходить или стоять. От этого возникает воспаление в суставе, что сопровождается симптомами боли. Если появляется острая боль, усиливающаяся при ходьбе, то это может означать ущемление нервов. Если не проводить лечение вальгуса, то заболевание будет прогрессировать, палец будет дальше деформироваться вовнутрь, что приведет к искривлению других пальцев стопы.
Лечение вальгусной деформации заключается в уменьшение нагрузки на стопы, особенно на палец. Для этого подбирается ортопедическая обувь, прописывается ношение шины или бандажа для пальца. Если при вальгусе начинает сильно болеть, то назначаются медикаменты из группы НПВС, которые снимают отечность, воспаление и уменьшают боль. При выборе консервативного лечения упор делается на гимнастику для стопы и физиотерапию, включая процедуры УВЧ, диадинамолечение, ударно-волновую терапию, озокеритолечение.
Если палец стал сильно искривленным и появилась шишка, то полностью избавиться от деформации в суставе можно только с помощью операции. Для этого назначается чаще всего операция по типу остеотомии.
Артроз
Еще одна патология, при которой болит большой палец стопы – это артроз. Артроз считается заболеванием, при котором поражается хрящевая ткань, которая окружает суставы и защищает их от повреждений. А также хрящи играют важную роль в питании самих суставов. Если нарушается метаболизм хрящевой ткани, то она перестает быть такой эластичной и не может выполнять функцию амортизации, что переходит в воспаление. Когда возникает воспалительный процесс, то он охватывает не только суставы, но и связки, сухожилия. Заболевание опасно разрастанием остеофитов, которые могут сдавливать сосуды и нервы.
Артроз поражает именно те суставы, на которые приходится нагрузка, поэтому часто страдают суставы в больших пальцах. Основные причины артроза:
- ношение неудобной обуви, почему чаще страдают женщины из-за своей любви к каблукам;
- работа, связанная с двигательной активностью ног;
- частые переохлаждения ног;
- травмы;
- заболевания, обусловленные нарушением обмена веществ;
- ревматизм или подагра.
Нередко артроз развивается как сопутствующая
Диагностика подагры: как выявить заболевание?
Подагра – это системное поражение организма. Толчок к развитию заболевания дает нарушение обменных процессов. Недуг характеризуется скоплением в суставах мочевой кислоты. Соли из организма обычно выводятся почками, но при развитии данной патологии наблюдается их накапливание. Со временем кристаллики начинают откладываться в суставах и органах, вызывая различные заболевания.
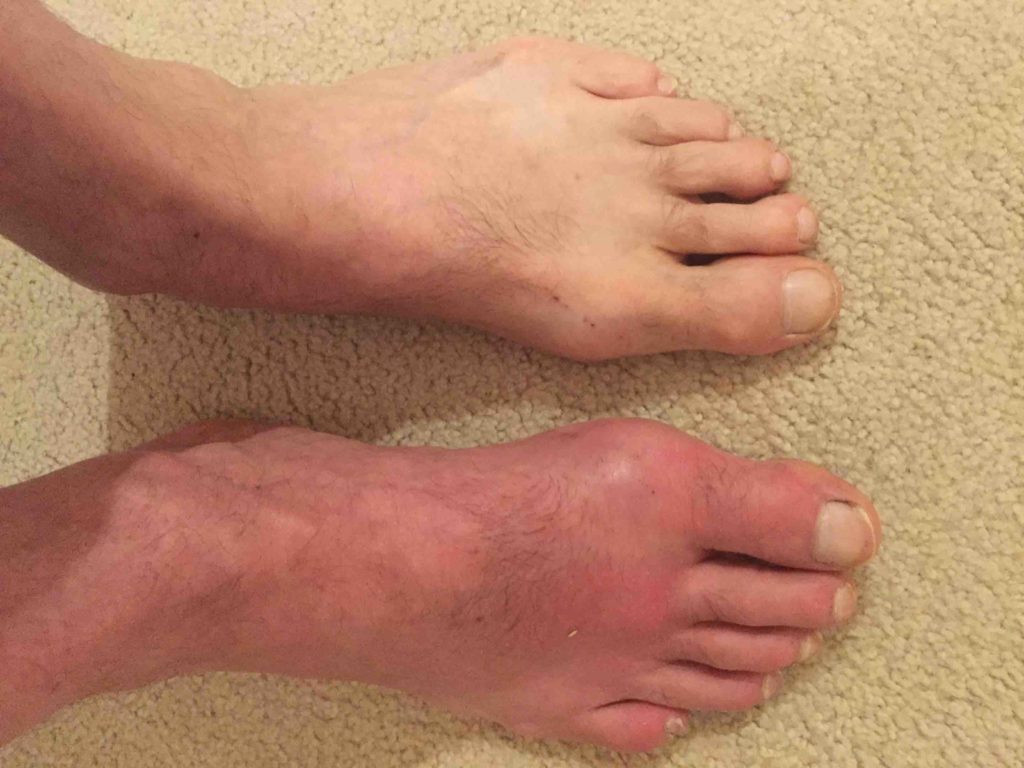 Опухшая ступня при подагре
Опухшая ступня при подагреПодагру диагностируют как у мужчин, так и у женщин. В дошкольном возрасте проявляются только первичные симптомы. Порой у ребенка эти признаки настолько слабо выражены, что их списывают на другие схожие заболевания.
Содержание страницы
Как проявляет себя подагра на различных стадиях
Симптомы болезни проявляются в зависимости от стадии течения. Больной ощущает приступообразную боль, которая чаще беспокоит по утрам и вечерам.
Развитие подагры подразделяется на:
- Преморбидную стадию. На ранней стадии диагностика ограничивается только выявлением гиперурикемии, которую определяют по анализу крови. Больной жалуется на слабость, потливость, нарушение работы ЖКТ, кожный зуд.
- Интермиттирующую или интервальную стадию. Определить развитие болезни можно по кристаллам, находящимся в мягких тканях возле сустава. Иногда на УЗИ могут выявить соли в почках. Велика вероятность развития нефропатии почек. Человек начинает испытывать острые приступы заболевания, которые длятся 3-7 дней с последующей завершающей ремиссией. Для уточнение диагноза специалист может направить больного на дуплексное сканирование вен нижних конечностей.
- Хроническую стадию. Здесь наблюдается развитие тофусов различной величины. Эти кристаллические образования доставляют больному интенсивные болезненные ощущения. Часто подагра способствует развитию мочекаменной болезни. Также недуг поражает суставы и близлежащие ткани. Например, локтевой сустав, который состоит из дистального конца плечевой, лучевой, локтевой кости при поражении подагрой будет с трудом сгибаться и разгибаться.
Каждая стадия имеет свои диагностические критерии и характерные признаки. Если своевременно не начать лечение, подагра может поразить межкостный нерв, суставные сумки и связки.
Диагностика заболевания
Диагноз больному устанавливается после прохождения комплексного обследования, которое состоит из:
- сбора анамнеза;
- обобщения признаков клинической картины;
- инструментальных исследований;
- анализов.
Своевременная диагностика и лечение заболевания предотвращают риск поражения новых суставов.
Сбор анамнеза
Больного опрашивают с целью выявления причины обращения. На ранней стадии недуг поражает мелкие суставы, расположенные на руках, ногах.
Если у больного отягощена наследственность, то вероятность развития подагры возрастает. Поэтому необходимо провести дифференциацию заболевания и уточнить перенесенные за последнее время болезни, которые могли спровоцировать возникновение недуга:
- оперативные вмешательства;
- сбой функциональной деятельности почек;
- длительный курс лечения антибиотиками или стероидами.
Следует также учитывать, что причиной развития заболевания могут стать вредные привычки у пациента и регулярное потребление неправильной пищи.
Оценка клинической картины
Опытный специалист может диагностировать болезнь без проведения клинических исследований путем осмотра и опроса пациента. Острый период характеризуется набуханием вен возле больного сустава, повышением температуры тела, острой болью во время движения. Очень часто пациенты жалуются на то, что немеют пальцы ног или ощущают тремор рук.
Инструментальные исследования
Инструментальная диагностика заболевания осуществляется в виде:
- УЗИ;
- компьютерной томографии;
- рентгенографии.
Какой способ лучше выбрать для уточнения диагноза определяет врач в зависимости от состояния пациента.
Ультразвуковое исследование (УЗИ)
Проведение УЗИ наиболее эффективно в момент обострения болезни. Диагностика при помощи ультразвука позволяет констатировать:
- увеличение суставной щели;
- появление отечности;
- уплотненное состояние мягких тканей возле сустава.
После окончания периода обострения интенсивность проявление симптомов значительно уменьшается.
Компьютерная томография (КТ)
С помощью КТ можно диагностировать точную картину происходящего. Исследование позволяет выявить расположение очагов воспаления и определить, какова степень деформации больного сустава на поздних стадиях развития подагры. На ранней стадии в период обострения на снимках будет заметно уплотнение мягких тканей вокруг поврежденного сустава.
Рентгенография
Рентген является самым распространенным и самым точным методом диагностики заболевания. С помощью рентгенограммы на раннем этапе развития болезни можно исключить ревматоидный артрит и наличие других патологий.
Главный признак, помогающий подтвердить подагрический артрит — «симптом пробойника». На рентгене такая патология выглядит как кистозное формирование, располагающееся на краю кости с четкими границами. Чем больше кальция в новообразованиях, тем они лучше видны на снимках.
Анализы при подагре
Для более достоверной диагностики больного направляют в лабораторию для сдачи анализов. Основным объектом исследования является кровь пациента. Результаты анализа мочи необходимы при подозрении почечной патологии. Итоги лабораторных анализов должны подтверждать клинические проявления.
Общий анализ крови (ОАК)
Во время обострения подагры скорость оседания эритроцитов повышается, увеличивается число лейкоцитов. В период между острыми приступами анализ крови не имеет существенных изменений. Чтобы подтвердить или опровергнуть наличие заболевания нужно продолжить дальнейшую диагностику.
Общий анализ мочи (ОАМ)
В разгаре заболевания возможно выделение мочи бурого или ржавого цвета из-за высокого содержания солей – уратов. Нарушается кислотно-щелочное равновесие. При запоздалой диагностике развивается вторичный пиелонефрит со всеми вытекающими последствиями – увеличенным содержанием лейкоцитов, слизи и солей в моче. В случае возникновения мочекаменной болезни, в анализах мочи обнаруживают эритроциты, повышенное выделение белка, цилиндры.
Биохимия крови
По результату биохимического анализа крови определяют уровень мочевой кислоты и развитие гиперурикемии в организме. Согласно таблице руководителя лаборатории микрокристаллических артритов Института ревматологии РАМН, Барсковой В.Г., наиболее частой причиной возникновения гиперурикемии является именно подагра.
Мочевую кислоту в крови могут выявить и при других патологиях, таких как: псориаз, гемоглобинопатия, миелолейкоз и т.д.
Как подготовиться к анализам и исследованиям
Для точного результата следует придерживаться некоторых правил сдачи анализов:
- Кровь сдается натощак.
- Биохимия берется после суточной диеты, которая включает растительную, молочную пищу.
- Рекомендуется исключить из своего меню кофе, чай и алкогольные напитки.
Проведение инструментальной диагностики каких-либо подготовительных действий не требует, разве что моральной подготовки больного к происходящему.
Дифференциальная диагностика подагры и схожих заболеваний
Для того чтобы верно поставить диагноз, важно выявить факторы, которые отличают подагру от следующих заболеваний:
- инфекции мягких тканей;
- остеоартроза;
- остеохондроза;
- бурсита.
Ревматоидные пробы берутся для выявления в крови уровня С-реактивного белка и ревматоидного фактора. Способ применяется в остром периоде, так как во время приступов наблюдается повышение указанных значений.
Врачи при утверждении диагноза вынуждены опираться на определенные признаки. Рекомендуется руководствоваться классификационными критериями, которые были разработаны Американской Ассоциацией ревматологов и допущены ВОЗ к использованию на практике. Они позволяют диагностировать заболевание и помогают распознать острое течение подагрического артрита.
Ответы на вопросы
Обязательно ли проведение МРТ для диагностики подагры?
Стоимость магнитно-резонансного сканирования очень высокая. Не каждая больница оснащена такой аппаратурой. МРТ не входит в список обязательных исследований и назначается врачом в случае наличия некоторых дифференциальных диагнозов.
Как обнаружить заболевание на ранней стадии?
Начальная фаза патологического процесса протекает обычно без каких-либо признаков. В этом случае подагру выявляют только по результатам биохимических анализов.
Заключение
Своевременная диагностика подагры позволяет быстрее начать курс медикаментозной терапии. Попытки самостоятельного лечения заболевания в домашних условиях могут привести к необратимым последствиям. Только врач по результатам разносторонних исследований может провести дифференциальную диагностику и поставить точный диагноз.
Трудности при ведении больных подагрой | Башкова И.Б., Мадянов И.В.
Статья посвещена вопросам и трудностям ведения больных подагрой
Для цитирования. Башкова И.Б., Мадянов И.В. Трудности при ведении больных подагрой // РМЖ. 2015. No 25. С. 1508–1514.
Подагра – системное тофусное заболевание, характеризующееся отложением кристаллов моноурата натрия в различных тканях и развивающимся в связи с этим воспалением у лиц с гиперурикемией (ГУ), обусловленной факторами внешней среды и/или генетическими факторами [1]. В последние два десятилетия наблюдается устойчивый рост заболеваемости подагрой, вероятно, связанный как с характерологическими особенностями пациентов (повышение уровня жизни, изменение характера питания, излишняя алкоголизация) [2], так и с распространением в популяции метаболических заболеваний (ожирение, метаболический синдром, сахарный диабет (СД), артериальная гипертензия (АГ)), часто сопутствующих подагре [3–5].Несмотря на успехи в диагностике, понимании патогенеза и разработке эффективных лекарственных средств для лечения подагры, ведение этой категории пациентов может представлять для интернистов определенные трудности. Диагноз «подагра» устанавливается в первый год заболевания только в 1/4 случаев, в среднем же проходит 7–8 лет до постановки правильного диагноза [1]. Причиной поздней диагностики может явиться естественное течение заболевания – чередование редких, к тому же кратковременных приступов моноартрита, с более длительными «светлыми промежутками» болезни вследствие присущего подагрическому артриту самолимитирующего характера.
Другим объяснением поздней диагностики подагры может служить и то, что врачом «первого контакта» при этом заболевании нередко становится хирург или травматолог, который, видя перед собой пациента с острым, крайне болезненным артритом, направляет его на рентгеновское исследование пораженного сустава, с помощью которого диагностировать дебют подагры зачастую не представляется возможным, поскольку крупные кисты в субхондральной зоне кости (так называемый симптом «пробойника» или рентгенонегативные внутрикостные тофусы) появляются значительно позже – в среднем через 7–8 лет от момента первого приступа подагры [6, 7].
В отсутствие костно-деструктивных изменений на рентгенограммах дистального отдела стопы состояние расценивается как «ушиб мягких тканей», что обычно сопровождается рекомендациями по приему нестероидных противовоспалительных препаратов (НПВП), которые в силу своей эффективности в данной ситуации убеждают врача и пациента в правомочности неверного диагноза. В ряде случаев можно предсказать сценарий дальнейшего развития заболевания: каждый последующий приступ моноартрита пациент будет стараться купировать самостоятельно, принимая «понравившийся с первого раза» НПВП, до тех пор, пока либо не проявится неблагоприятная реакция на препарат, либо НПВП перестанут оказывать ожидаемый эффект.
Среди типичных ошибок, которые допускаются врачами при ведении пациентов с острым подагрическим артритом, выделяют: назначение физиотерапевтических процедур, анальгетиков, мазей/гелей, наносимых локально в области пораженного сустава, назначение аллопуринола в момент приступа, промедление с назначением эффективной анальгетической и противовоспалительной терапии [8]. Несвоевременное и неэффективное лечение подагры способствует не только усугублению коморбидной патологии, которая свойственна этой категории больных, в частности ишемической болезни сердца (ИБС) [9], но и развитию фатальных осложнений.
Приводим собственное наблюдение, когда сочетание подагры, ГУ, нарушений углеводного и липидного обменов, АГ, а также невнимательное отношение пациента к своему здоровью стали причиной летального исхода у молодого мужчины.
Больной С., 42 года, был госпитализирован в ревматологическое отделение РКБ (Чебоксары) 29.04.2014 г. с жалобами на постоянные интенсивные боли в левом коленном, голеностопных, плюснефаланговых суставах 1-х пальцев обеих стоп, ряде проксимальных межфаланговых суставов кистей, усиливающиеся в ночное время. Из анамнеза заболевания: впервые приступ острого артрита плюснефалангового сустава 1-го пальца правой стопы развился 10 лет назад, в последующем артриты рецидивировали, суставной процесс постепенно принял полиартритический характер, наблюдалось закономерное сокращение интервалов между приступами до 2–3 мес. К врачам пациент не обращался, самостоятельно эпизодически принимал нимесулид. В 2009 г. перенес острый передне-перегородочно-верхушечный инфаркт миокарда с зубцом Q, в том же году впервые выявлена гипергликемия (уровень сахара крови натощак 13,6 ммоль/л) и ГУ (сывороточный уровень мочевой кислоты 572 мкмоль/л). Назначенные дезагрегантные (ацетилсалициловая кислота 100 мг/сут, клопидогрел 75 мг/сут), пероральные сахароснижающие (метформин 1000 мг/сут), гиполипидемические (аторвастатин 20 мг/сут), урикодепрессорные (аллопуринол 100 мг/сут) препараты, β-адреноблокаторы (бисопролол 5 мг/сут) пациент после выписки из стационара не принимал. С 2010 г. наблюдался стремительный рост тофусов с локализацией на ушных раковинах, в области суставов кистей, стоп, обострение подагрического артрита с кратностью до 5–6 р./год. В апреле 2014 г. после алкогольного эксцесса (злоупотребление алкоголем в течение 7 дней) развилось тяжелое обострение хронического подагрического артрита: боль, припухлость, локальная гиперемия и гипертермия левого коленного сустава, голеностопных, плюснефаланговых суставов 1-х пальцев стоп, ряда пястно-фаланговых и проксимальных межфаланговых суставов обеих кистей. Внутримышечное введение диклофенака по 75 мг 2 р./сут и пероральный прием нимесулида 400 мг/сут – без эффекта. В левой пяточной области рана размером 1,5×1,0 см (изъязвленный тофус) с белым творожистым отделяемым. Пациент самостоятельно обратился к хирургу, в амбулаторных условиях выявлено повышение уровня сахара крови до 27,8 ммоль/л и уровня мочевой кислоты до 686 мкмоль/л, в связи с чем пациент был направлен в ревматологический стационар 29.04.2014 г.
При поступлении состояние больного тяжелое, вынужденное положение из-за болей в левом коленном суставе, дефигурация коленных (больше левого), голеностопных суставов, множественные неизъязвленные тофусы с локализацией на ушных раковинах, в области суставов кистей (рис. 1) и стоп (рис. 2), изъязвленный тофус в левой пяточной области. Периферических отеков нет. Индекс массы тела – 25,6 кг/м2. Перкуторно по всем легочным полям ясный легочный звук. В легких дыхание везикулярное, хрипов на момент осмотра нет. Границы относительной тупости сердца: правая – по правому краю грудины, верхняя – в третьем межреберье, левая – на 1,0 см кнаружи от срединно-ключичной линии. Артериальное давление (АД) – 160/100 мм рт. ст. Тоны сердца ритмичные, систолический шум по левому краю грудины. Живот мягкий, чувствительный при пальпации в правом подреберье. Печень – по краю реберной дуги. Симптом поколачивания отрицательный с обеих сторон.


В общем анализе крови: эритроциты – 4,93×1012/л, гемоглобин – 149 г/л, тромбоциты – 61×109/л, лейкоциты – 4,2×109/л, сдвиг лейкоформулы влево (юные нейтрофилы – 2%, палочкоядерные нейтрофилы – 35%), абсолютная лимфопения (0,38×109/л), СОЭ по методу Панченкова – 36 мм/ч. В общем анализе мочи: протеинурия (0,36 г/л), при микроскопии мочевого осадка выявлены: лейкоцитурия (10–12 в поле зрения), микрогематурия (6–8 эритроцитов в поле зрения), цилиндурия (гиалиновые и зернистые), ураты в большом количестве. В биохимическом анализе крови: общий билирубин – 21 мкмоль/л, АлАТ – 89 Ед/л (при верхней границе нормы до 40 Ед/л), АсАТ – 135 Ед/л (при верхней границе нормы до 40 Ед/л), мочевина – 14,4 ммоль/л, креатинин – 215 мкмоль/л, общий белок – 62 г/л, общий холестерин – 3,64 ммоль/л, глюкоза – 15,0 ммоль/л, мочевая кислота – 761 мкмоль/л, высокочувствительный С-реактивный белок (СРБ) – 426 мг/л (при верхней границе нормы до 5 мг/л). На рентгенограмме суставов стоп в прямой проекции (от 28.04.2014 г.): крупные кисты в субхондральной зоне плюсневых и проксимальных фаланг 1-х пальцев стоп и мелкие эрозии на суставных поверхностях, значительное уплотнение околосуставных мягких тканей в области плюснефалангового сустава 1-го пальца правой стопы (рис. 3).
Был выставлен диагноз «Первичная хроническая тофусная подагра преимущественно метаболического типа тяжелого течения. Хронический подагрический полиартрит, активность 3-й степени, II рентгенологической стадии. Функциональная недостаточность суставов 3-й степени. ГУ (761 мкмоль/л). Множественные крупные неизъязвленные тофусы с локализацией на ушных раковинах, в области суставов кистей и стоп, изъязвленный тофус в левой пяточной области. Хроническая подагрическая нефропатия, азотемическая стадия, ХБП 3Б стадии. СД 2 типа, диабетическая нефропатия, диабетическая макроангиопатия, целевой уровень гликозилированного гемоглобина менее 7%. Категория риска развития синдрома диабетической стопы 2. ИБС: постинфарктный кардиосклероз (острый инфаркт миокарда с зубцом Q от 2009 г.). Гипертоническая болезнь III стадии. Степень АГ 2. Риск 4 (очень высокий). Хроническая сердечная недостаточность (ХСН) IIA стадии (ФК3)».
С учетом снижения экскреторной функции почек вследствие наличия у больного почечной недостаточности (скорость клубочковой фильтрации по EPI – 35 мл/мин), СД 2 типа применение НПВП и глюкокортикоидов (ГК) для купирования обострения хронического подагрического полиартрита было противопоказано. С анальгетической целью были назначены в/м инъекции трамадола 200 мг/сут, начата терапия инсулинами короткого действия (по 10 Ед каждые 4 ч). 30.04.2014 г. в 20.30 пациент почувствовал выраженную общую слабость, усилились жажда, сухость во рту, появился холодный пот. АД – 85/40 мм рт. ст. Экстренно выполнен анализ крови на сахар – выявлена небольшая гипергликемия (9,3 ммоль/л), пациенту были введены 5% раствор глюкозы, преднизолон 90 мг, после чего состояние больного несколько улучшилось, но уже через 1 ч вновь резкое нарастание общей слабости, профузное потоотделение. При попытке встать пациент упал, потерял сознание, появился цианоз лица и плечевого пояса, АД – 40/15 мм рт. ст. На электрокардиограмме зарегистрированы признаки перегрузки правых отделов сердца (отклонение электрической оси сердца вправо, P-pulmonale, глубокий зубец S в I отведении, отрицательный зубец Т в III отведении, блокада правой ножки пучка Гиса). Для исключения острого инфаркта миокарда исследован сывороточный уровень тропонина I, который составил 0,148 мкг/л (в норме менее 0,5 мкг/л). В то же время концентрация D-димера в сыворотке крови оказалась повышенной в несколько раз и составила 2021 мкг/л (при норме до 500 мкг/л). Начаты реанимационные мероприятия, которые оказались безуспешными – при нарастающих явлениях острой сердечно-легочной недостаточности через 80 мин была констатирована биологическая смерть. Причиной смерти явилась тромбоэмболия легочной артерии.
Подагра часто сопровождается коморбидными заболеваниями [10–12], которые могут влиять на ее течение и прогноз. АГ и ИБС осложняются развитием хронической сердечной недостаточности (ХСН), которая, бесспорно, требует от врача назначения диуретических препаратов. В этой ситуации важно помнить, что все диуретики способствуют повышению уровня мочевой кислоты. В популяционном исследовании, включившим 4249 жителей Великобритании в возрасте старше 30 лет, клинически верифицированный диагноз подагры был установлен у 164 пациентов, при этом у 25 (15%) больных подагра была индуцирована приемом диуретиков, 16 (64%) из них по-прежнему продолжали принимать мочегонные препараты [13].
ГУ, возникающая в период лечения диуретиками, может быть обусловлена повышением обратной реабсорбции и снижением секреции уратов в канальцах почек, что на фоне пониженного почечного кровообращения приводит к увеличению выработки ангиотензина, еще больше угнетающего выделение мочевой кислоты [14]. Кроме того, фуросемид приводит к повышению уровня молочной кислоты, которая в свою очередь ингибирует экскрецию уратов [15].
Существует непреложное правило – диуретики, назначенные по жизненным показаниям (ХСН) больным подагрой, необходимо обязательно компенсировать приемом аллопуринола с титрованием дозы под контролем врача-ревматолога [7].
Необходимо учитывать участившиеся факты злоупотребления диуретиками молодыми женщинами по косметическим соображениям (с целью улучшения фигуры и т. п.) [14, 16]. Приводим собственное наблюдение – случай аутоятрогении – развитие у молодой женщины вторичной подагры, индуцированной длительным приемом фуросемида.
Больная А., 34 года, поступила в ревматологическое отделение РКБ (Чебоксары) 05.10.2014 г. с жалобами на постоянные интенсивные боли, припухлость и покраснение в области плюснефалангового сустава 1-го пальца левой стопы, сохраняющиеся на протяжении недели. Из анамнеза заболевания: в 2000 г. (в возрасте 20 лет) пациентка с косметической целью за короткий период времени, придерживаясь жесткой диеты с ограничением животного белка, снизила массу тела на 20 кг. В последующем для поддержания «идеальной» массы тела самостоятельно начала принимать фуросемид по ½ таблетки 1 р./2–4 нед. Без приема диуретика пациентка стала субъективно ощущать одышку, тяжесть в области сердца, связывая эти явления с задержкой жидкости, она увеличила дозу препарата до 10–12 таблеток на один прием. В 2005 г. (5 лет постоянного приема фуросемида) впервые отметила появление болей, припухлости и локальной гиперемии в области правого голеностопного сустава, которые купировались самостоятельно через 3 дня, но, несмотря на это, она продолжала принимать фуросемид в прежней дозе. В 2010 г. боли и припухлость в области правого голеностопного сустава возникли вновь и в последующем повторялись с периодичностью каждые 2–3 мес., присоединился артрит плюснефалангового сустава 1-го пальца левой стопы. Для купирования суставных болей пациентка все чаще стала прибегать к в/м введениям кеторолака. В связи с отсутствием эффекта от применения НПВП в 2014 г. обратилась к ревматологу РКБ. При обследовании у пациентки были исключены ревматоидный артрит, урогенитальная форма реактивного артрита, спондилоартриты, системная красная волчанка. В биохимическом анализе крови обращало на себя внимание повышение сывороточных уровней мочевины (25,5 ммоль/л), креатинина (128 мкмоль/л), общего холестерина (9,4 ммоль/л), мочевой кислоты (495 мкмоль/л).
Для уточнения диагноза пациентка была госпитализирована в ревматологическое отделение. Из физикального осмотра: индекс массы тела – 18,2 кг/м2; по органам и системам – без особенностей; болезненность при пальпации и дефигурация плюснефалангового сустава 1-го пальца левой стопы с локальной гиперемией и гипертермией (рис. 4). При проведении дополнительного лабораторного исследования выявлены повышение СОЭ до 54 мм/ч, гипоизостенурия, никтурия, гипер-альфа-2-глобулинемия (14%), гиперлипопротеинемия IIb типа по Фредриксону, ГУ (654 мкмоль/л), снижение суточной экскреции мочевой кислоты до 0,8 ммоль/сут (при норме 1,5–4,5 ммоль/сут). По данным эзофагогастродуоденоскопии в полости желудка определялись слизь, прозрачная желчь, слизистая желудка была диффузно гиперемирована и отечна. На рентгенограмме суставов стоп в прямой проекции (от 12.10.2014 г.) отмечены незначительное сужение суставных щелей плюснефаланговых суставов 1-х пальцев стоп, единичные кистовидные просветления в головке 1-й плюсневой кости слева (рис. 5).

Был выставлен диагноз «Вторичная подагра, индуцированная длительным приемом фуросемида, почечный (гипоэкскреторный) тип. Хронический подагрический артрит правого голеностопного сустава, плюснефалангового сустава 1-го пальца левой стопы, активность 3-й степени, рентгенологическая стадия I. ГУ (654 мкмоль/л). Хронический интерстициальный нефрит, латентное течение. ХБП 2 стадии. Гиперлипопротеинемия IIb типа. Химическая гастропатия, обусловленная рефлюксом желчи». Был немедленно отменен фуросемид, расширен питьевой режим до 1,5–2 л/сут (раньше пила не более 300–500 мл). Уровень мочевой кислоты за 14 дней снизился до 631 мкмоль/л. Для купирования артрита пациентке был назначен амтолметин гуацил (АМГ) в дозе 1200 мг/сут в 2 приема. Переносимость препарата была удовлетворительной. После полного купирования воспалительных явлений в суставе (через 7 дней) на фоне продолжающегося приема АМГ в стационаре инициирована терапия аллопуринолом в начальной дозе 100 мг/сут с рекомендациями титрования дозы последнего до достижения нормоурикемии (целевой уровень мочевой кислоты в сыворотке крови – менее 360 мкмоль/л) в амбулаторных условиях.
Достаточно распространенными являются и ошибки, допускаемые в ведении пациентов с хроническим подагрическим артритом. Среди них:
1) назначение аллопуринола в острый период болезни;
2) в ряде случаев не проводится титрование дозы аллопуринола до максимально эффективной, позволяющей достичь целевого значения уровня мочевой кислоты;
3) прекращение приема аллопуринола при достижении нормоурикемии;
4) необоснованное назначение глюкокортикоидов (ГК) для купирования обострения хронического подагрического артрита, которые в свою очередь могут привести к усугублению сопутствующих подагре метаболических расстройств (АГ, СД 2 типа, дислипидемии), развитию вторичной надпочечниковой недостаточности при отмене лечения, стремительному росту интрадермальных тофусов при длительном применении, снижению эффективности ГК через 1 год терапии (по силе своего действия ГК становятся сопоставимыми с НПВП) [8, 17, 18];
5) резекция подкожных тофусов без достижения нормоурикемии, что создает угрозу для инфицирования длительно незаживающих кожных дефектов [19].
На аналогичные терапевтические ошибки, допускаемые врачами первичного звена здравоохранения в ведении пациентов с подагрическим артритом, указывают М.В. Склянова и А.Н. Калягин. При проведенном ими анонимном анкетировании 50 участковых терапевтов Иркутска выяснилось, что 56% врачей допускают возможность назначения аллопуринола в острый период болезни, каждый четвертый (26%) указал на необходимую отмену приема аллопуринола после достижения нормоурикемии, 10% врачей в своей клинической практике никогда не назначали пациентам с подагрой аллопуринол, в то время как 44% опрошенных указали на целесообразность применения аллопуринола у лиц с бессимптомной ГУ [20].
Приводим собственное наблюдение, когда бесконтрольное применение ГК в отсутствие достижения нормоурикемии послужило поводом для хирургического удаления подкожных депозитов солей мочевой кислоты, что неминуемо сопровождалось обострением хронического подагрического артрита и привело к длительному незаживлению раневой поверхности.
Больной А., 60 лет, поступил в ревматологическое отделение РКБ (Чебоксары) 19.10.2015 г. с жалобами на постоянные интенсивные боли, припухлость и покраснение в области правого голеностопного сустава, ряде плюснефаланговых суставов правой стопы, незаживающую в течение 1 года рану в области 2-го пальца правой стопы после ампутации, выполненной 08.09.2014 г. Из анамнеза заболевания: в возрасте 45 лет впервые развился острый артрит плюснефалангового сустава 1-го пальца правой стопы, который купировался самостоятельно через 7 дней. Первое обращение к врачу-терапевту – спустя несколько лет после череды рецидивирующих артритов одного и того же плюснефалангового сустава. При обследовании выявлена ГУ (сывороточный уровень мочевой кислоты на тот момент составил 456 мкмоль/л). Выставлен диагноз «подагра, хронический подагрический артрит», после купирования подагрической атаки НПВП (диклофенак 150 мг/сут в течение 10 дней) начата терапия аллопуринолом в дозе 100 мг/сут. Доза последнего препарата на протяжении 12 лет не пересматривалась. На этом фоне пациент отмечает присоединение артритов одноименного сустава левой стопы, голеностопных, локтевых, лучезапястных суставов, пястно-фалангового сустава 2-го пальца правой кисти. Обострение заболевания – более 5 р./год, в области суставов кистей и стоп в последние 7–8 лет появились подкожные образования (тофусы) с нарастанием их размеров и количества. Приступы артритов, по рекомендации врача-терапевта, купировал внутримышечными инъекциями кеторолака, реже – диклофенака или приемом нимесулида. Постоянно использовал мази/гели на область пораженных суставов в момент суставных атак, принимал широко рекламируемые в средствах массовой информации биологически активные добавки с целью снижения уровня мочевой кислоты в крови. Ретроспективный анализ амбулаторной медицинской карты выявил постоянную ГУ с минимальным значением мочевой кислоты 571 мкмоль/л. В сентябре 2014 г. обратился к хирургу в связи с появлением интенсивных болей, припухлости, покраснения в области 2-го пальца правой стопы с распространением отека и гиперемии на тыл стопы, а также повышением температуры тела. В анализах крови выявлены нейтрофильный лейкоцитоз без сдвига влево (11,0×109/л), повышение СОЭ (46 мм/ч) и уровня СРБ (85,8 мг/л). На рентгенограмме суставов правой стопы в прямой проекции (от 08.09.2014 г.): множественные кисты эпифизов плюсневых костей и фаланг пальцев и эрозии на суставных поверхностях, уплотнение околосуставных мягких тканей в области плюснефаланговых суставов правой стопы (рис. 6). Состояние было расценено как «острый гнойный артрит», вследствие чего 08.0.2014 г. выполнена ампутация 2-го пальца правой стопы (рис. 7) с последующим назначением антибактериальной терапии. В момент оперативного вмешательства получено большое количество творожистого белого отделяемого в отсутствие гнойного экссудата. Рана заживала вторичным натяжением, по настоящее время сохраняется кожный дефект в основании 2-го пальца правой стопы с периодическим отхождением из раны тофусных масс. В последние 2 года пациент отмечал частые рецидивы артрита правого лучезапястного, коленных и голеностопных суставов, применение НПВП (диклофенак, кеторолак, нимесулид, мелоксикам) стало неэффективным, вследствие чего для купирования хронического подагрического артрита в последующие месяцы использовались внутримышечные инъекции пролонгированного бетаметазона. Наблюдался стремительный рост тофусов (рис. 8).
В марте 2015 г. в связи с повышением температуры тела до 39°С, появлением болей в поясничной области, нарастанием общей слабости был госпитализирован в нефрологическое отделение ГКБ № 1 (Тольятти). При лабораторном исследовании выявлены лейкоцитоз (13,0×109/л) со сдвигом лейкоформулы влево (палочкоядерные нейтрофилы – 8%), повышение СОЭ до 55 мм/ч; в анализе мочи – протеинурия (1,19 г/л), лейкоцитурия и бактериурия при микроскопии мочевого осадка. Наблюдалось снижение скорости клубочковой фильтрации по EPI до 61 мл/мин на фоне гиперкреатининемии (125 мкмоль/л) и концентрационной функции почек (суточные колебания относительной плотности мочи от 1004 до 1009, никтурия – ночной диурез против дневного – 1,49 л против 0,8 л). При проведении ультразвукового исследования почек обнаружены уменьшение толщины паренхимы с повышением ее эхоплотности с множественными очагами фиброза до 4–5 мм, бугристость контура почки, расширение чашечно-лоханочной системы почки, что указывало на наличие у пациента хронического пиелонефрита, носящего, вероятно, вторичный характер. Был выставлен диагноз «Хроническая подагрическая нефропатия с поражением почек по типу хронического интерстициального нефрита. Вторичный хронический пиелонефрит, обострение. ХБП 2 стадии». На фоне проведенной антибактериальной (цефтриаксон 2 г/сут) и антигипертензивной (амлодипин 10 мг/сут и лозартан 100 мг/сут) терапии наблюдались улучшение показателей общего анализа крови и мочи, нормализация АД, снижение уровня креатинина в сыворотке крови до 102 мкмоль/л (СКФ по EPI – 79 мл/мин). При выписке пациенту рекомендовано обратиться к ревматологу для подбора дозы аллопуринола, однако больной продолжал принимать препарат в дозе 100 мг/сут, с последующей чередой обострений хронического подагрического артрита, для купирования которых неоднократно были использованы ГК.
Из анамнеза жизни известно, что пациент страдает язвенной болезнью желудка с редким рецивированием язв. Злоупотребление алкоголем отрицает.
При проведении физикального осмотра в момент госпитализации в ревматологическое отделение: индекс массы тела – 23,2 кг/м2; по органам и системам – без особенностей; болезненность при пальпации и дефигурация правых лучезапястного и голеностопного суставов с локальной гиперемией и гипертермией, отек тыла правой стопы, преимущественно у основания пальцев, множественные тофусы с локализацией на кистях и стопах. При проведении дополнительного лабораторного исследования выявлены повышение СОЭ (по методу Панченкова) до 21 мм/ч и СРБ до 18,9 мг/л, гипоизостенурия, ГУ (551 мкмоль/л) при снижении суточной экскреции мочевой кислоты до 1,0 ммоль/сут (при норме 1,5–4,5 ммоль/сут). На рентгенограмме суставов кистей в прямой проекции: кистовидные просветления в эпифизах костей, мелкие эрозии на суставных поверхностях, сужение суставных щелей ряда пястно-фаланговых и межфаланговых суставов, значительное уплотнение околосуставных мягких тканей в проекции плюснефаланговых суставов 3-х пальцев обеих кистей (рис. 9).



Был выставлен диагноз «Первичная хроническая тофусная подагра преимущественно метаболического типа тяжелого течения. Хронический подагрический полиартрит, активность 2-й степени, II рентгенологической стадии. Функциональная недостаточность суставов 2 степени. ГУ (551 мкмоль/л). Множественные крупные неизъязвленные тофусы с локализацией в области суставов кистей и стоп. Хроническая подагрическая нефропатия по типу хронического интерстициального нефрита, азотемическая стадия, ХБП 2 стадии. Состояние после экзартикуляции 2-го пальца правой стопы. Гипертоническая болезнь II стадии. Достигнутая степень АГ 1. Риск 3 (высокий)». Для купирования артрита пациенту был назначен АМГ по 600 мг 2 р./сут (с рекомендациями приема препарата строго натощак). На фоне продолжающегося приема АМГ была повышена доза аллопуринола до 200 мг/сут, через 1 нед. повторно был определен уровень мочевой кислоты в сыворотке крови, который составил 370 мкмоль/л, что требовало дальнейшего титрования дозы аллопуринола до достижения нормоурикемии (целевой уровень мочевой кислоты – менее 360 мкмоль/л) при продолжении превентивной противовоспалительной терапии АМГ.
В момент обострения хронического подагрического артрита перед врачом стоит задача максимально быстро, эффективно и безопасно купировать артрит. В этом случае препаратами первой линии становятся НПВП. По мнению М.С. Елисеева и В.Г. Барсковой, это может быть как неселективный, так и селективный ингибитор циклооксигеназы-2 при условии максимально быстрой реализации его противовоспалительного и анальгетического эффекта с минимальной частотой развития неблагоприятных реакций [18].
В последние годы в арсенале отечественных врачей появился принципиально новый неселективный НПВП – амтолметин гуацил (Найзилат®, Dr. Reddy’s Lab), обладающий наряду с выраженным анальгетическим и противовоспалительным действием гастропротективным эффектом. Последнее стало возможным благодаря модификации молекулы толметина путем введения аминокислоты ванилина, что позволило достичь реализации защитного действия АМГ по отношению к слизистой оболочке желудочно-кишечного тракта (ЖКТ) при сохранении класс-специфических положительных эффектов НПВП. Гастропротективные свойства препарата связаны со стимуляцией рецепторов капсаицина (так называемые ваниллоидные рецепторы, название которых происходит от наличия ванилиновой группы в молекуле АМГ), находящихся в стенках ЖКТ. Возбуждение капсаициновых рецепторов приводит к высвобождению пептида, кодируемого геном кальцитонина, что в свою очередь приводит к локальному повышению продукции оксида азота (NO) именно в слизистой оболочке желудка, а не в других органах и тканях [21, 22]. Как известно, NO является одним из важных компонентов эндогенной системы защиты слизистой оболочки верхних отделов ЖКТ от повреждений, он сохраняет целостность структуры путем увеличения образования слизи и секреции бикарбонатов, усиления кровотока и репарации эпителиальных клеток, снижения хемотаксиса нейтрофилов и перекисного окисления липидов.
Эффективность и безопасность АМГ продемонстрированы в ряде клинических исследований. Так, A. Tavella и G. Ursini показали большую эффективность 4-недельной терапии АМГ по сравнению с диклофенаком у больных с мышечно-скелетной болью по влиянию на снижение выраженности боли в покое, при движении, а также нарушения функции [23]. Метаанализ 18 клинических исследований, проведенный R. Marcolongo et al. по оценке безопасности применения АМГ у пациентов с остеоартрозом и ревматоидным артритом по сравнению с другими неселективными НПВП, такими как диклофенак, толметин, индометацин, напроксен, пироксикам и ибупрофен, показал, что частота побочных эффектов и случаев преждевременного прекращения терапии была более низкой в группе АМГ. Отношение шансов (ОШ) неблагоприятных реакций АМГ по сравнению с таковыми других НПВП, оцененных вместе, составило 0,2 (95% ДИ 0,1–0,3). При эндоскопической оценке частота и выраженность повреждений слизистой оболочки верхних отделов ЖКТ в группе пациентов, принимавших АМГ, оказались значимо ниже, чем в группах контроля, – ОШ умеренных и тяжелых эрозивно-язвенных изменений составило 0,1 (95% ДИ 0,1–04) [24].
Еще одно исследование безопасности и эффективности АМГ у больных ревматоидным артритом было проведено группой хорватских ученых. В 24-недельное рандомизированное плацебо-контролируемое исследование было включено 180 пациентов с ревматоидным артритом, из них 85 больных получали АМГ в дозе 1200 мг/сут и 95 – целекоксиб 200 мг/сут. Оба НПВП продемонстрировали одинаковую клиническую эффективность (по ACR-20) при ее оценке на 4-й, 12-й и 24-й нед. терапии. При анализе эндоскопических данных не было выявлено статистически значимой разницы в группах, применявших АМГ или целекоксиб, какие-либо гастроинтестинальные изменения по данным эзофагогастродуоденоскопии были отмечены у 24,8% и 22,3% больных соответственно. В то время как клинические проявления симптома диспепсии (боль и дискомфорт в эпигастральной области) через 4 нед. терапии встречались реже на фоне приема АМГ [25].
Рекомендуемая доза АМГ составляет 600 мг 2 р./сут (максимальная суточная доза – 1800 мг), поддерживающая доза – 600 мг 1 р./сут, для сохранения гастропротективного действия препарата АМГ следует принимать натощак. Как показали исследования, АМГ хорошо переносился пациентами и при длительном применении (в течение 6 мес.).
Среди зарегистрированных ревматологических показаний для применения АМГ значатся не только ревматоидный артрит, остеоартроз, анкилозирующий спондилит, поражение околосуставных мягких тканей (бурсит, тендовагинит), но и суставной синдром при обострении подагры. И хотя в настоящее время нет исследований, посвященных применению АМГ у больных подагрой, наш позитивный опыт использования нового эффективного неселективного НПВП с собственным гастропротективным эффектом в купировании обострения хронического подагрического артрита дает право надеяться на успешное применение препарата в борьбе с острой и хронической болью.
Подагра. Клинические признаки и симптомы
Основные клинические проявления подагры:■ рецидивирующие атаки острого артрита,
■ накопление кристаллов уратов в тканях с образованием тофусов,
■ нефролитиаз,
■ подагрическая нефропатия.
В развитии подагры выделяют четыре стадии:
■ острый подагрический артрит
■ межприступная (“интервальная”) подагра,
■ хронический подагрический артрит,
■ хроническая тофусная подагра.
Острый подагрический артрит
Обычно развивается через несколько лет бессимптомной гиперурикемии в ночном время или в ранние утренние часы, сразу после подъема с постели.Может быть спровоцирован:
■ травмой,
■ приемом алкоголя,
■ погрешностями в диете,
■ хирургическими процедурами,
■ обострением сопутствующих заболеваний,
■ локальным воспалением, например, при остеоартрозе.
Характеризуется быстрым нарастанием чрезвычайно интенсивных болей, как правило, в одном суставе, сочетающихся с припухлостью сустава и покраснением кожи. Интенсивные боли делают невозможными движения в воспаленном суставе, усилению болей способствует даже легкое прикосновение.
Длительность атаки варьирует от 1—2 (в легких случаях) до 7—10 дней.
У лиц пожилого возраста приступы протекают менее остро, чем у молодых, нередко по типу олигополиартрита.
У мужчин преимущественно поражаются суставы стопы, особенно большого пальца (артрит большого пальца в 50% случаев является первым проявлением подагры; в целом развивается более чем у 80% пациентов).
У женщин в начале заболевания чаще развивается олигополиартрит (по-видимому, связано с возрастными особенностями, поскольку у женщин подагра развивается в более пожилом возрасте), чаще поражаются суставы кистей.
Наряду с артритом у многих пациентов наблюдаются системные проявления (лихорадка и лейкоцитоз), симулирующие развитие инфекционной патологии.
Характерная особенность острого подагрического артрита — полное спонтанное выздоровление и отсутствие симптомов между приступами до развития хронического подагрического артрита. Наличие болей в суставах в этот период обычно связано с сотутствующими заболеваниями суставов, наиболее часто — остеоартрозом В отсутствие лечения наблюдается учащение атак, более затяжное течение, вовлечение в процесс новых суставов.
“Интервальная” (межприступная) подагра и рецидивирующий подагрический артрит
Хотя временные интервалы между атаками острого подагрического артрита варьируют в широких пределах, в отсутствие лечения повторный приступ обычно развивается в течение первого года у 60%, двух лет — у 78% пациентов.Характерно сокращение продолжительности бессимптомного периода. Приступы становятся более тяжелыми, затрагивают “новые” суставы, иногда имеют полиартикулярный мигрирующий характер, часто сочетаются с более выраженными системными проявлениями.
Отмечается воспаление периартикулярных тканей (связки, суставные сумки). Нередко наблюдается образование единичных тофусов в тканях, обычно безболезненных.
Иногда, главным образом у женщин пожилого возраста с почечной недостаточностью, принимающих диуретики, тофусы образуются до развития артрита Только у 7% пациентов не наблюдается рецидивирования артрита в течение 10 лет.
Хроническая тофусная подагра
Характеризуется развитием тофусов (часто множественных), хронического артрита, поражения почек, мочекаменной болезни.При отсутствии специфического лечения тофусы развиваются у 50% больных. Чаще они локализуются подкожно или внутрикожно в области пальцев кистей и стоп, коленных суставов, на локтях и в ушных раковинах, но могут образовываться практически на любых участках тела и во внутренних органах. У женщин в постменопаузе тофусы нередко располагаются в области узелков Гебердена. Иногда наблюдается изъязвление кожи над тофусами со спонтанным выделением содержимого в виде пастообразной белой массы.
Раннее появление тофусов наблюдается:
■ при некоторых формах ювенильной подагры,
■ у женщин пожилого возраста, принимающих диуретики,
■ при миелопролиферативных заболеваниях,
■ при некоторых заболеваниях почек, приводящих к ярко выраженной гиперурикемии
Почечные осложнения хронической гиперурикемии
Мочекаменная болезнь и хроническая уратная (подагрическая) нефропатия являются частыми проявлениями хронической подагры. У 20—40% пациентов наблюдаются протеинурия и “мягкая” артериальная гипертензия, реже нефросклероз, яжелая артериальная гипертензия, нарушение функции почек.Частота мочекаменной болезни коррелирует с концентрацией мочевой кислоты в сыворотке крови и моче. Камни обычно рентгеноконтрастны и состоят не только из уратов, но и оксалата и фосфата кальция.
У больных лимфопролисреративными заболеваниями выраженное увеличение уровня уратов на фоне противоопухолевой терапии может приводить к преципитации мочевой кислоты в почечных канальцах и развитию острой почечной недостаточности.
У больных подагрой увеличивается частота сопутствующих заболеваний:
■ артериальной гипертензии,
■ сахарного диабета,
■ атеросклеротического поражения сосудов,
■ гипертриглицеридемии.
Ю.Б. Белоусов
Опубликовал Константин Моканов























 Онемение руки или ноги испытывал каждый человек. Стоит лечь во сне в неудобную позу и перекрыть нормальное кровоснабжение, конечность начинает терять чувствительность. Пренеприятнейшее ощущение – колкие мурашки, а рука или нога словно неживая. Но данная ситуация легко поправима. Совсем другое дело, когда онемение вызвано внутренними причинами.
Онемение руки или ноги испытывал каждый человек. Стоит лечь во сне в неудобную позу и перекрыть нормальное кровоснабжение, конечность начинает терять чувствительность. Пренеприятнейшее ощущение – колкие мурашки, а рука или нога словно неживая. Но данная ситуация легко поправима. Совсем другое дело, когда онемение вызвано внутренними причинами. Состоянием наших рук главным образом управляют лестничные мышцы. Именно они отвечают за онемение. Эти мышцы протянуты от шейных позвонков к ребрам – первому и второму. Они не только помогают шее поворачиваться и наклоняться, но даже участвуют в дыхании. Между лестничными мышцами расположен специальный нервный пучок, который управляет всей конечностью. Также здесь находится подключичная артерия – главный поставщик крови в руку.
Состоянием наших рук главным образом управляют лестничные мышцы. Именно они отвечают за онемение. Эти мышцы протянуты от шейных позвонков к ребрам – первому и второму. Они не только помогают шее поворачиваться и наклоняться, но даже участвуют в дыхании. Между лестничными мышцами расположен специальный нервный пучок, который управляет всей конечностью. Также здесь находится подключичная артерия – главный поставщик крови в руку. Если не лечить ситуацию, то рука начинает неметь всё чаще и отчетливее. Пройдёт несколько месяцев, и чувствительность может снизиться до критических границ, оставшись таковой навсегда. Со временем к левой руке может присоединиться и правая. Физическая сила конечностей начнет убывать, и больному станет трудно выполнять простые бытовые дела.
Если не лечить ситуацию, то рука начинает неметь всё чаще и отчетливее. Пройдёт несколько месяцев, и чувствительность может снизиться до критических границ, оставшись таковой навсегда. Со временем к левой руке может присоединиться и правая. Физическая сила конечностей начнет убывать, и больному станет трудно выполнять простые бытовые дела. Доброго времени суток, дорогие читатели!
Доброго времени суток, дорогие читатели! Лечебные упражнения при остеохондрозе необходимо выполнять каждый день, в течение 15 минут!
Лечебные упражнения при остеохондрозе необходимо выполнять каждый день, в течение 15 минут!

 йным остеохондрозом. Присядьте в бассейне, опустите голову под воду, обхватите колени руками, подтягивая их к животу, и «зависните» на некоторое время, при этом выдыхая носом.
йным остеохондрозом. Присядьте в бассейне, опустите голову под воду, обхватите колени руками, подтягивая их к животу, и «зависните» на некоторое время, при этом выдыхая носом. Лечебная гимнастика на фитболе может включать следующие упражнения:
Лечебная гимнастика на фитболе может включать следующие упражнения: Этот спортивный снаряд распределяет нагрузку на позвоночный столб и расслабляет спинные мышцы. С палкой можно заниматься дома и на улице. Исходное положение во время лечебных занятий – стоя. Ноги держат на ширине плеч, а спину – прямо.
Этот спортивный снаряд распределяет нагрузку на позвоночный столб и расслабляет спинные мышцы. С палкой можно заниматься дома и на улице. Исходное положение во время лечебных занятий – стоя. Ноги держат на ширине плеч, а спину – прямо. Лежачие упражнения выполняют на ровной плоскости (жесткой кровати, полу). Такие занятия требуют бóльшего мышечного напряжения, чем комплексы, которые делают сидя, поэтому достаточно 10 повторов:
Лежачие упражнения выполняют на ровной плоскости (жесткой кровати, полу). Такие занятия требуют бóльшего мышечного напряжения, чем комплексы, которые делают сидя, поэтому достаточно 10 повторов:























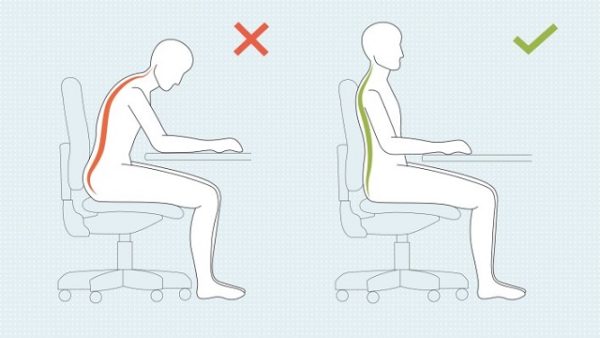
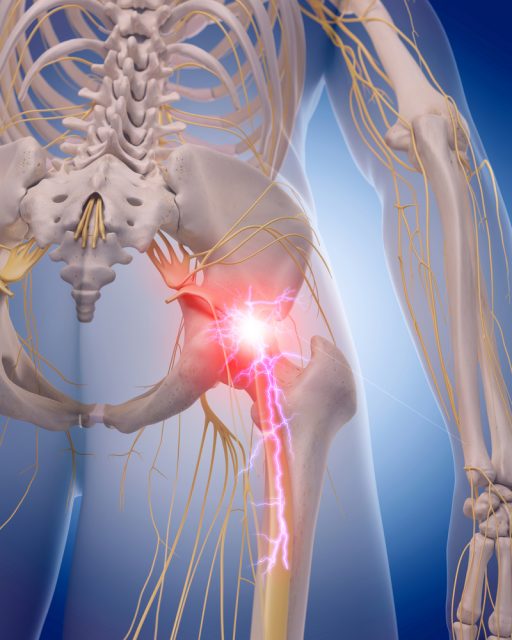
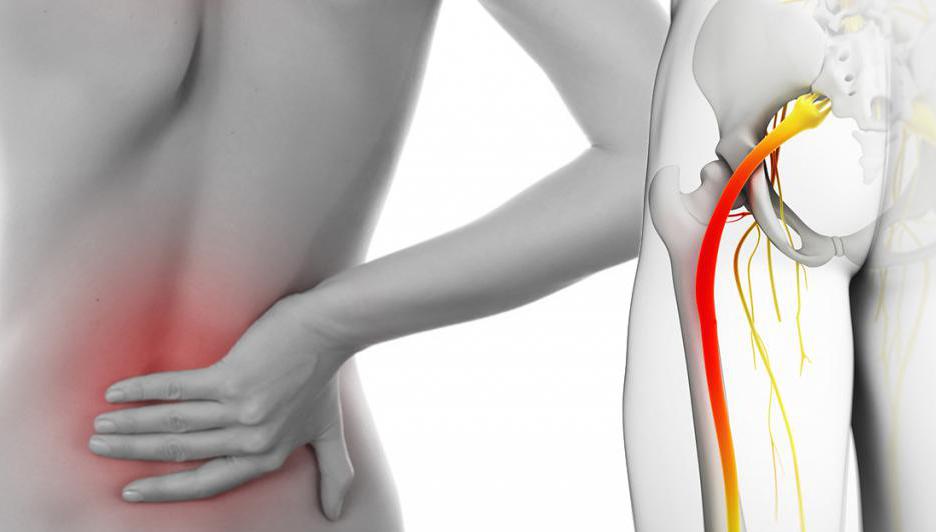


 Бардукова Елена Анатольевна
Бардукова Елена Анатольевна Что такое воспаление седалищного нерва
Что такое воспаление седалищного нерва Прострел в пояснице — внезапная острая боль, парализующая человека
Прострел в пояснице — внезапная острая боль, парализующая человека Эффективная поза при приступе боли в пояснице
Эффективная поза при приступе боли в пояснице Перед основным лечение ишиаса следует устранить острый болевой синдром
Перед основным лечение ишиаса следует устранить острый болевой синдром Кеторолак — очень эффективный препарат при сильнейшей боли
Кеторолак — очень эффективный препарат при сильнейшей боли Сирдалуд поможет расслабить напряжённые мышцы в поражённой области, что приведёт к ослаблению сдавливания седалищного нерва
Сирдалуд поможет расслабить напряжённые мышцы в поражённой области, что приведёт к ослаблению сдавливания седалищного нерва Паравертебральная блокада — эффективный метод снятия сильнейшей боли
Паравертебральная блокада — эффективный метод снятия сильнейшей боли Мильгамма, содержащая витамины группы B, необходима для восстановления повреждённых нервных окончаний
Мильгамма, содержащая витамины группы B, необходима для восстановления повреждённых нервных окончаний Пчелиный воск — популярный метод лечения ишиаса
Пчелиный воск — популярный метод лечения ишиаса Вакуумные силиконовые банки — замечательный способ лечения ишиаса в домашних условиях
Вакуумные силиконовые банки — замечательный способ лечения ишиаса в домашних условиях Лечение медицинскими пиявками при ишиасе
Лечение медицинскими пиявками при ишиасе Скипидар — дешёвое средство при ишиасе
Скипидар — дешёвое средство при ишиасе Ишиас
Ишиас Диагностика Ишиаса
Диагностика Ишиаса Упражнения помогают снять отек и боль
Упражнения помогают снять отек и боль


















 Что такое сом?
Что такое сом?














 Болезни легких. Боли в левом подреберье при вдохе и кашле ощущаются при левосторонней пневмонии. Боль может переходить на живот, вызывая напряжение его мышц. Также может быть лихорадочное состояние, покраснение кожи лица на соответствующей стороне, возникновение одышки при движении.
Болезни легких. Боли в левом подреберье при вдохе и кашле ощущаются при левосторонней пневмонии. Боль может переходить на живот, вызывая напряжение его мышц. Также может быть лихорадочное состояние, покраснение кожи лица на соответствующей стороне, возникновение одышки при движении.
 Многие не хотят применять лекарственные препараты, а прибегают к лечению народными средствами, в частности отварами и настоями трав.
Многие не хотят применять лекарственные препараты, а прибегают к лечению народными средствами, в частности отварами и настоями трав.







 Дисплазия локтевого сустава — одна из самых распространенных ортопедических патологий, которая вызывает боль и хромоту у подрастающих собак крупных и гигантских пород.
Дисплазия локтевого сустава — одна из самых распространенных ортопедических патологий, которая вызывает боль и хромоту у подрастающих собак крупных и гигантских пород.























 как следствие ущемления корешков спинномозговых нервов, а также могут развиваться и дегенеративно-дистрофические процессы, связанные с нарушением иннервации и кровообращения в околосуставных тканях коленных суставов. В народе такое заболевание называют «остеохондроз колена».
как следствие ущемления корешков спинномозговых нервов, а также могут развиваться и дегенеративно-дистрофические процессы, связанные с нарушением иннервации и кровообращения в околосуставных тканях коленных суставов. В народе такое заболевание называют «остеохондроз колена». , заключается в устранении ущемления корешков спинномозговых нервов и создании мышечного корсета, предупреждающего ущемления, что достигается в основном дозированными физическими нагрузками.
, заключается в устранении ущемления корешков спинномозговых нервов и создании мышечного корсета, предупреждающего ущемления, что достигается в основном дозированными физическими нагрузками. Остеохондроз — заболевание позвоночника, при его возникновении поражаются хрящи и межпозвонковые диски. В норме у здорового человека межпозвоночные диски способны выдерживать большую нагрузку, они довольно прочные, что позволяет сделать позвоночник более упругим и стойким к износу. Но при возникновении заболевания соединительные ткани быстро изнашиваются, начинается разрушение и стирание дисков.
Остеохондроз — заболевание позвоночника, при его возникновении поражаются хрящи и межпозвонковые диски. В норме у здорового человека межпозвоночные диски способны выдерживать большую нагрузку, они довольно прочные, что позволяет сделать позвоночник более упругим и стойким к износу. Но при возникновении заболевания соединительные ткани быстро изнашиваются, начинается разрушение и стирание дисков. Довольно быстро появляется постоянная головная боль, которая сложно поддается обезболиванию, вызывает головокружение и тошноту. Приступ часто похож на мигрень, не купируется лекарствами.
Довольно быстро появляется постоянная головная боль, которая сложно поддается обезболиванию, вызывает головокружение и тошноту. Приступ часто похож на мигрень, не купируется лекарствами. При заболевании очень важно начать лечение как можно раньше, тогда есть больше шансов на выздоровление.
При заболевании очень важно начать лечение как можно раньше, тогда есть больше шансов на выздоровление.
 Нужно понимать, что полное излечение практически невозможно, если уже началось разрушение костных тканей. Именно поэтому своевременное обращение к врачу просто необходимо при первых же болях в суставах.
Нужно понимать, что полное излечение практически невозможно, если уже началось разрушение костных тканей. Именно поэтому своевременное обращение к врачу просто необходимо при первых же болях в суставах. ревматоидный артрит. Данный тип имеет другую этиологию, связан с нарушениями обменных процессов. Один из самых опасных видов артрита потому, что вызван аутоиммунным процессом в организме. Такой процесс начинается в том случае, когда иммунитет перестает «узнавать» ферменты какого-то органа и воспринимает их как чужеродные. Чаще всего это происходит при нарушениях в работе щитовидной железы. Затягивать такое заболевание нельзя, поскольку погибнет либо вся имунная система, либо щитовидка. Иногда аутоиммунные артриты возникают на фоне серьезной дестабилизации других органов, например, поджелудочной железы;
ревматоидный артрит. Данный тип имеет другую этиологию, связан с нарушениями обменных процессов. Один из самых опасных видов артрита потому, что вызван аутоиммунным процессом в организме. Такой процесс начинается в том случае, когда иммунитет перестает «узнавать» ферменты какого-то органа и воспринимает их как чужеродные. Чаще всего это происходит при нарушениях в работе щитовидной железы. Затягивать такое заболевание нельзя, поскольку погибнет либо вся имунная система, либо щитовидка. Иногда аутоиммунные артриты возникают на фоне серьезной дестабилизации других органов, например, поджелудочной железы;

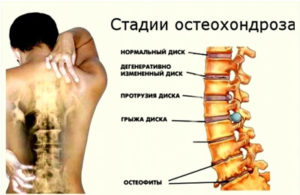
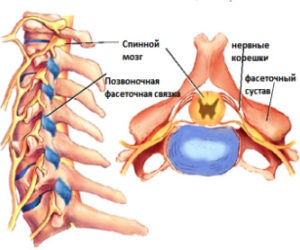
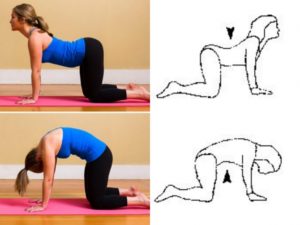
 Боль в поясничном отделе позвоночника, отдающая в тазобедренный сустав и колено. #8212; серьезный признак того, что у пациента может наблюдаться заболевание позвоночника. Болевой синдром может проявляться в умеренной степени, но это происходит только на первых стадиях заболевания. С течением времени боли будут только усиливаться. Такие проблемы с позвоночником может устранить вертебролог и невролог, также могут понадобиться сеансы остеопата.
Боль в поясничном отделе позвоночника, отдающая в тазобедренный сустав и колено. #8212; серьезный признак того, что у пациента может наблюдаться заболевание позвоночника. Болевой синдром может проявляться в умеренной степени, но это происходит только на первых стадиях заболевания. С течением времени боли будут только усиливаться. Такие проблемы с позвоночником может устранить вертебролог и невролог, также могут понадобиться сеансы остеопата.


 Часто происходит, что пациенты страдающие заболеванием коленных суставов, и испытывающие хронические боли в пояснице , не связывают эти состояния. К сожалению, врачи — хирурги, которые лечат боли в коленях и ставят диагноз: гонартроз . не опрашивают пациентов, не консультируют их у неврологов. В то же время, остеохондроз позвоночника зачастую вызывает поражения других органов. Так как значительно ухудшает иннервацию этих органов. При нарушении иннервации, орган теряет способность полноценно восстанавливаться после перегрузок, травм, инфекций. Именно от поясничного отдела позвоночника идут нервные стволы к коленным суставам. Поэтому, если вас беспокоят боли в пояснице и коленях, нужно, прежде всего, лечить остеохондроз. Причин для появления неврологического дефицита (нарушения иннервации) в коленных суставах предостаточно – это и смещение/подвывих позвонков , и артроз межпозвонковых суставов, и протрузия или грыжа диска . Сегодняшние методы диагностики позволяют установить точный диагноз. А точность диагноза – гарантия выздоровления.
Часто происходит, что пациенты страдающие заболеванием коленных суставов, и испытывающие хронические боли в пояснице , не связывают эти состояния. К сожалению, врачи — хирурги, которые лечат боли в коленях и ставят диагноз: гонартроз . не опрашивают пациентов, не консультируют их у неврологов. В то же время, остеохондроз позвоночника зачастую вызывает поражения других органов. Так как значительно ухудшает иннервацию этих органов. При нарушении иннервации, орган теряет способность полноценно восстанавливаться после перегрузок, травм, инфекций. Именно от поясничного отдела позвоночника идут нервные стволы к коленным суставам. Поэтому, если вас беспокоят боли в пояснице и коленях, нужно, прежде всего, лечить остеохондроз. Причин для появления неврологического дефицита (нарушения иннервации) в коленных суставах предостаточно – это и смещение/подвывих позвонков , и артроз межпозвонковых суставов, и протрузия или грыжа диска . Сегодняшние методы диагностики позволяют установить точный диагноз. А точность диагноза – гарантия выздоровления.









 »
Причины боли в пояснице
»
Причины боли в пояснице Многие люди, занимаясь повседневными делами, жалуются на боль в области поясницы. Она возникает неожиданно, доставляя человеку весьма неприятные ощущения. Какова причина такой боли. Человек, испытавший такую боль, может попытаться ответить на этот вопрос, делая предположения. Однако наиболее точно указать на причину недомогания в большинстве случаев может лишь врач.
Многие люди, занимаясь повседневными делами, жалуются на боль в области поясницы. Она возникает неожиданно, доставляя человеку весьма неприятные ощущения. Какова причина такой боли. Человек, испытавший такую боль, может попытаться ответить на этот вопрос, делая предположения. Однако наиболее точно указать на причину недомогания в большинстве случаев может лишь врач.

