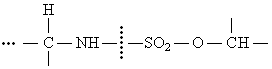Свойства гепарин – врачебный обзор: свойства, формы выпуска, порядок применения
Гепарин Распространение в природе
Гепарин – природный полисахарид класса сульфатированных гликозаминогликанов. Содержится в тканях млекопитающих: печени, легких, селезенке, почках, коже, в стенках кровеносных сосудов; синовиальной жидкости суставов; стекловидном теле глаза. В живом организме гепарин в свободном состоянии не встречается, поскольку всегда связан с молекулами белка, образуя так называемый углевод-белковый комплекс (протеогликан).
Получение
В организме животных и человека гепарин синтезируется (базофильными) тучными клетками, являющимися разновидностью клеточных элементов соединительной ткани. В связи с этим важнейшим источником для получения гепарина в фармакологических и медицинских целях является ткань легких и печени животных.
В промышленности получают два типа гепарина: высокомолекулярный
НМГ получают путем химической или ферментативной деполимеризации ВМГ.Например,далтепаринполучают методом деполимеризации с использованием азотистой кислоты,эноксапарин–методом бензилирования с последующей щелочной деполимеризацией, для получениятинзапаринаиспользуют метод ферментативного расщепления с помощьюгепариназы.
Один из методов получения НМГ заключается в использовании иммобилизованного на силохроме ферментного хитинолитического комплекса из Streptomyces kurssanovii.В процессе используется Na-ацетатный буфер с рН = 7–7.5, температура 40 – 45 С. Продолжительность гидролиза 3 ч. В зависимости от соотношения гепарин/иммобилизо-ванный ферментный комплекс были получены образцы с молекулярной массой от 1.7 до 4.7 кДа, обладающие ингибирующей фактор Ха активностью в 2.0 – 3.7 раз большей, чем у исходного гепарина.
Количественно гепарин определяют фотоколометрически по смещению длины волны максимума поглощения (макс) растворов некоторых красителей (например, азура А) в присутствии гепарина.
Химическое строение и молекулярная структура
Наиболее изучено химическое строение и молекулярная структура макромолекул гепарина различных видов соединительной ткани и некоторых жидкостей организма (синовиальная жидкость суставов, стекловидное тело глаза).
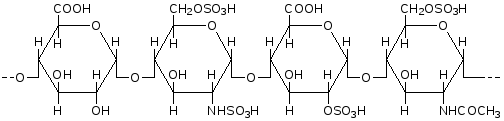
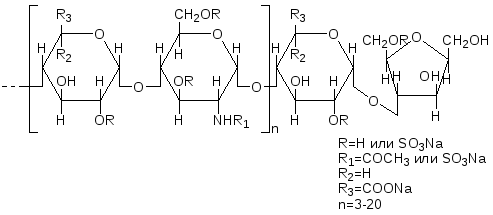
Гепарин – линейный гетерополисахарид, построенный в основном из чередующихся остатков
|
Рис.1. Структурная формула макромолекулы гепарина. |
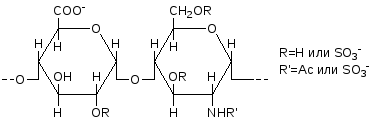
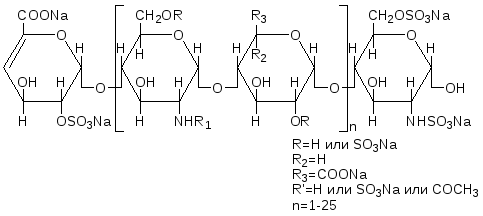
Таким образом, гепарин – типичный сополимер, содержащий в составе одной макромолекулы дисахаридные звенья нескольких типов (рис.2).
|
Рис.2.Повторяющаяся дисахаридная единица высокомолекулярного гепарина. |
Дисахаридной единице гепарина близка по структуре дисахаридная единица гепарансульфата.Отличие этих гликозаминогликанов заключается в следующем: в гепарине большеN–сульфатных групп, а в гепарансульфатеN-ацетильных. Гепарин и гепарансульфат отличаются по локализации и функции в животных тканях. Гепарансульфат в отличие от гепарина содержится в плазматических мембранах различных клеток и в межклеточном веществе.
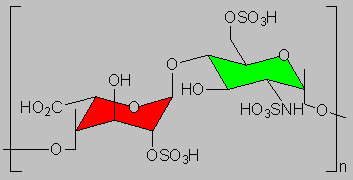
Изучение структуры гепарина методом ЯМР показало, что звенья остатков глюкуроновой кислоты находятся в макромолекуле в
|
Рис.3.Энергетически выгодная конформация повторяющейся дисахаридной единицы макромолекулы гепарина. |
По ширине рентгеновских отражений установлено, что молекула гепарина содержит 10 тетрасахаридных повторяющихся единиц.
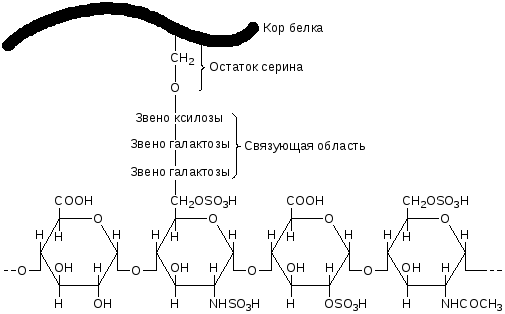
В молекуле нативного гепарина протяженные полисахаридные цепи присоединены к белковой молекуле, которая называетсякором (рис.4).Структура кора определяется местоположением и функциямиуглевод-белкового комплекса в живом организме. Связь белковой и углеводной компоненты осуществляется посредством трисахаридного мостика ксилоза – галактоза – галактоза (рис.4). Белковая часть протеогликана составляет ~5%, углеводная – ~95%.
|
Рис.4.Структура гепарин-белкового комплекса (протеогликана). |
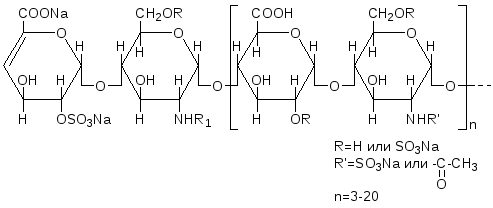
Препараты низкомолекулярного гепарина (НМГ) различаются по химической структуре, методам получения, периоду полураспада, специфическому действию на организм. Химическая структура некоторых НМГ представлена на рис.5.
(а) |
|
(б) |
 |
(в) |
|
Рис.5. Химическая структура некоторых низкомолекулярных гепаринов: далтепарин (а), эноксипарин (б), тинзапарин (в). |
Доказано, что ~1/3 молекулы гепарина обусловливает его антикоагулянтную активность. НМГ обладают более широким спектром фармакологических эффектов в сравнении с ВМГ.
studfile.net
Гепарин
Гепарин
Историческая справка. В 1916 г. студенту-медику Маклейну, изучавшему природу растворимых в эфире прокоагулянтов, посчастливилось открыть фосфолипидный антикоагулянт. Вскоре после этого Говелл, в чьей лаборатории работал Маклейн, открыл водорастворимый гликозаминогликан, названный из-за высокого содержания в печени гепарином (Jaques, 1978). Успешное предотвращение гепарином свертывания in vitro привело позднее к его использованию для лечения венозных тромбозов.
Химические свойства и механизм действия
Гепарин — гликозаминогликан, содержащийся в гранулах тучных клеток. В ходе его синтеза из различных УДФ-сахаров образуется полимер, состоящий из чередующихся остатков D-глюкуроновой кислоты и N-ацетил-глюкозамина (Bourin and Lindahl, 1993). Примерно 10— 15 таких гликозаминогликановых цепей (по 200—300 моносахаридов каждая) присоединяются к белковой части молекулы, образуя протеогликан с молекулярной массой 750 000—1 000 000. Затем происходит модификация гликозаминогликановых цепей: N-деацетилирование и N-cyльфатирование остатков глюкозамина, эпимеризация D-глюкуроновой кислоты в L-идуроновую, О-сульфатирование остатков этих кислот в положении 2, О-сульфатирование остатков глюкозамина в положениях 3 и 6 (рис. 55.2). Так как эти реакции затрагивают не все моносахариды, структура получающихся молекул весьма разнообразна. Гликозаминогликановые цепи гепарина, перенесенного в гранулы тучных клеток, в течение нескольких часов расщепляются p-глюкуронидазой на фрагменты с молекулярной массой 5000—30 000 (в среднем около 12 000, то есть 40 моносахаридов).
Родственные гликозаминогликаны
Гепарансульфат присутствует на клеточной мембране большинства эукариотических клеток и во внеклеточном матриксе. Он синтезируется из тех же повторяющихся последовательностей дисахаридов, что и гепарин (D-глюкуроновая кислота и N-ацетилглюкозамин), но подвергается меньшей модификации и поэтому содержит больше D-глюкуроновой кислоты и N-ацетилглюкозамина и меньше сульфатных групп. Гепарансульфат также обладает антикоагулянтными свойствами in vitro, но в значительно больших концентрациях.
Дерматансульфат представляет собой полимер L-идуроновой кислоты и N-ацетилгалактозамина с различной степенью О-сульфатирования L-идуроновой кислоты в положении 2 и га-лактозамина в положениях 4 и 6. Как и гепарансульфат, дерматансульфат присутствует на клеточной мембране и во внеклеточном матриксе и обладает антикоагулянтными свойствами in vitro.
Источники
Гепарин обычно получают из бычьих легких или слизистой свиного кишечника. Такие препараты могут содержать небольшую примесь других гликозаминогликанов. Хотя состав гепаринов различного производства несколько отличен, их биологическая активность примерно одинакова (около 150 ед/мг). За 1 ед принимается количество гепарина, предотвращающее свертывание 1 мл цитратной овечьей плазмы в течение часа после добавления 0,2 мл 1% СаС12.
Низкомолекулярные гепарины с молекулярной массой 1000— 10 000 (в среднем 4500, то есть 15 моносахаридов) получают из обычного препарата путем гельфильтрации, преципитации этанолом или частичной деполимеризации с помощью азотистой кислоты и других реагентов. Низкомолекулярные гепарины отличаются от обычного и друг от друга фармакокинетическими свойствами и механизмом действия (см. ниже). Их активность обычно определяют по ингибированию фактора Ха.
Физиологическая роль
Гепарин содержится в тканях внутри тучных клеток. По-видимому, он нужен для хранения внутри гранул этих клеток гистамина и некоторых протеаз (Humphries et al., 1999; Forsberg et al., 1999). После выхода из тучных клеток гепарин быстро захватывается и разрушается макрофагами. У здоровых людей в плазме его выявить не удается. Однако у больных системным мастоцитозом при массивной дегрануляции тучных клеток иногда наблюдается небольшое удлинение АЧТВ, предположительно связанное с выбросом гепарина в кровоток.
Молекулы гепарансульфата на поверхности эндотелиальных клеток и во внеклеточном матриксе субэндотелиального слоя взаимодействуют с антитромбином III, препятствуя тромбообразованию. При злокачественных новообразованиях иногда наблюдается кровоточивость, вызванная попаданием гепарансульфата или дерматансульфата в кровоток (вероятно, при распаде опухоли).
Механизм действия
В 1939 г. Бринкхаус и сотр. обнаружили, что антикоагулянтное действие гепарина опосредуется одним из компонентов плазмы, и назвали его кофактором гепарина. Тридцатью годами позже выяснилось, что им является антитромбин III — белок плазмы, который быстро инактивирует тромбин в присутствии гепарина (Olson and Bjork, 1992). Антитромбин III представляет собой гликозилированный одноцепочечный полипептид с молекулярной массой около 58 000, гомологичный семейству серпинов (спиновых яротеаз ингибиторов), в частности агантитрипсину. Антитромбин III синтезируется в печени, его сывороточная концентрация составляет 2,6 мкмоль/л. Он активен против факторов внутреннего и общего механизмов свертывания (в частности, 1Ха, Ха и тромбина), но слабо действует на фактор Vila. Механизм ингибирующего действия антитромбина III следующий. Перечисленные факторы свертывания, как уже говорилось, являются протеазами. Антитромбин III выступает в роли их субстрата: активные факторы свертывания атакуют определенную пептидную связь между аргинином и серином в реактивном центре его молекулы. Однако расщепления этой связи не происходит, и образуется устойчивый комплекс из фактора свертывания и антитромбина III в эквимолярном соотношении. В результате фактор свертывания теряет протеолитическую активность.
Гепарин ускоряет взаимодействие антитромбина III с тромбином более чем в 1000 раз благодаря тому, что служит матрицей, связывающей оба белка. Связывание с гепарином изменяет также конформацию антитромбина III, делая его реактивный центр более доступным для тромбина (Jin et al., 1997). После образования комплекса тромбин—антитромбин III молекула гепарина высвобождается. Участок молекулы гепарина, отвечающий за связывание с антитромбином III, представляет собой пентасахаридную последовательность, содержащую остаток глюкозамина, О-сульфатированный в положении 3 (рис. 55.2). Эта структура обнаруживается примерно в 30% молекул гепарина и, реже, в гепарансульфате. Другие гликозаминогликаны (дерматансульфат, хондрои-тинсульфаты) лишены этой структуры и не способны активировать антитромбин III. Гепарины с молекулярной массой менее 5400 (содержащие меньше 18 моносахаридов) не могут связывать одновременно антитромбин III и тромбин и потому не ускоряют инактивацию последнего. В то же время показанный на рис. 55.2 пентасахарид катализирует ингибирование антитромбином III фактора Ха (видимо, для этого достаточно только конформа-ционных изменений антитромбина III). Именно этим объясняется антикоагулянтное действие низкомолекулярных гепаринов, большинство молекул которых слишком коротки, чтобы связывать тромбин.
Антитромбин III быстро (Т1/2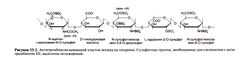 Рисунок 55.2. Антитромбинсвязываюший участок молекулы гепарина.
Рисунок 55.2. Антитромбинсвязываюший участок молекулы гепарина.Таким образом, гепарин ускоряет инактивацию фактора Ха и «юмбина лишь после их освобождения из мест связывания. Тромбоцитарный фактор 4, высвобождающийся из а-гранул при агрегации тромбоцитов, препятствует связыванию антитромбина III с гепарином и гепарансульфатом, способствуя образованию тромба в месте свертывания.
При концентрации гепарина или дерматансульфата выше 5 ед/мл их ингибирующее действие на тромбин опосредовано преимущественно кофактором гепарина П. Гепарин стимулирует также подавление активности тромбина антиактиватором плазминогена 1, ингибитором протеина С и протеазой нексин-1 и активности фактора Ха ингибитором внешнего механизма свертывания. Концентрации четырех последних ингибиторов в плазме в 100 с лишним раз меньше, чем концентрация антитромбина III. В/в введение гепарина повышает концентрацию ингибитора внешнего механизма свертывания в несколько раз (возможно, вызывая его высвобождение из мест связывания на эндотелии).
Другие свойства гепарина
Высокие дозы гепарина могут удлинять время кровотечения, нарушая агрегацию тромбоцитов. Не ясно, велик ли вклад антиагрегантного действия гепарина в вызываемую им кровоточивость. Гепарин просветляет хилезную плазму, вызывая выход в кровоток липопротеидлипазы, которая расщепляет триглицериды на жирные кислоты и глицерин. Этот феномен наблюдается даже при низких концентрациях гепарина, недостаточных для проявления антикоагулянтного действия. После отмены препарата возможна рикошетная гипер-липопротеидемия.
Гепарин подавляет рост многих клеток в культуре, в том числе эндотелиальных и гладкомышечных клеток сосудов, а также мезангиальных клеток почек. В опытах на животных он препятствовал пролиферации гладкомышечных клеток сосудов после повреждения эндотелия сонных артерий. Это действие гепарина никак не связано с его антикоагулянтной активностью (Wright et al., 1989).
Кислый и основный факторы роста фибробластов обладают высоким сродством к гепарину. Эти факторы стимулируют рост гладкомышечных, эндотелиальных и других мезенхимных клеток, а также ангиогенез. Сам гепарин подавляет рост эндотелиальных клеток капилляров, но в то же время потенцирует действие кислого фактора роста фибробластов на эти клетки (Sudhal-teretal., 1989). Это действие зависит не от его антикоагулянтной активности, а от размера и степени сульфатирования молекул гепарина. Гепарансульфат на поверхности мезенхимных клеток служит низкоаффинным участком связывания для основного фактора роста фибробластов, а во внеклеточном матриксе стабилизирует этот фактор и выступает в качестве депо, из которого основный фактор роста фибробластов высвобождается под действием гепаринсульфатлиазы или избытка гепарина. Кроме того, он, как и гепарин, необходим для проявления биологической активности основного фактора роста фибробластов, способствуя его связыванию с высокоаффинным рецептором с собственной тирозинкиназной активностью (Yayon et al., 1991).
Применение
Гепарин начинает действовать быстро, что позволяет использовать его при венозных тромбозах и ТЭЛА. Длительность лечения обычно составляет 4—5 сут. Сразу назначают и непрямые антикоагулянты внутрь, которые к моменту отмены гепарина начинают действовать в полную силу (см. ниже). При тромбозах и эмболиях, рецидивирующих на фоне обычного лечения непрямыми антикоагулянтами (например, при синдроме Труссо), проводят длительную гепаринотерапию. Гепарин применяют также: при нестабильной стенокардии и инфаркте миокарда; при баллонной коронарной ангиопластике и установке стента; при операциях, требующих искусственного кровообращения; у некоторых больных с ДВС-синдромом. Низкие дозы гепарина успешно предотвращают венозные тромбозы и ТЭЛА у больных из группы риска (например, после операций на костях и суставах). Недавно были разработаны подробные рекомендации по применению гепарина (Proceedings of the American College of Chest Physicians 5th Consensus Conference on Antithrombotic Therapy, 1998).
Первым утвержденным ФДА показанием к применению низкомолекулярных гепаринов стала профилактика венозных тромбозов и ТЭЛА. Недавно была показана их эффективность при венозных тромбозах, ТЭЛА и нестабильной стенокардии (Hirsh et al., 1998а). Главное их преимущество перед обычным гепарином — более предсказуемая фармакокинетика, позволяющая назначать их п/к без лабораторного контроля (см. ниже). Это дает возможность лечить многих больных на дому. Кроме того, лечение низкомолекулярными гепаринами реже осложняется гепариновой тромбоцитопенией и, по-видимому, остеопорозом и кровоточивостью.
В отличие от варфарина гепарин не проходит через плаценту и не вызывает пороков развития, что позволяет назначать его беременным. Гепарин не повышает перинатальную смертность и риск преждевременных родов (Ginsberg et al., 1989а, b). Для уменьшения риска послеродового кровотечения гепарин желательно отменять за сутки до родов. Вопрос об использовании низкомолекулярных гепаринов у беременных изучен недостаточно.
Фармакокинетика
Гепарин не всасывается из ЖКТ, и поэтому его вводят п/к или путем в/в инфузии. При в/в введении препарат начинает действовать немедленно. Напротив, при п/к введении его биодоступность может сильно различаться, а действие проявляется лишь через 1—2 ч. Биодоступность низкомолекулярных гепаринов примерно одинакова.
Т1/2 гепарина зависит от дозы. При в/в введении в дозе 100, 400 и 800 ед/кг его антикоагулянтная активность уменьшается наполовину соответственно за 1, 2,5 и 5 ч (Приложение II). Разрушение гепарина в основном идет в макрофагах; небольшое количество препарата выводится в неизмененном виде с мочой. Т1/2 гепарина может несколько укорачиваться при ТЭЛА и удлиняться в терминальных стадиях цирроза печени и ХПН. У низкомолекулярных гепаринов Т1/2 несколько больше.
Дозы и лабораторный контроль
Стандартные дозы гепарина обычно вводят путем в/в инфузии. Лечение венозных тромбозов и ТЭЛА начинают с введения 5000 ед гепарина струйно с последующей инфузией со скоростью 1200—1600 ед/ч. Контроль за лечением проводят, определяя АЧТВ. Терапевтической дозой гепарина считается доза, соответствующая концентрации гепарина в плазме 0,3—0,7 ед/мл, определенной по анти-Ха-активности (Hirsh et al., 1998а). Значения АЧТВ, соответствующие этим концентрациям гепарина, зависят от используемого оборудования и реагентов. Обычно считают достаточным удлинение АЧТВ в 1,7—2,5 раза, но некоторые наборы для определения АЧТВ завышают этот показатель, следствием чего становится назначение недостаточных доз гепарина. Введение недостаточных доз в первые сутки повышает риск повторных тромбозов и эмболий. АЧТВ определяют до начала лечения и затем каждые 6 ч; по этим данным проводится коррекция дозы препарата с помощью номограмм (Raschke et al., 1993). Когда подбор дозы завершен, контроль можно проводить 1 раз в сутки.
Профилактика свертывания крови в условиях искусственного кровообращения требует очень больших доз гепарина. АЧТВ при этом удлиняется настолько, что становится неинформативным, поэтому для контроля зале-чением применяют другие тесты (например, активированное время свертывания).
При необходимости длительного лечения антикоагулянтами в ситуации, когда варфарин противопоказан (например, при беременности), гепарин можно вводить п/к. При суточной дозе около 35 ООО ед (в 2—3 приема) АЧТВ, определяемое в промежутке между введениями, удлиняется обычно в 1,5 раза. После подбора дозы дальнейший контроль обычно не требуется.
Малые дозы гепарина профилактически назначают больным со склонностью к тромбозам глубоких вен и ТЭЛА. Рекомендуемый режим введения: по 5000 ед п/к 2—3 раза в сутки. Так как АЧТВ при этом не удлиняется, лабораторный контроль не нужен.
Низкомолекулярные гепарины (эноксапарин, далте-парин, ардепарин, надропарин, ревипарин, тинзапарин; в США сегодня применяют только первые три) весьма различны по составу. Сопоставимая анти-Ха-активность двух каких-либо препаратов еще не гарантирует их одинакового антитромботического действия. Низкомолекулярные гепарины вводят п/к 1—2 раза в сутки. Так как они почти не влияют на показатели свертываемости крови, лабораторный контроль обычно не нужен. В терминальной стадии ХПН Т,/2 низкомолекулярных гепаринов удлиняется, что требует контроля анти-Ха-активности. Особые указания по применению конкретных препаратов можно найти в прилагающихся к ним инструкциях.
Резистентность к гепарину
Дозы гепарина, необходимые для удлинения АЧТВ, зависят от содержания в плазме гепаринсвязываюших белков (например, богатого гистидином гликопротеида, витронектина и тромбоцитарного фактора 4), которые конкурентно ингибируют взаимодействие гепарина с антитромбином Ill. Иногда даже очень большие дозы гепарина (более 50 ООО ед/сут) не удлиняют АЧТВ. При этом концентрация гепарина в плазме, измеренная другими методами (например, с помощью титрования протамина сульфатом или по анти-Ха-активности), формально остается терапевтической. У некоторых из таких бальных АЧТВ исходно резко укорочено из-за высокой концентрации фактора VIII, и у них может не быть истинной резистентности к гепарину. У других больных (например, при массивной ТЭЛА) усилена элиминация препарата. Больные с наследственным дефицитом антитромбина III обычно хорошо отвечают на гепаринотерапию, так как концентрация антитромбина III у них составляет 40—60% нормы. Однако при приобретенном дефиците с концентрацией антитромбина III ниже 25% нормы (при циррозе печени, нефротическом синдроме, ЛВС-синдроме) эффекта может не быть даже при введении больших доз гепарина.
Побочные эффекты
Кровоточивость
Главные осложнения гепаринотерапии — геморрагические. Тяжелые кровотечения отмечались различными исследователями у 1— 33%больных; водном исследовании, включавшем 647 больных, было отмечено 3 смертельных исхода (Levine and Hirsh, 1986). В недавних исследованиях у больных ТЭЛА тяжелая кровоточивость отмечалась менее чем у 3% больных, получавших гепарин в/в (Levine et al., 1998). Сопоставимые данные получены при лечении ТЭЛА низкомолекулярными гепаринами. В целом риск кровоточивости возрастает с увеличением суточной дозы и АЧТВ, но корреляция между этими показателями слабая, и кровотечения могут отмечаться даже при терапевтических значениях АЧТВ. Обычно они вызваны сопутствующей патологией, например недавними операциями, травмами, язвенной болезнью или тромбоцитопатиями.
Антикоагулянтное действие гепарина прекращается через несколько часов после отмены препарата. При нетяжелой кровоточивости обычно нет необходимости в назначении антидота гепарина. При угрожающих жизни кровотечениях действие гепарина можно быстро остановить медленной инфузией протамина сульфата — смеси основных полипептидов, получаемой из спермы лосося. Протамин прочно связывается с гепарином, нейтрализуя его антикоагулянтное действие. Он связывается также с тромбоцитами, фибриногеном и другими белками плазмы и может сам по себе вызвать кровоточивость. Поэтому следует вводить лишь минимальную дозу протамина сульфата, обеспечивающую нейтрализацию гепарина. Эта доза обычно составляет 1 мг на каждые 100 ед оставшегося в организме гепарина, ее вводят в/в медленно (до 50 мгза 10 мин).
Протамина сульфат используют обычно для устранения действия гепарина после операций на сердце и сосудах. Анафилактические реакции возникают примерно у 1% больных сахарным диабетом, получавших протамин-содержащие инсулины (инсулин NPH или протамин-цинк-инсулин), но встречаются и у других больных. Реже наблюдается реакция в виде спазма легочных сосудов, правожелудочковой недостаточности, артериальной гипотонии и преходящей нейтропении.
Гепариновая тромбоцитопения
Этот диагноз ставят при уменьшении числа тромбоцитов ниже 150 000 мкл~’ или на 50% исходного уровня. Она возникает примерно у 3% больных после 5—10 сут лечения обычным гепарином (Warkentin, 1999). Низкомолекулярные гепарины реже вызывают тромбоцитопению. У трети больных с этим осложнением развиваются тяжелые тромбозы (иногда угрожающие жизни или требующие ампутации конечностей), которые могут предшествовать тромбоцитопении. Наиболее часты венозные тромбозы и ТЭЛА, но возможны и тромбозы периферических артерий, инфаркт миокарда, инсульт. Гепариновая тромбоцитопения может сопровождаться двусторонними некрозами надпочечников, кожными поражениями в местах инъекций и различными системными реакциями. Причиной этих осложнений считается выработка антител класса IgG к комплексу гепарина с фактором тромбоцитов 4 (реже с другими хемокинами). Эти комплексы связываются с Fcyl 1а-рецепторами тромбоцитов, вызывая агрегацию тромбоцитов, выброс еше большего количества фактора тромбоцитов 4 и образование тромбина. Кроме того, антитела могут повреждать сосудистую стенку, связываясь с комплексом фактора тромбоцитов 4 и гепарансул ьфата на поверхности эндотелия.
Появление тромбоцитопении или других упомянутых выше осложнений после 5 сут гепаринотерапии или позднее (независимо от дозы или пути введения) требует немедленной отмены препарата. У больных, получавших гепарин в предыдущие 3—4 мес, из-за оставшихся антител гепариновая тромбоцитопения может развиться быстрее. Диагноз можно подтвердить выявлением антител к комплексу гепарина с фактором тромбоцитов 4, а также исследованием гепарин-зависимой активации тромбоцитов. Так как после отмены препарата могут возникнуть тромбозы (Wallis et al., 1999; Warkentin, 1999), при гепариновой тромбоцитопении назначают другие антикоагулянты — лепирудин или данапароид (см. ниже). Низкомолекулярные гепарины в таких случаях применять нельзя, так как они зачастую перекрестно реагируют с антителами к обычному гепарину. Варфарин у больных париновой тромбоцитопенией может вызвать влажную гангрену (Warkentin et al., 1997) или множественные некрозы кожи (Warkentin et al., 1999), его можно назначать лишь после устранения тромбоцитопении и проведения лечения другими антикоагулянтами.
Другие осложнения
У больных, получающих гепарин в/в ри п/к, зачастую несколько повышается активность аминотрансфераз при нормальном уровне билирубина и нормальной активности щелочной фосфатазы. Длительное лечение терапевтическими дозами гепарина (более 20000 ед/сут на протяжении, например, 3—6 мес) иногда, хотя и редко, вызывает остеопороз с компрессионными переломами позвонков. Гепарин даже в небольших дозах ингибирует синтез альдостерона в надпочечниках и изредка вызывает гиперкалиемию. Аллергические реакции на гепарин (исключая тромбоцитопению) редки.
Читайте также
sportguardian.ru
ГЕПАРИН: инструкция, отзывы, аналоги, цена в аптеках
Гепарин – антикоагулянт (средство, тормозящее свертывание крови) прямого действия.
Гепарин является естественным противосвертываюшим фактором. Совместно с фибринолизином он входит в состав физиологической антисвертываюшей системы.
Относится к антикоагулянтам прямого действия, т. е. влияющим непосредственно на факторы свертывания, находящиеся в крови (XII, XI, X, IX, VII и II). Он блокирует также биосинтез (образование в организме сложных веществ из более простых) тромбина; уменьшает агрегацию (склеивание) тромбоцитов. Противосвертываюшее действие гепарина проявляется in vitro (в пробирке) и in vivo (в организме).
Гепарин обладает не только анткоагулируюшим действием, но угнетает активность гиалуронидазы (биологически активного вещества, участвующего в регуляции тканевой проницаемости), активирует в некоторой степени фибринолитические (растворяющие сгусток крови) свойства крови, улучшает коронарный (сердечный) кровоток.
Введение гепарина в организм сопровождается некоторым понижением содержания холестерина в бета-липопротеидах в сыворотке крови. Оказывает просветляющее действие на липемическую плазму. Гиполипидемическое (уменьшающие содержание липидов в крови) действие гепарина связано главным образом с повышением активности липопротеиновой липазы (фермента, расщепляющего жиры), участвующей в выведении хиломикронов из крови.
Из-за опасности кровотечений гепарин в качестве гипохолестеринемичсского (снижающего уровень холестерина в крови) средства, однако, не применяется.
Имеются данные о наличии у гепарина иммуносупрессивных (подавляющих защитные силы организма) свойств, что дает основание для возможного его использования при некоторых аутоиммунных заболеваниях (заболеваниях, в основе которых лежат аллергические реакции на собственные ткани или продукты жизнедеятельности организма) – гломерулонефрит (заболевание почек), гемолитическая анемия (снижение содержания гемоглобина в крови вследствие повышенного распада эритроцитов) и др., а также для предупреждения кризов отторжения при трансплантации (пересадке) почки у человека. Одним из механизмов иммуносупрсссивного действия является, по-видимому, подавление кооперативного взаимодействия (совместного действия) Т- и В-клеток (клеток крови, ответственных за иммунитет) (см. Препараты, корригирующие процессы иммунитета). Противосвертываюшее действие гепарина наступает при его введении в вену, мышцы и под кожу.
Гепарин действует быстро, но относительно кратковременно. При однократном введении в вену угнетение свертывания крови наступает почти сразу и продолжается 4-5 ч. При внутримышечном введении эффект наступает через 15-30 мин и продолжается до 6 ч, а при подкожном введении действие наступает через 40-60 мин и продолжается 8-12 ч. Наиболее постоянный гипокоагуляиионный (снижающий свертывание крови) эффект наблюдается при внутривенном введении. Однако для профилактических целей гепарин часто вводят внутримышечно и подкожно.
Показания к применению
Применяют для профилактики и терапии (лечения) различных тромбоэмболических (связанных с закупоркой сосудов сгустком крови) заболеваний и их осложнений: для предотвращения или ограничения (локализации) тромбообразования при остром инфаркте миокарда, при тромбозах (образовании сгустка крови в сосуде) и эмболиях (закупорке кровеносных сосудов) магистральных вен и артерий, сосудов мозга, глаза, при операциях на сердце и кровеносных сосудах, для поддержания жидкого состояния крови в аппаратах искусственного кровообращения и аппаратуре для гемодиализа (очистки крови), а также для предотвращения свертывания крови при лабораторных исследованиях.
Гепарин часто назначают в сочетании с ферментными фибринолитическими (растворяющими сгусток крови) препаратами (см. Фибринолизин, Стрептодеказа).
Способ применения
Дозы и способы применения гепарина должны быть индивидуализированы. При остром инфаркте миокарда рекомендуется уже в условиях оказания скорой помощи начинать (при отсутствии противопоказаний) с введения гепарина в вену в дозе 15 000-20 000 ЕД и продолжать в больничных условиях минимум S-6 дней внутримышечное введение гепарина по 40 000 ЕД в сутки (по 5000-10 000 ЕД каждые 4 ч). Вводят препарат под контролем свертываемости крови, следя за тем, чтобы время свертывания было в 2-2,5 раза выше нормы. За 1-2 дня до отмены гепарина суточную дозу постепенно понижают (на 5000-2500 ЕД при каждой инъекции без увеличения интервалов между введениями). С 3-4-го дня лечения присоединяют непрямые антикоагулянты (неодикумарин, фенилин и др. – см. стр. 456, 458). После отмены гепарина продолжают лечение непрямыми антикоагулянтами. Иногда переходят полностью на применение непрямых антикоагулянтов после 3-4 дней введения гепарина.
Гепарин может вводиться также в виде капельных инфузий. При массивном тромбозе легочной артерии обычно вводят капельно в дозе 40 000-60 000 ЕД в течение 4-6 ч с дальнейшим внутримышечным введением по 40 000 ЕД в сутки.
При периферических и особенно венозных тромбозах вводят сначала 20 000-30 000 ЕД гепарина внутривенно, затем по 60 000-80 000 ЕД в сутки (под контролем за коагулирующими свойствами крови). Применение гепарина обеспечивает улучшение состояния не только за счет непосредственного действия на тромб, но и вследствие развития коллатерального кровообращения, ограничения дальнейшего развития тромба и антиспастического (препятствующего развитию спазма /резкого сужения просвета сосудов/) действия.
Во всех случаях применения гепарина за 1-2-3 дня перед окончанием его введения начинают давать непрямые антикоагулянты, прием которых продолжают после отмены гепарина.
Для профилактики тромбоэмболии обычно вводят гепарин в подкожную жировую клетчатку в дозе 5000 ЕД 1-2 раза в сутки до и после проведенных оперативных вмешательств. Действие при однократном введении продолжается 12-14 ч.
При прямом переливании крови донору вводят в вену гепарин в дозе 7 500-10 000 ЕД.
Действие гепарина контролируют путем определения времени свертывания крови.
После его введения наблюдаются значительное замедление рекальиификации плазмы (показателя интенсивности процесса свертывания крови), понижение толерантности (устойчивости) к гепарину, удлинение тромбинового времени (показателя интенсивности процесса свертывания крови), резкое увеличение свободного гепарина (за счет введения антикоагулянта). Закономерных изменений протромбинового индекса (показателя интенсивности процесса свертывания крови) и содержания проконвертина и фибриногена (факторов свертываемости крови) под влиянием гепарина не отмечено.
Время свертывания крови определяют в течение первых 7 сут. лечения не реже 1 раза в 2 дня, далее 1 раз в 3 дня. В случае использования гепарина при оперативном лечении острой венозной или артериальной непроходимости (при тромбэктомии – удалении сгустка крови в сосуде) время свертываемости крови определяют в 1-й день послеоперационного периода не реже 2 раз, во 2-й и 3-й день – не реже 1 раза в сутки. При дробном введении гепарина пробы крови берут перед очередной инъекцией препарата.
Осторожность требуется при язвенных и опухолевых поражениях желудочно-кишечного тракта, кахексии (крайней степени истощения), высоком артериальном давлении (180/90 мм рт. ст.), в ближайшем послеродовом и послеоперационном периоде (в течение первых 3-8 сут.), за исключением случаев, когда гепаринотерапия необходима по жизненным показаниям.
Антагонистом (веществом с противоположным действием) гепарина является прогамина сульфат.
Побочные действия
Применяя гепарин, необходимо учитывать возможность развития геморрагии (кровотечений). Для предупреждения осложнений препарат следует вводить только в условиях стационара (больницы), при угрожающей гипокоагуляции (пониженной свертываемости крови) понизить дозу гепарина (без увеличения интервалов между инъекциями).
В случае индивидуальной непереносимости и появления аллергических реакций немедленно прекращают введение гепарина, назначают десенсибилизирующие (предупреждающие или тормозящие аллергические реакции) препараты, а при необходимости продолжения ан-тикоагулянтной терапии назначают непрямые антикоагулянты.
Противопоказания
Гепарин противопоказан при геморрагических диатезах (повышенной кровоточивости) и других заболеваниях, сопровождающихся замедлением свертывания крови, при повышенной проницаемости сосудов, кровотечениях любой локализации (за исключением геморрагии /кровотечения/ при эмболическом инфаркте легкого или почек), подостром бактериальном эндокардите /воспалении внутренних полостей сердца/, тяжелых нарушениях функции печени и почек, острых и хронических лейкозах (злокачественной опухоли, возникающей из кроветворных клеток и поражающей костный мозг /раке крови/), апластических и гипопластических анемиях (снижении содержания гемоглобина в крови, обусловленном угнетением кроветворной функции костного мозга), остро развившейся аневризме (выпячивании стенки) сердца, венозной гангрене.
Форма выпуска
В герметически закрытых флаконах по 5 мл с активностью 5000; 10 000 и 20 000 ЕД в 1 мл. Инъекционный раствор в ампулах по 0,1 мл. Гепарибене-Na-5000 шприц-тюбики. Один шприц-тюбик с 0,2 мл инъекционного раствора. Гепарибене-Nа-25 000 флаконы. Один прокалываемый флакон с 5 мл инъекционного раствора.
Условия хранения
В прохладном, защищенном от света месте.
Синонимы
Гепарина натриевая соль, Гепарин натрия, Гепарин-Рихтер, Тромбофоб, Ликвэмбин, Пуларин, Тромболиквин, Ветрен, Гепаринбене натрий, Тромбофот.
Основные параметры
| Название: | ГЕПАРИН |
| Код АТХ: | B01AB01 – Гепарин |
www.medcentre.com.ua
|
|
ГЕПАРИН (от греч. hepar- печень), протеогликан соединительной
ткани, обладающий антикоагулянтным и гиполипидемич. действием. В молекуле
нативного гепарина протяженные полисахаридные цепи присоединены к белковой цепи,
структура к-рой полностью не выяснена. В узле углевод-белковой связи содержится
фрагмент галактоза – галактоза-ксилоза, в к-ром ксилоза присоединена О-гликозидной
связью к группе ОН остатка L-серина или L-треонина. Полисахаридные цепи
молекулы гепарина (см. ф-лу) построены из чередующихся остатковD-глюкозамина
и уроновой к-ты с 1 -> 4-связями между ними. Большинство остатков глюкозамина
сульфатировано по аминогруппе и группе ОН в положении 6; небольшая часть
аминогрупп м. б. ацетилирована, а О-сульфатные группы могут отсутствовать
или занимать положение 3. Звенья уроновой к-ты представляют собой остаткиL-идуроновой
к-ты (гл. обр. в виде 2-сульфата) или эпимерные по С5 остатки-D-глюкуроновой
к-ты.
Биол. активность гепарина обусловлена его углеводными цепями; при получении мед. препарата гепарина осуществляется их отщепление от белковой части молекулы. Выделенный поли-сахарид довольно устойчив к кислотному гидролизу, однако в кислой среде легко десульфатируется (в первую очередь у атомов N) и теряет антикоагулянтные св-ва. Механизм действия гепарина обусловлен его способностью специфически связываться с антитромбином III, что резко повышает ингибирующее действие последнего по отношению к тромбину и др. протеазам, участвующим в свертывании крови. Для такого связывания необходима вполне определенная комбинация моносахаридных звеньев на достаточно протяженных участках полисахарида. Активному антикоагулянтному центру соответствует последовательность остатков 2-6, среди к-рых остатки 2, 3 и 4-минорные компоненты молекулы. Гепарин вырабатывается в тканях специализированными (т. наз. тучными) клетками.
Препарат гепарина получают из легких и печени рогатого скота в виде Na-соли (мол.
м. 17-20 тыс.)-аморфного продукта, легко р-римого в воде. Количеств. определение
гепарина основано на измерении биол. активности препарата или смещения
р-ров нек-рых красителей (напр., азура А) в присут. гепарина.
Препараты гепарина применяют в хирургии для предотвращения свертывания крови при длительных операциях с искусств. кровообращением, для предупреждения послеоперационных тромбозов, лечения инфарктов миокарда и атеросклероза и др.
Страница «ГЕПАРИН» подготовлена по материалам химической энциклопедии. Еще по теме: |
www.xumuk.ru
Гепарин (стр. 1 из 4)
-1-
СОВРЕМЕННЫЕ ДАННЫЕ О ГЕПАРИНЕ И
ЕГО БИОХИМИЧЕСКИЕ СВОЙСТВА
Гепарин – чрезвычайно важное соединение , синтезируемое в организме животных и человека . Это биологически активное вещество , антикоагулянт широкого спектра действия , регулятор многих биохимических и физиологических процессов , протекающих в животном организме , в настоящее время приковывает к себе пристальное внимание биологов , физиологов , фармакологов и клиницистов . Весьма эффективное использование гепарина в клинической практике выдвигает этот препарат в число перспективных фармакологических агентов .
ХИМИЧЕСКАЯ СТРУКТУРА ГЕПАРИНА
В исследованиях структуры гепарина большое значение имеет изучение типа гликозидной связи , определение содержания серы и сульфамидных карбоксиль- ных и других групп , количества ветвей в молекуле , а также выяснение природы уроновокислого компонента и т.д. Изучение молекулярной структуры гепарина очень важно , во-первых , с точки зрения сопоставления химической структуры этого вещества и его антикоагулянтных и других физиологических свойств , например , таких, как способность образовывать комплексы со многими веществами. Здесь можно указать на большую роль комплексных соединений гепарина с рядом тромбогенных белков плазмы крови и некоторыми биогенными аминами в регуляции жидкого состояния крови . Во-вторых , детальное выяснение структуры гепарина открывает определенные перспективы на пути исскуственного синтеза этогонезаменимого медикамента . По химическому строению гепарин представляет собой высокосульфированный мукополи-
сахарид , состоящий из последовательно чередующихся остатков -D-
– глюкороновой кислоты и 2-амино-2-дезокси – – D – глюкозы , соединенных связями 1—4 . Основная связь в гепарине — это 1—6 гекзоамин . Вольфром и соавторы (Wolfrom et al.,1966) обнаружили , что конфигурация 2-амино-2-дезокси–D – глюкороновокислотной связи представляет собой -D-связь. Наряду с этим отмечается существование и некоторой – конфигурации. В молекуле гепарина на тетрасахаратную единицу приходится по 5—6, 5 сульфатных групп . Остатки серной кислоты присоединены к ОН-группам глюкозамина . Высокое содержание сульфогрупп обусловливает значительный от рицательный заряд и , следовательно , большую подвижность в электрическом поле . Около 10% аминогрупп гепарина находится в свободном состоянии . Большинство же из них сульфатированны.
Сульфокислотные группы, вероятно, присоединены к аминогруппам с обра-
зованием аминосульфокислоты.
Молекулу гепарина принято рассматривать как протяженную, неразветв-
леннуюлинейную структуру. Так, электронно-микроскопические исследования
показали, что длина молекулы гепарина равна 160=40 А . Наряду с этим некоторые авторы высказываются в пользу разветвленной структуры.
По данным Вольфрома и Вэнга, гидроксильная группа с-6 2-амино-2-де-
зокси-D-глюкозной единицы гепарина сульфатированы. Видимо, в указанной выше единице гепарина существуют две сульфатные группы.
Причем остаток D-глюкуроновой кислоты не сультирован. Денишефски и
соавторы считают, что в гепарине сульфатировано по атому углерода в
положении 2 1/3 глюкуроновокислотного компонента и большая часть глю-
козаминов сульфатирована по атому углерода в положении 6.
До сих пор окончательно не решен вопрос о том,содержит ли гепарин
ацетильные группы. В то же время при исследовании бычьего, свиного и
китового гепарина установлено, что химическое строение и распреднление
остатков N-ацетилглюкозамина одинаково во всех препаратах.
Изучение структуры гепарина методом ЯМР показало,что гексуроновые
остатки находятся в молекуле в конформации С-1.
В содержании и составе гексуроновых кислот в гепаринах и гепарино-
вых фракциях различных млекопитающих обнаружены значительные раз-
личия. D-глюкуроновая кислота – основная уроновая кислота, входящая в состав гепарина. В гепарине также отмечено наличие кетуроновой и L-
идуроновой кислот и найдено, что их соотношение равно 2,6 1. Для ге-
парина характерно присутствие относительно большого количества ( до
1/3) L- идопираносилуровых остатков. Определение уровня уроновых кис-
лот ( идуроновой и D- глюкуроновой), входящих в различные гепарины и гепарансульфаты, показало, что содержание идуроновой кислоты не зависит от источника гепарина или гепарансульфатов и составляет соот-
ветственно 50-90 и 30-55 %. В исследуемых мукополисахаридах увеличивалась величина соотношения N- к О- сульфатам по мере возрастания в них уровня идуроновой кислоты. Величины отношений N-
сульфата к глюкозамину в гепарине и гепарансульфатах составляют 0,7-
1,0 и 0,3- 0,6. Отношение S- сульфата к глюкозамину изменяется в пределах 0,9- 1,5 для гепарина и 0,2- 0,8 для гепарансульфата. Видимо, это свидетельствует в пользу того, что гепарансульфаты представляют собой предшественники гепарина при его биосинтезе.
Изучение продуктов деградации гепарина под действием ферментов,
выделяемых из среды бактерий Flavobacterium heparinum, позволило сде-
лать вывод, что его молекула состоит из ряда последовательно распо-
ложенных стуктурных элементов, которые могут быть представлены как
1 – 4 связанные биозные остатки 2- сульфата 4-О-( a- L- идопираносульфу-
роновой кислоты) и 2-( дезокси- 2 – сульфамино-a-D- глюкопираносил-6-
сульфата). Повторяющиеся тетрасахаридные единицы, включающие в себя два уроновых и идуроновых остатка,-такова структура молекулы ге-
парина по представлениям Хелтинг и Линдал.
Данные о способе связей между повторяющимися единицами гепарина
весьма разноречивы. По ширине рентгеновских отражений установлено, что молекула гепарина содержит 10 тетрасахаридных поаторяющихся еди-
ниц.
При выделении гепарина из печени быка были получены три фракции, две из которых гомогенны. Биологическая активность этих фракций росла пропорционально молекулярному весу. Так, максимальная активность бы-
ла у фракции с молекулярным весом 16200, а минимальная – у фракции
7600. Установлено, что во фракциях с молекулярными весами 16200 и
15500 белковых примесей больше, чем во фракции 7600. Во всех фрак-
циях был обнаружен глюкозамин, галактозамин, гексуронат, сульфат, га-
лактоза и ксилоза в разных количествах. Некоторые незначительные отличия,наблюдаемые в структуре гепарина , видимо объясняются тем , что
исследуемые препараты получены из различных тканевых источников и мо-
гут быть обусловлены стабильными комплексами гепарина с белками , а
также наличием примесей . По разным данным , молекулярный вес гепарина
составляет от 4800 до 20000 . Метод низкого угла рассеяния Х-лучей дает
значение молекулярного веса в 12900 , что хорошо согласуется с результата-
ми , полученными с помощью равновесной седиментации и внутренней вяз-
кости : 12500 и 12600 соответственно . Методом гельфильтрации на сефа-
дексе G-200 показано, что молекулярные веса гепарина , полученного из
мукозы собаки и быка , а также из легких быка , равны 11000 – 12000 .
Как известно в ряду моносахарид ® олигосахарид ® полисахарид ИК-
– спектры поглощения упрощаются в связи с перекрыванием многих полос .
И хотя в настоящее время интерпретация ИК-спектров ВМС подобной слож-
ной структуры крайне затруднена и точный метод анализа еще не разработан,
полученный А.М.Ульяновым и др. ИК-спектр гепарина фирмы “СПОФА” (ЧССР)
позволил идентифицировать наличие максимумов поглощения , соответствую-
щих валентным колебаниям следующих групп : SO2N ,SO3 ,COO-, а также груп-
пировки С—С , ОН – и ряд других , присущих структуре молекулы гепарина .
В спектре поглощения гепарина в УФ-области области слабый максимум при
267 нм . возможно это обусловлено незначительными примесями белка или
аминокислот . Так , А.Ф.Алекперов (1972) пришел к выводу , что чистые образцы гепарина не дают полос поглощения в УФ-области спектра . Однако
при исследовании водных растворов ряда коммерческих препаратов гепарина
удалось выявить максимум поглощения при 258 нм . Автор отмечает ,что ука-
занную полосу поглощения дает фенилаланин . С помощью фотометрии и хроматографии на бумаге показано , что в препаратах гепарина в небольших
количествах присутствует белок : минимум в гепарине фирм “ПОЛЬФА” и
“РИХТЕР” (0,0026 и 0,0035 г) и максимум в гепарине фирмы “СПОФА “ и Бакин-
ского завода (0,0045 и 0,006 г ). Алекперов отмечает ,что полученные данные
могут служить критерием чистоты этих препаратов .
Седиментационный анализ гепарина дал коэффициент седиментации для
1% – ного водного раствора фирмы “СПОФА” 2,65 S.
Описаны различия в биологической активности между L- и b- гепаринами .
Это обусловлено тем , что у L-гепарина глюкозамин присоединен L-гликозид-
ной связью , b-гепарин имеет в своем составе галактозамин , соединенный
b-гликозидной связью . b-гепарин , имеющий в своем составе более низкое содержание серы и меньший молекулярный вес ,чем L- гепарин , обладает
и меньшей биологической активностью . По химической структуре он предста-
вляет собой хондроитинсерную кислоту с ацилированной аминогруппой и со-
держит галактозамин вместо глюкозамина .
ЗАВИСИМОСТЬ МЕЖДУ СТРУКТУРОЙ ГЕПАРИНА И
ЕГО БИОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ
Понятие биологической активности гепарина весьма широко , так как спектр
его физиологического действия очень велик . Сюда можно отнести анти -коагулянтную активность , антилипемическое , антимитотическое влияния,
регуляторное воздействие в отношении ряда ферментативных систем и т.д.
Однако наиболее изученным и имеющим большое практическое применение
является антикоагулянтный эффект гепарина . Поэтому говоря о биологическом действии гепарина, в основном говорят о его антикоагулянт-
ных свойствах .
Обнаружено , что антикоагулянтная активность гепарина связана с особенностями строения его молекулы . Так , антикоагулянтная активность зависит от содержания серы , степени сульфатированния , количества
mirznanii.com
Биосинтез гепарина
Биосинтез макромолекул гепарина включает, предположительно, построение полимерных аналогов с последующей их модификацией путем эпимеризации остатков D-глюкуроновой кислоты вL-идуроновую,N-деацетилирование с последующимN-сульфатированием остатковN-ацетил-D-глюкозамина, а также сульфатирование гидроксильных групп.
Физические свойства
Гепарин – аморфно-кристаллический полимер. Молекулярная масса препаратов гепарина варьирует в пределах (6 –25)∙103 Да, гепарансульфата – (5 – 12)∙103 Да. Коммерческие препараты низкомолекулярных гепаринов имеют молекулярную массу (4 – 6.5) 103Да.
Предполагается, что макромолекулы нативного гепарина (активная форма) связаны друг с другом посредством внутримолекулярных сульфатных мостиков типа:
|
Гепарин относится к классу сильных полиэлектролитов.Высокое содержание сульфогрупп придает макромолекуле гепарина значительный отрицательный заряд.
Как в виде кислоты, так и в виде калиевой или натриевой соли, гепарин хорошо растворим в воде; бариевая и свинцовая соли плохо растворимы в воде. Гепарин не растворим в органических растворителях.
Гепарин является оптически активным
соединением и характеризуется
положительной величиной удельного
оптического вращения. Например, водные
растворы гепарина имеют 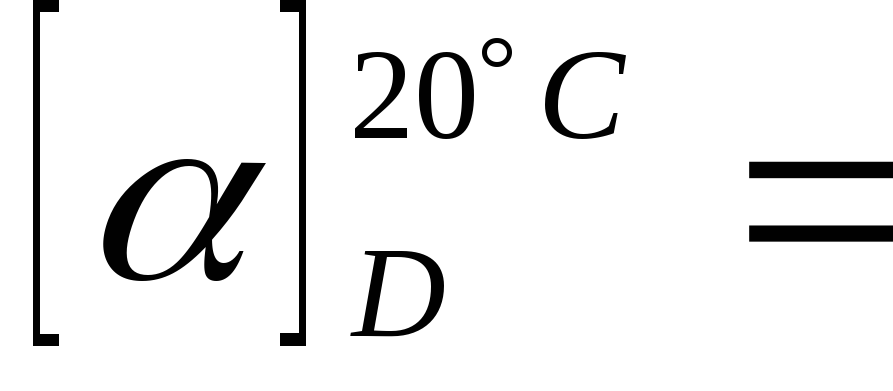 (+36)–(+70) град.
(+36)–(+70) град.
Химические свойства
Гепарин расщепляется специфическими ферментами, которые могут катализировать гидролиз отдельных гликозидных связей (гидролазы), элиминирование заместителя из положения С4остатка уроновой кислоты с образованием 4,5-ненасыщенной уроновой кислоты(лиазы)или десульфатирование в кислотной среде (в первую очередь у атомов N)(сульфатазы).
Методы определения гепарина основаны на колориметрировании продуктов его деструкции: уроновых кислот (с карбазолом, по Дише), гексозаминов (метод Эльсона – Моргана) или нейтральных сахаров (с антроновым реактивом) в составе гепарина после их осаждения с помощью N-ацетилпиридинийхлорида или выделения методами ионообменной хроматографии.
Биологическая активность
Основная функция гепарина в живом организме – участие в системе разрушения тромбов. Рассмотрим процесс тромбообразования.
Известно, что кровь содержит много веществ, участвующих в процессе ее коагуляции. Они называются факторамисвертывания крови. За исключением ионов кальция, эти вещества представляют собой белки. Индексация и некоторые характеристики факторов свертывания крови представлены в табл.1.
Таблица 1.
Факторы свертывания крови
Фактор | Название | Молекулярная масса | Концентрация в плазме крови (мг/100мл) | Активная фаза |
I | Фибриноген | 340000 | 200-400 | Фибрин |
II | Протромбин | 72000 | 10-15 | Тромбин (39000) |
III | Тканевый тромбопластин | − | − | − |
IV | Кальций | − | − | − |
V | Ас-глобулин | 290000 | 5-10 | Неизвестна |
VII | Проконвертин | 65000 | 0,4-0,7 | VIIа |
VIII | Кровоостанавливающий (антигемофильный) фактор | 400000 | 15-20 | Неизвестна |
IX | Кристмас-фактор | 55000 | 3-5 | IXа (45000) |
X | Фактор Стюарта | 55000 | 5-10 | Xа(44000) |
XI | РТА | 160000 | 0,5-0,9 | XIа(160000) |
XII | Фактор Хагемана | 90000 | 0,1-0,5 | XIIа(8800) |
XIII | Протрансглутаминаза | 330000 | 1-2 | XIIIа(320000) |
Примечание. Существование фактора VIсомнительно. В настоящее время порядковый номер этого фактора принято опускать.
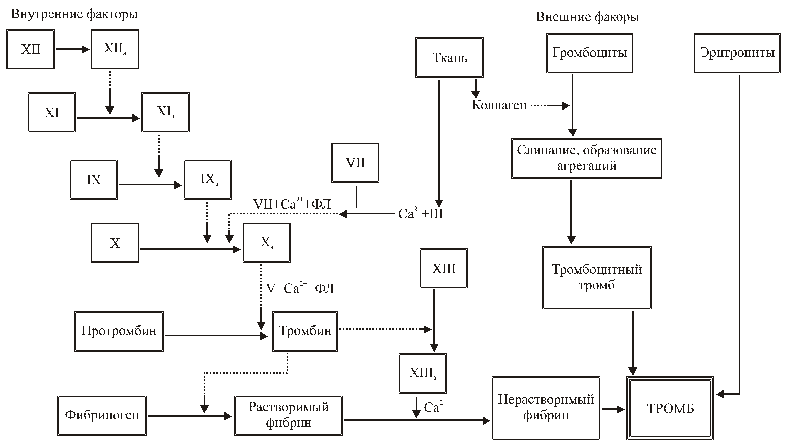
По современным воззрениям, процесс коагуляции крови инициируется и стимулируется системами внутренних ивнешних факторов. Первая система основана на активации фактораXIIраневым участком. Вторая состоит в том, что в результате освобождения тканевого тромбопластина инициируется активация факторов свертывания, протекающая в каскадной последовательности. Конечным ее итогом является формирование нерастворимойфибриновойсетки, которая обволакивает и «укутывает» тромбы из кровяных пластинок и эритроциты, т.е. происходиттромбообразование.Схема процесса представлена на рис.6.
|
Рис.6. Схема процесса тромбообразования: ФЛ – фосфолипиды; сплошные линии – превращение веществ; пунктирные – направление действия. |
Гепарин является естественным антикоагуляционнымфактором. Совместно с фибринолизином он входит в состав физиологической системы свертывания крови и тромбообразования. Относится к антикоагулянтам прямого действия, т. е. влияющим непосредственно на факторы свертывания, находящиеся в крови (XII, ХI, Х, IX, VII и II) и на реакции, описываемые схемами: протромбин→тромбин, фибриноген→фибрин (рис.6, 7).
Кроме того, гепарин активирует фибринолиз, снижает ретракцию кровяного сгустка, повышает отрицательный заряд сосудистой стенки, снижает проницаемость эндотелия сосудов, снижает активность гиалуронидазы, уменьшает степень гемолиза, стабилизирует мембраны эритроцитов, снижает артериальное давление, обладает сосудорасширяющим эффектом, повышает диурез и др.
|
Рис.7. Основные направления биологического действия гепарина. |
Гепарин блокирует также биосинтез тромбина и уменьшает агрегацию тромбоцитов. Причем, антикоагуляционное действие гепарина проявляется как in vitro, так и in vivo.
Гепарин обладает не только антикоагулирующим действием, но угнетает активность гиалуронидазы, активируетфибринолитическиесвойства крови, улучшаеткоронарный кровотоки др. На рис.8 на примере НМГ показана многофакторность проявлений биологической активности гепарина.
|
Рис.8. Многофакторность проявлений биологической активности НМГ. |
Введение гепарина в организм сопровождается понижением содержания холестерина и β-липопротеидов в сыворотке крови. Гепарин оказывает положительное действие на липемическую плазму. Обладает иммуносупрессивными свойствами.
studfile.net
ГЕПАРИН гель – инструкция по применению, состав, аналоги, форма выпуска, побочные эффекты, противопоказания
Действующее вещество
– гепарин натрия (heparin sodium)Состав и форма выпуска препарата
◊ Гель для наружного применения прозрачный или почти прозрачный, бесцветный или со слегка желтоватым оттенком, со специфическим запахом.
Вспомогательные вещества: троламин (триэтаноламин) – 1.8 г, карбомер 940 – 1.5 г, метилпарагидроксибензоат – 0.12 г, пропилгидроксибензоат – 0.03 г, вода очищенная – до 100 г.
30 г – тубы алюминиевые (1) – пачки картонные.
Фармакологическое действие
Антикоагулянт прямого действия, относится к группе среднемолекулярных гепаринов. В плазме крови активирует антитромбин III, ускоряя его противосвертывающее действие. Нарушает переход протромбина в тромбин, угнетает активность тромбина и активированного фактора X, в некоторой степени уменьшает агрегацию тромбоцитов.
Для нефракционированного стандартного гепарина соотношение антиагрегантной активности (антифактора Xa) и антикоагулянтной активности (АЧТВ) составляет 1:1.
Увеличивает почечный кровоток; повышает сопротивление сосудов мозга, уменьшает активность мозговой гиалуронидазы, активирует липопротеинлипазу и обладает гиполипидемическим действием. Снижает активность сурфактанта в легких, подавляет чрезмерный синтез альдостерона в коре надпочечников, связывает адреналин, модулирует реакцию яичников на гормональные стимулы, усиливает активность паратгормона. В результате взаимодействия с ферментами может увеличивать активность тирозингидроксилазы мозга, пепсиногена, ДНК-полимеразы и снижать активность миозиновой АТФазы, пируваткиназы, РНК-полимеразы, пепсина.
Имеются данные о наличии у гепарина иммунодепрессивной активности.
У больных с ИБС (в комбинации с АСК) снижает риск развития острых тромбозов коронарных артерий, инфаркта миокарда и внезапной смерти. Уменьшает частоту повторных инфарктов и летальность больных, перенесших инфаркт миокарда. В высоких дозах эффективен при тромбоэмболиях легочной артерии и венозном тромбозе, в малых – для профилактики венозных тромбоэмболий, в т.ч. после хирургических операций.
При в/в введении свертывание крови замедляется почти сразу, при в/м – через 15-30 мин, при п/к – через 20-60 мин, после ингаляции максимум эффекта – через сутки; продолжительность антикоагулянтного действия соответственно – 4-5, 6, 8 ч и 1-2 нед., терапевтический эффект – предотвращение тромбообразования – сохраняется значительно дольше. Дефицит антитромбина III в плазме или в месте тромбоза может снизить антитромботический эффект гепарина.
При наружном применении оказывает местное антитромботическое, антиэкссудативное, умеренное противовоспалительное действие. Блокирует образование тромбина, угнетает активность гиалуронидазы, активирует фибринолитические свойства крови. Проникающий через кожу гепарин уменьшает воспалительный процесс и оказывает антитромботическое действие, улучшает микроциркуляцию и активирует тканевой обмен, благодаря этому ускоряет процессы рассасывания гематом и тромбов и уменьшения отечности тканей.
Новости по теме
Фармакокинетика
После п/к введения Cmax активного вещества в плазме наблюдается через 3-4 ч. Гепарин плохо проникает через плаценту вследствие большого молекулярного веса. Не выделяется с грудным молоком.
T1/2 из плазмы составляет 30-60 мин.
Показания
Профилактика и терапия: тромбоз глубоких вен, тромбоэмболия легочной артерии (в т.ч. при заболеваниях периферических вен), тромбоз коронарных артерий, тромбофлебиты, нестабильная стенокардия, острый инфаркт миокарда, мерцательная аритмия (в т.ч. сопровождающаяся эмболией), ДВС-синдром, профилактика и терапия микротромбообразования и нарушения микроциркуляции, тромбоз почечных вен, гемолитикоуремический синдром, митральный порок сердца (профилактика тромбообразования), бактериальный эндокардит, гломерулонефрит, волчаночный нефрит.
Профилактика свертывания крови во время операций с использованием экстракорпоральных методов кровообращения, при проведении гемодиализа, гемосорбции, перитонеального диализа, цитафереза, форсированного диуреза, при промывании венозных катетеров.
Приготовление образцов несвертывающейся крови для лабораторных целей и переливания крови.
Противопоказания
Кровотечения, заболевания, сопровождающиеся нарушением процессов свертывания крови, подозрение на внутричерепное кровоизлияние, аневризма сосудов головного мозга, геморрагический инсульт, расслаивающая аневризма аорты, антифосфолипидный синдром, злокачественная артериальная гипертензия, подострый бактериальный эндокардит, эрозивно-язвенные поражения ЖКТ, тяжелые поражения паренхимы печени, цирроз печени с варикозным расширением вен пищевода, злокачественные новообразования в печени, шоковые состояния, недавно проведенные хирургические вмешательства на глазах, мозге, предстательной железе, печени и желчных путях, состояние после пункции спинного мозга, менструация, угрожающий выкидыш, роды (в т.ч. недавние), повышенная чувствительность к гепарину.
Не наносят на открытые раны, на слизистые оболочки, не применяют при язвенно-некротических процессах.
Дозировка
Индивидуальный, в зависимости от применяемой лекарственной формы, показаний, клинической ситуации и возраста пациента.
Побочные действия
Со стороны свертывающей системы крови: возможны кровотечения ЖКТ и мочевых путей, кровотечение в месте введения, в областях, подвергающихся давлению, из операционных ран, а также кровоизлияния в других органах, гематурия, тромбоцитопения.
Со стороны пищеварительной системы: тошнота, снижение аппетита, рвота, диарея, повышение активности печеночных трансаминаз.
Аллергические реакции: гиперемия кожи, лекарственная лихорадка, крапивница, ринит, кожный зуд и ощущение жара в подошвах, бронхоспазм, коллапс, анафилактический шок.
Со стороны свертывающей системы крови: тромбоцитопения (может быть тяжелой вплоть до летального исхода) с последующим развитием некроза кожи, артериального тромбоза, сопровождающегося развитием гангрены, инфаркта миокарда, инсульта.
Со стороны костно-мышечной системы: при длительном применении – остеопороз, спонтанные переломы, кальцификация мягких тканей.
Местные реакции: раздражение, боль, гиперемия, гематома и изъязвления в месте введения.
Прочие: преходящая алопеция, гипоальдостеронизм.
Лекарственное взаимодействие
Противосвертывающее действие гепарина усиливается при одновременном применении антикоагулянтов, антиагрегантов и НПВС.
Алкалоиды спорыньи, тироксин, тетрациклин, антигистаминные средства, а также никотин уменьшают действие гепарина.
Особые указания
C осторожностью применять у пациентов, страдающих поливалентной аллергией (в т.ч. при бронхиальной астме), при артериальной гипертензии, стоматологических манипуляциях, сахарном диабете, эндокардите, перикардите, при наличии внутриматочного контрацептива, при активном туберкулезе, лучевой терапии, печеночной недостаточности, хронической почечной недостаточности, у пациентов пожилого возраста (старше 60 лет, особенно женщины).
Не рекомендуется в/м введение гепарина из-за возможности развития гематомы, а также в/м введение других препаратов на фоне лечения гепарином.
С осторожностью применяют наружно при кровотечениях и состояниях повышенной кровоточивости, тромбоцитопении.
Во время лечения гепарином необходим контроль показателей свертывания крови.
Для разведения гепарина используют только физиологический раствор.
При развитии тяжелой тромбоцитопении (снижение количества тромбоцитов в 2 раза от первоначального числа или ниже 100 000/мкл) необходимо срочно прекратить применение гепарина.
Риск кровотечения может быть сведен до минимума при тщательной оценке противопоказаний, регулярном лабораторном контроле свертывания крови и адекватном дозировании.
Беременность и лактация
Применение при беременности возможно только по строгим показаниям, под тщательным медицинским контролем.
Возможно применение в период лактации (грудного вскармливания) по показаниям.
При нарушениях функции почек
C осторожностью применять у пациентов с хронической почечной недостаточностью.
При нарушениях функции печени
Противопоказан при тяжелых поражениях паренхимы печени, циррозе печени с варикозным расширением вен пищевода, злокачественных новообразованиях в печени, после недавно проведенных хирургических вмешательств на печени и желчных путях. C осторожностью применять при печеночной недостаточности.
Применение в пожилом возрасте
C осторожностью применять у пациентов пожилого возраста (старше 60 лет, особенно у женщин).
Описание препарата ГЕПАРИН основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
health.mail.ru