Дисплазия легких у недоношенных: Опасная и необратимая бронхолегочная дисплазия у детей: почему возникает, клинические рекомендации, последствия | Пульмонология.com – Бронхолёгочная дисплазия — Википедия
Бронхолегочная дисплазия у недоношенных детей: лечение, последствия, рекомендации
Малыши, появившиеся на свет раньше положенного срока, являются функционально незрелыми. Особенностью органов дыхания у недоношенных детей является высокое расположение диафрагмы, узость верхних дыхательных путей. На этом фоне часто возникают дыхательные расстройства. Выхаживание таких детей подразумевает организацию особого ухода – проведение искусственной вентиляции легких. Вследствие безалаберности или некомпетентности медицинского персонала при проведении ИВЛ развивается бронхолегочная дисплазия у недоношенных детей. Из-за возрастных особенностей прогноз заболевания серьезный – в течение года умирает каждый четвертый ребенок.
Что такое бронхолегочная дисплазия?
Акт дыхания безусловный: диафрагма вызывает движение мышц, создается легкий вакуум, и туда под давлением проникает воздух. Объем воздуха зависит от способности межреберных мышц растягиваться полностью. У малышей, родившихся преждевременно, мышцы полностью не растягиваются, из-за этого часть альвеол вообще не заполняется воздухом. Для того чтобы не возникло гипоксии, ребенка подключают к аппарату ИВЛ.
Бронхолегочная дисплазия у недоношенных детей – это патология дыхательной системы, возникшая в результате ИВЛ с большими концентрациями кислорода. По сути, заболевание не врожденное, возникает вследствие деонтологических ошибок медицинских сотрудников. По неутешительной статистике, практически у каждого второго недоношенного ребенка, которому необходима ИВЛ, возникает данная патология.
Почему возникает заболевание?
У недоношенных детей бронхолегочная дисплазия развивается на фоне нескольких этиологических факторов.
- Незрелость функционально-активных клеток легких. Незрелые легкие родившегося раньше срока ребенка отличаются дефицитом сурфактанта, который препятствует спаданию пузырьковых образований (буллы) легких и нужного для вывода слизи реснитчатым эпителием. Нормального уровня вещество достигает к 36 неделе. Наиболее сильный выброс сурфактанта происходит во время родов. У недоношенных детей недостаток вещества связан не только с преждевременным рождением, но и с угнетением его выработки из-за сопутствующей патологии.
- Баротравма легочной ткани. При проведении ИВС нарушается разница между давлением кислорода, подаваемого через аппарат, и давлением в легких ребенка, возникает множество мелких повреждения легочной ткани. Через разрывы пузырьки газа попадают в сосуды малого круга кровообращения, при этом пузырьки могут закупоривать сосуды, что приводит к кислородному голоданию.
- Токсическое воздействие больших доз кислорода. Высокие концентрации О₂ вызывают выраженную гиперемию, отек легкого с переходом в фибринозную пневмонию. Токсическое воздействие усиливают воспалительные процессы в легких.
- Присоединение вторичных инфекций. Чтобы улучшить респираторную функцию, ребенку вводят экзогенные сурфактанты. При наличии в организме инфекции иммунная система начинает отторгать экзогенное вещество, что ведет к разрушению дыхательной системы.
Помимо вышеперечисленного, причинами развития бронхолегочной дисплазии могут стать легочная гипертензия, дефицит в организме ретинола и альфа-токоферола, генетическая предрасположенность.
Классификация патологии: формы
Согласно общепринятой систематизации бронхолегочную дисплазию у недоношенных детей классифицируют по форме, степени тяжести и течению болезни. Различают две формы детской дисплазии:
- Классическая форма, также ее часто называют «жесткая». Развивается у детей, к которым не применялись препараты сурфактанта. Предупреждение респираторного дистресс-синдрома проводилось «жесткими» режимами ИВЛ. Рентгенологические исследования показывают вздутие легких, фиброз, пузырьки (буллы) в легочной ткани.
- Новая форма. Наблюдается у малышей, родившихся в гестационным возрасте 28-32 недели. Для профилактики РДС детям применялись препараты сурфактанта, и параллельно проводилась щадящая респираторная поддержка. Основные признаки: субтотальное затемнение легких без вздутия.
Стадии БЛД
В педиатрии и неонатологии выделяют 3 степени тяжести патологии:
- Легкая. Ребенок может дышать комнатным воздухом. Вздутие грудной клетки выражено слабо или вовсе не наблюдается, так же как и дистрофические процессы.
- Среднетяжелая. Потребность ребенка в кислороде составляет менее 30 %. При физической нагрузке или присоединении вторичной инфекции наблюдаются признаки бронхиальной обструкции. Рентгенологическое исследование выявляет вздутие грудной клетки, локальный пневмосклероз.
- Тяжелая. Ребенок нуждается в респираторной поддержке. Наблюдается выраженное учащенное поверхностное дыхание, бронхиальная обструкция. Снимки показывают выраженное вздутие грудной клетки, буллы, во многих участках легочной ткани наблюдаются воспалительно-дистрофические процессы.
Как проявляется заболевание
Специфических симптомов бронхолегочной дисплазии у недоношенных малышей нет. Общее состояние зависит от степени тяжести заболевания. Основными признаками являются:
- Дыхательная недостаточность.
- Грудная клетка по внешнему виду напоминает бочку.
- Учащенное поверхностное дыхание (тахипноэ).
- Кожа и слизистые приобретают синюшный оттенок (диффузный цианоз).
- При переводе ИВЛ на щадящий режим у ребенка развивается гиперкапния.
- На фоне ненормальной легочной вентиляции отхождение слизи затрудненно.
Также у детей отмечаются следующие патологические состояния:
- Наличие в тканях средостения буллов, поступающих из легких при их повреждении.
- Эмфизема легких.
- Снижение частоты сердечных сокращений (менее 60 уд./мин).
- Периодически возникает остановка дыхательных движений.
Диагностика БЛД
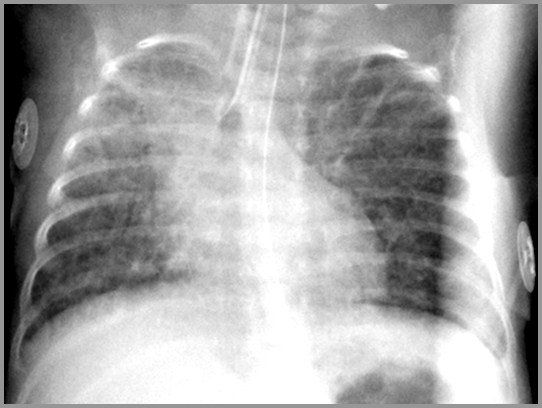
Для того чтобы избежать тяжелых последствий, лечение бронхолегочной дисплазии у недоношенных начинается одновременно с диагностикой. Процесс установления заключения включает сбор анамнеза, тщательный осмотр, лабораторные анализы, инструментальные исследования.
При сборе анамнестических данных неонатолог и педиатр выясняют, на каком сроке беременности появился на свет ребенок, наличие наследственных заболеваний, способствующих факторов.
При осмотре обращают внимание на деформацию грудной клетки, дыхательные движения, цвет кожи и слизистых и пр.
Лабораторные анализы:
- ОАК. При дисплазии в анализе наблюдается увеличение нейтрофилов, эозинофилов, ретикулоцитов, резкое снижение эритроцитов.
- Биохимия крови. Повышенное содержание креатин и мочевины, снижение концентрации калия, натрия, уменьшение рН.
- Давление кислорода в крови очень низкое – 40-55 мм. рт. ст.
Аппаратная диагностика:
- Рентгенография ОГК (обычно флюорография) дает наиболее исчерпывающую информацию о степени тяжести патологии.
- КТ и МРТ позволяют оценить структуру тканей легких.
Как проводят терапию
Лечение бронхолегочной дисплазии у недоношенных малышей проводится комплексно.
- Кислородная поддержка. При проведении ИВЛ ставят максимально щадящий режим. Основная задача кислородотерапии – поддержание показателей крови в необходимых пределах: рН – 7,25, сатурация – от 90 %, парциальное давление – 50-70 мм. рт. ст.
- Питание ребенка. У детей с дисплазией высокая метаболическая потребность. Ребенка в основном кормят через соску 7-8 раз в сутки. Рекомендованная калорийность 110-150 калорий на килограмм веса в день. Ребенку должен быть обеспечен максимальный покой, температура должна быть постоянной на уровне 36,5 °С.
Медикаментозное лечение. Для лечения детской бронхолегочной дисплазии используют различные препараты:
- Метилксалтины – препараты, обладающие сердечно-сосудистыми эффектами, способствуют экстубации и снижению формирования БДЛ. Детям назначают «Теофиллин», «Кофеин».
- Глюкокортикостероиды обладают противовоспалительным противоаллергическим действием. Наиболее эффективным считается применение препарата «Дексаметазон».
- Ингаляционные кортикостероиды («Бедусонид», «Фенотерол»).
- Растворы витаминов А и Е.
- Антибактериальная терапия назначается индивидуально, в зависимости от тяжести состояния и возбудителя инфекционного заболевания.
Клинические рекомендации

Длительность госпитализации определяется тяжестью течения патологии, наличием осложнений и может продолжаться несколько месяцев. При адекватной терапии и видимой ее эффективности ребенка выписывают домой.
Клиническими рекомендациями бронхолегочной дисплазии у недоношенных детей являются:
- Дома у детей ведется постоянный контроль прибавок роста, массы тела, психомоторного развития.
- Ребенку в обязательном порядке проводят противогриппозную и противопневмококковую вакцинацию. Причем вакцину вводят в течение 48-72 часов после выписки.
- Кислородозависимые дети нуждаются в домашней оксигенотерапии.
- Малыши с тяжелым БДЛ, имеющие осложнения, должны наблюдаться у пульмонолога.
- Дети до трех лет обязаны проходить физиопроцедуры, лечебную физкультуру.
- Плановый осмотр педиатра и пульмонолога должен осуществляться 2-3 раза в год.
Последствия бронхолегочной дисплазии

Патология тяжелая и часто наблюдаются осложнения. Некоторые из них могут возникнуть только через несколько лет.
Последствия бронхолегочная дисплазия у недоношенных:
- Рецидивирующие бронхиты.
- Пневмония.
- Железодефицитная анемия.
- Недостаток витаминов А, Е, D.
- Гастроэзофагеальная рефлюксная болезнь.
- Гипертрофия и дилатация правого предсердия.
- Коллапс легкого.
- Бронхиальная астма.
- Развитие стойкого повышенного артериального давления.
- Серьезная задержка в развитии малыша.
Прогноз
Прогноз, к сожалению, неутешительный. Смертность в первые три месяца достигает 20-35% и 25 % за год. У выживших функциональность легких с возрастом восстанавливается, но структурные изменения все же сохраняются в половине случаев.
В дошкольном возрасте у детей наблюдается повышенная сопротивляемость бронхиального дерева. Адекватная терапия позволяет добиться практически полного выздоровления.
Профилактика БЛД

Профилактические рекомендации во избежание бронхолегочной дисплазии подразумевают следующее:
- Комплекс мероприятий, проводимых для обеспечения нормального дородового развития организма.
- Проведение ИВЛ в щадящих режимах.
- Применение препаратов сурфактанта.
- Витаминотерапия.
- Профилактика преждевременных родов. При угрозе рождения ребенка раньше положенного срока матери показана госпитализация с последующей глюкокортикостероидной терапией.
Бронхолегочная дисплазия – причины, симптомы, диагностика и лечение
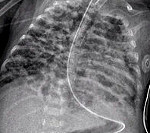
Бронхолегочная дисплазия (БЛД) – это хроническое заболевание дыхательной системы у новорожденных, которое возникает при проведении ИВЛ с использованием высоких концентраций кислорода на фоне респираторных нарушений. Основные проявления – синдром дыхательной недостаточности (ДН) и бронхиальной обструкции, деформация грудной клетки. Основа диагностики бронхолегочной дисплазии – рентгенография ОГК. Лечение при данной патологии включает в себя неспецифические терапевтические меры: рациональное питание и режим, адекватную респираторную поддержку, симптоматические медикаментозные препараты.
Общие сведения
Бронхолегочная дисплазия (БЛД) – это гетерогенная патология периода новорожденности, которая возникает при проведении ИВЛ с высокими концентрациями кислорода, сопровождается дыхательной недостаточностью, бронхообструктивным синдромом и гипоксемией. Впервые ввел этот термин, а также описал его рентгенологическую картину по стадиям американский педиатр и радиолог Нортвей в 1967 году. По своей сути БЛД является не врожденным, а ятрогенным заболеванием, что противоречит его названию, однако другого термина на данный момент не предложено. Она возникает у 16-40% новорожденных с массой тела менее 1500 г, которым необходима ИВЛ по поводу РДС. Общий показатель летальности при бронхолегочной дисплазии в течение первых 12 месяцев жизни составляет 10-25%.
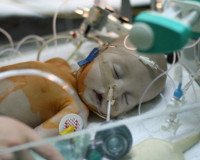
Бронхолегочная дисплазия
Причины бронхолегочной дисплазии
Бронхолегочная дисплазия – это полиэтиологическое заболевание, которое формируется на фоне воздействия нескольких потенциальных этиологических факторов. К таковым относятся баротравма при нерациональной ИВЛ, морфологическая незрелость паренхимы легкого, системы сурфактанта и антиоксидантной системы, токсическое воздействие высоких концентраций кислорода, инфекции (микоплазмы, пневмоцисты, уреаплазмы, хламидии, ЦМВ), отек легких различного генеза, легочная гипертензия, ГЭРХ, гиповитаминозы А и Е, генетическая склонность.
Морфологически бронхолегочная дисплазия проходит четыре стадии. На I стадии развивается классический РДС. На II стадии происходит деструкция эпителия альвеол и его последующая регенерация, формируются персистирующие гиалиновые мембраны. Также возникает отек интерстиция, некроз бронхиол. III стадия характеризуется образованием ограниченных эмфизематозных изменений, ателектазов и фиброза. На IV стадии в альвеолах накапливаются ретикулярные, эластические и коллагеновые волокна – окончательно формируются ателектазы, эмфизема, участки фиброза легкого.
Классификация бронхолегочной дисплазии
Согласно общепринятой классификации, существует две основные формы бронхолегочной дисплазии:
- Классическая или «тяжелая» форма.
- Новая или «легкая» форма бронхолегочной дисплазии. Наблюдается у детей, родившихся после 32 недели беременности, которым с целью профилактики вводился сурфактант. Рентгенологически проявляется гомогенным затемнением легких и отсутствием участков вздутия.
Также в отечественной педиатрии и неонатологии клинически выделяют три степени тяжести бронхолегочной дисплазии:
- Легкая БЛД. В состоянии покоя ЧД в переделах физиологической нормы (до 40 в мин.), реже отмечается незначительное тахипноэ при нагрузке (до 60 в мин.). Возможны признаки бронхиальной обструкции при респираторных инфекциях, умеренная эмфизема. Потребности в кислородной поддержке при гестационном возрасте старше 36 недель не возникает.
- Среднетяжелая бронхолегочная дисплазия. На фоне плача, кормления, беспокойства развивается тахипноэ (60-80 в мин.). В состоянии покоя могут прослушиваться сухие или мелкопузырчатые хрипы. Часто наблюдается бронхиальная обструкция на фоне инфекционных заболеваний. Рентгенологически отмечается эмфизема, пневмосклероз. Существует потребность в респираторной поддержке <30% кислородом.
- Тяжелая бронхолегочная дисплазия. Выраженное тахипноэ (80 в мин. и более) в состоянии покоя. Ярко выраженная бронхиальная обструкция, аускультативные признаки недостаточности дыхательной системы. Зачастую формируется легочное сердце, возникает задержка физического развития. Рентгенологически выявляется эмфизема, бедность легочного рисунка, пневмосклероз, множество ателектазов и перибронхиальных изменений. Требуется респираторная поддержка с использованием концентрации кислорода >30%.
Симптомы бронхолегочной дисплазии
Специфических проявлений бронхолегочной дисплазии не существует. Заболевание характеризуется выраженной дыхательной недостаточностью на фоне высоких концентраций кислорода при ИВЛ. Общее состояние зависит от степени тяжести, однако, в большинстве случаев оно среднетяжелое или тяжелое. Грудная клетка приобретает характерный для эмфизематозных заболеваний вид: «бочкообразная форма» и горизонтальный ход ребер, увеличение размера в переднезаднем направлении, выпячивание межреберных промежутков и их втяжение при выдохе-вдохе. Также при бронхолегочной дисплазии возникает тахипноэ до 90-100 в 1 мин, наблюдается акро- или диффузный цианоз. При попытках перевести ИВЛ на более щадящий режим развивается острая недостаточность дыхательной системы, которая сопровождается выраженной гиперкапнией и гипоксемией. При прекращении респираторной поддержки на фоне спонтанного дыхания сохраняются признаки бронхиальной обструкции.
У детей с бронхолегочной дисплазией также отмечается пневмомедиастинум, эмфизема и пневмоторакс, брадикардия и приступы апноэ, рецидивирующие бронхиты и пневмонии, дефицитные состояния (дефицит витаминов D, А, Е, анемия), частая рвота, гастроэзофагеальный рефлюкс и аспирация пищевых масс. Нередко наблюдаются неврологические расстройства, поражения сетчатки. К основным осложнениям бронхолегочной дисплазии относятся правожелудочковая недостаточность и «легочное сердце», ограниченные или долевые ателектазы легких, рецидивирующие бронхиты, бронхиолиты и воспаления легких, хроническая дыхательная недостаточность, атопическая бронхиальная астма, артериальная гипертензия, анемия, задержка психофизического развития.
Диагностика бронхолегочной дисплазии
Диагностика бронхолегочной дисплазии включает в себя сбор анамнестических данных, объективный осмотр, лабораторные и инструментальные методы исследования. При сборе анамнеза неонатолог или педиатр обращает внимание на сроки, в которые произошли роды, наличие возможных этиологических и способствующих факторов. При объективном обследовании выявляются характерные клинические проявления бронхолегочной дисплазии: дыхательная недостаточность, деформация грудной клетки и т. д. В ОАК определяется нормохромная гипорегенераторная анемия, увеличение числа нейтрофилов и эозинофилов. В биохимическом анализе крови могут быть обнаружены гипокалиемия, гипонатриемия, гипохлоремия, уменьшение рН, повышение креатинина и мочевины. Одним из характерных признаков бронхолегочной дисплазии является низкое парциальное давление кислорода в крови (РаО2) – 40-55 мм.рт.ст.
Среди инструментальных методов диагностики при бронхолегочной дисплазии наиболее информативными считаются рентгенография ОГК, компьютерная и магнитно-резонансная томография. Чаще всего используется именно рентгенологический метод исследования, который позволяет выявить характерные признаки БЛД, определить степень тяжести и стадию морфологических изменений легких. КТ и МРТ дают возможность выявить аналогичные проявления и детально оценить структуру паренхимы легких. Однако они применяются не так часто в связи с отсутствием выраженных преимуществ перед рентгенографией и высокой стоимостью.
Лечение бронхолегочной дисплазии
Специфического лечения бронхолегочной дисплазии не существует. Основные терапевтические средства при данном заболевании включают в себя кислородную поддержку, рациональное питание, режим, симптоматические медикаментозные препараты. Несмотря на то, что ИВЛ – это основная причина развития БЛД, она является одним из наиболее важных аспектов лечения. Ее основная цель – поддержание показателей крови в допустимых пределах: рН крови на уровне 7,25, сатурация – 90% и более, парциальное давление крови – 55-70 мм.рт.ст.
Также важную роль в лечении бронхолегочной дисплазии играет питание ребенка. У больных детей имеется высокая метаболическая потребность на фоне необходимости адекватного роста легких. В таких условиях наиболее благоприятной считается суточная калорийность в пределах 115-150 ккал/кг/день. Суточный режим ребенка должен включать максимальный покой, многоразовое кормление, поддержание температуры тела на уровне 36,5 °C. Среди медикаментозных препаратов, которые могут применяться при БЛД, наиболее часто используются бронхолитики, муколитические и диуретические средства, глюкокортикостероиды, β2-агонисты, антибиотики и витамины А, Е.
Прогноз и профилактика бронхолегочной дисплазии
Прогноз при бронхолегочной дисплазии всегда серьезный. Показатель смертности в первые 3 месяца жизни колеблется в пределах 15-35%, за 12 месяцев – 10-25%. У выживших с возрастом происходит восстановление функции легких, однако морфологические изменения сохраняются в 50-75% случаев. У таких детей уже в дошкольном возрасте отмечается повышенная резистентность бронхиального дерева, после 7 лет появляется склонность к гиперреактивности. Адекватно проведенное лечение существенно снижает уровень летальности в первые 1-2 года, позволяет добиться клинического выздоровления до четырехлетнего возраста.
Профилактика бронхолегочной дисплазии подразумевает антенатальную охрану плода, предотвращение преждевременных родов, использование щадящих режимов ИВЛ и сведение длительности ее проведения к минимуму, витаминотерапию, использование препаратов сурфактанта. При угрозе преждевременного рождения ребенка показано введение матери глюкокортикостероидов с целью профилактики СДР и БЛД в дальнейшем.
Бронхолегочная дисплазия > Клинические рекомендации РФ (Россия) > MedElement
Жалобы и анамнез
Классическая форма БЛД развивается обычно у пациентов в результате тяжелого поражения легких, требующего ИВЛ с «жесткими режимами» и высокими концентрациями кислорода. Кроме РДС, такое поражение легких у недоношенных детей может явиться результатом врожденной пневмонии/сепсиса, вызванного стрептококком группы В (Streptococcus agalactiae).
В отличие от детей с классической БЛД, которым требуется многодневная ИВЛ с высоким содержанием кислорода, пациенты с новой БЛД нередко в первые дни и недели жизни имеют минимальную потребность в кислороде. И только после нескольких дней или недель («медовый месяц») у этих детей начинается прогрессирующее ухудшение функции легких, которая характеризуется увеличением потребности в вентиляции и кислорода и признаков текущей дыхательной недостаточности. Следовательно, особенностью клинической картины новой БЛД также является позднее, отсроченное развитие кислорозависимости [5]. Длительная кислородозависимость у таких пациентов часто обусловлена функционирующим ОАП или инфекцией [6].
Физикальный осмотр
Первым признаком возможного формирования БЛД является затяжное течение РДС. Клиническая картина БЛД представлена симптоматикой хронической дыхательной недостаточности у недоношенных новорожденных детей, зависимых от высоких концентраций кислорода во вдыхаемом воздухе и ИВЛ в течение более или менее продолжительного времени. Стойкая дыхательная недостаточность развивается после первичного улучшения состояния на фоне ИВЛ. При легком течении наблюдается невозможность снижения концентрации кислорода и смягчения параметров ИВЛ в течение 1-2 недель, удлинение периода выздоровления после дыхательной недостаточности; в тяжелых – на фоне ИВЛ сохраняется гипоксемия, гиперкапния, «снять» ребенка с ИВЛ не удается в течение нескольких месяцев. Реинтубации являются фактором риска тяжелого течения заболевания (1С) [2].
При объективном исследовании обычно выявляют бледные кожные покровы, с цианотичным оттенком. На фоне терапии глюкокортикостероидами возможно развитие кушингоидного синдрома. Грудная клетка эмфизематозно вздута, характерны тахипноэ до 80-100 в минуту, одышка с западением межреберных промежутков и втяжением грудины, симптом «качелей» (западение грудины при вдохе в сочетании с усиленным участием в акте дыхания мышц брюшного пресса), затрудненный удлиненный выдох. Перкуссия грудной клетки не проводится детям с ОНМТ и ЭНМТ в связи с риском интракраниальных кровоизлияний. Для аускультативной картины БЛД типичны ослабление дыхания и крепитация, отражающие развитие интерстициального отека, и появление свистящих, мелкопузырчатых хрипов при отсутствии сердечной недостаточности. К проявлениям бронхообструктивного синдрома (БОС) у недоношенных детей с БЛД относятся также эпизоды падения сатурации кислорода, клинически сопровождающиеся свистящими хрипами, ослабленным дыханием, затруднением вдоха и выдоха, ригидностью грудной клетки, падением растяжимости и увеличением резистентности дыхательных путей. У части пациентов с БЛД возможен стридор, при его развитии требуется исключить постинтубационное повреждение гортани. У ребенка, находящегося на ИВЛ, трактовка физикальных изменений в легких затруднена.
• Рекомендуется проведение клинического анализа крови [1,2].
(Сила рекомендации 1; уровень доказательств С).
Комментарии: у большинства больных с БЛД выявляет анемию, нейтрофилез и эозинофилию.
• Рекомендовано исследование кислотно-основного состояния и мониторинг оксигенации в спокойном состоянии [1,2].
(Сила рекомендации 1; уровень доказательств С).
Комментарии: у кислородозависимых младенцев с БЛД возможны эпизоды десатурации и гипоксии при стрессе, энтеральном кормлении, чрезмерном возбуждении, бронхоспазме. Идеальным для мониторинга оксигенации является транскутанная пульсоксиметрия. Дети с высокой легочной гипертензией и длительно кислородозависимые нуждаются в пролонгированной пульсоксиметрии.
• Рекомендуется контроль системного артериального давления [1,2].
(Сила рекомендации 1; уровень доказательств С).
Комментарии: рекомендуется как на стационарном этапе, так и при каждом амбулаторном визите пациента в связи с возможностью такого осложнения БЛД как системная артериальная гипертензия.
Инструментальная диагностика
• Рекомендовано проведение рентгенографии грудной клетки [1,2].
(Сила рекомендации 1; уровень доказательств С).
Комментарии: рентгенография грудной клетки необходима для выявления и оценки выраженности вздутия легочной ткани, фиброзных, интерстициальных и кистозных изменений.
• Рекомендовано проведение высокоразрешающей компьютерной томографии (КТ) [1,2].
(Сила рекомендации 1; уровень доказательств С).
Комментарии: КТ необходима в следующих случаях:
1) при проведении дифференциальной диагностики с другими бронхолегочными заболеваниями, например, ИЗЛ;
2) при повторных пневмотораксах;
3) при задержке клинического выздоровления и персистенции респираторных симптомов, не объяснимых тяжестью БЛД;
4) при необходимости верификации хронического заболевания легких в исходе БЛД, например, при подозрении на развитие облитерирующего бронхиолита;
5) для исключения врожденных пороков развития легких. Для объективизации данных ВРКТ-исследований в настоящее время применяется отечественная рентгенологическая шкала балльной оценки степени тяжести БЛД (табл.4) [7].
Таблица 4 – Рентгенологическая шкала оценки степени тяжести БЛД у детей
| Признаки | Баллы | ||
| 0-1 | 2 | 3 | |
Умеренное повышение | Повышение, неравномерность | Резкое повышение, неравномерность, буллы | |
Архитектоника лёгочного рисунка по долям лёгких | Обеднён, не деформирован | Обеднён, умеренно деформирован, интерстиций подчёркнут | Резко обеднён на периферии, деформирован |
Перибронхиальные изменения лёгочной ткани | Незначительные | Умеренные, просветы бронхов сужены | Выраженные, просветы деформированы |
Распространённость пневмофиброза | Отсутствует | Невыраженный, единичные спайки | Грубый фиброз с признаками объёмного уменьшения сегментов, множественные транспульмональные тяжи |
Сердечно – сосудистые изменения: лёгочная гипертензия, кардиомегалии | Отсутствуют | Умеренная лёгочная гипертензия, может быть кардиомегалия | Выраженная кардиомегалия или гипертрофия правого желудочка, лёгочная гипертензия |
Результат оценки степени тяжести БЛД | Лёгкая 1 – 5 баллов | Среднетяжёлая 6 – 10 баллов | Тяжёлая 11 – 15 баллов |
Уменьшение суммы баллов происходит, преимущественно, за счет снижения гиперинфляции и распространённости фиброзных проявлений. Вместе с тем, рентгенологические изменения при проведении ВРКТ в той или иной степени остаются у всех больных с БЛД до 2-х-летнего возраста и далее, независимо от степени тяжести заболевания.
• Рекомендовано проведение электрокардиографии (ЭКГ) [1,2,].
(Сила рекомендации 1; уровень доказательств С).
Комментарии: ЭКГ позволяет выявить признаки перегрузки, гипертрофии правых отделов сердца, при осложнении БЛД легочной гипертензией, однако, имеет недостаточные чувствительность и положительную прогностическую ценность для выявления гипертрофии ПЖ как маркера ЛГ, и поэтому не должна использоваться в качестве метода скрининга развития ЛГ (2C).
• Рекомендовано проведение допплер-эхокардиографии с определением кровотока через открытый артериальный проток (ОАП) и для диагностики ЛГ [1,2].
(Сила рекомендации 2; уровень доказательств С).
Комментарии: для скрининга ЛГ необходимо проведение ЭхоКГ каждому пациенту со среднетяжелой/тяжелой БЛД в 36 нед. постконцептуального возраста, то есть нуждающемуся в этом возрасте в кислородотерапии [8,9].
• Рекомендовано проведение флоуметрии спокойного дыхания для оценки параметров функции внешнего дыхания у больных с БЛД [1,10].
(Сила рекомендации 2; уровень доказательств С).
Комментарии: Регистрация респираторного паттерна в состоянии естественного сна ребенка (без необходимости сотрудничества пациента с исследователем) доступна для детей с БЛД в любом возрасте в ремиссии или обострении бронхолегочного процесса, что может быть использовано для коррекции бронхолитической терапии, а также в прогностических целях [10].
Иная диагностика
• Рекомендована полисомнография (ПСГ) [1,11].
(Сила рекомендации 2; уровень доказательств С).
Комментарии: Полное ПСГ-исследование желательно при появлениях апноэ, симптомов обструкции верхних дыхательных путей и брадикардии [11].
• Рекомендована катетеризация сердца и тест на вазореактивность в случае осложнения заболевания легочной гипертензией с угрозой формирования легочного сердца. [1,2,9].
(Сила рекомендации 2; уровень доказательств С).
Комментарии: Критерием наличия ЛГ при БЛД, по данным катетеризации правых отделов сердца, является повышение среднего давления в легочной артерии (СрДЛА) выше 25 мм рт. ст. при индексе резистентности легочных сосудов >3.0 единиц Вуда (WU)·м2 для ситуации двухжелудочкового кровообращения [9].
Последствия бронхолегочной дисплазии у детей
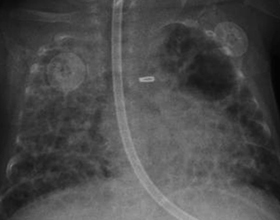
Лёгкие – важный орган в человеческом организме. Малейший сбой в их функционировании может привести к тяжёлым последствиям для здоровья. А если эти патологические изменения происходят у детей, то тяжесть последствий этих заболеваний усиливается в несколько раз. Бронхолёгочная дисплазия – это одна из самых тяжёлых лёгочных патологий, которая наблюдается в раннем детском возрасте.
Что такое бронхолёгочная дисплазия
Бронхолёгочная дисплазия – это хроническое заболевание лёгких, которое развивается у недоношенных детей. Это происходит из-за искусственной вентиляции лёгких, которую проводят ребёнку, не умеющему самостоятельно дышать.
Причины:
- Длительное ИВЛ (искусственная вентиляция лёгких).
- Внутриутробная инфекция.
- Пороки развития сердца и лёгких.
- Лёгочная гипертензия.
- Отёк лёгких.
- Недоразвитие лёгких.
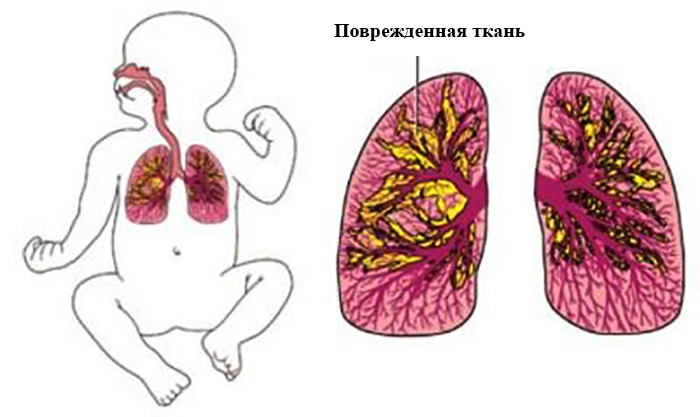
Симптомы:
- Зависимость от вводимого кислорода. При снижении концентрации происходит развитие дыхательной недостаточности.
- Отдышка с хрипами.
- Бледность и цианоз кожных покровов.
- Остановка дыхания.
- Снижение частоты сердечных сокращений.
- Падение артериального давления.
- Присоединение инфекционных осложнений.
Принципы лечения основывается на применении кислорода и медикаментозных средств, которые включают в себя приём диуретиков, антибиотиков, глюкокортикостероидов, бронхолитиков и препаратов, снимающих интоксикацию организма.
Последствия бронхолёгочной дисплазии
Прогноз при бронхолёгочной дисплазии может быть очень серьёзным. Риск развития осложнений для детского организма возрастает исходя из гестационного возраста ребёнка, тяжести проявлений патологии:
- Хроническая дыхательная недостаточность. В связи с длительным нарушением функции лёгких, может развиться хроническая дыхательная недостаточность.
- Бронхит. Проявляется воспалением бронхов. Эта патология может сопровождать детей с бронходисплазией на протяжении всей жизни. Является самым частым осложнением.
- Бронхиолит. Представляет собой острую инфекцию вирусного происхождения, которая вызывается респираторно-инициальным вирусом и поражает нижние дыхательные пути.
- Пневмония. Характеризуется воспалением лёгочной ткани и часто встречается у недоношенных детей, вследствие незрелости лёгких.
- Круп. Существует теория о предрасположенности к развитию ложного крупа в будущем, у детей с дисплазией. Ложный круп является опасным состоянием, которое характеризуется отёком голосовой щели (у детей довольно узкая), происходит приступ удушья, он требует быстрого медицинского вмешательства. Перед приступом наблюдается охриплость голоса. Такие приступы могут сопровождать ребёнка вплоть до достижения им 6-летнего возраста.
- Бронхиальная астма. У детей, перенёсших дисплазию в раннем возрасте чаще, чем у других детей развиваются приступы бронхиальной астмы. Они характеризуются приступами удушья, когда человек не может сделать полноценный вдох.
- Расстройство питания. Это происходит из-за длительного нахождения на ИВЛ. В результате нарушается сосательный рефлекс, а в дальнейшем может наблюдаться расстройство глотания.
- Иммунодефицит. При нарушении функции лёгких часто наблюдается сильное снижение иммунного ответа организма. В связи с этим повышается риск развития инфекционных заболеваний, которые поражают дыхательные пути.
- Лёгочная гипертензия. Эта патология представляет собой повышение давления в малом круге кровообращения, что ведёт к развитию обструкции крупных сосудов в сердце и лёгких. Состояние ведёт к потере функции сердца.
- Ателектаз. Представляет собой спадание доли лёгкого, с невозможностью его полного расправления. Это происходит из-за недостаточного количества сурфактанта, который ответственен за расправление лёгочной ткани.
- Гипоксия. Характеризуется недостаточным поступлением кислорода в организм (кислородное голодание). Недостаток кислорода приводит к осложнениям со стороны сердечно-сосудистой системы, а также ведёт к застойным явлениям в лёгких.
- Отёк лёгких. Возникает из-за переизбытка жидкости в лёгких. Возникает из-за длительного ИВЛ.
- Апноэ. Это патологическое состояние представляет собой внезапное прекращение дыхания. Особенно часто это наблюдается у детей до 6 месяцев. Чаще всего апноэ развивается ночью или в ранние утренние часы. Апноэ требует реанимационных мероприятий.
 Апноэ
АпноэВывод
Бронходисплазия является тяжёлым заболеванием, которое грозит серьёзными последствиями для организма. Поэтому важную роль отводят профилактике дисплазии. Первичная профилактика включает в себя сохранение нормально протекающей беременности до 37–38 недель беременности. Вторичная профилактика подразумевает введение адекватных доз кислорода для недоношенного ребёнка, чтобы не вызвать нарушение лёгочной ткани.
Прогноз при дисплазии условно благоприятный. Это значит, что большая часть детей успешно справляется с этой патологией и в будущем не имеет существенных проблем с органами дыхания. Важным моментом для родителей является полное следование врачебным назначениям. Нужно наблюдаться у врачей-специалистов (пульмонолог и педиатр), а также выполнять УЗИ сердца. Частоту осмотров назначают исходя из степени тяжести патологии.
Родителям нужно помнить о создании адекватного режима реабилитации. Необходимо обеспечивать пребывание ребёнка на свежем воздухе не менее 2 часов в день, профилактика вирусных заболеваний (ограждение от контактов с большим количеством людей). Необходимо также увлажнять воздух в комнате ребёнка и выполнять ежедневную влажную уборку без применения агрессивных моющих средств. В тяжёлых случаях нужно ориентироваться на рекомендации лечащего врача.
Похожие записи
Бронхолегочная дисплазия у новорожденных | LadyCaramelka
I. Определение. Бронхолегочная дисплазия (БЛД) — одна из форм хронических заболеваний легких, описанная у выживших недоношенных новорожденных с болезнью гиалиновых мембран (БГМ). Термин БЛД предложил Northway в 1967 г. для обозначения хронического заболевания легких, обусловленного применением механической вентиляции легких и высоких концентраций кислорода у недоношенных новорожденных с БГМ. Он отметил определенную последовательность прогрессирования клинических, морфологических и рентгенологических изменений со стороны легких, начиная с ранних, практически не отличимых от тяжелой БГМ (стадия 1), и заканчивая тяжелым хроническим заболеванием легких (стадия 4). У недоношенных новорожденных описаны две другие формы хронического поражения легких. Синдром Вильсон—Микити характеризуется незаметным появлением симптомов дыхательной недостаточности в возрасте 1—5 нед у недоношенных детей с минимальной выраженностью этих симптомов при рождении. Третий синдром, хроническая недостаточность легких у недоношенных детей (ХНЛН), также характеризуется постепенным развитием респираторного дистресса у новорожденных, выглядевших абсолютно здоровыми при рождении. У таких детей в возрасте 5—10 дней появляются апноэ и гипоксемия. На рентгенограмме грудной клетки определяется лишь уменьшение объема легких. На практике часто бывает трудно или невозможно поставить точный диагноз ребенку с хроническим заболеванием легких. Широко используемым рабочим определением БЛД является следующее: БЛД — это заболевание легких у ребенка в возрасте 30 дней и старше с патологическими изменениями на рентгенограмме грудной клетки, который нуждается в дополнительной оксигенации.
II. Частота. Риск развития бронхолегочной дисплазии возрастает с уменьшением гестационного возраста и массы тела при рождении. Недоношенность, БГМ, мужской пол и семейная предрасположенность к реактивным заболеваниям дыхательных путей являются факторами риска БЛД. Ряд авторов считают, что к факторам риска относится также принадлежность к кавказским национальностям.
Данные о частоте БЛД достаточно разноречивы и зависят от того, что подразумевается под термином БЛД, и какие группы больных были обследованы. Среди новорожденных с массой тела при рождении менее 1000 г, которым проводилась механическая вентиляция легких, частота БЛД, определенная с использованием диагностических критериев стадий 3 или 4 по Northway, составила всего 3%, в то время как при использовании в качестве критериев БЛД клинических симптомов респираторного заболевания, патологических изменений газов крови и необходимости в дополнительной оксигенации у ребенка в возрасте 30 дней она достигла 70%.
III. Патофизиология. БЛД является полиэтиологическим заболеванием. Оно начинается с острого повреждения легких у ребенка с соответствующей предрасположенностью. Продолжающаяся травматизация легких и плохое заживление ведут к патологическим изменениям и хроническому нарушению функции легких.
А. Повреждение легких может быть результатом действия любого из названных ниже факторов:
1. Дефицит сурфактанта. Коллапс альвеолярных мешочков с расширением дистальных альвеолярных ходов и дальнейшим усилением неравномерности вентиляции могут вызывать прямое повреждение легочной ткани.
2. Отек легких. БГМ почти всегда сопровождается отеком легких, который может усугубляться гипопротеинемией и объемной перегрузкой малого круга кровообращения (как, например, при функционировании артериального протока).
3. Кислород. Длительное применение высоких концентраций кислорода может иметь множество отрицательных эффектов, включая нарушение подвижности ресничек эпителия дыхательных путей, ухудшение лимфооттока из легких, задержку созревания легких, а также смерть в результате продукции токсичных свободных радикалов кислорода. Патологические изменения в легких после дыхания чистым кислородом в течение длительного времени такие же, как при БГМ.
4. Механическая вентиляция легких. Важную роль могут играть положительное расширяющее давление в легких, наличие интубационной трубки в трахее, аспирация слизи из трахеи, неадекватное согревание и увлажнение газовой смеси.
5. Воспаление. Нейтрофилы способны высвобождать протеазы (у недоношенных новорожденных имеется относительный дефицит ингибиторов протеаз) и продуцировать свободные радикалы кислорода. Нейтрофилы обнаруживаются в трахее новорожденных семи дней жизни, не имеющих признаков инфекционного заболевания, у которых впоследствии формируется БЛД. К сожалению, для развития хронического заболевания легких не обязательно наличие всех этих факторов. БЛД формируется у новорожденных, которым проводят механическую вентиляцию легких по поводу апноэ без дополнительной оксигенации; с другой стороны, она развивается также у детей, получающих дополнительный кислород без искусственной вентиляции легких.
Б. Патоморфология. В легких новорожденных, умерших от БЛД, находят изменения, зависящие от стадии заболевания. На ранних стадиях обнаруживают участки ателектазов, содержащие белковую жидкость, чередующиеся с участками вздутия легочной ткани, содержащими гиалиновые мембраны. Отмечается также повреждение дыхательных путей с разрушением эпителия и ресничек или развитием некротического бронхиолита. Изменения на поздних стадиях включают интерстициальный фиброз, кистозную дилатацию, ателектазы, межклеточный отек и расширение лимфатических сосудов.
IV. Клинические проявления
А. Общие признаки. Как правило, БЛД развивается у новорожденных с массой тела менее 2000 г и гестационным возрастом менее 34 нед, которым требуется искусственная вентиляция легких и дополнительная оксигенация по поводу БГМ. Для новорожденных, у которых в конечном счете формируется БЛД, характерно отсутствие увеличения диуреза и улучшения состояния, что обычно наблюдается при неосложненной БГМ. Напротив, они нуждаются в длительной механической вентиляции легких и дополнительной оксигенации, часто осложняющимися утечкой воздуха из легких и функционированием артериального протока.
Б. Физикальное обследование
1. К общим симптомам БЛД относятся тахипноэ, тахикардия и цианоз при дыхании комнатным воздухом или при возбуждении.
2. Исследование легких. Отмечаются выраженные втяжения межреберий и подреберий, с обеих сторон выслушиваются хрипы.
3. Исследование сердечно-сосудистой системы. «Легочное сердце» может сопровождаться усиленным толчком правого желудочка, единственным зубцом S2 или высоким P2 на ЭКГ.
4. При осмотре живота можно выявить увеличение печени вследствие правожелудочковой недостаточности или смещение ее вниз в результате гипераэрации легких.
V. Диагноз
А. Лабораторные исследования. Лабораторные данные отражают хроническую природу заболевания легких.
1. Показатели газов артериальной крови свидетельствуют о гиперкапнии. Однако вследствие длительного течения заболевания pH обычно нормальное. Гипоксемия развивается в том случае, если не проводится дополнительная оксигенация.
2. Электролитные нарушения включают увеличение концентрации в крови бикарбоната, а также осложнения вследствие терапии диуретиками (гипонатриемия, гипокалиемия, гипохлоремия) или из-за ограничения введения жидкости (повышение уровня азота мочевины и креатинина в сыворотке крови).
Б. Радиологические исследования
1. Рентгенография грудной клетки. Рентгенологические изменения в легких могут быть самыми разными. Обычно наблюдаются тяжистый интерстициальный рисунок, ателектазы, кисты, эмфизематозные изменения и гипераэрация в различных комбинациях. Часто бывает трудно отличить вновь появившиеся изменения от уже длительно существующих. Northway описал определенную последовательность прогрессирования рентгенологических изменений при БЛД:
а. Тяжелая БГМ (стадия 1).
б. Полное снижение прозрачности легочных полей (стадия 2).
в. Пузыревидные кисты, сопровождающиеся увеличением, эмфиземой и гипераэрацией легких (стадия 3 и 4).
2. На рентгенограммах или эхограммах могут обнаруживаться кальцификаты в почках, являющиеся следствием применения диуретиков, способствующих выведению кальция (например, фуросемида), в течение длительного времени.
В. Другие методы исследования. С помощью электрокардиографии и эхокардиография выявляют гипертрофию правого желудочка с отклонением электрической оси сердца вправо, увеличение систолических временных интервалов или утолщение стенки правого желудочка.
VI. Лечение.
А. Профилактика. В последние годы все больше внимания уделяется путям профилактики и БГМ, и БЛД,
1. Профилактика преждевременных родов. Терапия, направленная на уменьшение риска преждевременных родов и частоты БГМ, включает введение токолитиков и стероидных гормонов матери и экзогенного сурфактанта в трахею новорожденному.
2. Профилактика БЛД. Лечение недоношенного новорожденного с БГМ направлено одновременно и на снижение риска последующего развития БЛД.
а. Общепринятые меры профилактики. К ним относятся уменьшение до минимума длительности оксигенотерапии и баротравмы легких, ограничение объема вводимой жидкости и активная терапия функционирующего артериального протока.
б. Другие методы
(1) Предпринимались попытки проведения антиоксидантной терапии витамином Е, но у новорожденных без дефицита витамина E они оказались безуспешными. Кроме того, длительное применение витамина E приводило к увеличению частоты язвенно-некротического энтероколита.
(2) Дексаметазон. Есть данные о том, что лечение дексаметазоном новорожденных, находящихся на искусственной вентиляции легких до 2-недельного возраста, у которых еще нет рентгенологических признаков БЛД, предотвращает ее развитие.
Б. Лечение хронического заболевания легких. Лечение новорожденных, у которых сформировалось хроническое заболевание легких, представляет собой большую проблему. Важно диагностировать переходную фазу от БГМ к хроническому заболеванию легких, так как при этом необходимо изменить тактику лечения ребенка. С момента развития у новорожденного хронического заболевания легких основные усилия должны быть направлены на улучшение функции легких, профилактику легочного сердца и обеспечение нормального роста и развития.
1. Респираторная терапия
а. Непрерывный мониторинг оксигенотерапии и оксигенации тканей. В отличие от новорожденных с БГМ, для которых важное значение имеет максимально возможное уменьшение концентрации кислорода в используемых газовых смесях, детям с БЛД требуется поддержание адекватной оксигенации с целью предупреждения развития легочного сердца, угрожающего жизни больного. Обязательным является контроль за оксигенацией крови и концентрацией кислорода во вдыхаемой воздушно-кислородной смеси при проведении оксигенотерапии, если она показана. Определение газов артериальной крови не имеет особого значения, так как позволяет получить данные об оксигенации лишь в определенные моменты времени. Предпочтение отдается непрерывному транскутанному мониторингу PО2 (TcPО2) или показателям насыщения крови кислородом. Это позволяет рутинно в течение всех суток Оценивать потребности ребенка в кислороде и соответствующим образом изменять концентрацию кислорода в подаваемой газовой смеси. Например, с помощью транскутанного мониторинга можно выявить необходимость в увеличении концентрации кислорода во вдыхаемом воздухе во время кормления. У новорожденных в возрасте менее 3 мес жизни значения TcPО2 следует поддерживать более 60 мм рт, ст., у детей более старшего возраста — более 50 мм рт. ст. Насыщение крови кислородом должно составлять 90% и выше.
б. Искусственная вентиляция легких под положительным давлением. Часто требуется длительная механическая вентиляция легких. Образование в легких «воздушных ловушек» заставляет уменьшать частоту дыхания с удлинением выдоха. Перевод ребенка на самостоятельное дыхание должен быть постепенным. При смягчении параметров вентиляции, если pH в норме, можно допускать повышение PО2 до 50 мм рт. ст. и выше. В клиниках, имеющих большой опыт в использовании ППД, при переводе ребенка с механической вентиляции легких на спонтанное дыхание эффективную помощь может оказать применение ППД через носовые канюли (5 см вод. ст).
в. Бронходилататоры. Считают, что у здоровых новорожденных тонус гладких мышц бронхов является недостаточным для того, чтобы у них мог значительно меняться просвет дыхательных путей, но это не относится к детям с БЛД. Положительный эффект в лечении таких новорожденных дают ингаляции β2-адреномиметиков и теофиллина.
(1) Ингаляции изопротеренола 0,1%, β2-адреномиметика снижают сопротивление дыхательных путей.
(2) Подкожное введение тербуталина (5 мкг/кг), другого β2-адреномиметика, снижают сопротивление дыхательных путей и увеличивают растяжимость легких.
(3) Теофиллин вызывает несколько положительных эффектов, включая расслабление гладких мышц дыхательных путей, улучшение сократимости диафрагмы, стимуляцию дыхательного центра и небольшое увеличение диуреза.
2. Лечение отека легких является сложной задачей.
а. Ограничение объема вводимой жидкости затруднено из-за необходимости обеспечения ребенка адекватным количеством питательных веществ.
б. Лечение диуретиками
(1) Преимущества. Исследования показали, что лечение диуретиками способствует улучшению проходимости дыхательных путей и растяжимости легких и снижает общее сопротивление легких.
(2) Недостатки. Длительное применение диуретиков может привести к выраженным электролитным расстройствам и нефрокальцинозу.
(3) Препараты. Применение фуросемида или комбинации фуросемида с хлоротиазидом позволяет уменьшить частоту нефрокальциноза. При использовании сочетания спиронолактона (верошпирон) и хлоротиазида в течение длительного времени в качестве диуретиков вызывает менее выраженные электролитные нарушения.
3. Стероидные гормоны. Другим методом лечения БЛД, эффективность которого является спорной, считают гормональную терапию. В некоторых исследованиях отмечено кратковременное улучшение состояния новорожденных на фоне введения стероидных гормонов. Это улучшение не всегда сохранялось после отмены гормонов, а высокий уровень смертности помешал оценить отдаленные результаты лечения. Длительная гормональная терапия несет риск инфекционных осложнений, гипергликемии, артериальной гипертензии и язвы желудка.
4. Питание. Обеспечение новорожденного с БЛД адекватным количеством энергии имеет принципиальное значение. Если ребенок может получить необходимое количество калорий с молоком, его следует кормить грудью. Однако наряду с высокой потребностью в энергии, свойственной вообще недоношенным детям, больным с БЛД требуется дополнительное ее количество за счет увеличенной работы дыхательной мускулатуры. Часто для того, чтобы удовлетворить энергетические потребности ребенка при ограничении введения жидкости, приходится увеличивать энергетическую ценность питательной смеси (до 80—95 ккал/100 г). У детей, получающих концентрированные смеси, необходимо тщательно контролировать функцию почек. Новорожденных, получающих диуретики, особенно фуросемид, рекомендуют кормить питательными смесями для недоношенных детей с высоким содержанием кальция и фосфора.
5. Решение вопроса о выписке. Оксигенотерапию часто можно отменить еще до выписки ребенка домой. Из небольшого числа сообщений о применении кислорода на дому следует, что оно является безопасным и позволяет значительно сократить сроки госпитализации. Вопрос о необходимости использования в домашних условиях кардиореспираторного мониторинга должен решаться на основе индивидуального подхода, но его рекомендуется проводить всем детям, выписываемым с назначением кислорода. Все родители обязаны получить инструкции по проведению сердеччно-легочной реанимации.
6. Общий уход. Уход за детьми с БЛД более старшего возраста предусматривает участие в этом родителей и строгое соблюдение режима дня. Рекомендуется периодически выполнять биохимические исследования с целью выявления рахита и эхокардиографические — для выявления гипертрофии правого желудочка. Должна быть полностью проведена иммунизация. Осмотр ребенка специалистами по физиотерапии и трудотерапии и невропатологом помогает дать прогноз и оптимизировать лечение.
VII. Прогноз. Прогноз новорожденных с БЛД зависит от степени нарушения функции легких и наличия других заболеваний. Хотя большинство больных, впервые описанных Northway, умерли, в настоящее время смертность детей с БЛД составляет 23—39%. Основными причинами смерти являются сепсис и сердечно-легочная недостаточность. Риск синдрома внезапной смерти у больных с БЛД, выписанных домой, достигает 1%. У выживших детей с БЛД до 10 лет сохраняются повышенные сопротивление и реактивность дыхательных путей. После выписки домой может прогрессировать правожелудочковая недостаточность, если ребенку проводится неадекватная оксигенотерапия. Роль БЛД (в противоположность другим осложнениям недоношенности) в формировании нарушений нервно-психического развития точно не установлена. В ряде исследований показано, что БЛД, независимо от других причин, ухудшает познавательные функции. В других работах отклонение в нервно-психическом развитии связывают с действием повреждающих факторов в перинатальном и неонатальном периодах, а не с наличием или отсутствием у ребенка БЛД.
Бронхолегочная дисплазия у недоношенных детей: симптомы, лечение, последствия
Недоношенные дети часто рождаются с незрелыми легкими, в результате чего их подключают к аппарату искусственной вентиляции легких. Посредством этой процедуры в детский организм поступает высокая концентрация чистого кислорода, что в будущем может привести к патологиям дыхательной системы. Бронхолегочная дисплазия у недоношенных является одним из таких заболеваний.

Причины бронхолегочной дисплазии легких
Стоит отметить, что искусственная вентиляция легких далеко не всегда провоцирует осложнения. К тому же, она является не единственной причиной, из-за которой развивается БЛД. Чаще всего заболевание развивается у младенцев, родившихся до 34 недели, масса тела которых не превышает 2 кг. На развитие заболевания могут также влиять:
- инфекционные заболевания;
- повышенное кровяное давление;
- пневмония;
- травмы.
Что интересно, у недоношенных мальчиков заболевание легких отмечается чаще, чем у недоношенных девочек. Медицина до сих пор не может объяснить причину такого явления.
Разновидности бронхолегочной дисплазии легких у младенцев
Заболевание протекает в легкой, средней и тяжелой форме. Все зависит от того, насколько легкие младенца нуждаются в кислороде.
 Бронхолегочная дисплазия в легкой форме характеризуется частотой дыхания до 60. При респираторных заболеваниях появляются симптомы бронхоспазма и небольшая одышка.
Бронхолегочная дисплазия в легкой форме характеризуется частотой дыхания до 60. При респираторных заболеваниях появляются симптомы бронхоспазма и небольшая одышка.
Бронолегочная дисплазия средней тяжести характеризуется увеличением частотой дыхания до 80. У младенцев отмечаются сухие хрипы в легких и средняя одышка, которые усугубляются при респираторной инфекции.
Бронхолегочная дисплазия в тяжелой форме обладает выраженными симптомами бронхообструкции. Частота дыхания переваливает за 80, появляются осложнения со стороны сердца и легких, ребенок отстает в развитии.
Важно отметить, что заболевание характеризуется периодами ремиссии, которые резко сменяются обострениями.
Стадии БЛД
Бронхолегочная дисплазия у детей имеет 4 стадии. Первая стадия начинается с первых дней заболевания, проявляется одышкой, тахикардией, учащенным дыханием и сухим кашлем. Начиная с 5-го дня, разрушается эпителий альвеол, из-за чего ткани легких отекают. Этот процесс начинается на второй стадии.
С 10 по 20 дней протекает 3 стадия. В этот период происходит повреждение бронхиол. На последней, четвертой стадии в легких появляются участки спавшейся легочной ткани. После 20 дня развивается эмфизема. Также этот период характеризуется развитием хронической обструктивной болезни.

Симптомы, которые помогут своевременно выявить заболевание
Симптомы БЛД неспецифичны. Они могут указывать на многие другие патологии. Их проявление должно стать незамедлительным поводом для обращения за медицинской помощью. К таковым симптомам относят:
- посинение кожи;
- интенсивное вытягивание шеи при вдыхании воздуха;
- сухой кашель;
- затрудненное, быстрое и поверхностное дыхание.

Диагностические мероприятия
Для выявления патологии у недоношенных младенцев собираются данные анамнеза: имеет ли младенец кислородозависимость, на каком сроке и с каким весом родился, была ли искусственная вентиляция легких, какие симптомы беспокоят на момент обращения к врачу. В дальнейшем потребуется анализ крови, рентгенография грудной клетки. Также в диагностических целях применяют импульсную оксиметрию, этот метод предполагает крепление на ножку младенца датчика кислорода, который помогает определить работоспособность легких.
Лечение заболевания
Бронхолегочная дисплазия новорожденных опасна тем, что может в любой момент перейти в пневмонию. Чтобы этого не допустить, проводится антибактериальная терапия. Чтобы поддержать нормальную работу легких, младенцам назначают диуретики. Их действие направлено на предотвращение скопления жидкости в легких. Чтобы дыхательные пути оставались открытыми, назначают бронхорасширяющие препараты. Также применяются мочегонные средства, которые препятствуют отеку легких. Особо тяжелые случаи БЛД требуют применения стероидных препаратов.
Несмотря на то, что бронхолегочная дисплазия провоцируется искусственной вентиляцией легких, очень часто младенцы длительное время нуждаются в обеспечении кислородом. Лечение таким методом предполагает максимальное понижение давления в аппарате. Концентрация кислорода в крови у новорожденных постоянно контролируется.
При возникновении проблем с легкими, затрудняется кормление младенцев. В этом случае необходимо наладить правильное питание. Сделать это можно несколькими способами:
- вливать смеси через катетер, введенный в вену;
- установить специальную трубочку для питания в желудок младенца;
- если состояние позволяет, проводить кормление смесями через обычную бутылочку.
В сутки младенцы должны получать 130 ккал на каждый кг веса. Необходимо обеспечить крохам оптимальную температуру воздуха и покой.
По мере выздоровления ребенка, обычный режим приема пищи будет налаживаться.
Осложнения
Хотя бронхолегочная дисплазия и склонна к частым рецидивам, легкое и среднетяжелое течение болезни имеют хорошие прогнозы. Состояние малышей постепенно стабилизируется в течение 6-12 месяцев. БЛД у недоношенных детей, которая протекает в тяжелой форме, имеет менее благоприятные прогнозы.
Практически в 20% случаев заболевание приводит к гибели. Младенцы, которые перенесли тяжелую форму заболевания, могут испытывать симптомы еще несколько месяцев, затем наступает клиническое улучшение. У части из них диагноз остается на всю жизнь, что становится причиной инвалидности.
Бронхолегочная дисплазия может спровоцировать ряд осложнений:
- хроническая дыхательная недостаточность, при которой младенец испытывает длительную потребность в кислороде;
- пневмония и инфекции бронхов; это крайне опасные состояния для детей младше 5 лет;
- развитие бронхиальной астмы;
- возникновение ателектазов – спавших участков легких;
- изменение в правом желудочке сердца, которое в медицине называют «легочным сердцем»;
- увеличение сердца, что приводит к развитию сердечной недостаточности;
- длительные апноэ;
- задержка развития, которая выражается медленным набором массы тела, задержкой роста, отставанием в развитии;
- повышение АД, которое успешно лечится гипотензивными средствами;
- развитие анемии.
Профилактические меры
Поскольку бронхолегочная дисплазия, как правило, развивается у недоношенных детей, самые важные меры профилактики заключаются в предотвращении преждевременных родов. Для этого женщины должны соблюдать следующие рекомендации:
- правильно и своевременно питаться;
- полностью исключить курение и прием алкогольных напитков;
- своевременно лечить хронические патологии;
- стараться избегать стрессов и психоэмоциональной нестабильности;
- избегать интенсивной физической нагрузки.
При возникновении угрозы преждевременных родов, женщине проводят глюкокортикоидную терапию, которая ускоряет созревание легочных альвеол у плода.
Недоношенным младенцам проводят следующие мероприятия:
- вводят сурфактант;
- грамотно проводят искусственную вентиляцию легких;
- обеспечивают правильное питание;
- назначают антибактериальную терапию при возникновении инфекции;
- ограничивают введение жидкости через вену.
Препараты сурфактанта необходимы для поддержания легких малыша в раскрытом состоянии, что позволяет поступать в них достаточному количеству кислорода. Все реанимационные мероприятия должны проводиться грамотно и с максимальной осторожностью.
Видео: Бронхолегочная дисплазия у недоношенных детей
лечение, последствия, причины, симптомы, признаки, что это такое
Бронхолегочная дисплазия — приобретенное заболевание незрелых легких, обусловленное интенсивной вентиляцией с высокой концентрацией кислорода.
Встречаемость/эпидемиология: БЛД — хроническое неонатальное заболевание легких, частота возрастает по мере снижения массы тела. Заболевают:
- Примерно 1—2 % новорожденных на стационарном лечении.
- Около 10 % недоношенных с массой тела < 1500 г.
- 30-60 % с массой тела < 1000 г.
Факторы риска: среди прочих дискутируются баротравма, волюмотравма, инфекции, токсичность кислорода, открытый артериальный проток (ОАП) и перегрузка легких жидкостью.
Патоморфология: перестройка нормальной структуры легких с перераздутыми участками легких, Рубцовыми ателектазами (фиброателектазами) и обеднением сосудистого русла легких.
Определения
Существуют различные определения в зависимости от автора; обращают внимание на потребность в кислороде при соответствующей степени зрелости: БЛД имеется при FiO, от >0,21:
- В возрасте после 28 дня жизни (определение по Bancalari).
- С 36 недели (определение по Shennan).
- С 36 недели, насыщение крови по пульсоксиметру достигается от 92 % (определение по Garland).
Новое определение, охватывающее степень тяжести БЛД и учитывающее гестационный возраст в родах, предложено Jobe и Bancalari.
БЛД имеется, если потребность в кислороде (FiO2 не менее 28 дней была выше 0,21 и на этот срок существует следующая ситуация:
- FiO2 = 0,21 –> мягкая форма БЛД.
- FiO2 < 0,30 –> умеренная БЛД.
- FiO2 > 0,30 и ИВЛ или СРАР –> тяжелая БЛД.
Срок варьирует в зависимости от срока гестации:
- Для детей с ГВ < 32 недель имеет значение FiO2 с 36 недели или при выписке домой; в зависимости от того, что происходит раньше.
- Для детей с ГВ > 32 нед. — Fi02 после 28 дня жизни, но не позднее 56 дня или при выписке (что происходит раньше).
Пример: недоношенный с 28 недели получает кислород, FiO2 > 0,21. С 8 недель (36 неделя) ребенок еще нуждается в кислороде, FiO2 < 0,30 –> умеренная БЛД.
Особую группу представляют экстремально незрелые (и малые для гестационного возраста) недоношенные, вначале с относительно интактной функцией легких, у которых позднее развивается тяжелая, нередко смертельная БЛД. Причины и профилактика такого хода событий до сих пор неясны.
Симптомы бронхолегочной дисплазии у недоношенных детей
- Диспноэ, втяжения, хронический кашель, часто колоколообразная грудная клетка.
- Гиперкапния. повышенная потребность в кислороде, при обстоятельствах от недель до месяцев.
- Частые легочные инфекции, обструктивные бронхиты, в дальнейшем бронхиальная астма.
- Cor pulmonale, увеличение печени.
- Длительная потребность в ИВЛ и оксигенотерапии.
- Хроническая гиперкапния, одышка, втяжение межреберных промежутков, усиленное выделение мокроты.
- Пневмонии, приступы бронхоспазма.
- Поздний симптом: правосторонняя сердечная недостаточность.
Диагностика бронхолегочной дисплазии у недоношенных детей
ЭКГ: P-pulmonale.
Эхокардиография: перегрузка правых отделов сердца.
Рентгенография ОГК: ателектазы и перераздутые участки легких.
Анализ газов крови, увеличение рС02, BE.
Дифференциальный диагноз бронхолегочной дисплазии у недоношенных детей
Другие легочные заболевания: пневмония (хламидии, уреаплазмы). Отек легких, пневмоторакс, ателектазы.
Врожденные пороки сердца: легочная гипертензия, ДМЖП, ДМПП и др.
Лечение бронхолегочной дисплазии у недоношенных детей
- Оксигенотерапия.
- Медикаментозное лечение: бронходилятаторы, антибиотики при инфекции, диуретики, дексаметазон (спорно), возможно — сердечные гликозиды.
- Ограничение жидкости, высококалорийное питание.
Системная фармакотерапия:
- Диуретики (раннее применение): гидрохлортиазид (Esidrix) и спиронолактон (Aldactone), можно фуросемид (Lasix), если недостаточен эффект гидрохлортиазида.
- Бронходилататоры (раннее применение): теофиллин.
- Глюкокортикоиды. Применение очень ограничено! Дексаметазон 0,1 мг/кг/сутки в 2 введения. Введение преимущественно в «пульсовом режиме», т.е. в течение 3 дней, затем отменить. Если необходимо, приемлемо повторное применение после возможно длительной паузы. Обдумать альтернативу — гидрокортизон 5 мг/кг/сутки.
- Возможно, необходима хорошая аналгоседация. Часто полезен морфин!
Внимание: обращать внимание на АД, глюкозу крови (особенно у недоношенных < 30 недель гестации –> редукция дозировки), гипертрофия желудочков эхокардиография, желудочно-кишечные кровотечения и перфорации.
Опасность: гиповолемия и потери Na+, Са++, Cl–! Обращать внимание на гипохлоремический алкалоз во время терапии.
Ингаляционная фармакотерапия: ингаляции 3 раза в сутки (спорно, до сих пор нет доказательств эффективности):
- Сальбутамол: 1 капля/кг = 0, 25 мг/кг, максимум 3 капли.
- NaCl 0,9 %: 2 мл.
- Возможно, дополнительно ипратропиум бромид: 1 капля/кг = 0,01 мг/ кг, максимум 3 капли.
- Возможно, дополнительно хромоглициновая кислота: 1/2 ампулы = 5 мг = 1 мл.
- В дискуссии до сих пор без однозначных доказательств эффективности— будесонид 0,25 мг ингаляционно 2 раза в сутки.
Физиотерапия: при БЛД особенно важна!
Кислород: возможно применение при тяжелом течении легочной гипертензии (внимание: состояние зрелости сосудов сетчатки). Целью является пульсоксиметрическое насыщение крови > 90 %.
Питание: повышенная потребность в калориях из-за усиленной работы дыхания. Дотации витамина А должны оказывать протективный эффект.
Наблюдение за больным
Непрерывно следить за пульсом, дыханием и сатурацией крови кислородом.
Уход
Облегчить дыхание: приподнятое положение верхней части тела, валик под плечи.
Физиотерапия, при необходимости — аспирация мокроты из бронхов.
Следить за объемом принятой и выделенной жидкости или ежедневно взвешивать ребенка.
Наблюдать за оксигенотерапией.
Вскармливание: высококалорийное обогащенное питание, частые небольшие порции пищи, возможно — через зонд.
Психическое окружение: тихая обстановка, не изнурять ребенка. По возможности, работа с ребенком и родителями маленьких групп специалистов (врач и ухаживающий персонал).
Мероприятия по уходу проводить в тишине, специально выделять для ребенка время; стресс и изнурение отрицательно влияют на ребенка: могут вызвать приступ удушья или бронхоспазм.
При тяжелом течении заболевания оксигенотерапию следует проводить в домашних условиях, своевременно обучить родителей аспирации и зондированию, обращению с прибором (пульсоксиметрия, концентратор кислорода, аспирационная установка), последовательности действий в экстренной ситуации.
Выделить время для разговора с родителями об их страхах.
Предложить родителям контактную информацию родителей других детей.
Профилактика бронхолегочной дисплазии у недоношенных детей
Снижения частоты БЛД с помощью:
- Пренатального применения стероидов.
- Ранней сурфактантной терапии.
- Ограничения введения жидкости.
- Раннего лечения клинически значимого ОАП.
- Ранней экстубации.
- Возможно наименьшей волюмотравмы, связанной с ИВЛ
- Дотации витамина А.
Прогноз при бронхолегочной дисплазии у недоношенных детей
По сравнению со здоровыми сверстниками у детей, которые болели БЛД, отмечаются отставание нервно-психического развития, моторные, визуальные и слуховые нарушения. В среднем у них ниже IQ, хуже академическая успеваемость, и они имеют больше проблем с поведением.
Смертность при БЛД составляет 10-25%. Наибольшая смертность – среди нуждающихся в ИВЛ более 6 мес. Самые частые причины смерти: сердечно-легочная недостаточность, связанная с легочным сердцем, и респираторные бактериальные и вирусные инфекции. Изменение качества интенсивной терапии в настоящее время снизило тяжесть БЛД и смертность от нее.

