Дисплазия крови – причины развития и формы недуга, особенности диагностики и характерные симптомы, современные методы лечения и показания к операции, прогноз для жизни
Миелодиспластический синдром — Википедия
Миелодиспластический синдром (МДС) — группа гетерогенных клональных заболеваний, характеризующаяся наличием цитопении в периферической крови, дисплазии в костном мозге и риском трансформации в острый лейкоз.
МДС сегодня является одной из самых сложных проблем гематологии. Лишь недавно лечение МДС вышло за рамки поддерживающей терапии, проводившейся с целью облегчения симптомов.
МДС — это патология старшей возрастной группы. 80 % случаев МДС приходится на лица старше 60 лет. МДС в детском возрасте встречается крайне редко. В европейских странах среди лиц 50-69 лет регистрируется 40 новых случаев МДС на 1 млн населения, а среди лиц 70 лет и старше — 150 новых случаев на 1 млн населения. Заболеваемость МДС в РФ в среднем составляет 3-4 случая на 100 тыс. населения в год и увеличивается с возрастом.[2]
Первичный (идиопатический) тип — 80-90 % случаев, вторичный (вследствие предшествующей химиотерапии и др. факторов) — 10-20 %. Большинство (80 %) случаев МДС являются первичными — идиопатическими или de novo (лат. — вновь появившийся, новый).
Вторичный МДС является значительно более неблагоприятным и резистентным к лечению типом МДС, обладающим заведомо более худшим прогнозом в сравнении с первичным МДС. 10-20 % случаев МДС возникают вследствие предшествующей химиотерапии по поводу других новообразований. К препаратам, обладающим доказанной способностью повреждать геном с последующим развитием МДС, относятся алкилирующие агенты (циклофосфан), ингибиторы топоизомеразы — противоопухолевые агенты растительного происхождения (топотекан, иринотекан и др.), антрациклины (доксорубицин) и подофиллотоксины (этопозид). К МДС также могут приводить радиотерапия и контакт с токсическими материалами.
- Факторы риска, первичный МДС
- Факторы риска, вторичный МДС
Предшествующая химиотерапия онкологического заболевания или после ТКМ.
Прогноз: 5-летняя выживаемость при МДС не превышает 60 %. Трансформация в острый лейкоз ~30 % случаев. [3][4]
Причины МДС до конца не известны. В основе патогенеза МДС лежит воздействие повреждающих факторов на полипотентную стволовую клетку, приводящее к появлению в ней генетических аномалий, а также феномена гиперметилирования ДНК.
Указанные нарушения приводят к нарушению продукции клеток миелоидного ростка и появлению миелобластов в костном мозге и периферической крови, вследствие чего появляются диспластические изменения в зрелых клетках и их функциональная недостаточность, приводящие к описанным клиническим проявлениям.
Феномен гиперклеточности костного мозга на фоне периферической цитопении объясняется ускоренным апоптозом аномально пролиферирующих клеток костного мозга.[5]
МДС отличает отсутствие типичной клинической картины. Симптоматику МДС составляют последствия дисмиелопоэза, то есть цитопении: анемия, нейтропения и тромбоцитопения (анемия Hb меньше 110 г/л, нейтрофилы меньше 1,800 на 1 микролитр крови; гематокрит меньше 36 % эритроцитов в общем объёме крови в организме; тромбоциты меньше 100,000 на 1 микролитр крови).
Наиболее часто МДС манифестирует цитопениями, главным образом анемией. При этом необходимо дифференцировать МДС от железо- или B12- дефицитной анемии, постгеморрагической анемии, анемии при хронических заболеваниях и онкологии или связанной с хронической почечной недостаточностью, а также апластической анемией, пароксизмальной ночной гемоглобинурией. У 10 % пациентов имеются признаки инфекции, а у несколько меньшей доли пациентов болезнь проявляется кровотечениями.
В связи с этим диагностика МДС базируется исключительно на лабораторно-инструментальных методах, из которых ключевыми являются полный клинический анализ периферической крови, некоторые биохимические исследования и морфологический анализ аспиратов и биоптатов костного мозга.
Дифференциальная диагностика МДС также затруднена в силу множества состояний, имеющих общие с МДС клинико-лабораторные проявления.
Для анализа изменений в периферической крови проводится полный, с подсчетом ретикулоцитов (ускоренный эритропоэз с макроцитозом в ответ на гемолиз и острую кровопотерю приводит к увеличению ретикулоцитов), тромбоцитов и лейкоцитов клинический анализ крови. Типичными находками являются изменения формы клеток, патологические включения и уменьшение числа клеток одного или нескольких ростков кроветворения.
Другим ключевым с точки зрения диагностики МДС оценки прогноза и выработки тактики лечения больных исследованием является морфологическое, иммуногистохимическое и цитогенетическое исследования ткани костного мозга. Исследование костномозгового пунктата в этом отношении является несравненно более информативным, чем определение морфологического состава периферической крови.
Используются два способа получения материала: 1) аспирационная биопсия костного мозга и 2) трепанобиопсия из гребня подвздошной кости.
При цитологическом исследовании костного мозга (миелограмма) можно оценить наличие дисплазии миелоидного ростка.
Дизэритропоэз: многоядерность Костный мозг больного рефрактерной сидеробластной анемией: кольцевые сидеробласты- Дизэритропоэз
Ядро
- Межъядерные цитоплазматические мостики
- Кариорексис
- Многоядерность
- Баббл-формы
- Мегалобластоидность
Цитоплазма
- Кольцевидные сидеробласты
- Вакуолизация
- Положительная реакция с Шифф-йодной кислотой
- Дисгранулопоэз
- Маленькие или чрезмерно большие клетки
- Гиполобулярность ядер (псевдо-Пельгер-Хюит аномалия)
- Неравномерная гиперсегментация
- Гипо-/агрануляция
- Гранулы псевдо Чедиак-Хагаси
- Палочки Ауэра
- Дисмегакариопоэз
- Микромегакариоциты
- Гиполобулярные ядра
- Многоядерность
Гистологическое исследование костного мозга (трепанобиопсия) позволяет оценить архитектонику костного мозга, диффузный или очаговый характер изменений в нём, изучить соотношение кроветворной и жировой ткани, выявить атипичные клетки и т. п. Аспирация костного мозга при стернальной пункции так или иначе нарушает структуру костного мозга и не исключает примешивание к пунктату периферической крови. В связи с этим выполнение трепанобиопсии обязательно для подтверждения диагноза МДС.
Биохимические исследования обмена железа, содержания витамина В12 и фолиевой кислоты, иммунологические пробы призваны помочь провести дифференциальную диагностику с анемиями иного генеза, с учётом того, что у 80 % пациентов с МДС отмечается анемия.
МДС следует дифференцировать с другими онкогематологическими заболеваниями, включая острые и хронические лейкозы, а также лимфопролиферативные заболевания.
Часть изменений, свойственных МДС (в частности, моноцитоз, цитопенические нарушения), могут отмечаться при некоторых инфекционных процессах.
При отравлении тяжелыми металлами могут отмечаться изменения эритроцитарного ростка, сходные с таковыми при сидеробластных анемиях.
У пациентов с наследственными цитопениями рекомендуется проведение дополнительного генетического исследования, которое поможет выявить анемию Фанкони и врождённый дискератоз.
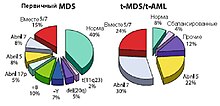 Повторяющиеся хромосомные аномалии при MDS
Повторяющиеся хромосомные аномалии при MDSПри диагностике хромосомные аномалии обнаруживаются у 40-70 % пациентов с первичным MDS и у 95 % пациентов, MDS которых связан с терапией (вторичный).
К наиболее часто встречающимся при MDS цитогенетическим аномалиям относятся del(5q), −7 и +8.[6]
| Группа риска | Кариотип (22 группы) | Средняя выживаемость (мес) | Время, к которому 25 % пациентов развили ОМЛ |
|---|---|---|---|
| Благоприятная | 5q-, 12p-, 20q-, +21, -Y, 11q-, t(11(q23)), норма; любые 2 аномалии, включающие 5q- | 51 | 71,9 |
| Промежуточная-1 | +1q, аномалии 3q21/q26, +8, t(7q), +19, −21, любая др. одиночная поломка; любые двойные аномалии, не затрагивающие хр. 5q и 7 | 29 | 16 |
| Промежуточная-2 | -X, −7 или 7q-, любые двойные аномалии с −7 or 7q-, комплекс из 3х аномалий | 15,6 | 6 |
| Неблагоприятная | Более 3х аномалий | 5,9 | 2,8 |
Минимальные диагностические критерии[править | править код]
Минимальные диагностические критерии МДС включают обязательные диагностические условия (цитир. По NCCN, 2009)[7] — стабильная цитопения не менее 6 месяцев, (за исключением случаев, когда цитопения сопровождается специфическим кариотипом или дисплазией двух ростков кроветворения — в этих случаях длительность стабильной цитопении должна составлять не менее 2 месяцев).
- исключение других заболеваний, которые могут стать причиной развития дисплазии или/и цитопении.
В дополнение к этим двум диагностическим условиям для установления диагноза МДС необходимо соответствие хотя бы одному из трёх основных критериев:
- дисплазия (≥ 10 % клеток одного или более из трёх основных ростков кроветворения в костном мозге).
- содержание бластов в костном мозге 5-19 %.
- специфический кариотип, например делеция (5q), делеция (20q), +8 или −7/делеция (7q).
Кроме того, для диагностики МДС используются дополнительные критерии, в том числе результаты проточной цитометрии, гистологического и иммуногистохимического исследования костного мозга, выявления молекулярных маркеров.
Морфологическое исследование биоптатов, полученных путём билатеральной трепанобиопсии, является полезным, помимо верификации диагноза самого МДС, с точки зрения дифференциальной диагностики с лимфопролиферативными и другими миелопролиферативными заболеваниями. [7]
Дифференциальная диагностика проводится с:
- А. Мегалобластными анемиями (заболевания, характеризующиеся изменениями морфологии клеток к.м. вследствие нарушения синтеза ДНК. Более 90 % — В-12 и фолиево-дефицитные анемии).
После начала терапии витамином В-12 или фолиевой кислотой в анализе крови выявляется ретикулярный криз на 5-7 сутки и повышение показателей красной крови, что нехарактерно для больных рефрактерной анемией. Изменения кариотипа клеток костного мозга не встречаются при мегалобластных анемиях.
Апластическая анемия может быть врождённой, приобретённой и идиопатической. Врождённая апластическая анемия — анемия Фанкони сочетается с другими генетическими аномалиями (кожная пигментация, гипоплазия почек, микроцефалия), приобретённая связана с действием химических и физических агентов, инфекциями, нарушениями обмена веществ.
Для АА нехарактерны изменение кариотипа, гиперклеточный костный мозг.
- В. Анемии при ХПН.
- В. Анемии при хроническом активном гепатите характерно выявление маркеров вирусных инфекций, гепатоспленомегалия, клиническая картина хр. гепатита, изменения биохимических показателей крови (метаболизма билирубина, функции печени).
Разработка этой системы классификации франко-американо-британской группой была начата в 1976 году и позже, в 1982 году, она приняла свой окончательный вид.
В основе классификации лежит ключевой для МДС синдром — рефрактерная, то есть устойчивая к лечению препаратами витамина В12 и фолиевой кислоты, анемия (РА). Четыре типа РА являются последовательными стадиями, с нарастанием тяжести МДС, что имеет своё отражение в прогнозе выживаемости. В этой связи появление в КМ бластов резко меняет прогноз выживаемости в худшую сторону.
| Тип МДС | Бластов в периферической крови | Бластов в КМ | Другие патологические изменения | Выживаемость (лет) |
|---|---|---|---|---|
| Рефрактерная анемия (РА) | меньше 1 % | меньше 15 % кольцевых сидеробластов | меньше 5 % | 4,2 |
| РА с кольцевыми сидеробластами | меньше 1 % | больше 15 % кольцевых сидеробластов | меньше 5 % | 6,9 |
| РА с избытком бластов (РАИБ) | меньше 5 % | 5-20 % | — | 1,5 |
| РАИБ в стадии трансформации | больше 5 % | 21-29 % | Возможно наличие палочек Ауэра в КМ | 0,6 |
| ХММЛ | меньше 5 % | меньше 20 % | Моноциты больше 1х109/л | 2,4 |
Французско-американско-британская классификация позволяет отнести пациента к той или иной группе миелодиспластических синдромов в зависимости от морфологических показателей. Группа миелодиспластических синдромов включает пять заболеваний: рефрактерную анемию, рефрактерную анемию с кольцевыми сидеробластами, рефрактерную анемию с избыточным количеством бластов, рефрактерную анемию с избыточным количеством бластов на стадии трансформации и хронический миеломоноцитарный лейкоз. Согласно французско-американско-британской номенклатуре пациентам, у которых содержание бластов в костном мозге превышает 30 %, устанавливается диагноз острого миелоидного лейкоза.
В данной классификации хронический миеломоноцитарный лейкоз относится к группе миелодиспластических синдромов, несмотря на то, что это заболевание часто характеризуется признаками миелопролиферативного расстройства.[8]
В 2002 году Всемирная организация здравоохранения предложила новую классификацию миелодиспластических синдромов[9][10][11] в 2008 году были сделаны предложения по её пересмотру.[12][13]
Подгруппы, выделяемые в классификации ВОЗ включают: рефрактерную анемию и рефрактерную анемию с кольцевыми сидеробластами, рефрактерную цитопению с множественной дисплазией, рефрактерную анемию с избыточным количеством бластов-1 (содержание бластов в костном мозге составляет менее 10 %), рефрактерную анемию с избыточным количеством бластов-2 (содержание бластов в костном мозге превышает 10 %), синдром делеции 5q и миелодиспластический синдром неклассифицированный (с наличием или отсутствием кольцевых сидеробластов).
Пациенты, ранее классифицировавшиеся как страдающие хроническим миеломоноцитарным лейкозом, относятся к группе миелодиспластических синдромов/миелопролиферативных заболеваний.
Синдром делеции 5q, выделяемый в классификации Всемирной организации здравоохранения в отдельную подгруппу, характеризуется изолированной делецией 5q[14][15][16] и содержанием бластов в костном мозге меньше 5 %, часто в сочетании с тромбоцитозом.
| Тип МДС | Изменения в крови | Изменения в КМ |
|---|---|---|
| Рефрактерная анемия (РА) | Анемия, меньше 1 % бластов | Дисплазия эритроидного ростка, меньше 5 % бластов |
| Рефрактерная анемия с кольцевыми сидеробластами (РАКС) | То же, что и РА | то же, что и РА, ≥ 15 % кольцевых сидеробластов |
| Рефрактерная цитопения с многоростковой дисплазией (РЦМД) | Цитопения по 2-3 росткам, меньше 1 % бластов | Дисплазия в больше 10 % клеток 2 или 3 ростков, меньше 5 % бластов, меньше 15 % кольцевых сидеробластов |
| Рефрактерная цитопения с мультилинейной дисплазией и кольцевыми сидеробластами (РЦМД-КС) | То же, что и РЦМД | То же, что и РЦМД, ≥ 15 % кольцевых сидеробластов |
| Рефрактерная анемия с избытком бластов, тип I (РАИБ-1) | Цитопении, меньше 5 % бластов | 5-9 % бластов |
| Рефрактерная анемия с избытком бластов, тип II (РАИБ-2) | Цитопении, 5-19 % бластов | 10-19 % бластов |
| Синдром 5q- | Анемия, нормальное или повышенное содержание тромбоцитов | Нормальное или увеличенное количество мегакариоцитов с гипосегментированными ядрами; изолированная делеция 5q31 |
| МДС неклассифицированный (МДС-Н) | Цитопения | Унилинейная дисплазия в нейтрофильном или мегакариоцитарном ростках, Бласты менее 5 %, Палочки Ауэра отсутствуют |
Всемирная организация здравоохранения предложила исключить рефрактерную анемию с избыточным количеством бластов на стадии трансформации из группы миелодиспластических синдромов (диагноз острого миелоидного лейкоза устанавливается, если содержание бластов в костном мозге превышает 20 %, тогда как ранее для установления этого диагноза содержание бластов должно было превышать 30 %). Однако миелодиспластические синдромы отличаются от вновь диагностированного острого миелоидного лейкоза не только содержанием бластов, но и течением заболевания, обусловленным определёнными биологическими свойствами. Кроме того, эти группы заболеваний обычно отличаются и по частоте терапевтических ответов.
Шкала IPSS (International Scoring Prognostic System — Международная шкала оценки прогноза) была разработана в 1997 году с целью дать специалистам, помимо классификации, практический инструмент по оценке прогноза и выбора тактики лечения для пациентов с впервые установленным диагнозом МДС (то есть не подходит для прогноза уже леченных пациентов с МДС).
Вторичный МДС оценивается как изначально неблагоприятный, автоматически попадающий в категорию наиболее высокого риска согласно IPSS.
Тремя факторами, которые учитывает IPSS для оценки прогноза, являются количество бластов, категория цитогенетического риска и количество поражённых цитопенией линий.
Трактовка результатов суммирования баллов по этим трем параметрам представлена в таблице:[16]
| Количество балов | ||||||
|---|---|---|---|---|---|---|
| Прогностический фактор | 0 | 0,5 | 1,0 | 1,5 | 2,0 | |
| Бласты в костном мозге | меньше 5 % | 5-10 % | — | 11-20 % | 21-30 % | |
| Прогноз с учётом характеристик кариотипа | Хороший (норма, del(5q) del(20q) -Y) | Промежуточный (+8 хромосома, 2 аномалии и др.) | Плохой (аномалии 7 хромосомы, ≥ 3 аномалии) | — | — | |
| Цитопения (количество поражённых линий) | 0/1 | 2/3 | — | — | — | |
Сумма баллов, соответствующая высокому риску по IPSS (больше 2,5) складывается из мультилинейной дисплазии, плохого цитогенетического прогноза и высокого бластоза, на грани перехода в ОМЛ (срок трансформации в который в категории высокого риска составляет всего 2 месяца).
Категория промежуточного-2 риска также складывается из выраженного цитопенического синдрома и высокого, в пределах 10-20 % бластоза.
То, что в категории низкого риска медиана общей выживаемости ниже срока перехода в ОМЛ, объясняется меньшим сроком жизни больных с МДС, что отражает последствия осложнений цитопенического синдрома.[17]
| Сумма баллов | Риск по IPSS | Срок до перехода в ОМЛ у 25 % пациентов (лет) | Медиана общей выживаемости (лет) | % Пациентов |
|---|---|---|---|---|
| 0 | Низкий | 9,4 | 5,7 | 31 % |
| 0,5-1,0 | Промежуточный-1 | 3,3 | 3,5 | 39 % |
| 1,5-2,0 | Промежуточный-2 | 1,1 | 1,2 | 22 % |
| ≥ 2,5 | Высокий | 0,2 | 0,4 | 8 % |
| Баллы | 0 | 1 | 2 | 3 |
|---|---|---|---|---|
| Вид МДС по классификации ВОЗ | РА, РАКС, 5q- | РЦМД, РЦМД-КС | РАИБ1 | РАИБ2 |
| Кариотип | Хороший | Средний | Плохой | — |
| Потребность в гемотрансфузиях | Нет | Регулярная | — | — |
Кариотип:
- Хороший: нормальный, -Y, del 5q, del 20q
- Плохой: более 3х аномалий или аномалии 7 хромосомы
- Средний: все другие
Регулярные гемотрансфузии — переливание минимум 1 ЭМ каждые 8 недель в течение 4 месяцев.
| Группа риска | Баллы | Медиана выживаемости (мес) |
|---|---|---|
| Очень низкий | 0 | 136 |
| Низкий | 1 | 63 |
| Средний | 2 | 44 |
| Высокий | 3-4 | 19 |
| Очень высокий | 5-6 | 8 |
Не все пациенты с МДС нуждаются в терапии. Пациенты без анемического, геморрагического синдрома, инфекционных осложнений могут наблюдаться и не получать лечения (тактика «watch and wait»).
Выбор терапевтической тактики во многом определяется возрастом пациента, соматическим статусом, степенью риска по шкале IPSS, WPSS, наличием совместимого донора.
Можно выделить следующие направления терапии МДС:
- Сопроводительная терапия включает в себя переливание различных гемокомпонентов (эритроцитарной массы, тромбоконцентрата), терапию эритропоэтином, тромбопоэтином. У больных, часто получающих гемотрансфузии, развивается перегрузка организма железом. Железо обладает токсическим действием на различные ткани и органы, в первую очередь сердце, печень, поэтому такие пациенты должны получать препараты, связывающие железо, — хелаторы (десферал, эксиджад).
- Иммуносупрессивная терапия наиболее эффективна у пациентов с гипоклеточным костным мозгом, нормальным кариотипом и наличием HLA-DR15. Леналидомид, обладающий иммуномодулирующим и антиангиогенным действием, показал свою эффективность у трети пациентов с рефрактерной анемией (согласно критериям ВОЗ) и низким риском (по IPSS), а также у больных с 5q-синдромом. Эффективность лечения в данном случае весьма высока; 95 % больных достигают цитогенетической ремиссии.
- Аллогенная трансплантация гемопоэтических стволовых клеток от совместимых доноров является методом выбора у пациентов с миелодиспластическим синдромом.[19][20][21]
Пациентам с МДС моложе 65 лет, с хорошим соматическим статусом, при наличии HLA-совместимого донора показано проведение аллогенной трансплантации костного мозга, так как трансплантация является потенциально радикальным методом лечения МДС.
- Цитарабин, низкие дозы. Широко используются в России, да и во всей Европе, для лечения пациентов с МДС и ОМЛ, которым не подходит терапия методом ТКМ или применение интенсивной химиотерапии.
Мнения исследователей относительно целесообразности использования низкоинтенсивной терапии расходятся. Bowen D[22] считает, что нет оснований рекомендовать её рутинное использование при МДС: было выполнено 3 рандомизированных крупных исследования (141 пац.), которые показали, что применение низких доз цитарабина не увеличивает продолжительность жизни пациентов с МДС.[23] Вместе с тем, в более позднем исследовании у пациентов с ОМЛ и МДС высокого риска[24] было показано, что продолжительность жизни у больных, у которых применялся LDAC более, чем в 1 цикле, выше, чем при поддерживающей терапии.
Таким образом, необходимость в низкоинтенсивной терапии с доказанной эффективностью и лучшей переносимостью, чем LDAC, которая будет способствовать увеличению выживаемости пациентов с МДС высокого риска, остаётся актуальной.
- Высокодозная химиотерапия используется у больных с РАИБ с гипер- и нормоклеточным костным, при трансформации в ОМЛ. Пятилетняя выживаемость составляет около 18 %.
- Гипометилирующие препараты
Новые многообещающие терапевтические подходы, широко обсуждающиеся в последнее время, по поводу которых проводятся многочисленные клинические исследования, возникли в результате глубокого изучения биологии МДС. Среди них следует отметить ингибиторы метилирования ДНК (5-азацитидин, децитабин) и иммуномодулятор — леналидомид. 5-азацитидин обладает двойным механизмом действия. Он встраивается не только в молекулу ДНК, но и в молекулу РНК. В процессе метилирования ДНК гипометилирующие агенты ковалентно связываются с ДНК-метилтрансферазой, что приводит к реактивации генов, после чего восстанавливается дифференцировка гемопоэтических клеток-предшественников и нормальное кроветворение. Азацитидин, встраиваясь в РНК молекулу, тем самым понижает её количество в клетках, что приводит к цитостатическому эффекту вне зависимости от клеточной фазы. На основании результатов исследования 3 фазы AZA-001 — международное, мультицентровое, контролируемое, в параллельных группах, в котором пациенты МДС высокого риска/ОМЛ (ВОЗ критерии) сравнивались со стандартным лечением (сопроводительная терапия, интенсивная химиотерапия, низкие дозы цитарабина), азацитидин был зарегистрирован, в том числе и в РФ, для лечения этих больных. Было показано, что азацитидин в 2,5 раза увеличивает общую выживаемость.
- ↑ 1 2 Monarch Disease Ontology release 2018-06-29sonu — 2018-06-29 — 2018.
- ↑ Гематология / Под редак. О. А. Рукавицына. СПб.: 2007. С. 193—226
- ↑ Corey SJ, Minden MD, Barber DL et al. Myelodysplastic syndromes: the complexicity of stem-cell diseases. Cancer. Nature reviews. 2007. V.7; 118—129
- ↑ Pedersen-Bjergaard J, Pedersen M, Roulston D, Philip P. (1995) Different genetic pathways in leukemogenesis for patients presenting with therapy-related myelodysplasia and therapy-related acute myeloid leukemia. Blood. 86(9): 3542-3552.
- ↑ Greenberg P.L. Apoptosis and its role in the in the myelodysplastic syndromes; implications for disease natural history and treatment. Leuk res, 1998; 22: 1123—1136
- ↑ Onley HJ, Le Beau MM. Cytogenetic Diagnosis of Myelodysplastic syndromes. in book H.J.Deeg, D.T. Bowen, S.D.Gore, T.Haferlach, m.M.Le Beau and C.Niemeyr. Hematologic Malignancies: Myelodysplastic syndromes// Springler Berlin Heidelbery. 2006, P.55-79
- ↑ 1 2 NCCN Clinical Practice Guidelines in oncology. Myelodisplastic syndromes. V.1.2009 (англ.) : journal. Архивировано 31 октября 2010 года.
- ↑ Bennett JM, Catovsky D, Daniel MT, Flandrin G, Galton DA, et al. (1982) Proposals for the classification of the myelodysplastic syndromes. Br.J Haematol. 51(2): 189—199.
- ↑ Brunning R, Bennett J, Flandrin G et al. Myelodysplastic Syndromes. In: Jaffe E, Harris N, Stein H et al, eds. WHO Classification of Tumours. Pathology and Genetics of Haematopoietic and Lymphoid Tissues. Lyon: IARC Press 2001;61-73.
- ↑ Harris N, Jaffe E, Diebold J et al. WHO Classification of Neoplastic Diseases of the Hematopoietic and Lymphoid Tissues: Report of the Clinical Advisory Committee Meeting. J Clin Oncol 1999;17:3835-3849.
- ↑ Vardiman JW, Harris NL, Brunning RD. The World Health Organization (WHO) classification of the myeloid neoplasms. Blood 2002;100:2292-2302.
- ↑ Bruning RD, Orazi A., Germing U. Et al., 2008. WHO classification of tumors of hematopoietic and lymphoid tissues. Chapter 5, pp 88-107
- ↑ Hollstrem Lindberg E., Cazzola M. The role of JAK2 mutations in RARS and other MDS. 2008. Hematology, 52-59
- ↑ Greenberg PL, Baer M, Bennett J et al. NCCN Practice Guidelines for Myelodysplastic Syndromes, Version1, 2001, In “The Complete Library of NCCN Guidelines [CD-ROM], ” Rockledge, PA.
- ↑ Cheson BD, Bennett JM, Kantarjian H et al. Report of an international working group to standardize response criteria for myelodysplastic syndromes. Blood 2000;96:3671-3674.
- ↑ 1 2 Greenberg P., Cox c., Le Beau MM et al., International scoring system for evaluating prognosis in myelodysplastic syndromes. Blood 1997; 89:2079-2088
- ↑ Malcovati L., Germing U., Kuendgen A. Et al. Time-dependant prognostic scoring system for predicting survival and leukemic evolution in myelodysplastic syndromes. J Clin Oncol 2007; 25: 3503-10
- ↑ A WHO Classification-Based Prognostic Scoring System (WPSS) for Predicting Survival in Myelodysplastic Syndromes. Luca Malcovati et al. ASH Annual Meeting Abstracts 2005 106: Abstract 788
- ↑ Scott BL, Sandmaier BM, Storer B et al. Myeloablative vs nonmyeloablative allogeneic transplantation for patients with myelodysplastic syndrome or acute myelogenous leukemia with multilineage dysplasia: a retrospective analysis. Leukemia 2006;20:128-135.
- ↑ Wallen H, Gooley TA, Deeg HJ et al. Ablative allogeneic hematopoietic cell transplantation in adults 60 years of age and older. J Clin Oncol 2005;23:3439-3446.
- ↑ Demuynck H, Verhoef GE, Zachee P et al. Treatment of patients with MDS with allogeneic bone marrow transplantation from genotypically similar HLA-identical sibling and alternative donors. Bone Marrow Transplant 1996;17:745-751.
- ↑ Bowen D. Is traditional low dose chemotherapy (cytarabine/melphalan) still on option? Leukemia Research, Volume 31, Supplement 1, May 2007, Page S19
- ↑ Miller K.B. et al. The evaluation of low-dose cytarabine in the treatment of myelodisplastic syndromes: a phase III intergroup study. Annals of hematology, 1992; 65: 162—168.
- ↑ Burnett A.K., Milligan D., Prentice A.G. et al. A comparison of low-dose cytarabine and hydroxyurea with or without all-trans retinoic for acute myeloid leukemia and high-risk myelodysplastic syndrome in patients not considered fit for intensive treatment. Cancer. 2007. 109: 1114—1124
Образовательный видеоролик в помощь пациентам с миелодиспластическим синдромом
Миелодиспластический синдром – причины, симптомы, диагностика и лечение, прогноз
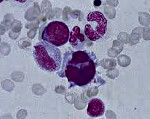
Миелодиспластический синдром – группа гематологических заболеваний, при которых наблюдаются цитопения, диспластические изменения костного мозга и высокий риск возникновения острого лейкоза. Характерные симптомы отсутствуют, выявляются признаки анемии, нейтропении и тромбоцитопении. Диагноз устанавливается с учетом данных лабораторных анализов: полного анализа периферической крови, гистологического и цитологического исследования биоптата и аспирата костного мозга и т. д. Дифференциальный диагноз может представлять значительные затруднения. Лечение – переливание компонентов крови, химиотерапия, иммуносупрессивная терапия, пересадка костного мозга.
Общие сведения
Миелодиспластический синдром – группа заболеваний и состояний с нарушениями миелоидного кроветворения и высоким риском развития острого лейкоза. Вероятность развития увеличивается с возрастом, в 80% случаев данный синдром диагностируется у людей старше 60 лет. Мужчины страдают несколько чаще женщин. У детей миелодиспластический синдром практически не встречается. В последние десятилетия гематологи отмечают увеличение заболеваемости среди лиц трудоспособного возраста. Предполагается, что причиной «омоложения» болезни могло стать существенное ухудшение экологической обстановки.
До недавнего времени лечение миелодиспластического синдрома было только симптоматическим. Сегодня специалисты разрабатывают новые методы терапии, однако эффективное лечение этой группы болезней все еще остается одной из самых сложных проблем современной гематологии. Пока прогноз при миелодиспластическом синдроме, в основном, зависит от особенностей течения болезни, наличия или отсутствия осложнений. Лечение осуществляют специалисты в сфере онкологии и гематологии.

Миелодиспластический синдром
Причины и классификация миелодиспластического синдрома
С учетом причин развития различают два типа миелодиспластического синдрома: первичный (идиопатический) и вторичный. Идиопатический вариант выявляется в 80-90% случаев, диагностируется преимущественно у пациентов старше 60 лет. Причины возникновения установить не удается. В числе факторов риска первичного миелодиспластического синдрома – курение, повышенный уровень радиации при выполнении профессиональных обязанностей или проживании в неблагоприятной экологической зоне, частый контакт с бензином, пестицидами и органическими растворителям, некоторые наследственные и врожденные заболевания (нейрофиброматоз, анемия Фанкони, синдром Дауна).
Вторичный вариант миелодиспластического синдрома наблюдается в 10-20% случаев, может возникать в любом возрасте. Причиной развития становится химиотерапия или радиотерапия по поводу какого-то онкологического заболевания. В число лекарственных средств с доказанной способностью вызывать миелодиспластический синдром включают циклофосфан, подофиллотоксины, антрациклины (доксорубицин) и ингибиторы топоизомеразы (иринотекан, топотекан). Вторичный вариант отличается более высокой резистентностью к лечению, более высоким риском развития острого лейкоза и более неблагоприятным прогнозом.
В современной редакции классификации ВОЗ различают следующие типы миелодиспластического синдрома:
- Рефрактерная анемия. Сохраняется более полугода. В анализе крови бласты отсутствуют либо единичные. В костном мозге дисплазия эритроидного ростка.
- Рефрактерная анемия с кольцевыми сидеробластами. Сохраняется более полугода. В анализе крови бласты отсутствуют. В костном мозге дисплазия эритроидного ростка.
- Рефрактерная цитопения с многолинейной дисплазией. В анализе крови тельца Ауэра отсутствуют, бласты отсутствуют либо единичные, выявляются панцитопения и увеличение количества моноцитов. В костном мозге диспластические изменения менее 10% клеток в 1 миелоидной клеточной линии, бластов менее 5%, телец Ауэра нет.
- Рефрактерная анемия с избытком бластов-1. В анализе крови тельца Ауэра отсутствуют, бластов более 5%, цитопения и увеличение количества моноцитов. В костном мозге дисплазия одной либо нескольких клеточных линий, бластов 5-9%, телец Ауэра нет.
- Рефрактерная анемия с избытком бластов-2. В анализе крови увеличение количества моноцитов, цитопения, бластов 5-19%, могут выявляться тельца Ауэра. В костном мозге дисплазия одной либо нескольких клеточных линий, бластов 10-19%, обнаруживаются тельца Ауэра.
- Неклассифицируемый миелодиспластический синдром. В анализе крови цитопения, бласты отсутствуют либо единичные, тельца Ауэра отсутствуют. В костном мозге дисплазия одного мегакариоцитарного либо гранулоцитарного ростка, бластов более 5%, тельца Ауэра отсутствуют.
- Миелодиспластический синдром, ассоциированный с изолированной делецией 5q. В анализе крови анемия, бластов более 5%, возможен тромбоцитоз. В костном мозге более 5% бластов, тельца Ауэра отсутствуют, изолированная делеция 5q.
Симптомы миелодиспластического синдрома
Клиническая симптоматика определяется степенью нарушений миелопоэза. При мягко протекающих расстройствах возможно длительное бессимптомное или стертое течение. Из-за слабой выраженности клинических проявлений некоторые больные не обращаются к врачам, и миелодиспластический синдром обнаруживается во время проведения очередного медицинского осмотра. При преобладании анемии наблюдаются слабость, одышка, плохая переносимость физических нагрузок, бледность кожных покровов, головокружения и обморочные состояния.
При миелодиспластическом синдроме с тромбоцитопенией возникает повышенная кровоточивость, отмечаются десневые и носовые кровотечения, на коже появляются петехии. Возможны подкожные кровоизлияния и меноррагии. Миелодиспластический синдром с выраженными нейтропенией и агранулоцитозом проявляется частыми простудами, стоматитом, синуситом или стрептодермией. В тяжелых случаях возможно развитие пневмонии или сепсиса. Инфекционные заболевания нередко вызываются грибками, вирусами или условно-патогенными микробами. У каждого пятого пациента с миелодиспластическим синдромом выявляется увеличение лимфоузлов, селезенки и печени.
Диагностика миелодиспластического синдрома
Диагноз выставляется с учетом данных лабораторных исследований: анализа периферической крови, биопсии костного мозга с последующим цитологическим исследованием, цитохимических и цитогенетических тестов. В анализе периферической крови больных миелодиспластическим синдромом обычно обнаруживается панцитопения, реже выявляется дву- или одноростковая цитопения. У 90% пациентов наблюдается нормоцитарная либо макроцитарная анемия, у 60% – нейтропения и лейкопения. У большинства больных миелодиспластическим синдромом отмечается тромбоцитопения.
При исследовании костного мозга количество клеток обычно нормальное либо повышенное. Уже на ранних стадиях обнаруживаются признаки дизэритропоэза. Количество бластов зависит от формы миелодиспластического синдрома, может быть нормальным либо увеличенным. В последующем наблюдаются дисгранулоцитопоэз и дисмегакариоцитопоэз. У некоторых больных признаки дисплазии костного мозга выражены очень слабо. В процессе цитогенетического исследования у ¾ больных выявляются хромосомные нарушения. Дифференциальный диагноз миелодиспластического синдрома проводят с В12-дефицитной анемией, фолиево-дефицитной анемией, апластической анемией, острым миелолейкозом и другими острыми лейкозами.
Лечение и прогноз при миелодиспластическом синдроме
Тактика лечения определяется выраженностью клинической симптоматики и лабораторных изменений. При отсутствии явных признаков анемии, геморрагического синдрома и инфекционных осложнений осуществляется наблюдение. При миелодиспластическом синдроме с выраженной анемией, тромбоцитопенией и нейтропенией, а также при высоком риске возникновения острого лейкоза назначают сопроводительную терапию, химиотерапию и иммуносупрессивную терапию. При необходимости осуществляют пересадку костного мозга.
Сопроводительная терапия является самым распространенным методом лечения миелодиспластического синдрома. Предусматривает внутривенные инфузии компонентов крови. При длительном применении может провоцировать повышение уровня железа, влекущее за собой нарушения деятельности жизненно важных органов, поэтому переливания гемокомпонентов производят при одновременном приеме хелаторов (лекарственных средств, связывающих железо и способствующих его выведению).
Иммуносупрессоры эффективны при лечении миелодиспластического синдрома с отсутствием хромосомных аномалий, наличием гена HLA-DR15 и гипоклеточном костном мозге. Химиотерапию применяют при невозможности трансплантации костного мозга. Высокие дозы препаратов используют при трансформации миелодиспластического синдрома в острый лейкоз, а также при рефрактерных анемиях с избытком бластов при нормоклеточном и гиперклеточном костном мозге, низкие – при невозможности пересадки костного мозга. Наряду с перечисленными средствами пациентам назначают гипометилирующие средства (азацитидин). Наиболее надежным способом достижения полноценной длительной ремиссии является трансплантация костного мозга.
Прогноз зависит от типа миелодиспластического синдрома, количества хромосомных аномалий, необходимости в регулярных переливаниях компонентов крови, выраженности клинических проявлений и наличия осложнений. Различают 5 групп риска. Средняя выживаемость больных миелодиспластическим синдромом, входящих в группу с самым низким уровнем риска, составляет более 11 лет; с самым высоким – около 8 месяцев. Вероятность отторжения костного мозга после трансплантации – около 10%.
Миелодиспластический синдром: развитие, лечение, прогноз

Миелодиспластический синдром (МДС) — тяжелое гематологическое заболевание, которое относится к группе онкопатологий и плохо поддается терапии. В основе недуга лежит нарушение процесса воспроизведения клеток крови: их развития и деления. В результате подобных аномалий образуются онкологические структуры, и формируются незрелые бласты. Постепенно количество нормально функционирующих, зрелых клеток в организме уменьшается. Данный синдром называют «дремлющим лейкозом» из-за скопления в крови бластных клеток.
Костный мозг — важный кроветворный орган, в котором происходят процессы образования, развития и созревания клеток крови, то есть осуществляется гемопоэз. Этот орган также принимает участие в иммунопоэзе — процессе созревания иммунокомпетентных клеток. У взрослого человека в костном мозге содержатся незрелые, недифференцированные и низкодифференцированные клетки – стволовые.

Большинство заболеваний костного мозга обусловлены мутацией стволовой клетки крови и нарушением ее дифференциации. МДС не является исключением. Расстройство кроветворения приводит к развитию острого лейкоза. Причина первичного МДС неизвестна. Мутагенные факторы оказывают негативное воздействие на стволовую клетку крови, что приводит к нарушению ДНК и выработке в костном мозге аномальных клеток, постепенно вытесняющих нормальные. Вторичный синдром развивается в результате длительного лечения цитостатиками, при частом контактировании с химическими веществами, в следствии облучения. Заболевание чаще развивается у пожилых лиц старше 60 лет, чаще у мужчин. Раньше среди детей синдром практически не встречался. В настоящее время недуг «помолодел». Все чаще случаи МДС наблюдаются у больных среднего возраста, что связано с экологическими проблемами крупных городов. Миелодиспластический синдром имеет код по МКБ-10 D46.
Цитопения — клиническое проявление патологий системы кроветворения. Симптоматика недуга определяется поражением определенной клеточной линии. У больных возникает слабость, утомляемость, бледность, головокружение, лихорадка, кровоточивость, кровоизлияния. Специфические признаки при этом отсутствуют. Диагностика патологии основывается на результатах гемограммы и гистологического исследования биоптата костного мозга. Лечение заключается в переливании основных компонентов крови, проведении химиотерапии, иммуносупрессивной терапии и пересадке костного мозга.

цитопения с нарушением созревания клеток крови по нескольким росткам
Эффективное лечение МДС – одна из самых сложных проблем современной медицины. Его проводят специалисты в области онкогематологии. Синдром в запущенных случаях приводит к онкологии. Но так происходит не всегда. Легкие формы недуга типа рефракционной анемии обычно не заканчиваются формированием рака. Недостаток клеток крови приводит к анемии, кровоточивости, сердечной дисфункции, увеличению риска развития инфекционных заболеваний. Прогноз МДС определяется особенностями течения патологического процесса, своевременностью диагностических и общетерапевтических мероприятий. Своевременная терапия – единственный реальный шанс сохранить и продлить жизнь больных.
Этиология и патогенез
Гемопоэз – процесс кроветворения, который заключается в образовании и созревании клеток крови. Он происходит непрерывно, что связано с коротким сроком жизни клеток: от нескольких дней до 3-4 месяцев. Ежедневно в живом организме синтезируется огромное количество новых кровяных телец из клеток-предшественников. В процессе миелопоэза образуются миелоидные клетки – эритроцитарные, лейкоцитарные и тромбоцитарные клеточные элементы. Под воздействием негативных экзогенных и эндогенных факторов в костном мозге происходят патологические изменения, возникает расстройство кроветворения.

Этиология и патогенез МДС в настоящее время полностью не изучены. Ученые установили факторы, провоцирующие развитие патологии:
- загрязнения окружающей среды,
- радиоактивное излучение,
- табакокурение,
- опасные и вредные производственные факторы,
- контакты с агрессивными веществами,
- длительное проведение иммуносупрессивной терапии,
- врожденные генетические заболевания.
Первичный или идиопатический синдром — недуг невыясненной этиологии, который развивается в 80% случаев у лиц в возрасте 60-65 лет.
Вторичный синдром обусловлен воздействием на организм химиотерапевтических препаратов или лучевой терапии. Эта форма обычно развивается у молодых людей, быстро прогрессирует, отличается высокой устойчивостью к лечению и максимальным риском развития острого лейкоза.
В костном мозге вырабатываются все клеточные элементы крови. Там они находятся в незрелом состоянии, то есть являются предшественниками зрелых форм. По мере необходимости каждая из них превращается в полноценные клетки и выполняет жизненно важные функции, от которых зависит процесс дыхания, гемостаз, иммунная защита. При МДС стволовые клетки погибают до выхода в кровяное русло и не достигают своей функциональной зрелости. Это приводит к дефициту нормальных клеточных форм в крови и нарушению их функций, связанному с клеточной дисплазией.
МДС часто называют тлеющей лейкемией или предлейкозом, обусловленном генной мутацией стволовых клеток. Клональная пролиферация эритроидных, миелоидных и мегакариоцитарных форм приводит к неэффективному гемопоэзу и панцитопении. В костном мозге и крови происходят характерные морфологические изменения, обусловленные аномальной клеточной продукцией. У больных увеличивается печень и селезенка. Нестабильность синдрома обусловлена тенденцией к переходу в острый миелобластный лейкоз.
Симптоматические проявления
МДС не имеет специфической симптоматики. Его клинические проявления определяются степенью тяжести и формой недуга.
 Анемический синдром — постоянный и обязательный признак патологии. Для него характерны гиперхромия и макроцитоз. Большой размер эритроцитов и их интенсивное окрашивание, зависящее от повышенного содержания гемоглобина, – признаки анемии при МДС и остром лейкозе. При анемии больные быстро утомляются, плохо переносят физические нагрузки, жалуются на головокружение, одышку, боль в груди, костях и суставах, невозможность сосредоточится. Их кожа становится бледной, ухудшается аппетит, снижается вес и работоспособность, возникает нервозность, цефалгия, дрожь в теле, шум в ушах, сонливость, тахикардия, обмороки. Плохо переносят анемию престарелые больные, а также лица с сердечно-легочной патологией. У них могут развиться тяжелые последствия – стенокардия, инфаркт миокарда, аритмии.
Анемический синдром — постоянный и обязательный признак патологии. Для него характерны гиперхромия и макроцитоз. Большой размер эритроцитов и их интенсивное окрашивание, зависящее от повышенного содержания гемоглобина, – признаки анемии при МДС и остром лейкозе. При анемии больные быстро утомляются, плохо переносят физические нагрузки, жалуются на головокружение, одышку, боль в груди, костях и суставах, невозможность сосредоточится. Их кожа становится бледной, ухудшается аппетит, снижается вес и работоспособность, возникает нервозность, цефалгия, дрожь в теле, шум в ушах, сонливость, тахикардия, обмороки. Плохо переносят анемию престарелые больные, а также лица с сердечно-легочной патологией. У них могут развиться тяжелые последствия – стенокардия, инфаркт миокарда, аритмии.- Нейтропения характеризуется лихорадкой, снижением сопротивляемости организма к патогенным биологическим агентам, частым развитием инфекционных заболеваний бактериальной и вирусной этиологии. У больных повышается температура тела, потливость, возникает слабость, увеличиваются лимфоузлы. Сепсис и пневмония у таких пациентов часто заканчиваются летальным исходом.
- При тромбоцитопении кровоточат десна, появляются гематомы и петехии, часто течет кровь из носа, возникают длительные кровотечения после мелких хирургических вмешательств и различных инвазивных манипуляций. Возможно развитие внутренних кровотечений, меноррагий, кровоизлияний в головной мозг. Массивная потеря крови часто становится причиной смерти пациентов.
- У больных возникает лимфаденит, гепатомегалия, спленомегалия, специфическое поражение кожи — лейкемиды.
МДС долгое время может протекать бессимптомно или иметь стертое течение. Больные часто не обращают внимание на слабовыраженные клинические проявления и не посещают своевременно врача. Обычно МДС обнаруживают случайно во время проведения очередного медосмотра.
Диагностика
Диагноз МДС ставят после проведения лабораторного исследования периферической крови и гистологического исследования биоптата костного мозга. Специалисты изучают образ жизни больного, его анамнез, наличие профессиональных вредностей.

наиболее достоверный диагностический метод – трепанбиопсия костного мозга
Диагностические методы при МДС:
- гемограмма — анемия, лейкопения, нейтропения, моноцитоз; панцитопения – абсолютное показание для цитологического исследования костного мозга;
- биохимия крови – определение уровня железа, фолиевой кислоты, эритропоэтина, ЛДГ и АСТ, АЛТ, щелочной фосфатазы, мочевины;
- иммунограмма – специальный комплексный анализ, позволяющий определить, в каком состоянии находится иммунная система;
- гистология костного мозга выявляет деструкцию ткани, очаги поражения, наличие аномальных клеток, дисбаланс кроветворной и жировой ткани, гиперплазию всех ростков кроветворения, признаки дисплазии клеток;

- цитохимическое исследование – нарушение обмена микроэлементов и витаминов: щелочной фосфатазы в лейкоцитах, миелопероксидазы, железа;
- цитогенетический анализ – выявление хромосомных аномалий;
- дополнительные инструментальные исследования, позволяющие оценить состояние внутренних органов — УЗИ, КТ и МРТ.
Только после полноценной диагностики и постановки правильного диагноза можно переходить к лечению недуга.
Лечение
Интенсивное лечение МДС заключается в применении целого комплекса мероприятий. В тяжелых случаях медикаментозную терапию проводят в условиях стационара. Больные с более легкими формами синдрома лечатся амбулаторно или на дневном стационаре. Основными среди общетерапевтических мероприятий являются химиотерапия и иммуносупрессивные методики. Трансплантация костного мозга проводится при тяжелом течении болезни и повышает шансы больных на выздоровление.

Лечение МДС проводится с целю нормализации показателей периферической крови, устранения симптомов патологии, предупреждения трансформации недуга в острый лейкоз, улучшения и продления жизни больных.
Симптоматическая терапия направлена на устранение клинических проявлений синдрома и сопутствующих заболеваний, осложняющих течение основного недуга.
- Внутривенное капельное введение кровяных ингредиентов – тромбоконцентрата или эритроцитарной массы. Тромбоцитарную массу переливают редко.
- Для профилактики гемосидероза – «Дисферал».
- Иммуносупрессоры – «Леналидомид», антитимоцитарный и антилимфоцитарный глобулин, «Циклоспорин А», комбинации глюкокортикоидов.
- Химиотерапевтические средства – «Цитарабин», «Дакоген», «Мельфалан».
- Препараты-стимуляторы эритропоэза — железосодержащие препараты: «Ферроплекс», «Фенюльс», «Сорбифер дурулес»; препараты витаминов: «Цианкобаламин», «Фолиевая кислота»; анаболики-стероиды: «Анаполон», «Нандролон»; препараты эритропоэтина: «Эральфон», «Эпокомб»
- Стимуляторы лейкопоэза – «Нейпоген», «Лейкоген», «Метилурацил», «Интерлейкин».
- Ингибирование апоптоза – естественной гибели клеток – «Сандиммун», «Весаноид».
- Ингибиторы развития кровеносных сосудов – «Талидамид», «Ревлимид».
- Гипометилирующие средства – «Азацитидин».
- При развитии инфекционных осложнений — антибиотики и антимикотики.
Схема лечения и дозировка препаратов зависят от возраста пациента, степени тяжести заболевания и общего состояния здоровья. Эффективность медикаментозной терапии достаточно низкая и непродолжительная. Единственный способ спасти больного — выполнить пересадку костного мозга. В тяжелых случаях также проводят трансплантацию стволовых клеток. Несмотря на свою эффективность, эти способы лечения имеют много недостатков: являются дорогостоящими, имеют высокую вероятность отторжения трансплантата, требуют дополнительной подготовки пациента к операции, вызывают трудности в поиске подходящего донора.
В настоящее время развитие генной инженерии и культивирование клеток крови достигли нового уровня. С их помощью процесс кроветворения можно регулировать. Специалисты определяют сколько клеток недовырабатывается индивидуально у каждого больного, а затем переходят непосредственно к лечению.
С помощью любого из вышеперечисленных методов можно добиться полной ремиссии синдрома.
Профилактика
Специфической профилактики синдрома не существует. Профилактические мероприятия, не допускающие ухудшения состояния больных и предупреждающие трансформацию синдрома в лейкоз:
- укрепление иммунитета,
- сбалансированное питание,
- поддержание гемоглобина на оптимальном уровне,
- частые прогулки на свежем воздухе,
- своевременное обращение к врачу при появлении первых признаков синдрома,
- периодическая сдача анализов и прохождение необходимых исследований,
- гигиена кожи,
- защита от контактов с химическими веществами,
- защита от радиации,
- ограничение активной физической нагрузки,
- своевременное лечение простудных и инфекционных заболеваний.
Прогноз
Прогноз МДС неоднозначный. Он зависит от тяжести патологии и своевременности лечения. Продолжительность жизни при легких формах синдрома составляет 15 лет, при наличии тяжелого течения недуга она не превышает 10 месяцев. При отсутствии или неэффективности лечения МДС трансформируется в острый лейкоз. Адекватная терапия обеспечивает максимальное продление жизни. Наблюдение за больными, имеющими стертую клиническую картину и относительно благоприятное течение недуга, осуществляют постоянно, даже в период стабильных показателей крови и костного мозга.
У пожилых людей синдром протекает особенно тяжело и плохо лечится. Это связано с наличием у них хронических заболеваний и подавлением иммунитета. Их организм не справляется, и процесс выздоровления затягивается.
Видео: базовая информация о миелодиспластическом синдроме
Миелодиспластический синдром – это… Что такое Миелодиспластический синдром?
Миелодиспластический синдром (МДС) — группа гетерогенных клональных заболеваний, характеризующаяся наличием цитопении в периферической крови, дисплазии в костном мозге и риском трансформации в острый лейкоз.
МДС сегодня является одной из самых сложных проблем гематологии. Лишь недавно лечение МДС вышло за рамки поддерживающей терапии, проводившейся с целью облегчения симптомов.
МДС — это патология старшей возрастной группы. 80 % случаев МДС приходится на лица старше 60 лет. МДС в детском возрасте встречается крайне редко. В европейских странах среди лиц 50-69 лет регистрируется 40 новых случаев МДС на 1 млн населения, а среди лиц 70 лет и старше — 150 новых случаев на 1 млн населения. Заболеваемость МДС в РФ в среднем составляет 3-4 случая на 100 тыс. населения в год и увеличивается с возрастом.[1]
Типы, факторы риска
Первичный (идиоптический) тип — 80-90 % случаев, вторичный (вследствие предшествующей химиотерапии и др. факторов) — 10-20 %. Большинство (80 %) случаев МДС являются первичными — идиопатическими или de novo (лат. — вновь появившийся, новый).
Вторичный МДС является значительно более неблагоприятным и резистентным к лечению типом МДС, обладающим заведомо более худшим прогнозом в сравнении с первичным МДС. 10-20 % случаев МДС возникают вследствие предшествующей химиотерапии по поводу других новообразований. К препаратам, обладающим доказанной способностью повреждать геном с последующим развитием МДС, относятся алкилирующие агенты (циклофосфан), ингибиторы, топоизомеразы — противоопухолевые агенты растительного происхождения (топотекан, иринотекан и др.), антрациклины (доксорубицин) и подофиллотоксины (этопозид). К МДС также могут приводить радиотерапия и контакт с токсическими материалами.
- Факторы риска, первичный МДС
- Факторы риска, вторичный МДС
Предшествующая химиотерапия онкологического заболевания или после ТКМ.
Прогноз: 5-летняя выживаемость при МДС не превышает 60 %. Трансформация в острый лейкоз ~30 % случаев.[2][3]
Патогенез
Причины МДС до конца не известны. В основе патогенеза МДС лежит воздействие повреждающих факторов на полипотентную стволовую клетку, приводящее к появлению в ней генетических аномалий, а также феномена гиперметилирование ДНК.
Указанные нарушения приводят к нарушению продукции клеток миелоидного ростка и появлению миелобласты в костном мозге и периферической крови, вследствие чего появляются диспластические изменения в зрелых клетках и их функциональная недостаточность, приводящие к описанным клиническим проявлениям.
Феномен гиперклеточности костного мозга на фоне периферической цитопении объясняется ускоренным апоптозом аномально пролиферирующих клеток костного мозга.[4]
Клиническая картина
МДС отличает отсутствие типичной клинической картины. Симптоматику МДС составляют последствия дисмиелопоэза, то есть цитопении: анемия, нейтропения и тромбоцитопения (анемия Hb меньше 110 г/л, нейтрофилы меньше 1,800 на 1 микролитр крови; гематокрит меньше 36 % эритроцитов в общем объёме крови в организме; тромбоциты меньше 100,000 на 1 микролитр крови).
Наиболее часто МДС манифестирует цитопениями, главным образом анемией. При этом необходимо дифференцировать МДС от железа или B12- дефицитной анемии, постгеморрагической анемии, анемии при хронических заболеваниях и онкологии или связанной с хронической почечной недостаточностью, а также апластической анемией, пароксизмальной ночной гемоглобинурией. У 10 % пациентов имеются признаки инфекции, а у несколько меньшей доли пациентов болезнь проявляется кровотечениями.
В связи с этим диагностика МДС базируется исключительно на лабораторно-инструментальных методах, из которых ключевыми являются полный клинический анализ периферической крови, некоторые биохимические исследования и морфологический анализ аспиратов и биоптатов костного мозга.
Дифференциальная диагностика МДС также затруднена в силу множества состояний, имеющих общие с МДС клинико-лабораторные проявления.
План обследования пациентов
Для анализа изменений в периферической крови проводится полный, с подсчетом ретикулоцитов (ускоренный эритропоэз с макроцитозом в ответ на гемолиз и острую кровопотерю приводит к увеличению ретикулоцитов), тромбоцитов, лейкоцитов и клинического анализа крови. Типичными находками являются изменения формы клеток, патологические включения и уменьшение числа клеток одного или нескольких ростков кроветворения.
Другим ключевым с точки зрения диагностики МДС оценки прогноза и выработки тактики лечения больных исследованием является морфологическое, иммуногистохимическое и цитогенетическое исследования ткани костного мозга. Исследование костномозгового пунктата в этом отношении является несравненно более информативным, чем определение морфологического состава периферической крови.
Используются два способа получения материала: 1) аспирационная биопсия костного мозга и 2) трепанобиопсия из гребня подвздошной кости.
При цитологическом исследовании костного мозга (миелограмма) можно оценить наличие дисплазии миелоидного ростка.
Дизэритропоэз: многоядерность Костный мозг больного рефрактерной сидеробластной анемией: кольцевые сидеробласты- Дизэритропоз
Ядро
- Межъядерные цитоплазматические мостики
- Кариорексис
- Многоядерность
- Баббл-формы
- Мегалобластоидность
Цитоплазма
- Кольцевидные сидеробласты
- Вакуолизация
- Положительная реакция с Шифф-йодной кислотой
- Дисгранулопоэз
- Маленькие или чрезмерно большие клетки
- Гиполобулярность ядер (псевдо-Пельгер-Хюит аномалия)
- Неравномерная гиперсегментация
- Гипо-/агрануляция
- Гранулы псевдо Чедиак-Хагаси
- Палочки Ауэра
- Дисмегакариопоэз
- Микромегакариоциты
- Гиполобулярные ядра
- Многоядерность
Гистологическое исследование костного мозга (трепанобиопсия) позволяет оценить архитектонику костного мозга, диффузный или очаговый характер изменений в нём, изучить соотношение кроветворной и жировой ткани, выявить атипичные клетки и т. п. Аспирация костного мозга при стернальной пункции так или иначе нарушает структуру костного мозга и не исключает примешивание к пунктату периферической крови. В связи с этим выполнение трепанобиопсии обязательно для подтверждения диагноза МДС.
Биохимические исследования обмена железа, содержания витамина В12 и фолиевой кислоты, иммунологические пробы призваны помочь провести дифференциальную диагностику с анемиями иного генеза, с учётом того, что у 80 % пациентов с МДС отмечается анемия.
МДС следует дифференцировать с другими онкогематологическими заболеваниями, включая острые и хронические лейкозы, а также лимфопролиферативные заболевания.
Часть изменений, свойственных МДС (в частности, моноцитоз, цитопенические нарушения), могут отмечаться при некоторых инфекционных процессах.
При отравлении тяжелыми металлами могут отмечаться изменения эритроцитарного ростка, сходные с таковыми при сидеробластных анемиях.
У пациентов с наследственными цитопениями рекомендуется проведение дополнительного генетического исследования, которое поможет выявить анемию Фанкони и врожденный дискератоз.
Цитогенетические нарушения
 Повторяющиеся хромосомные аномалии при MDS
Повторяющиеся хромосомные аномалии при MDSПри диагностике хромосомные аномалии обнаруживаются у 40-70 % пациентов с первичным MDS и у 95 % пациентов, MDS которых связан с терапией (вторичный).
К наиболее часто встречающимся при MDS цитогенетическим аномалиям относятся del(5q), −7 и +8.[5]
| Группа риска | Кариотип (22 группы) | Средняя выживаемость (мес) | Время, к которому 25 % пациентов развили ОМЛ |
|---|---|---|---|
| Благоприятная | 5q-, 12p-, 20q-, +21, -Y, 11q-, t(11(q23)), норма; любые 2 аномалии, включающие 5q- | 51 | 71,9 |
| Промежуточная-1 | +1q, аномалии 3q21/q26, +8, t(7q), +19, −21, любая др. одиночная поломка; любые двойные аномалии, не затрагивающие хр. 5q и 7 | 29 | 16 |
| Промежуточная-2 | -X, −7 или 7q-, любые двойные аномалии с −7 or 7q-, комплекс из 3х аномалий | 15,6 | 6 |
| Неблагоприятная | Более 3х аномалий | 5,9 | 2,8 |
Минимальные диагностические критерии
Минимальные диагностические критерии МДС включают обязательные диагностические условия (цитир. По NCCN, 2009)[6] — стабильная цитопения не менее 6 месяцев, (за исключением случаев, когда цитопения сопровождается специфическим кариотипом или дисплазией двух ростков кроветворения — в этих случаях длительность стабильной цитопении должна составлять не менее 2 месяцев).
- исключение других заболеваний, которые могут стать причиной развития дисплазии или/и цитопении.
В дополнение к этим двум диагностическим условиям для установления диагноза МДС необходимо соответствие хотя бы одному из трех основных критериев:
- дисплазия (≥ 10 % клеток одного или более из трех основных ростков кроветворения в костном мозге).
- содержание бластов в костном мозге 5-19 %.
- специфический кариотип, например делеция (5q), делеция (20q), +8 или −7/делеция (7q).
Кроме того, для диагностики МДС используются дополнительные критерии, в том числе результаты проточной цитометрии, гистологического и иммуногистохимического исследования костного мозга, выявления молекулярных маркеров.
Морфологическое исследование биоптатов, полученных путем билатеральной трепанобиопсии, является полезным, помимо верификации диагноза самого МДС, с точки зрения дифференциальной диагностики с лимфопролиферативными и другими миелопролиферативными заболеваниями.[6]
Дифференциальная диагностика
Дифференциальная диагностика проводится с:
- А. Мегалобластными анемиями (заболевания, характеризующиеся изменениями морфологии клеток к.м. вследствие нарушения синтеза ДНК. Более 90 % — В-12 и фолиево-дефицитные анемии).
После начала терапии витамином В-12 или фолиевой кислотой в анализе крови выявляется ретикулярный криз на 5-7 сутки и повышение показателей красной крови, что нехарактерно для больных рефрактерной анемией. Изменения кариотипа клеток костного мозга не встречаются при мегалобластных анемиях.
Апластическая анемия может быть врожденной, приобретенной и идиопатической. Врожденная апластическая анемия — анемия Фанкони сочетается с другими генетическими аномалиями (кожная пигментация, гипоплазия почек, микроцефалия), приобретенная связана с действием химических и физических агентов, инфекциями, нарушениями обмена веществ.
Для АА нехарактерны изменение кариотипа, гиперклеточный костный мозг.
- В. Анемии при ХПН.
- В. Анемии при хроническом активном гепатите характерно выявление маркеров вирусных инфекций, гепатоспленомегалия, клиническая картина хр. гепатита, изменения биохимических показателей крови (метаболизма билирубина, функции печени).
ФАБ-классификация
Разработка этой системы классификации франко-американо-британской группой была начата в 1976 году и позже, в 1982 году, она приняла свой окончательный вид.
В основе классификации лежит ключевой для МДС синдром — рефрактерная, то есть устойчивая к лечению препаратами витамина В12 и фолиевой кислоты, анемия (РА). Четыре типа РА являются последовательными стадиями, с нарастанием тяжести МДС, что имеет свое отражение в прогнозе выживаемости. В этой связи появление в КМ бластов резко меняет прогноз выживаемости в худшую сторону.
| Тип МДС | Бластов в периферической крови | Бластов в КМ | Другие патологические изменения | Выживаемость (лет) |
|---|---|---|---|---|
| Рефрактерная анемия (РА) | меньше 1 % | меньше 15 % кольцевых сидеробластов | меньше 5 % | 4,2 |
| РА с кольцевыми сидеробластами | меньше 1 % | больше 15 % кольцевых сидеробластов | меньше 5 % | 6,9 |
| РА с избытком бластов (РАИБ) | меньше 5 % | 5-20 % | — | 1,5 |
| РАИБ в стадии трансформации | больше 5 % | 21-29 % | Возможно наличие палочек Ауэра в КМ | 0,6 |
| ХММЛ | меньше 5 % | меньше 20 % | Моноциты больше 1х109/л | 2,4 |
Французско-американско-британская классификация позволяет отнести пациента к той или иной группе миелодиспластических синдромов в зависимости от морфологических показателей. Группа миелодиспластических синдромов включает пять заболеваний: рефрактерную анемию, рефрактерную анемию с кольцевыми сидеробластами, рефрактерную анемию с избыточным количеством бластов, рефрактерную анемию с избыточным количеством бластов на стадии трансформации и хронический миеломоноцитарный лейкоз. Согласно французско-американско-британской номенклатуре пациентам, у которых содержание бластов в костном мозге превышает 30 %, устанавливается диагноз острого миелоидного лейкоза.
В данной классификации хронический миеломоноцитарный лейкоз относится к группе миелодиспластических синдромов, несмотря на то, что это заболевание часто характеризуется признаками миелопролиферативного расстройства.[7]
Классификация ВОЗ
В 2002 году Всемирная организация здравоохранения предложила новую классификацию миелодиспластических синдромов[8][9][10] в 2008 году были сделаны предложения по её пересмотру.[11][12]
Подгруппы, выделяемые в классификации ВОЗ включают: рефрактерную анемию и рефрактерную анемию с кольцевыми сидеробластами, рефрактерную цитопению с множественной дисплазией, рефрактерную анемию с избыточным количеством бластов-1 (содержание бластов в костном мозге составляет менее 10 %), рефрактерную анемию с избыточным количеством бластов-2 (содержание бластов в костном мозге превышает 10 %), синдром делеции 5q и миелодиспластический синдром неклассифицированный (с наличием или отсутствием кольцевых сидеробластов).
Пациенты, ранее классифицировавшиеся как страдающие хроническим миеломоноцитарным лейкозом, относятся к группе миелодиспластических синдромов/миелопролиферативных заболеваний.
Синдром делеции 5q, выделяемый в классификации Всемирной организации здравоохранения в отдельную подгруппу, характеризуется изолированной делецией 5q[13][14][15] и содержанием бластов в костном мозге меньше 5 %, часто в сочетании с тромбоцитозом.
| Тип МДС | Изменения в крови | Изменения в КМ |
|---|---|---|
| Рефрактерная анемия (РА) | Анемия, меньше 1 % бластов | Дисплазия эритроидного ростка, меньше 5 % бластов |
| Рефрактерная анемия с кольцевыми сидеробластами (РАКС) | То же, что и РА | то же, что и РА, ≥ 15 % кольцевых сидеробластов |
| Рефрактерная цитопения с многоростковой дисплазией (РЦМД) | Цитопения по 2-3 росткам, меньше 1 % бластов | Дисплазия в больше 10 % клеток 2 или 3 ростков, меньше 5 % бластов, меньше 15 % кольцевых сидеробластов |
| Рефрактерная цитопения с мультилинейной дисплазией и кольцевыми сидеробластами (РЦМД-КС) | То же, что и РЦМД | То же, что и РЦМД, ≥ 15 % кольцевых сидеробластов |
| Рефрактерная анемия с избытком бластов, тип I (РАИБ-1) | Цитопении, меньше 5 % бластов | 5-9 % бластов |
| Рефрактерная анемия с избытком бластов, тип II (РАИБ-2) | Цитопении, 5-19 % бластов | 10-19 % бластов |
| Синдром 5q- | Анемия, нормальное или повышенное содержание тромбоцитов | Нормальное или увеличенное количество мегакариоцитов с гипосегментированными ядрами; изолированная делеция 5q31 |
| МДС неклассифицированный (МДС-Н) | Цитопения | Унилинейная дисплазия в нейтрофильном или мегакариоцитарном ростках, Бласты менее 5 %, Палочки Ауэра отсутствуют |
Всемирная организация здравоохранения предложила исключить рефрактерную анемию с избыточным количеством бластов на стадии трансформации из группы миелодиспластических синдромов (диагноз острого миелоидного лейкоза устанавливается, если содержание бластов в костном мозге превышает 20 %, тогда как ранее для установления этого диагноза содержание бластов должно было превышать 30 %). Однако миелодиспластические синдромы отличаются от вновь диагностированного острого миелоидного лейкоза не только содержанием бластов, но и течением заболевания, обусловленным определенными биологическими свойствами. Кроме того, эти группы заболеваний обычно отличаются и по частоте терапевтических ответов.
Шкала IPSS
Шкала IPSS (International Scoring Prognostic System — Международная шкала оценки прогноза) была разработана в 1997 году с целью дать специалистам, помимо классификации, практический инструмент по оценке прогноза и выбора тактики лечения для пациентов с впервые установленным диагнозом МДС (то есть не подходит для прогноза уже леченных пациентов с МДС).
Вторичный МДС оценивается как изначально неблагоприятный, автоматически попадающий в категорию наиболее высокого риска согласно IPSS.
Тремя факторами, которые учитывает IPSS для оценки прогноза, являются количество бластов, категория цитогенетического риска и количество пораженных цитопенией линий.
Трактовка результатов суммирования баллов по этим трем параметрам представлена в таблице:[15]
| Количество балов | ||||||
|---|---|---|---|---|---|---|
| Прогностический фактор | 0 | 0,5 | 1,0 | 1,5 | 2,0 | |
| Бласты в костном мозге | меньше 5 % | 5-10 % | — | 11-20 % | 21-30 % | |
| Прогноз с учётом характеристик кариотипа | Хороший (норма, del(5q) del(20q) -Y) | Промежуточный (+8 хромосома, 2 аномалии и др.) | Плохой (аномалии 7 хромосомы, ≥ 3 аномалии) | — | — | |
| Цитопения (количество пораженных линий) | 0/1 | 2/3 | — | — | — | |
Прогноз у пациентов
Сумма баллов, соответствующая высокому риску по IPSS (больше 2,5) складывается из мультилинейной дисплазии, плохого цитогенетического прогноза и высокого бластоза, на грани перехода в ОМЛ (срок трансформации в который в категории высокого риска составляет всего 2 месяца).
Категория промежуточного-2 риска также складывается из выраженного цитопенического синдрома и высокого, в пределах 10-20 % бластоза.
То, что в категории низкого риска медиана общей выживаемости ниже срока перехода в ОМЛ, объясняется меньшим сроком жизни больных с МДС, что отражает последствия осложнений цитопенического синдрома.[16]
| Сумма баллов | Риск по IPSS | Срок до перехода в ОМЛ у 25 % пациентов (лет) | Медиана общей выживаемости (лет) | % Пациентов |
|---|---|---|---|---|
| 0 | Низкий | 9,4 | 5,7 | 31 % |
| 0,5-1,0 | Промежуточный-1 | 3,3 | 3,5 | 39 % |
| 1,5-2,0 | Промежуточный-2 | 1,1 | 1,2 | 22 % |
| ≥ 2,5 | Высокий | 0,2 | 0,4 | 8 % |
Прогностическая система ВОЗ (WPSS)
| Баллы | 0 | 1 | 2 | 3 |
|---|---|---|---|---|
| Вид МДС по классификации ВОЗ | РА, РАКС, 5q- | РЦМД, РЦМД-КС | РАИБ1 | РАИБ2 |
| Кариотип | Хороший | Средний | Плохой | — |
| Потребность в гемотрансфузиях | Нет | Регулярная | — | — |
Кариотип:
- Хороший: нормальный, -Y, del 5q, del 20q
- Плохой: более 3х аномалий или аномалии 7 хромосомы
- Средний: все другие
Регулярные гемотрансфузии — переливание минимум 1 ЭМ каждые 8 недель в течение 4 месяцев.
| Группа риска | Баллы | Медиана выживаемости (мес) |
|---|---|---|
| Очень низкий | 0 | 136 |
| Низкий | 1 | 63 |
| Средний | 2 | 44 |
| Высокий | 3-4 | 19 |
| Очень высокий | 5-6 | 8 |
Методы лечения
Не все пациенты с МДС нуждаются в терапии. Пациенты без анемического, геморрагического синдрома, инфекционных осложнений могут наблюдаться и не получать лечения (тактика «watch and wait»).
Выбор терапевтической тактики во многом определятся возрастом пациента, соматическим статусом, степенью риска по шкале IPSS, WPSS, наличием совместимого донора.
Можно выделить следующие направления терапии МДС:
- Сопроводительная терапия включает в себя переливание различных гемокомпонентов (эритроцитарной массы, тромбоконцентрата), терапию эритропоэтином, тромбопоэтином. У больных часто получающих гемотрансфузии развивается перегрузка организма железом. Железо обладает токсическим действием на различные ткани и органы, в первую очередь сердце, печень, поэтому такие пациенты должны получать препараты, связывающие железо — хелаторы (десферал, эксиджад).
- Иммуносупрессивная терапия наиболее эффективна у пациентов с гипоклеточным костным мозгом, нормальным кариотипом и наличием HLA-DR15. Леналидомид, обладающий иммуномодулирующим и антиангиогенным действием, показал свою эффективность у трети пациентов с рефрактерной анемией (согласно критериям ВОЗ) и низким риском (по IPSS), а также у больных с 5q- синдромом. Эффективность лечения в данном случае весьма высока; 95 % больных достигают цитогенетической ремиссии.
Пациентам с МДС моложе 65 лет, с хорошим соматическим статусом, при наличии HLA-совместимого донора показано проведение аллогенной трансплантации костного мозга, так как трансплантация является потенциально радикальным методом лечения МДС.
- Цитарабин, низкие дозы. Широко используются в России, да и во всей Европе, для лечения пациентов с МДС и ОМЛ, которым не подходит терапия методом ТКМ или применение интенсивной химиотерапии.
Мнения исследователей относительно целесообразности использования низкоинтенсивной терапии расходятся. Bowen D[21] считает, что нет оснований рекомендовать её рутинное использование при МДС: было выполнено 3 рандомизированных крупных исследования (141 пац.), которые показали, что применение низких доз цитарабина не увеличивает продолжительность жизни пациентов с МДС.[22] Вместе с тем, в более позднем исследовании у пациентов с ОМЛ и МДС высокого риска[23] было показано, что продолжительность жизни у больных, у которых применялся LDAC более, чем в 1 цикле, выше, чем при поддерживающей терапии.
Таким образом, необходимость в низкоинтенсивной терапии с доказанной эффективностью и лучшей переносимостью, чем LDAC, которая будет способствовать увеличению выживаемости пациентов с МДС высокого риска, остается актуальной.
- Высокодозная химиотерапия используется у больных с РАИБ с гипер- и нормоклеточным костным, при трансформации в ОМЛ. Пятилетняя выживаемость составляет около 18 %.
- Гипометилирующие препараты
Новые многообещающие терапевтические подходы, широко обсуждающиеся в последнее время, по поводу которых проводятся многочисленные клинические исследования, возникли в результате глубокого изучения биологии МДС. Среди них следует отметить ингибиторы метилирования ДНК (5-азацитидин, децитабин) и иммуномодулятор — леналидомид. 5-азацитидин обладает двойным механизмом действия. Он встраивается не только в молекулу ДНК, но и в молекулу РНК. В процессе метилирования ДНК гипометилирующие агенты ковалентно связываются с ДНК-метилтрансферазой, что приводит к реактивации генов, после чего восстанавливается дифференцировка гемопоэтических клеток-предшественников и нормальное кроветворение. Азацитидин, встраиваясь в РНК молекулу, тем самым понижает её количество в клетках, что приводит к цитостатическому эффекту вне зависимости от клеточной фазы. На основании результатов исследования 3 фазы AZA-001 — международное, мультицентровое, контролируемое, в параллельных группах, в котором пациенты МДС высокого риска/ОМЛ (ВОЗ критерии) сравнивались со стандартным лечением (сопроводительная терапия, интенсивная химиотерапия, низкие дозы цитарабина), азацитидин был зарегистрирован, в том числе и в РФ, для лечения этих больных. Было показано, что азацитидин в 2,5 раза увеличивает общую выживаемость.
Примечания
- ↑ Гематология / Под редак. О. А. Рукавицына. СПб.: 2007. С. 193—226
- ↑ Corey SJ, Minden MD, Barber DL et al. Myelodysplastic syndromes: the complexicity of stem-cell diseases. Cancer. Nature reviews. 2007. V.7; 118—129
- ↑ Pedersen-Bjergaard J, Pedersen M, Roulston D, Philip P. (1995) Different genetic pathways in leukemogenesis for patients presenting with therapy-related myelodysplasia and therapy-related acute myeloid leukemia. Blood. 86(9): 3542-3552.
- ↑ Greenberg P.L. Apoptosis and its role in the in the myelodysplastic syndromes; implications for disease natural history and treatment. Leuk res, 1998; 22: 1123—1136
- ↑ Onley HJ, Le Beau MM. Cytogenetic Diagnosis of Myelodysplastic syndromes. in book H.J.Deeg, D.T. Bowen, S.D.Gore, T.Haferlach, m.M.Le Beau and C.Niemeyr. Hematologic Malignancies: Myelodysplastic syndromes// Springler Berlin Heidelbery. 2006, P.55-79
- ↑ 1 2 «NCCN Clinical Practice Guidelines in oncology. Myelodisplastic syndromes. V.1.2009».
- ↑ Bennett JM, Catovsky D, Daniel MT, Flandrin G, Galton DA, et al. (1982) Proposals for the classification of the myelodysplastic syndromes. Br.J Haematol. 51(2): 189—199.
- ↑ Brunning R, Bennett J, Flandrin G et al. Myelodysplastic Syndromes. In: Jaffe E, Harris N, Stein H et al, eds. WHO Classification of Tumours. Pathology and Genetics of Haematopoietic and Lymphoid Tissues. Lyon: IARC Press 2001;61-73.
- ↑ Harris N, Jaffe E, Diebold J et al. WHO Classification of Neoplastic Diseases of the Hematopoietic and Lymphoid Tissues: Report of the Clinical Advisory Committee Meeting. J Clin Oncol 1999;17:3835-3849.
- ↑ Vardiman JW, Harris NL, Brunning RD. The World Health Organization (WHO) classification of the myeloid neoplasms. Blood 2002;100:2292-2302.
- ↑ Bruning RD, Orazi A., Germing U. Et al., 2008. WHO classification of tumors of hematopoietic and lymphoid tissues. Chapter 5, pp 88-107
- ↑ Hollstrem Lindberg E., Cazzola M. The role of JAK2 mutations in RARS and other MDS. 2008. Hematology, 52-59
- ↑ Greenberg PL, Baer M, Bennett J et al. NCCN Practice Guidelines for Myelodysplastic Syndromes, Version1, 2001, In “The Complete Library of NCCN Guidelines [CD-ROM], ” Rockledge, PA.
- ↑ Cheson BD, Bennett JM, Kantarjian H et al. Report of an international working group to standardize response criteria for myelodysplastic syndromes. Blood 2000;96:3671-3674.
- ↑ 1 2 Greenberg P., Cox c., Le Beau MM et al., International scoring system for evaluating prognosis in myelodysplastic syndromes. Blood 1997; 89:2079-2088
- ↑ Malcovati L., Germing U., Kuendgen A. Et al. Time-dependant prognostic scoring system for predicting survival and leukemic evolution in myelodysplastic syndromes. J Clin Oncol 2007; 25: 3503-10
- ↑ A WHO Classification-Based Prognostic Scoring System (WPSS) for Predicting Survival in Myelodysplastic Syndromes. Luca Malcovati et al. ASH Annual Meeting Abstracts 2005 106: Abstract 788
- ↑ Scott BL, Sandmaier BM, Storer B et al. Myeloablative vs nonmyeloablative allogeneic transplantation for patients with myelodysplastic syndrome or acute myelogenous leukemia with multilineage dysplasia: a retrospective analysis. Leukemia 2006;20:128-135.
- ↑ Wallen H, Gooley TA, Deeg HJ et al. Ablative allogeneic hematopoietic cell transplantation in adults 60 years of age and older. J Clin Oncol 2005;23:3439-3446.
- ↑ Demuynck H, Verhoef GE, Zachee P et al. Treatment of patients with MDS with allogeneic bone marrow transplantation from genotypically similar HLA-identical sibling and alternative donors. Bone Marrow Transplant 1996;17:745-751.
- ↑ Bowen D. Is traditional low dose chemotherapy (cytarabine/melphalan) still on option? Leukemia Research, Volume 31, Supplement 1, May 2007, Page S19
- ↑ Miller K.B. et al. The evaluation of low-dose cytarabine in the treatment of myelodisplastic syndromes: a phase III intergroup study. Annals of hematology, 1992; 65: 162—168.
- ↑ Burnett A.K., Milligan D., Prentice A.G. et al. A comparison of low-dose cytarabine and hydroxyurea with or without all-trans retinoic for acute myeloid leukemia and high-risk myelodysplastic syndrome in patients not considered fit for intensive treatment. Cancer. 2007. 109: 1114—1124
Ссылки
Образовательный видеоролик в помощь пациентам с миелодиспластическим синдромом
Дисплазия
Дисплазия согласно определению ВОЗ – это состояние, которое является переходным предраковым изменением и складывается из трех частей:
– атипия клеток;
– нарушения дифференцировки клеток;
– нарушения нормального строения ткани.
То есть дисплазия не ограничена только клеточной атипией, а включает в себя также и отклонения от нормальной структуры тканей.
В большинстве органов дисплазия возникает на фоне гиперплазии (увеличения числа клеток), которая чаще всего связана с хроническим воспалительным процессом. Часто гиперплазия и дисплазия комбинируются между собой. При дисплазии возникают отчетливые изменения всех межклеточных отношений.
Относительно некоторых органов термин «дисплазия» не применяется для описания переходных предраковых изменений. Например, подобное состояние в простате носит название неоплазия простаты, в шейке матки – цервикальная неоплазия, в матке – железистая гиперплазия, или аденоматоз.
Дисплазия бывает трех степеней выраженности:
– слабовыраженная;
– умеренно выраженная;
– выраженная.
По мере нарастания степени дисплазии все более увеличивается степень атипии клеток, они теряют черты нормальных клеток и становятся все более похожими на раковые клетки. Дисплазия – это обратимый процесс, она может регрессировать, длительное время существовать без изменений или прогрессировать. Чаще может наблюдаться регрессия слабовыраженной или умеренно выраженной дисплазии, но чем больше степень выраженности, тем меньше шансов на обратное развитие процесса и больше шансов на переход в рак in situ, который можно рассматривать как крайнюю степень выраженности процесса.
Сильно выраженные изменения клеток можно расценивать как облигатный предрак – стадия онкозаболевания, которая рано или поздно перейдет в рак. Это требует обязательного проведения комплекса мероприятий по профилактике и лечению.
Понятие «предрак» четко сформулировано именно в отношении рака, то есть злокачественных опухолей из эпителиальных тканей. Но в других областях не все так просто, в настоящее время онкологи обсуждают понятие «предлейкоз», состояние, которое может предшествовать раку крови. К нему относят различные нарушения кроветворения – цитопения, анемия, миелодиспластический синдром. Миелодиспластический синдром может развиваться после агрессивной химиотерапии многих опухолей.
Дисплазия шейки это рак? 50 ответов врачей на СпросиВрача

Фармацевт
ВПЧ теоретически может стать одним из факторов возникновения рака шейки матки. Анализ крови на онкомаркеры все бы вам показал.
Наталья, 17 февраля 2018
Клиент
Виолетта, спасибо,очень надеемся,что результаты биопсии будут хорошие,как получим,обратимся за консультацией.

Маммолог, Онколог
Здравствуйте, онкомаркеры не всегда показывают имеющуюся онкопатологию, тем более если она на ранней стадии. Рак в принципе может быть, все-таки имеется дисплазия 3 степени , а это предраковое состояние, к тому же выявлены онкогенны вирусы ВПЧ. Но все это необязательно говорит о раке. Возможно, что дисплазия и есть дисплазия, не более. И при раннем выявлении и лечении рак не возникнет.

Педиатр, Аллерголог-Иммунолог, Терапевт
Здравствуйте, скорее проблема в впч. Вам предлагали лечение?
Наталья, 17 февраля 2018
Клиент
Елена, изопринозин по2 три раза на 28 дней и свечи точно назвпние не скажу.дочь в другом городе,ей всегл 24 года,откуда такие болячки не поймём.

Акушер, Гинеколог
Без гистологического заключения сказать абсолютно ничего нельзя. Либо подтвердится дисплазия и тогда необходимо удалять пораженную ткань методом эксцизии или конизации, на этом собственно лечение и заканчивается. Либо, что хуже, имеет место рак in situ, тогда лечение в онкодиспансере. Кровь покажет в запущенной стадии.

Маммолог, Онколог
В любом случае окончательный диагноз можно сказать только после гистологии, а сейчас переживать и накручивать себя ни к чему.
Наталья, 17 февраля 2018
Клиент
Алина, спасибо.

Педиатр, Аллерголог-Иммунолог, Терапевт
По две таблетки?
Наталья, 17 февраля 2018
Клиент
Елена, да по две таблетки три раза в день.

Акушер, Гинеколог
Здравствуйте. Дисплазия третьей степени это предрак. Диагностика только биопсия и цитологический анализ. Никакими лекарствами его лечить нельзя. Это однозначно операция – вопрос в том, это будет операция Штурмдорфа (укороченные шейки и удаление пораженеой части) или же “прижигание” глубокая эксцизия или кони зайдя шейки матки. Не верьте тем кто будет говорить вам про лечение дисплазии 3 волшебным таблетками или свечами. Поправляйтесь,!
Наталья, 17 февраля 2018
Клиент
Александра, а после этих операций есть шансы родить?она ещё даже не замужем.

Педиатр, Аллерголог-Иммунолог, Терапевт
Лечение было нормально,тогда только биопсия вам точно скажет онкология или нет.
Наталья, 17 февраля 2018
Клиент
Елена, спасибо.

Акушер, Гинеколог
Конечно, даже и не думайте об этом. Каждое полугодие у меня ходят беременными и рожают такие девочки. Все прекрасно.

Акушер, Гинеколог
Простите эксцизия или конизация. Телефон(((
Наталья, 17 февраля 2018
Клиент
Александра, а вообще за какое время дисплазия может перерасти в рак,исходя из вашей практики?

Акушер, Гинеколог
Изопринозин – пустая трата денег и ложные надежды. Лечение только хирургическое. К сожалению, ВПЧ не знает возраста и подвержены в том числе и молодые девочки, ведущие половую жизнь. Профилактика – прививка от ВПЧ, но эффективна она до начала половой жизни. Если процесс ограничен шейкой матки, родить она безусловно может
Наталья, 17 февраля 2018
Клиент
Юлия, а для чего его тогда выписали,чтоб фармацевтам прибыль была?и что если рак ин ситу?тоже операция?

Акушер, Гинеколог
Здравствуйте! Дисплазия 3 – показание к конизации шейки матки, если подтверждение диагноза придёт по гистологии.

Маммолог, Онколог
Конечно сможет родить, даже не переживайте об этом!
Наталья, 17 февраля 2018
Клиент
Алина, молю всех богов,чтоб не рак ин ситу, или что похуже.

Маммолог, Онколог
Удачи Вам и пусть Ваши молитвы будут услышаны, чтобы обошло стороной это испытание!
Наталья, 17 февраля 2018
Клиент
Алина, спасибо.

Хирург
Здравствуйте!
Не переживайте раньше времени! Без гистологии сказать нельзя. Если это будет дисплазия 3 ст срочно делайте конизацию! Что бы забыть о раке.
Надеюсь у Вас все будет хорошо! Не болейте!
Наталья, 17 февраля 2018
Клиент
Рузанна, спасибо.

Акушер, Гинеколог
Всё очень индивидуально. Кто-то ходит с дисплазией 3 годами(асоциальные барышни, заключённые, словом те кто ничего не делает) и в итоге все неплохо. А бывает один раз дисплазия 1-2, а через полгода рак in situ. Поэтому всегда нужно делать все максимально быстро
Наталья, 17 февраля 2018
Клиент
Александра, вот и я о том же,не пьёт,не курит,партнёр один и был то всего.И раз сразу 3 стадия.
Наталья, 17 февраля 2018
Клиент
Александра, так и как быстрл то,биопсия будет готова в конце февраля,а на приём онколог назначила на 22марта.

Акушер, Гинеколог
Даже если выявят рак in situ, лечат его так же, как и дисплазию 3 (cin III) путем конизации шейки матки. Больший объем операций нецелесообразен при данной стадии процесса.
Девушки после конизации вырашивают и рожают.
Главное сейчас все делать быстро, так как заболевание у всех течёт по-разному.
Наталья, 17 февраля 2018
Клиент
Маргарита, а результаты биопсит можно будет кзнать только у врача,или как по готовности?я же до конца марта с умв сойду.
Наталья, 17 февраля 2018
Клиент
Маргарита, простите за неправильные слова.волнуюсь очень.

Акушер, Гинеколог
К сожалению, во всех странах гистологическая диагностика не быстро делается и в онкодиспансерах очереди ((( поверьте, вы ещё быстро идете(((
Наталья, 17 февраля 2018
Клиент
Александра, спасибо за ответы.

Акушер, Гинеколог
Не существует препаратов с доказанной эффективностью, способных уничтожить вирус папилломы человека. Ни изопринозин, ни аллокин-альфа, ни прочие иммуномодуляторы не гарантируют излечения от ВПЧ. ВПЧ способен к самоэлиминации, т.е.способен исчезнуть сам. При его обнаружении делают онкоцитологию и кольпоскопию,и если изменений нет, можно наблюдать каждые 6 месяцев. Если же изменения уже произошли ( как в Вашем случае), то только удаление пораженной ткани избавит от вируса. Дальше шейки ВПЧ не проникнет. Удалили ткань, сделали гистологию, она подтверждает, что конизация или эксцизия проведены в пределах здоровых тканей, всё. Контроль ВПЧ и онкоцитологии через 3 месяца. Согласно всем международным руководствам этого достаточно. Многие назначают, в российских руководствах эти препараты есть, но высокая цена, отсутствие доказательной базы и каких-либо гарантий на излечение не позволяют использовать их в своей практике. При in situ объём тот же, но там в зависимости от гистологии могут подключить лучевую или химиотерапию. Что-то с гистоогией у Вас действительно долго, хуже нет ждать.
Наталья, 17 февраля 2018
Клиент
Юлия, спасибо.Как всё это страшно.
Наталья, 17 февраля 2018
Клиент
Юлия, читала много о фотодинамической терапии при дисплазит и раке in situ,как Вы считаете,реально это,или просто очередное выкачивание денег?

Акушер, Гинеколог
Результат можно получить до посещения врача, надо позвонить и спросить, готовы ли результаты и можно ли их получить.
Обычно с этим не возникает проблем.
Не нервничайте, главное все делать вовремя!
Наталья, 17 февраля 2018
Клиент
Маргарита, спасибо

Гинеколог, Кардиолог, Венеролог
Здравствуйте. Обычно если есть рак то кровь на онко должна показать сильный скачок, скорее всего у вас просто дисплазия, но стадия у вас приличная. Поэтому вам необходимо лечение и его откладывать не надо. А более точный результат можен сказать только гистология. Желаю вам удачи.
Наталья, 17 февраля 2018
Клиент
Татьяна, спасибо.будем ждать и очень надеятся,что рака нет.И лечиться конечно же сразу по результатам.

Акушер, Гинеколог
Фотодинамческая тераия может быть эффективна, но опять же на ранних стадиях.

Хирург
Здравствуйте. Уреаплазма это нормальная флора. Последнее время ее перестают лечить грамотные венерологи. А дисплазия это заполнение эрозии восстановительной ткани. Ее ещё азывбт дисплазией. И пугают раком.
Наталья, 18 февраля 2018
Клиент
Роман, а зачем тогда пугают?Ведь весь интернет гудит,что предрак,и всё очень плохо.

Терапевт
Здравствуйте, Наталья. Единственный показатель, по которому достоверно устанавливают диагноз-результат биопсии. Онкомаркеры могут не показать, особенно на ранней стадии.

Гинеколог, Маммолог, Акушер
Здравствуйте!Кровь не покажет, рак может быть. Надо подождать биопсию- тогда будет точно известно.
Удачи!здоровья вам и вашей дочери!

Терапевт
Здравствуйте.узнать ли дисплазия это или рак можно только с помощью биопсии.
Но если врачи говорят об дисплазии 3 степени,то так оно и есть.Это предраковый стан.
Лечить можно в два способа:или удалять пораженные ткани или прижигание.
Насчет беременности,оно все индивидуально.Одни после операции могут рожать,другие нет.
Но будем надеяться на лучший исход в этой ситуации.
Будут ко мне вопросы-пишите в чат.Жду ваших сообщений.Здоровья вам и всех благ.

Уролог
Онкомаркеры не всегда показывают. Биопсия самый надежный тест. Клиника такая возникает как из за ВПЧ, так и из за уреоплазмы. После правильного лечения все нормализуется.

Акушер, Гинеколог
Здравствуйте, Наталья! Нужно дождаться биопсии. Это будет самый информативный метод. Кровь может ничего не показать( быть в норме). Здоровья Вашей дочке и Вам!

Гематолог, Маммолог, Онколог
Здравствуйте. Не накручивайте себя. Дождитесь гистологии. Сдача онкомаркеров ничего не показывают, они не специфичны.
И меньше читайте интернет, он может вас завести в такие дебри. Которых на самом деле и нет.
Дисплазия молочной железы: виды, признаки и лечение


Дисплазия молочной железы – одно из самых распространенных заболеваний груди. Опасность патологии заключается в возможностях ее перерастания в онкологическую болезнь. Избежать развития заболевания можно, если тщательно следить за состоянием своего здоровья.
Дисплазия молочной железы — что это такое?
Дисплазия — аномальное развитие органов и тканей человеческого организма. Патология грудных желез является самой распространенной. Может выражаться в гиперплазии и гипоплазии. Первую нередко именуют мастопатией. Гиперплазия, или чрезмерное разрастание железистых тканей, характеризуется появлением в груди узелковых уплотнений. Относится к фиброзному виду патологии. Именно эта форма дисплазии способна перерастать в рак, что является внушительным поводом для обращения к врачу при появлении болей или уплотнений в молочной железе.
Гипоплазия не приносит в жизнь женщины таких глобальных проблем. Единственным недостатком является недоразвитие груди, что не влияет на ее функционирование.
Факторы, провоцирующие развитие фиброзно-кистозной болезни
Причин, способных вызвать подобное патологическое отклонение, достаточно много. Но для постановки диагноза, и назначения правильного лечения, врачу необходимо их выяснить. Рассмотрим самые частые из них:
- Гормональный дисбаланс. Развитие заболевания может вызвать увеличение или уменьшение прогестерона, повышенное содержание андрогенов, гипофункция щитовидки или гиперфункция гипофиза.
- Апоптоз. Подобная патология провоцирует самоуничтожение клеток и воспаление, нарушение структуры сосудов и ткани желез.
- Ранее наступление менопаузы. Если явление возникает в 50-52 года, риск развития дисплазии увеличивается.
- Нарушение физиологического и патологического плана в репродуктивной системе представительницы слабого пола.
- Частые аборты или срывы беременности.
- Стрессовые ситуации, нервные срывы, сексуальная неудовлетворенность.
- Генетическая предрасположенность.
- Курение, алкоголизм и употребление психотропных веществ, проблемы ЖКТ хронического вида.
- Применение гормонов долгое время без назначения врачом дозировки.
- Нарушение метаболизма, патологическое состояние печени.
Если у женщины мать или бабушка страдала от подобного рода заболевания, стоит тщательно следить за состоянием своей груди. Ведь при таких обстоятельствах риск развития дисплазии увеличивается в десять раз.
Характерные признаки патологии
Симптоматика зависит от формы заболевания. Каждому виду болезни характерна своя клиническая картина. Но общим признаком являются болевые ощущения в зоне груди, нередко иррадиирующие в область подмышки, в плечо или в лопатку. Их интенсивность будет зависеть от степени прогрессирования патологии.
Из-за постоянно неутихающих болей развивается неврогенная симптоматика: плохой сон, раздражительность и прочее. Многие женщины, узнав свой диагноз, начинают страдать канцерофобией, то есть боязнью перерастания образования в злокачественную опухоль.
Доброкачественная дисплазия молочных желез
Дисплазия доброкачественного типа – это самая распространенная форма болезни. Ей характерны регрессивные и пролиферативные изменения структуры ткани железы, а ее протоки поражают фиброзные и кистозные нарушения.
В свою очередь этот вид патологического состояния имеет подвиды:
- Пролиферативный тип. Выражается поражением ткани долей, протоков и миоэпителия. Иногда повреждает соединительную ткань. Чаще всего переходит в рак.
- Фиброаденома. Возникает в результате разрастания соединительной и железистой ткани. В 25-40% случаев перерастает в злокачественное образование.
- Непролиферативная форма. Находится в фиброзной ткани, а в соединительной возникают кисты. Вероятность озлокачествления немного ниже, чем в случае развития пролиферативного типа патологии.
- Внутрипротоковая папиллома. Располагается в области сосков. При минимальном количестве образований болезнь редко переходит в онкологию. Но риск перерастания становится выше с увеличением числа папиллом.
Дисгормональная дисплазия молочных желез
Дисгормональную дисплазию вызывает гормональный сбой в женском организме. Здесь существует несколько разновидностей патологического состояния:
- Фиброзно-кистозная мастопатия. Представляет собой смешанный вид дисплазии, характеризующийся воспалением и небольшими выделениями. Может развиваться как одностороннее, так и двухстороннее поражение.
- Фиброаденоматоз. Имеет фиброзный характер. Основой является фиброзная структура. На снимке различаются участки с однородными затемнениями. Болевой синдром умеренный.
- Узловая дисплазия. Основной признак – образования в форме узла. Диагностируется также фиброматоз, фиброз, киста, аденофиброма и фиброаденома. Наблюдаются выделения крови или молока из груди, сильные болезненные ощущения, не унимающиеся после окончания менструации.
- Диффузная дисплазия. Выражается кистозными образованиями, которые на снимке выглядят как округлые полости. Может проявляться в виде поликистоза с образованием множества пустых полостей. При пальпации прощупываются эластичные комочки. Больного беспокоят боли распирающего характера.
- Аденоз. Развивается зачастую у представительниц слабого пола, которые не рожали. Состоит опухоль из ткани железы. Болевые ощущения беспокоят пациентку при ощупывании образования, размер которого достигает 20 миллиметров, не более.
Тяжелая форма дисплазии молочной железы
Когда патология игнорируется, и не предпринимаются необходимые лечебные меры, заболевание прогрессирует, что способствует развитию тяжелых форм дисплазии. Например, болезнь 3 степени называют предраковым состоянием. На этом этапе грудь лишь на треть состоит из нормальных клеток. Все остальное – аномальная ткань.
В результате структурного изменения желез происходит нарушение секреторных функций. Все аномальные процессы на этой стадии прогрессирования патологии необратимы. Такая ситуация имеет высокий уровень скорого озлокачествления.
Фиброзное поражение
В результате развития фиброза из-за постоянного воспаления происходит изменение клеточной структуры соединительного эпителия с возникновением рубцов. Такое развитие событий в любом виде ведет к онкологии. На раннем этапе прогрессирования такой вид болезни никак себя не проявляет. Симптоматика начинает появляться при усугублении заболевания.
Для фиброзной дисплазии характерно увеличение груди при месячных и болезненные ощущения при прикосновениях. Такой вид отличается наличием предменструального синдрома, серозными выделениями из груди. Отмечаются ощущения распирания молочных желез, болевой синдром не зависит от месячных.
Диагностика молочных желез при подозрении развития патологии
Для точной постановки диагноза, в особенности на ранней стадии прогрессирования дисплазии, необходимо применении новейшего оборудования. При каких-либо сомнениях женщине назначается повторная диагностика, но в другой больнице. Таким образом, доктор получит полную клиническую картину для назначения правильной терапии.
Для начала врач опрашивает пациента, собирает весь необходимый анамнез и визуально осматривает, ощупывает молочную железу представительницы слабого пола. Обязательно проводится пальпация лимфатических узлов под и над ключицей, в подмышечной впадине. Самые точные данные для осмотра будут получены при обследовании в определенный промежуток времени: 7-10 день менструального цикла.
Из аппаратных исследований самым информативным является рентген (билатеральная маммография). Снимок позволяет распознать болезнь, выяснить месторасположение образования и его объем. Точность исследования достигает 95 %.
Нередко врачи назначают ультразвуковое исследование (допплерографическое сканирование). Оно позволяет рассмотреть орган в цвете. Обследование дает возможность дополнить клиническую картину патологии, уточняя некоторые нюансы. Является самым безопасным и безвредным для организма методом диагностики.
При очаговой узловой дисплазии назначается биопсия и магнитно-резонансная томография.
При развитии подобной патологии необходима комплексная диагностика, чтобы рассмотреть образование со всех сторон, получить исчерпывающую информацию. Иногда может понадобиться консультация гинеколога, эндокринолога.
Методы лечения
Для лечения дисплазии в основном применяется консервативная терапия, в запущенных случаях есть необходимость проведения оперативного вмешательства.
Первая и основная цель лечения патологии – это устранение причины прогрессирования болезни. Основным провоцирующим фактором здесь является гормональный дисбаланс. Для его нормализации активно применяют такие препараты, как Дериват этистерона синтетического производства, Данол, и прочие препараты, обладающие фолликулостимулирующими, лютеинизирующими свойствами.
Прием Даназола (Данола) назначается лечащим врачом, длительность и дозировка подбирается лично для каждой больной. Противопоказан при вынашивании ребенка и лактации, при порфирии. С осторожностью назначается людям, имеющим проблемы с сердцем, почками, или болеющим сахарным диабетом.
Для восстановления уровня прогестерона и эстрогена доктор выписывает Линэстренол, Тамоксифен или Прогестин. Врачом назначаются и антипролактивные лекарства: Парлодел, Нор-пролак, Бромокиптин.
Последний препарат вводят женщине вместе с пищей. Для начала дозировка составляет 1,25 миллиграммов. Со временем ее увеличивают до 2,5 миллиграммов. Вводят средство перед тем, как человек ляжет спать. Его применение не рекомендуется при индивидуальной непереносимости компонентов, гипертонии, ишемической болезни сердечной мышцы, психологических расстройствах.
Дополнительно, на усмотрение лечащего врача, пациентке назначаются антигистаминные и обезболивающие препараты. В комплекс лечения входят и иммуностимуляторы, состоящие из витаминов и микроэлементов, способные укреплять иммунитет. При эмоциональной нестабильности женщины уместным будет прием тонизирующих и успокоительных средств.
Хирургическое лечение применяется редко. При кистозном виде патологии используют биопсию. С помощью тонкой иглы из полости отсасывается жидкость, а обратно вводится вещество, склеивающее стенки кисты. Это способствует устранению рецидива скопления жидкости. При вязком содержимом образования с прожилками крови проводится секторная резекция грудной железы.
Профилактические меры
Для ограждения себя от развития дисплазии, женщине нужно выполнять ряд определенных правил:
- придерживаться здорового, активного образа жизни;
- своевременно лечить заболевания репродуктивной системы;
- поддерживать психологическое равновесие и постоянную половую жизнь;
- отказаться от ВП;
- исключить факторы, способные привести к сбою гормонального фона;
- контролировать свой вес, проводить профилактику ожирения;
- ежедневно выполнять ряд умеренных физических упражнений или заняться каким-либо видом спорта;
- питаться полноценно, сбалансировано;
- не пренебрегать профилактическими визитами к гинекологу;
- проводить мероприятия по укреплению иммунитета.
Каждая женщина должна периодически самостоятельно обследовать свою грудь, следить за правильным окрасом кожного покрова, и отсутствием патологического увеличения лимфатических узлов.
Для всех представительниц слабого пола грудь является ее гордостью и органом вскармливания будущего ребенка. Поэтому очень важно следить и поддерживать здоровье молочной железы. Здоровый образ жизни и своевременное обращение за помощью к медицинскому работнику поможет оградить женщину от дисплазии или провести нужное лечение для полного выздоровления.


 Анемический синдром — постоянный и обязательный признак патологии. Для него характерны гиперхромия и макроцитоз. Большой размер эритроцитов и их интенсивное окрашивание, зависящее от повышенного содержания гемоглобина, – признаки анемии при МДС и остром лейкозе. При анемии больные быстро утомляются, плохо переносят физические нагрузки, жалуются на головокружение, одышку, боль в груди, костях и суставах, невозможность сосредоточится. Их кожа становится бледной, ухудшается аппетит, снижается вес и работоспособность, возникает нервозность, цефалгия, дрожь в теле, шум в ушах, сонливость, тахикардия, обмороки. Плохо переносят анемию престарелые больные, а также лица с сердечно-легочной патологией. У них могут развиться тяжелые последствия – стенокардия, инфаркт миокарда, аритмии.
Анемический синдром — постоянный и обязательный признак патологии. Для него характерны гиперхромия и макроцитоз. Большой размер эритроцитов и их интенсивное окрашивание, зависящее от повышенного содержания гемоглобина, – признаки анемии при МДС и остром лейкозе. При анемии больные быстро утомляются, плохо переносят физические нагрузки, жалуются на головокружение, одышку, боль в груди, костях и суставах, невозможность сосредоточится. Их кожа становится бледной, ухудшается аппетит, снижается вес и работоспособность, возникает нервозность, цефалгия, дрожь в теле, шум в ушах, сонливость, тахикардия, обмороки. Плохо переносят анемию престарелые больные, а также лица с сердечно-легочной патологией. У них могут развиться тяжелые последствия – стенокардия, инфаркт миокарда, аритмии.