Диафрагмальные грыжи у детей врожденные – Диафрагмальная грыжа у детей > Клинические протоколы МЗ РК
Диафрагмальные грыжи у детей. Врожденная диафрагмальная грыжа (ВДГ)
Врожденная диафрагмальная грыжа (ВДГ)
ВДГ встречается с частотой 1 на 2000 рождений, включая мертворожденных. Истинная природа ВДГ стала значительно более понятной с тех пор, как в практику было широко внедрено ультразвуковое обследование плода. Из всех случаев ВЛГ, выявленных внутриутробно, 70—75% связаны с многоводней. Этот показатель частоты многоводия, возможно, несколько завышен, поскольку одним из основных поводов для ультразвукового исследования являются именно большие размеры матки, не соответствующие гестациошюму сроку, т. е. женщины с многоводном более часто подвергаются обследованию.Тем не менее не вызывает сомнений тот факт, что при наличии многоводия летальность среди детей с ВДГ особенно высокая и составляет 72—89%. При отсутствии же многоводия этот показатель ниже, но до настоящего времени все еще превышает 50%. Многие из детей с ВДГ и многоводном у матери умирают сразу посте рождения от легочной недостаточности, несмотря на оптимально проводимые реанимационные мероприятия.
Причина многоводия, по-видимому, заключается в перегибе гастроэзофагеального перехода и/или пилоруса, когда желудок выпячивается в грудную клетку, что препятствует продвижению заглоченной амниотической жидкости. При пролабировании в плевральную полость желудка летальность обычно более высокая, чем в тех случаях, когда желудок расположен иа своем месте в брюшной полости. Желудок является содержимым грыжи, как правило, у больных, имеющих медиально расположенный большой дефект диафрагмы. Ясно, что чем больше количество перемещенных в грудную клетку органов, тем более недоразвито легкое.
При ВДГ часто встречаются сочетанные аномалии других органов и систем, поскольку неблагоприятное воздействие на эмбрион возникает в раннем периоде формирования внутренних органов (на 8-й неделе гестации). Из всех детей с ВДГ 32% рождаются мертвыми. Около 36% умирают до поступления в Центр хирургии новорожденных. Почти у всех мертворожденных и тех, кто умирает вскоре после рождения, обнаруживаются тяжелые аномалии нервной системы, такие как анэнцефалия, миеломенингоцеле, гидроцефалия, энцефалоцеле и тяжелые сердечные пороки, а также трисомия 13 и 18.
Около 65% умирающих рано детей — недоношенные, родившиеся раньше 36 недель гестации с массой тела меньше 2500 г. Эта комбинация тяжелых аномалий и недоношенности и обусловливает высокую летальность. Большинство новорожденных, которые доживают до оперативного вмешательства, как правило, доношенные и не имеют других аномалий.
Хотя причины возникновения ВДГ неизвестны, однако нельзя исключить, что определенную роль играет генетический фактор, ибо имеются сообщения о ВДГ у однояйцевых близнецов, сиблингов и двоюродных родственников. Девочки поражаются почти в два раза чаще мальчиков.
Дефект диафрагмы может представлять собой небольшую щель или тотальное отсутствие всех компонентов грудобрюшной преграды, включая ножки (см. рис. 19-1). ВДГ в 80% случаев, по данным самых разных авторов, встречается слева, в 1% — с двух сторон. Интактный плевроперитонеальный грыжевой мешок имеется у 20—40% больных. Когда он ограничивает пролабирование кишечника, дети, как правило, выживают.

Патофизиология. При рождении ребенка возникают трудности прохождения воздуха в легкие, поскольку отсутствует наиболее важный механизм вдоха — сокращение диафрагмы, а, кроме того, средостение смещено в противоположную сторону и соответственно сдавленными оказываются оба легких. Отрицательное давление, развивающееся во время вдоха, способствует еще большему выпячиванию кишечника в грудную клетку.
Имеет значение и то. что при респираторном дистрессе ребенок заглатывает большое количество воздуха, который растягивает кишечник, а это приводит к дальнейшему сдавлению легкого. Грыжа сама по себе, даже при нормально развитых легких, может привести к дыхательной недостаточности. А любая степень легочной гипоплазии вызывает тяжелые нарушения оксигенации и выведения углекислоты.
В гипоплазированных легких снижен газообмен за счет уменьшения поверхности как альвеол, так и капиллярного русла. Эти легкие мало податливы и медленно расправляются. Количество ветвей легочной артерии уменьшено, поэтому правый желудочек вынужден с усилием проталкивать кровь через небольшое сосудистое русло, что приводит к расширению легочной артерии и увеличению давления в правом сердце.
Легочные артерии имеют необычно толстые мышечные волокна, распространяющиеся дистальнее терминальных бронхиол. Этот мышечный слой особенно восприимчив к медиаторам вазоконстрикции (табл. 19-1). В результате развиваются нарушения газообмена и легочного кровотока, легочная гипертензия и правожслулочковая недостаточность. Возникает также шунтирование крови справа-налево через артериальный проток и овальное окно, что усугубляет системную гипоксию, гиперканнию и ацидоз и приводит к нарастанию сужения легочных сосудов. Гели клинически сужение легочных сосудов уже наступило, то корригировать его чрезвычайно трудно. Поэтому, как только установлен диагноз ВДГ, необходимо незамедлительно начинать очень активное лечение.
Диагностика. Диагноз может быть установлен пренатально при ультразвуковом обследовании беременных женщин. Наличие многоводия или растянутого желудка, расположенного в грудной клетке, говорит о плохом прогнозе. Если диагностирована ВДГ, то необходимо обследовать плод на наличие других пороков, тщательно осматривая голову, позвоночник, сердце и почки. Для выявления хромосомных и обменных аномалий производят амниоцентез или хорион-биопсию. Если ВДГ является единственной изолированной аномалией, то следует рассмотреть вопрос о возможности и критериях для коррекции порока внутриутробно у плода.
После рождения диагноз устанавливают но наличию затрудненного дыхания, цианоза, ладьевидного живота, смещения тонов сердца, а также отсутствию дыхания на стороне грыжи. Смещение трахеи в сторону or средней линии и кишечные шумы в грудной клетке обычно не определяются. Тяжесть перечисленных симптомов имеет большой диапазон: около 65% всех детей с ВДГ умирают вскоре после рождения, в то время как 5% и больше иногда живут бессимптомно месяцы и годы, прежде чем устанавливается диагноз.
Перед рентгенографией грудной клетки (основной метод диагностики) желательно ввести в желудок зонд. Если рентгенограмма делается до того, как воздух заполнил кишечник, то грудная клетка на стороне поражения затенена, но трахея и сердце смещены в противоположную сторону и контрлатеральное легкое уменьшено в размерах. Чаще всего кишечник заполнен воздухом, причем иногда эти воздушные тени ошибочно принимаются за различные формы легочных кист (рис. 19-4).

Рис. 19-4. Рентгенограмма грудной клетки — заполненный газом кишечник находится в левой половине грудной клетки. Трахея, контурирующийся воздухом пищевод и сердце смещены вправо настолько, что лишь небольшая часть правого легкого остается воздушной
ВДГ с поздним началом проявлений. По данным разных авторов, от 5 до 25% диафрагмальных грыж выявляются после периода новорожденности — в возрасте от 1 месяца до поздней старости. Диагноз иногда устанавливают случайно, при рентгенологическом исследовании грудной клетки у пациентов с бессимптомным течением грыжи. Если же появляются симптомы, то они могут быть очень легкими либо, наоборот, чрезвычайно тяжелыми — как со стороны дыхательных путей в виде реснираторного дистресса, так и со стороны ЖКТ — в виде непроходимости. Респираторные симптомы иногда напоминают проявления легочной инфекции с температурой и кашлем. Сдавление легких может вызывать укорочение дыхания. Данные физикального и рентгенологического обследований помогают отдифференцировать плевральный выпот, эмпиему или кисты легких. Боли в животе, тошнота, рвота бывают связаны со сдавлеиием кишечника в отверстии диафрагмы, что приводит к непроходимости, либо с нарушением кровообращения кишечника (с заворотом или без него). Если на рентгенограмме грудной клетки диафрагма контурируется нечетко, определяются «легочные кисты», а при исследовании пассажа контрастного вещества по желудочно-кишечному тракту видно проникновение тонкой кишки через диафрагму, операцию необходимо осуществлять из трансабдоминального доступа.
К.У. Ашкрафт, Т.М. Холдер
Опубликовал Константин Моканов
medbe.ru
Исход врожденной диафрагмальной грыжи. Сочетанная патология при диафрагмальной грыже. – диафрагмальная грыжа у плода – запись пользователя Надежда (newlogin) в сообществе Диафрагмальная грыжа в категории **Статьи, информация о ДГ**
источникантенатальная смертностьИсход врожденной диафрагмальной грыжи. Сочетанная патология при диафрагмальной грыже.
Пренатальное консультирование семей с диафрагмальной грыжей у плода принципиально отличается от постнатальных консультаций, поскольку в общей структуре исходов беременностей при этом пороке, надолю благоприятных исходов приходится не более 10%. Так, по данным Российского мультицентрового исследования, при ДГ, выявленной пренатально, выжили ли шь 2 (7,1 %) ребенка из 28. В 64,3% наблюдений семьи приняли решение в пользу прерывания беременности независимо от наличия или отсутствия сочетанных аномалий развития и/или ХА. В оставшейся группе в 17,8% случаев беременность закончилась срочными родами, в 14,3% -преждевременными родами, в 3,6% - антенатальной гибелью плода. Из 9 детей, родившихся живыми, 3 умерли до операции, 6 были оперированы. После хирургической коррекции погибли 4 детей из 6. Только 2 ребенка были живы на момент сбора катамнестических данных.
Печальные результаты исходов при врожденной диафрагмальной грыже диктуют необходимость расширения комплекса обследований плода с целью уточнения постнатального прогноза. В настоящее время большое значение в клинической практике уделяется изучению возможных прогностических факторов и дополнительных методов исследования плода при ДГ. Некоторые авторы выделяют главные и второстепенные прогностические факторы. К главным, по их мнению, относятся объем легких, вычисленный пренатально, характер дыхательных движений и характеристики кривых скоростей кровотока в легочных артерии и вене; к второстепенным -расположение грыжи, наличие печени в грудной полости, присоединение многоводия, а также раннее обнаружение порока. Это мнение, безусловно, заслуживает внимания, хотя до сих пор окончательный перечень основных прогностических пренатальных факторов при ДГ не установлен.
Одним из основных неблагоприятных факторов, влияющих на исход при диафрагмальной грыже, является наличие сочетанных аномалий развития или другой патологии. По нашим данным, в такой ситуации большинство пациенток приняли решение о прерывании беременности по медицинским показаниям. В 6% от общего количества пациенток с сочетанными ДГ наступила антенатальная гибель, в 19% -дети родились живыми, но погибли до операции в связи с респираторными проблемами. В 13% случаев ДГ сочеталась только с задержкой внутриутробного развития. Эти дети были оперированы, но умерли в связи с развитием легочной недостаточности и послеоперационными осложнениями (кишечная непроходимость). Таким образом, все случаи сочетания ДГ с пороками развития других органов и систем, а также с задержкой развития плода, имели неблагоприятный исход.
При изолированных диафрагмальных грыжах прогноз для жизни представляется более благоприятным. В отличие от группы с сочетанными изменениями среди пациенток с изолированными ДГу плода при пролонгировании беременности не было ни одного случая антенатальной гибели. Все новорожденные были оперированы, т. е. доля детей, дожившихдо операции, при изолированной ДГ была в 2 раза больше, чем при сочетанной ДГ (соответственно 25 и 13%). После операции умер 1 ребенок в связи с послеоперационными осложнениями, развившимися на 9-е сутки, что существенно ниже, чем при сочетанных ДГ (соответственно 8 и 13% в общей структуре перинатальных исходов). В отличие от случаев сочетанной ДГ, при изолированных ДГ 17% беременностей закончились благополучно: 2 ребенка живы и на момент сбора данных здоровы. По данным литературы, в зарубежных клиниках этот показатель существенно выше, варьирует от 28 до 50% и в среднем составляет 37%.
Большое значение для точного составления прогноза при диафрагмальной грыже имеет срок пренатального выявления этого порока. Раннее выявление ДГ позволяет не только более полно обследовать пациентку, но дает возможность семье принять взвешенное решение о прерывании или пролонгировании беременности. По нашим данным, в группе, где диагноз был поставлен до 24 нед, в 85% случаев беременность была прервана по медицинским показаниям по сравнению с 40% в группе с поздней диагностикой ДГ. Законодательство нашей страны позволяет прервать патологическую беременность в любом сроке, поэтому такая разница в показателях, по нашему мнению, связана исключительно с ранним выявлением ДГ. Чем больше времени до родов остается у родителей на раздумья, тем более сложным представляется решение о пролонгировании беременности. Груз моральной ответственности за нездорового будущего ребенка, а также материальные затраты необходимые на лечение становятся основными причинами решения о прерывании беременности. Следовательно, срок пренатальной диагностики порока принципиально влияет на исходы беременностей.
Помимо отсутствия сочетанной патологии и срока выявления диафрагмальной грыжи, важное значение при прогнозировании возможных до- и послеоперационных осложнений имеет пренатальная оценка состояния легких, поскольку именно респираторные проблемы стоят на первом месте в перечне причин, приводящих к летальным исходам при ДГ.
Легочная гипоплазия при диафрагмальной грыже возникает в результате сдавления развивающихся легких плода смещенными в грудную полость брюшными органами. Возникновение ДГ приводит не только куменьшению объема функционально полноценной легочной паренхимы, но и к нарушению всех трех стадий (железистая, каналикулярная, альвеолярная) формирования легких плода. Гипоплазия легких при ДГ характеризуется уменьшением количества бронхиальных ветвей и альвеол, а также поражением сосудистой сети легких. Количество ветвей легочной артерии не соответствует количеству бронхов, артерии имеют меньший диаметр и более толстую мышечную стенку.
В настоящее время предпринимаются различные попытки дородовой оценки состояния легких. Прежде всего, следует обращать внимание на размеры грыжи и, соответственно, на объем функционирующей легочной ткани, а также на срок первого обнаружения ДГ.
Очевидно, что пренатальное ультразвуковое исследование не позволяет достоверно оценить размеры грыжевого выпячивания. Косвенным признаком значительных размеров грыжи и, соответственно, неблагоприятного постнатального прогноза может служить наличие печени в грудной клетке. Тем не менее, поданным К. Heling и соавт., корреляция между положением печени и исходом беременности не выявлена.
Величина грыжи - это не единственный фактор, влияющий на состояние ткани легких. Фактор времени также оказывает действие на постнатальный прогноз. Чем дольше незрелые легкие плода находятся под давлением смещенных органов, тем хуже прогноз, поскольку это создает неблагоприятные условия для их развития и созревания. Поданным G. Sharland и соавт., показатели смертности при ДГ коррелируют с временем обнаружения порока. При ранней (до 25 нед) диагностике ДГ выжили только 33% новорожденных, при поздней манифестации порока и, соответственно, поздней диагностике - 67%. Однако некоторые авторы не подтверждают эти закономерности. По данным К. Heling и соавт., при ранней (22-27 нед) диагностике ДГ выживаемость составила 80%.
При составлении постнатального прогноза при пренатально выявленной диафрагмальной грыже многие исследователи наибольшее значение придают оценке объема легких. Этот показатель тесно связан с площадью легкого, которую можно оценить при поперечном сканировании грудной клетки. В конце 90-х годов для оценки постнатального прогноза было предложено использование индекса, отражающего степень гипоплазии легких. Для его вычисления значение двух взаимно перпендикулярных диаметров легкого с противоположной от грыжи стороны следует перемножить, и результат разделить на значение окружности головы. По данным G. Lipshutz и соавт., при значении индекса< 0,6 в 100% исходы были летальными, тогда как при его значении >1,4 все плоды выжили. По данным J. Deprest и соавт., основным прогностическим критерием по легочной гипоплазии является значение индекса менее 1 при наличии смещения печени в грудную клетку. Некоторые авторы опровергают значение этого параметра. Так, в исследованиях К. Heling и соавт. при индексе менее 1,0 смертность составила 25% вместо ожидаемой 100%, а при индексе 1,4 выживаемость не превысила 40% вместо ожидаемой 100%. Так или иначе, до сегодняшнего дня этот индекс остается одним из основных прогностических пренатальных критериев, однако поиски дополнительных эхографических маркеров несостоятельности легких при ДГ продолжаются.
Несколько лет назад были предприняты попытки найти корреляцию между повышением индекса резистентности в легочной артерии и развитием гипоплазии легких и легочной гипертензией в неонатальном периоде. Известно, что причинами повышения давления в системе легочной артерии при ДГ является уменьшение количества легочных сосудов и объема капиллярного русла, а также повышенная резистентность аномально толстой мышечной артериальной стенки. Еще в начале 90-х годов были проведены исследования, демонстрирующие связь между гипоплазией легких, вызванной ДГ, и появлением реверсного кровотока в легочных венах. Несмотря на очевидную связь сосудистого компонента и постнатальных легочных осложнений, допплерографическая оценка кровотока в легочных артерии и венах при ДГ не нашла широкого распространения в связи с низкой воспроизводимостью и значительными погрешностями при пренатальном исследовании.
Недостаточно эффективной оказалась и оценка активности дыхательных движений плода. В 1993 г. Н. Fox и соавт. показали, что при наличии ДГ у плода и регистрации движения жидкости через полость носа и рта прогноз для жизни лучше, чем при отсутствии таких движений. Движение жидкости можно оценить с помощью цветового допплеровского картирования (ЦДК). Изменение амплитуды коррелирует с частотой гипоплазии легких и ухудшает прогноз для жизни, однако оценка этого параметра достаточно субъективна, поэтому он также не нашел применения в клинике.
Косвенным признаком постнатального неблагополучия при диафрагмальной грыже у плода может служить присоединение многоводия. Возникновение многоводия при ДГ можно объяснить сдавлением пищевода и, соответственно, нарушением процесса глотания вод плодом. Кроме того, глотание меняется при перемещении в грудную полость желудка или его части. При наличии многоводия летальность в постнатальном периоде может достигать 89%, тогда как при его отсутствии - составляет около 50%.
>>мой комментарий - мне врачи говорили шансы 50/50, приведенная здесь статистика звучит страшнее как то
www.babyblog.ru
симптомы, причины, лечение, профилактика, осложнения
Отчего может быть патология у ребёнка? Факторы, которые провоцируют возникновение диафрагмы грыжи, разделяются на предрасполагающие и производящие. К предрасполагающим причинам можно отнести:
- врождённую слабость мышц;
- приобретённую слабость мышц;
- получение травмы диафрагмы;
- изменения, затрагивающие мышечно-связочный аппарат.
Производящие причины возникновения диафрагмальной грыжи у ребёнка обычно связаны с повышением давления внутри брюшной полости:
- поднятие тяжестей;
- тяжёлые физические нагрузки;
- частые запоры;
- не проходящий кашель;
- истеричный, надрывный и непрекращающийся плач;
- постоянные переедания, и как следствие, лишний вес.
Как определить диафрагмальную грыжу у ребёнка? Распознать патологию у малыша можно по некоторым признакам.
- Органы брюшной полости могут быть перемещены в грудную клетку и наоборот;
- Может быть небольшое выпячивание органов в области диафрагмы.
Опредёленные признаки заболевания возникают в зависимости от органов, в которых возникает патология:
- Если у ребёнка грыжа пищевода, у него наблюдается изжога, отрыжка, болезненные ощущения вверху живота, а также в грудной клетке и области рёбер. У малыша наблюдается отдышка, увеличенный ритм сердцебиения после приёма пищи;
- В некоторых случаях у ребёнка, с грыжей диафрагмы, после еды возникает рвота, после чего наступает облегчение;
- В грудной клетке у малыша слышны урчания и булькающие звуки;
- У малыша может начаться анемия, что удаётся выявить с помощью анализов.
Диагностика грыжи диафрагмы у ребёнка
Диагностировать патологию у ребёнка можно при своевременном обращении к врачу-педиатру. Врач сможет при первичном осмотре определить предварительный диагноз на основании осмотра и учёта жалоб ребёнка и его родителей. Чтобы поставить точный диагноз, назначается проведение рентгенографии. С помощью контрастного вещества можно определить характер диафрагмальной грыжи.
Для определения состояния органов брюшной полости, назначается ультразвуковое исследование.
Ребёнок сдаёт анализы крови и мочи.
Чем опасно возникновение диафрагмальной грыжи у ребёнка? Некоторые виды грыжи вызвают опасные осложнения, которые могут нанести вред детскому организму.
- При возникновении скользящей грыжи, чаще всего начинается воспалительный процесс в пищеводе. Это происходит из-за регулярного воздействия желудочного сока на слизистую оболочку пищеварительного органа;
- Грыжа пищевода может осложниться дуоденогастральным рефлюксом. Симптом этого осложнения является горечь во рту после употребления пищи;
- Ущемление грыжи или соседних органов является одним из опасных осложнений. Из-за повышения давления внутри брюшной полости вероятность ущемления возрастает;
- При ущемлении происходит нарушение функциональности органов брюшной полости и грудной клетки, что может привести к летальному исходу;
- Определить ущемление грыжевого выпячивания можно по резкой боли вверху живота, а также в левой стороне грудной клетки. Может начаться тошнота и приступы рвоты, происходит задержка стула. В случае ущемления диафрагмальной грыжи необходимо экстренное хирургическое вмешательство.
Что можете сделать вы
Вылечить диафрагмальную грыжу у ребёнка можно только с помощью врача. Самостоятельное лечение родителями запрещено.
При появлении симптомов, малыша следует показать специалисту для осмотра и назначения правильного лечения. Часто для устранения грыжи диафрагмы назначается оперативное вмешательство. Для этого родители должны следить за питанием малыша перед операцией. Из рациона следует исключить жирную и острую пищу, сладости, полуфабрикаты и фаст-фуды.
Ребёнка следует оградить от физической нагрузки и поднятия тяжестей. Ребёнку нельзя носить бандажи и утягивающую одежду, которая провоцирует повышение внутрибрюшное давление.
Что делает врач
Определить, как лечить диафрагмальную грыжу, врач решит после получения результатов исследования:
- Если грыжа скользящая, и не может спровоцировать ущемление, чаще всего операция не проводится. Ребёнку назначается диета с дробным питанием, которое должно происходить часто, но маленькими порциями. Малышу необходимо принимать лекарственные препараты, которые уменьшают выделение желудочного сока и снижают уровень кислотности желудка. Для устранения анемии назначаются препараты с высоким содержанием железа.
- При возникновении грыжи, которая может привести к осложнениям, назначается хирургическое вмешательство. Операция проводится детям после пяти лет. Но если в более раннем возрасте есть угроза жизни ребёнка, хирургическое вмешательство проводится в соответствии с правилами.
Как предотвратить возникновение диафрагмальной грыжи у малыша? Родители должны регулярно отводить ребёнка к врачу для обследования организма. Чем раньше будет выявлена патология, тем выше вероятность предотвращения осложнений грыжи диафрагмы:
- Питание ребёнка должно быть рациональным. В детском меню должны присутствовать продукты с высоким содержанием клетчатки, чтобы предотвратить возникновение запоров;
- Приёмы пищи ребёнком должны быть частыми, но небольшими порциями. Это позволяет избежать переедания и предотвратить набор лишнего веса;
- Малыш не должен перенапрягаться физически, не поднимать тяжести, не соответствующие его массе тела;
- Для укрепления мышц диафрагмы ребёнок должен с ранних лет приучаться к простым физическим упражнениям. Ежедневная зарядка по утрам и лечебная физкультура благотворно влияет на состояние мышечной ткани диафрагмы;
- При возникновении инфекционных заболеваний, необходимо в короткие сроки начать лечение. Родители должны с помощью врачей не допускать развития хронического кашля у малыша;
- Мамы и папы должны успокаивать малыша во время плача, чтобы предотвратить развитие надрывной истерики;
- Ребёнок должен знать правила поведения на дома, на улице, в детских учреждениях, в транспорте. Это необходимо, чтобы предотвратить получение травмы диафрагмы.
Вооружайтесь знаниями и читайте полезную информативную статью о заболевании грыжа диафрагмы у детей. Ведь быть родителями – значит, изучать всё то, что поможет сохранять градус здоровья в семье на отметке «36,6».
Узнайте, что может вызвать недуг , как его своевременно распознать. Найдите информацию о том, каковы признаки, по которым можно определить недомогание. И какие анализы помогут выявить болезнь и поставить верный диагноз.
В статье вы прочтёте всё о методах лечения такого заболевания, как грыжа диафрагмы у детей. Уточните, какой должна быть эффективная первая помощь. Чем лечить: выбрать лекарственные препараты или народные методы?
Также вы узнаете, чем может быть опасно несвоевременное лечение недуга грыжа диафрагмы у детей, и почему так важно избежать последствий. Всё о том, как предупредить грыжа диафрагмы у детей и не допустить осложнений.
А заботливые родители найдут на страницах сервиса полную информацию о симптомах заболевания грыжа диафрагмы у детей. Чем отличаются признаки болезни у детей в 1,2 и 3 года от проявлений недуга у деток в 4, 5, 6 и 7 лет? Как лучше лечить заболевание грыжа диафрагмы у детей?
Берегите здоровье близких и будьте в тонусе!
detstrana.ru
Диафрагмальные грыжи у детей – клинические рекомендации
Это врожденная грыжа, встречающаяся у одного из пяти тысяч новорожденных. Суть патологии в том, что внутриутробно формирование диафрагмы происходит неправильно – в ней образуется отверстие. В этой статье мы рассмотрим диафрагмальные грыжи у детей – клинические рекомендации, причины заболевания.
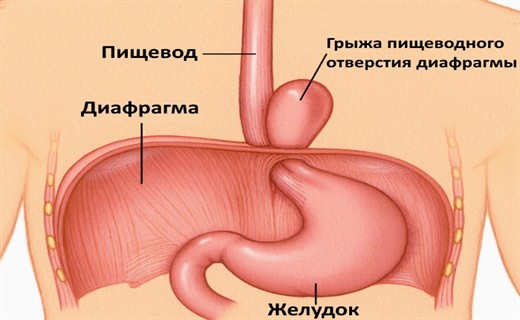
Причины
Под этим заболеванием следует понимать перемещение органов брюшной полости в грудную через естественное или патологическое отверстие в диафрагме. В отличие от грыж других локализаций диафрагмальная грыжа не всегда содержит весь комплекс таких обязательных компонентов, как грыжевой мешок, грыжевые ворота.
Врожденная диафрагмальная грыжа
В основном у грудничков отмечаются эти диафрагмальные грыжи, являющиеся пороком развития диафрагмы. Частота возникновения колеблется, по данным разных авторов, в больших пределах – от 1:2000 до 1:4000 новорожденных, при этом не учитывается большая группа мертворожденных с пороками развития диафрагмы. Истинная природа грыжи стала значительно более понятной с тех пор, как в практику было широко внедрено ультразвуковое обследование плода.
При врожденной диафрагмальной грыже часто встречаются сочетанные аномалии других органов и систем, поскольку неблагоприятное воздействие на эмбрион возникает в раннем периоде формирования внутренних органов (на 8-й неделе гестации). Недоразвитие мышц в отдельных участках грудобрюшной преграды приводит к возникновению грыж с мешком, стенки которого состоят из серозных покровов – брюшного и плевральных листков. Такие грыжи являются истинными.
При ложных грыжах имеется сквозное отверстие в диафрагме, которое образуется или в результате недоразвития плевроперитонеальной перепонки, или из-за разрыва ее вследствие перерастяжения. Механизм образования травматической диафрагмальной грыжи несложен. К разрыву диафрагмы ведет, по-видимому, резкое повышение внутрибрюшного давления, которое может наступить при тяжелых закрытых повреждениях грудной клетки, живота и таза.
Клинические рекомендации о диафрагмальной грыже
Каждый вид диафрагмальных грыж имеет довольно специфическую симптоматологию, хотя можно выделить два ведущих симптомокомплекса:
- сердечно-легочные нарушения, отмечаемые при ДПГ, сопровождающихся внутригрудным напряжением,
- и желудочно-пищеводный рефлюкс – при грыжах пищеводного отверстия диафрагмы.
Симптоматология ложных ДПГ в основном обусловлена степенью сдавления органов грудной полости. Ложные диафрагмальные грыжи у детей чаще, чем истинные, приводят к выраженному компрессионному синдрому.
Основные симптомы заболевания
Ведущими и наиболее частыми клиническими симптомами являются цианоз, одышка и другие признаки гипоксии. При осмотре, помимо цианоза, обращает на себя внимание асимметрия грудной клетки с выбуханием ее на стороне поражения. Живот за счет переместившихся в грудную полость органов часто выглядит запавшим и имеет ладьевидную форму. Перкуторно над соответствующей половиной грудной клетки определяется тимпанит, при аускультации – резкое ослабление дыхания. Сердечные тоны (при левосторонней грыже) слева почти не определяются, справа – громкие, ясные, что говорит о смещении сердца в здоровую сторону (декаропозиция.
Ухудшение состояния больных при кормлении обычно зависит от переполнения содержимым желудка и петель кишечника, находящихся в грудной полости. При истинных диафрагмально-плевральных грыжах выраженность симптомов в основном зависит от степени компрессии органов грудной полости. Чем больше грыжевое выпячивание, тем больше внутригрудное напряжение и ярче клиническая картина респираторных нарушений. В отличие отложных грыж этой локализации у малышей значительно реже отмечаются симптомы, связанные с ущемлением петель кишечника и кишечной непроходимости. Аускультация и перкуссия выявляют некоторое ослабление дыхания и тимпанит на стороне поражения.
Признаки диафрагмальной грыжи
При парастернальных грыжах симптомы не выражены и непостоянны, чаще выявляются у малышей ясельного и школьного возраста, когда они начинают жаловаться на болезненные, неприятные ощущения в эпигастрии. Иногда бывает тошнота и даже рвота. Респираторные и сердечно-сосудистые нарушения при этом виде грыж не характерны. Почти в половине всех случаев дети жалоб не предъявляют. Методом перкуссии и аускультации удается определить в этой зоне тимпанит и ослабление сердечных тонов.
Ведущими симптомами в клинической картине френоперикардиальных грыж являются цианоз, одышка, беспокойство, рвота. Возникают эти симптомы в результате нарушения сердечной деятельности, вызванной смещением в полость перикарда петель кишечника и развитием частичной тампонады сердца. Симптомы заболевания чаще появляются в первые недели и месяцы жизни. При осмотре, особенно у ребят старше 1-2 лет, выявляются деформации грудной клетки в виде выбухания со сглаживанием межреберных промежутков на стороне поражения. Возможна асимметрия живота с втяжением в области левого подреберья. Наблюдается исчезновение абсолютной или даже относительной сердечной тупости, определяется тимпанит, сердечные тоны приглушены, часто смещены. При ретроградных френоперикардиальных грыжах, когда наблюдается проллабирование сердца через имеющийся дефект, отмечаются сердечно-сосудистые нарушения.
Классификация
По происхождению и локализации диафрагмальную грыжу следует разделять следующим образом:
I.
Врожденные:
- диафрагмально-плевральные (ложные и истинные),
- парастернальные (истинные),
- френоперикардиальные (истинные),
- грыжи пищеводного отверстия (истинные),
II.
Приобретенные грыжи – травматические (ложные).
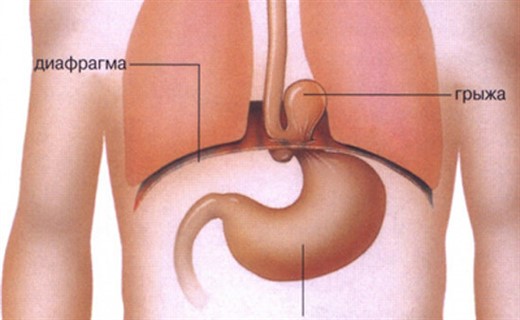
Парастернальные грыжи
Это истинные грыжи, различают загрудинные и загрудинно-реберные (щель Ларрея) парастернальные грыжи. Впервые грудино-реберную грыжу описал в 1761 г. G. P. Morgagni, в связи с этим многие авторы ее называют морганьевой грыжей. Ряд авторов левостороннюю грыжу называют грыжей Ларрея, а правостороннюю – грыжей Морганьи (М. Rizscher, 1957).
Френоперикардиальные грыжи
Это ложные грыжи, обусловлены дефектом в сухожильной части диафрагмы и прилежащем к нему отделе перикарда. Через дефект органы брюшной полости могут непосредственно смещаться в полость перикарда и наоборот – сердце может частично вывихиваться через дефект в брюшную полость.
Грыжи пищеводного отверстия диафрагмы
Диафрагмальные грыжи у детей всегда относятся к истинным и разделяются на две большие группы – параэзофагеальные и эзофагеальные. Для параэзофагеальных характерно смещение желудка вверх рядом с пищеводом. При эзофагеальных пищеводно-желудочный переход располагается выше уровня диафрагмы. При этом степень смещения желудка может быть разной и даже меняться в зависимости от положения ребенка и объема заполнения желудка.
Диафрагмально плевральная грыжа
Наиболее часто у мальчиков и девочек встречаются диафрагмально плевральные грыжи. Парастернальные грыжи встречаются значительно реже, френоперикардиальные, в сущности, являются казуистикой.
Диафрагмально плевральная грыжа может быть как истинной, так и ложной. Часто они бывают левосторонними. Ложные грыжи справа наблюдаются очень редко. Истинные грыжи могут занимать ограниченную часть диафрагмы, но бывают значительных размеров и полными. При ложных грыжах дефект в диафрагме чаще всего щелевидный и располагается в реберно-позвоночном отделе (грыжа Богдалека). Из-за отсутствия грыжевого мешка при этих видах грыж органы брюшной полости перемещаются в грудную полость без ограничения, что чаще приводит к синдрому грудного напряжения. При диафрагмально плевральных грыжах часто отмечаются недоразвитие легких, пороки сердца, центральной нервной системы и желудочно-кишечного тракта.
Теперь вам известны клинические рекомендации о диафрагмальной грыже у детей, причины и классификацию заболевания.
www.medmoon.ru
Диафрагмальная грыжа у новорожденного: причины, симптомы и лечение
У новорождённых детей диафрагмальная грыжа имеет врожденный характер. Аномалия развития является сопутствующим заболеванием при патологиях желудочно-кишечного тракта, почек, сердечно-сосудистой и центральной нервной системы. Редкий недуг связан с изменением естественного положения органов брюшной полости. Желудок, пищевод, кишечник при диафрагмальной грыже у маленьких детей смещается в область грудной клетки.

Особенности развития заболевания
Аномалия начинает активно развиваться еще во время вынашивания плода. На 2 месяце беременности начинается формирование естественного барьера между органами брюшной полости и соединительной тканью сердца. В этот момент в некоторых случаях происходит нарушение сокращения мышц, образование грыжевого мешка, в результате чего наблюдается расширение пищеводного отверстия диафрагмы.
Через разрыв соединительной мембраны желудок может перемещаться в грудную зону. Степень тяжести заболевания зависит от объема органов пищеварительной системы, переместившихся из брюшной полости, сопутствующих аномалий развития: почечная недостаточность, порок сердца и нервной системы, патологии кишечного тракта.
Классификация
У плода может развиться диафрагмальная грыжа разной формы: по времени возникновения, наличию обволакивающей пленки, месту расположения и стороне расположения.
Время возникновения:
- врожденные;
- приобретенные.
Наличие обволакивающей пленки:
- истинная;
- ложная.

Место расположения:
- диафрагмально – плевральная;
- парастернальная окологрудинная;
- френоперикардиальная;
- пищеводное отверстие.
Сторона расположения:
- левосторонняя;
- правосторонняя.
Появление грыжевого мешка свидетельствует об истинной форме патологии, отсутствие – ложной разновидности. Обволакивающая пленка может располагаться в окологрудинном, френоперикардиальном отделе, полости плевры, пищеводном отверстии. При ложной форме у грудничка происходит внутриутробное перемещение органов пищеварительной системы. У новорожденных детей чаще встречается левосторонняя грыжа, но разрыв может наблюдаться и в правой стороне диафрагмы.
Причины возникновения
Патология развивается вследствие генетических мутаций эмбриона на начальном периоде формирования внутренних органов в утробе матери. Причинами появления врожденной формы диафрагмальной грыжи являются:
- тяжелое протекание беременности;
- ранний токсикоз;
- сбои функционирования желудочно-кишечного тракта у беременной женщины: нарушение стула, вздутие;
- перенесенные вирусные, инфекционные, простудные заболевания во время беременности;
- употребление алкоголя, табачной продукции, наркотических веществ на ранних сроках;
- заболевания органов дыхания хронической формы;
- длительный прием токсичных медикаментов во время вынашивания ребенка;
- эмоциональное перенапряжение, частая подверженность стрессовым ситуациям;
- негативное воздействие факторов окружающей среды: экология, вредные химические выбросы на производстве, радиация.
Врожденная истинная или ложная разновидность заболевания связана с наличием у матери внутренних патологий, характером протекания беременности.
Приобретенная форма грыжи диафрагмы обусловлена частыми запорами у младенца, постоянным сильным плачем, криком. В результате чего происходит ослабевание тонуса дыхательной мышцы, повышение внутрибрюшного давления.
Проявления патологии
Порок внутриутробного развития сопровождается другими аномалиями, связанными с функционированием жизненно важных органов новорожденного. Это обусловлено смещением желудка, пищевода, что приводит к давлению на легкие, сердце. Симптомы врожденной или приобретенной формы диафрагмальной грыжи не зависят от наличия мешка, места образования разрыва соединительной мембраны. Признаки патологии после рождения ребенка бывают основные и общие.
Основные:
- рвота;
- тошнота;
- негромкий плач;
- кашель;
- ассиметричное расположение грудной клетки;
- одышка, прерывистое дыхание;
- учащенный пульс.
Общие:
- низкие показатели массы тела;
- бледный цвет кожных покровов;
- сниженный аппетит;
- выделение рвотных, каловых масс с примесями крови;
- патологии сердечно-сосудистой, дыхательной системы.

Основным признаком образования диафрагмальной грыжи у детей является цианоз – бледность кожных покровов. Заболевание связано с недостаточным насыщением крови кислородом. При разрыве соединительной мембраны малыш задыхается, не заглатывает достаточное количество воздуха. Нехватка кислорода может привести к летальному исходу. Серьезным осложнением диафрагмальной грыжи вследствие выпячивания органов пищеварительной системы является изменение положения сердечной мышцы, что приводит к асимметрии грудной клетки, западанию живота.
На симптоматику заболевания влияет размер грыжевого мешка, расположение выпяченных органов пищеварительного тракта, сопутствующие пороки развития ребенка. Косвенные признаки указывают на нарушения функционирования, наличие воспалительных процессов, ВДГ.
При поражении пищеводного отверстия может наблюдаться отрыжка, срыгивание после кормления, трудное проглатывание пищи. При парастернальной окологрудинной форме грыжи появляются болевые ощущении в области живота, тошнота, но отсутствуют проблемы с дыханием.
Диагностирование порока развития
Установить образование грыжи можно на ранних сроках беременности. В течение всего периода вынашивания плода будущая мама проходит ультразвуковое обследование, результаты которого показывают внутриутробное развитие малыша. Признаком патологии диафрагмы является многоводие у беременной женщины и смещение сердца, печени, нарушение венозного оттока у ребенка.

При подозрении на порок развития берется забор околоплодной жидкости путем прокола амниотической оболочки плода для проведения лабораторного исследования. Для рассмотрения органов брюшной, грудной полости по назначению лечащего врача могут провести магнитно-резонансную томографию. После появления на свет младенца назначается рентгенография для исключения серьезных заболеваний: внутренних кровоизлияний в мозг, кисты, пороков сердечно-сосудистой и дыхательной системы, раковых новообразований, опухолей.
Методы лечения грыжи
Если патология обнаружена во время вынашивания плода, то лечение диафрагмальной грыжи подразумевает внутриутробное хирургическое вмешательство. Операция проводится на разрешенном сроке – 26-28 недель беременности. Задача хирургического лечения диафрагмальной грыжи у малыша – введение баллона через разрезанную матку в область трахеи плода для стимуляции работы органа дыхательной системы, вытеснения обволакивающей пленки. Извлечение аппарата происходит во время родовой деятельности. Внутриутробная операция назначается только при тяжелой форме патологии.
При обнаружении патологии после рождения ребенка хирургическое вмешательство назначается до достижения малышом 1 года. Экстренная госпитализация осуществляется при внутреннем кровотечении, ущемлении грыжи.
В ходе операции выпяченные органы перемещают в искусственно созданный мешок, а затем устраняют разрыв дыхательной мышцы через некоторое время после первого этапа хирургического вмешательства. После проведенной процедуры у ребенка могут наблюдаться опасные осложнения:
- воспаление, отек легких;
- непроходимость пищи через кишечник;
- обезвоживание;
- лихорадка.

Возможные серьезные последствия встречаются после удаления парастернальной формы грыжи. После операции ребенку искусственно продувают легкие. Во избежание рецидива патологии врач назначает режим питания, грудного вскармливания малыша.
Меры профилактики
Чтобы избежать внутриутробной аномалии развития плода, необходимо заранее планировать беременность, соблюдать рекомендации в период вынашивания ребенка. Перед зачатием женщине нужно пройти комплексное обследование, сдать лабораторные анализы, пропить курс витаминно-минеральных препаратов, вести здоровый образ жизни.
Основными правилами на ранних сроках беременности являются:
- избегание стресса, умственного и физического перенапряжения;
- физические упражнения: йога, дыхательная гимнастика;
- отказ от курения, употребления алкоголя, наркотиков;
- активный образ жизни: правильное, сбалансированное питание, регулярные прогулки на свежем воздухе.
Информация на нашем сайте предоставлена квалифицированными врачами и носит исключительно ознакомительный характер. Не занимайтесь самолечением! Обязательно обратитесь к специалисту!

Автор: Румянцев В. Г. Стаж 34 года.
Гастроэнтеролог, профессор, доктор медицинских наук. Назначает диагностику и проводит лечение. Эксперт группы по изучению воспалительных заболеваний. Автор более 300 научных работ.
gastrot.ru
Родители, которым говорили, что нужно позволить ребенку умереть, делятся историей о своем чудесном растущем младенце
Сегодня все больше родителей осведомлены о заболевании, которое называется ВДГ (врожденная диафрагмальная грыжа). Несмотря на всю серьезность данного заболевания, стоит знать, что оно не является смертным приговором вашему ребенку.
 Врожденная диафрагмальная грыжа
Врожденная диафрагмальная грыжаПри врожденной диафрагмальной грыже органы брюшной полости (чаще всего желудок и кишечник) перемещаются через щель в диафрагме вверх, начиная давить на сердце и легкие. Такая аномалия может начать развиваться на 4-й неделе беременности, когда формируется перегородка между местом расположения сердца и легких и туловищем. Выявить развитие этого заболевания можно во второй половине беременности, когда на УЗИ будет отчетливо видно, что кишечник давит на легкие плода. Для того, чтобы поставить точный диагноз дополнительно проводят рентген органов брюшной полости. Если у ребенка действительно есть это заболевание — на рентгене будет видно перемещение кишечных петель.
Диафрагмальная грыжа нередко сопутствует таким хромосомным заболеваниям, как:
- синдром Дауна;
- синдром Эдвадса;
- синдром Патау.
Выраженность симптомов диафрагмальной грыжи зависит от того, насколько сильное давление внутренние органы.
Родители, ребенку которых был поставлен диагноз «врожденная диафрагмальная грыжа» еще в утробе, не пожелали слушать советов по поводу того, что нужно дать этому ребенку умереть, решив бороться за его жизнь до конца. И не прогадали.
Отец поделился историей своей дочери на сайте Imgur. Малышке был поставлен этот страшный диагноз на 20-й неделе.
«Шанс выжить с этим заболеванием может составлять меньше 50% — все зависит от нескольких факторов. Один из наших врачей сказал нам с женой, что лучше просто позволить «этому ребенку уйти»
— говорит отец девочки
They told us to «let this one go»
Но такая рекомендация не устраивала родителей.
Консультация по поводу тяжести состояния их дочери, натолкнула родителей на мысль, что нужно искать помощи в месте, где специалисты хорошо осведомлены об этой болезни и уже лечили детей с подобной проблемой. Таким образом, новоиспеченным родителям пришлось отправиться в длительное путешествие из Санкт-Петербурга в Детскую больницу в Джексонвилле.
«Уже через пять минут после встречи с доктором Кейсом и его командой мы знали, что рождение каждого ребенка является правильным выбором. Наша дочь появилась на свет на 39 неделе. Ее сразу же интубировали, всячески успокаивали, для поддержания артериального давления в пределах нормы ей давали дофамин, также ей установили периферийный и центральный катетеры, некоторое время она находилась на парентеральном питании»
На четвертый день жизни ей провели операцию по восстановлению диафрагмы. Когда малышке исполнилось 29 дней, благодарный отец написал в своем аккаунте:
«Я никогда не собираюсь отпускать ее».
«Во время общения с другими родителями, мы обнаружили, что их опыт был во многом похож на наш. Их также убеждали сделать аборт, и они также отчаянно искали альтернативный вариант решения проблемы»
— рассказывает отец
Многие неправильно понимают диагноз «врожденная диафрагмальная грыжа», полагая, что он является смертельным приговором, но это не так. Есть высокие шансы, что при должной медицинской помощи, ребенок с этим диагнозом сможет избавиться от своего недуга. Герой этой истории надеется, что поделившись своим опытом, он хоть немного повысит осведомленность окружающих об этом заболевании, которое пугает многих будущих родителей, и поможет им обрести надежду на то, что несмотря на диагноз, их ребенок может вырасти здоровым и счастливым.
Автор admin Комментариев: 0
puziko.org
Пороки развития диафрагмы у новорожденных > Клинические протоколы МЗ РК
Далее параметры корректируют под контролем PaCO2 и PaO2.(D)
• Ингаляция оксида азота [4,9] используется для снижения легочного сосудистого сопротивления пациентов, которые плохо отвечают на механическую вентиляцию легких и заместительную терапию сурфактантом. Молекула оксида азота NO продуцируется эндогенно при взаимодействии фермента нитроксидсинтетазы и аргинина, что ведет к вазодилатации. Ингаляция оксида азота позволяет достичь селективнойвазодилатации сосудов легких. Доза iNO подбирается от 1 до 20 ppm до получения клинического эффекта. Продолжительность не более 7 сут. При положительном эффекте (улучшение оксигенации и степени легочной гипертензии) концентрацию NO снижают ступенчато до 5 ppmв первые 4-6 часов. Далее снижение на 1ppm медленно, в течении 1-5 сут. критериями отмены ингаляции NO является РаО2 более 50-60 мм.рт.ст. при FiO2 менее 0,6 и концентрация NO, равной 1ppm в течении 60 мин.Перед разъединением с контурам пациента необходимо увеличить FiO2 на 10-15%.При ингаляции оксид азота возможно образование метгемоглобина: его уровень в крови не должен превышать 2,5%. (D)
Респираторная терапия после операции [4] : (D)
• После операции продолжают проводить ИВЛ с параметрами, которая проводилась во время операции.
• Переход от ВЧ на традиционную ИВЛ проводиться пари снижени Paw ниже 12,0 и FiO2<0,4 : PIP до 25 см. вод. ст., PEEP 3-5 см вод.ст., Tin 0,35 сек.
• При появлении попыток адекватного спонтанного дыхания ребенок переводится на вспомогательную вентиляцию.
• Прекращение МВ с экстубацией и переводом на СРАР необходимо осуществлять в как можно более ранние сроки после операции, в том случае, если это клинически безопасно и концентрации газов крови приемлемы (D)
• Критерии Экстубации [5.4.3.] (D)
PIP менее 14-18 см. вод. Ст
PEEP менее 4 см вод.ст
FiO2=0,4
Частота дыхания менее 60 в минуту
• При отлучении от МВ допускается умеренная степень гиперкапнии, при условии, что рН сохраняется на уровне выше 7,22
Медикаментозное лечение [2,3,4]
Обезболивание (D)
До операции показано инфузионное введение седативных, обезболивающих или миорелаксирующих препаратов:
– Диазепам или медозалам 0,1 мг/кг/час
– Промедол 0,1-0,2 мг/кг/час
– Фентанил 1-3 мкг/кг /час(для предотвращения симпатической легочной вазоконстрикции в ответ на серьезные внешние воздействия (такие, как санация трахеи).
– Пипекурония бромид 0,025мг/кг/час
Послеоперационное обезболивание:
внутривенная постоянная инфузия фентанила 5-10мкг/кг/час в сочетании ацетаминофеном (парацетамол) ректально или внутривенно в разовой дозе 10-15 мг/кг 2-3 раза в сутки или метамизолом натрия 5-10 мг/кг 2-3 раза внутривенно;
• Дозировка анальгетиков и длительность введения подбираются индивидуально в зависимости от выраженности болевого синдрома(D)
• При десинхронизации ребенка с аппаратом ИВЛ вводятся седативные препараты:
– Мидозалам (реланиум) до 0,17 мг/кг/час (с постоянной инфузией). Следует избегать применения у новорожденных до 35 недель гестации
– Фенобарбитал (10-15 мг/кг/сутки)Антибактериальная терапия [4] (D)
Всем новорожденным антибактериальную терапию следует начинать сразу после рождения до полного исключения возможной реализации тяжелой бактериальной инфекции (сепсис, пневмония, нагноение послеоперационной раны).
При эмпирическом лечении в качестве «стартовой терапии» схема должна включать 2 антибиотика широкого спектра действия.[1,5,10] (таблица 2).
Выбор антибактериальных препаратов.
Антимикробные химиопрепараты | Показания к применению |
| Препараты «стартовой» терапии | |
Антибиотики: ∼ Цефалоспорины I-IIпоколения ∼ Аминогликозиды ∼ Аминопенициллины ∼ Макролиды(по показаниям) | Инвазивный – с целью профилактики тяжелой бактериальной инфекции (пневмоний, сепсиса), как монотерапия, так и в комбинации. |
| Препараты «резерва» | |
∼ Цефалоспорины III-IV поколения ∼ АминогликозидыII-III поколения ∼ Карбапенемы (имипенем, меропенем) ∼ Рифампицин | Инвазивные – тяжелые формы с гнойно-воспалительным компонентом в очаге или осложнениями (гнойный плеврит, пневмоторакс), среднетяжелые – при неэффективности препаратов стартовой терапии. |
«Препаратами резерва» при лечении ВПР легких у новорожденных служат карбапенемы, которые при проведении эмпирической терапии назначаются в случаях неэффективности предшествующего лечения или по витальным показаниям.
В каждом неонатальном отделении должны разрабатываться собственные протоколы по использованию антибиотиков, основанных на анализе спектра возбудителей, вызывающих ранний сепсис.
Антибактериальные препараты для лечения инфекций у доношенных новорожденных. [10] (D)
Таблица 2
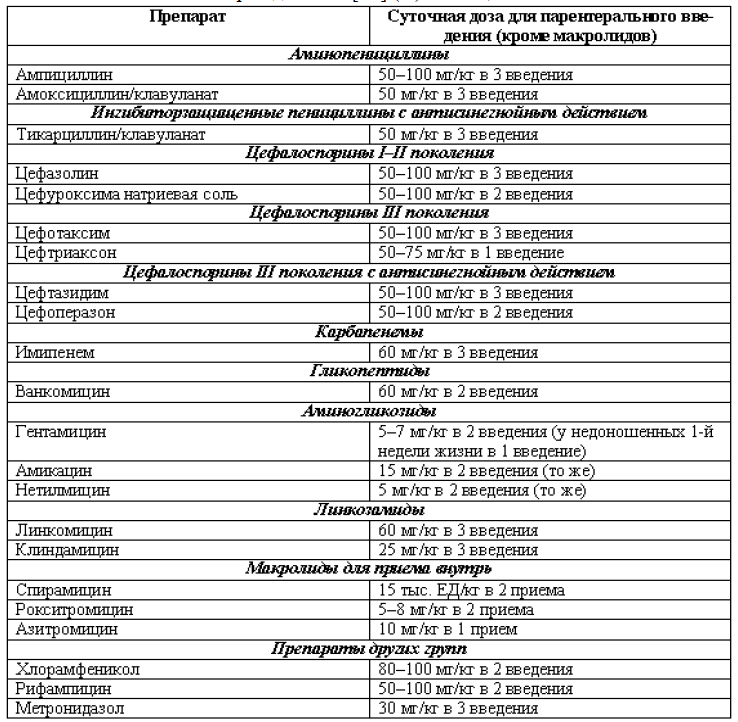
Противогрибоковая терапия [4] (D)
Со 2-3 суток жизни назаначается протвогрибковый препарат:
– флуконазол в дозе 3мг/кг два раза в неделю в течение 6 недель
В отделениях с высокой частотой инвазивных грибковых инфекций рекомендуется проводить профилактическое лечениеИнфузионная терапия [3,4,5] (D)
• Большинству новорожденных должно быть начато внутривенное введение жидкостей по 70-80 мл/кг в день. Объем инфузионной терапии может быть очень вариабельным, но редко превышает 100-150 мл/кг/сут.
• У новорожденных объем инфузии и электролитов должен рассчитываться индивидуально, допуская 2,4-4% потери массы тела в день (15% в общем) в первые 5 дней
• Прием натрия должен быть ограничен в первые несколько дней постнатальной жизни и начат после начала диуреза с внимательным мониторингом баланса жидкости и уровня электролитов.
Если есть гипотензия или плохая перфузия 10-20 мл / кг 0,9% NaCl следует вводить один или два раза . [4] (D)
РАСЧЕТ НЕОБХОДИМОГО ОБЪЕМА ЭЛЕКТРОЛИТОВ [11] (А)
Введение натрия и калия целесообразно начинать не ранее третьих суток жизни, кальция с первых суток жизни.
РАСЧЕТ ДОЗЫ НАТРИЯ
− Потребность в натрии составляет 2 ммоль/кг/сутки
− Гипонатрийемия<130 ммоль/л, опасно < 125 ммоль/л
− Гипернатрийемия> 150 ммоль/л, опасно > 155 ммоль/л
− 1 ммоль (мЭкв) натрия содержится в 0,58 мл 10% NaCl
− 1 ммоль (мЭкв) натрия содержится в 6,7 мл 0,9% NaCl
1 мл 0,9% (физиологического) раствора хлорида натрия содержит 0,15 ммольNaКОРРЕКЦИЯ ГИПОНАТРИЕМИИ (Na< 125 ммоль/л)
Объем 10% NaCl(мл) = (135 –Naбольного) ×mтела×0.175
РАСЧЕТ ДОЗЫ КАЛИЯ
− Потребность в калии составляет 2 –3 ммоль/кг/сутки
− Гипокалиемия< 3,5 ммоль/л, опасно < 3,0 ммоль/л
− Гиперкалиемия>6,0 ммоль/л (при отсутствии гемолиза), опасно > 6,5 ммоль/л (или если на ЭКГ имеются патологические изменения)
− 1 ммоль (мЭкв) калия содержится в 1 мл 7,5% KCl
− 1 ммоль (мЭкв) калия содержится в 1,8 мл 4% KCl
V(мл 4% КCl) = потребность в К+(ммоль) ×mтела×2
РАСЧЕТ ДОЗЫ КАЛЬЦИЯ
− Потребность в Са++у новорожденных составляет 1-2 ммоль/кг/сутки
− Гипокальциемия<0,75 –0,87 ммоль/л (доношенные –ионизированный Са++), < 0,62 –0,75 ммоль/л (недоношенные –ионизированный Са++)
− Гиперкальциемия>1,25 ммоль/л (ионизированный Са++)
− 1 мл 10% хлорида кальция содержит 0,9 ммольСа++
− 1 мл 10% глюконата кальция содержит 0,3 ммольСа++РАСЧЕТ ДОЗЫ МАГНИЯ:
− Потребность в магнии составляет 0,5 ммоль/кг/сут
− Гипомагниемия< 0,7 ммоль/л, опасно <0,5 ммоль/л
− Гипермагниемия> 1,15 ммоль/л, опасно > 1,5 ммоль/л
− 1 мл 25% магния сульфата содержит 2 ммоль магния
Поддерживать необходимый уровень артериального давления с помощью адекватной объемной нагрузки
• Восполнение ОЦК при гипотензии рекомендуется проводить 0,9% раствором хлорида натрия по 10-20 мл/кг, если была исключена дисфункция миокарда (коллоидные и кристаллоидные растворы)[5,11] (D)
• и инотропных препаратов [5](D)
− дофамин 5-15 мкг/кг/мин,
− добутамин 5-20 мкг/кг/мин,
− адреналин 0,05-0,5 мкг/кг/мин.• Поддержание тканевой перфузии. Алкализация является важнейшим звеном терапии пациентов с ВДГ, так как позволяет быстро достичь и эффективно поддерживать легочнуювазодилатацию. Алкалоз может быть достигнут благодаря гипервентиляции (гипокапния) или внутривенному введению бикарбоната натри 4%, т.е. посредством продолжительного микроструйного переливания под контролем рН. Рекомендуемый уровень рН – более 7,4-7,45. (D)
Персистирующая легочная гипертензия. Неселективные вазодилататоры – это препараты-донаторы NO-группы. Следует помнить, что необходимым условием их безопасного применения является стабильная системная гемодинамика.(D)
• Силденафил натрия [3,4,12,13] (относится к препаратам Off label- нет показаний в инструкции применения в использованию при легочной гипертензии у новорожденного) в начальной дозировке 1 мг/кг/сут в 4 приема. Максимально допустимая доза до 8 мг/кг/сут. (D)
• Раствор магния сульфата 25% разводят в двукратном объеме 5% раствора глюкозы для получения концентрации 8,5%. Начальную дозу 20-250мг/кг вводят в течении 30 мин. повторную дозу вводят через 8-12 часов с индивидуальным титрованием дозы 10-50 мк/кг/час. Максимально допустимая доза 400мг/кг.[4] (D)
• Концентрации гемоглобина должны поддерживаться в пределах нормального диапазона значений. Предполагаемое п
diseases.medelement.com

