Неспецифический спондилит: Неспецифический спондилит
Воспалительные заболевания позвоночника – операции и лечение в Москве, цены на сайте ГВКГ им. Н.Н. Бурденко
Воспалительные заболевания позвоночника (спондилиты), могут возникать после любого общего инфекционного заболевания. Спондилиты бывают первичными и вторичными, могут протекать острои хронически. В клинической картине спондилитов существуют значительные различия, обусловленные локализацией воспалительного процесса в позвоночнике и распространенностью костных разрушений. Наиболее частым признаком является боль и повышение температуры тела, позже присоединяются неврологические и септические осложнения.
Спондилиты могут быть неспецифическими (гнойными), вызываться различными бактериями и специфическими (туберкулез, сифилис, гонорея, актиномикоз, бруцеллёз).
Гематогенный остеомиелит позвоночника (спондилит) – тяжелое заболевание, которое распознается с трудом, часто в поздние сроки, когда уже происходит деструкция (разрушение) тел позвонков.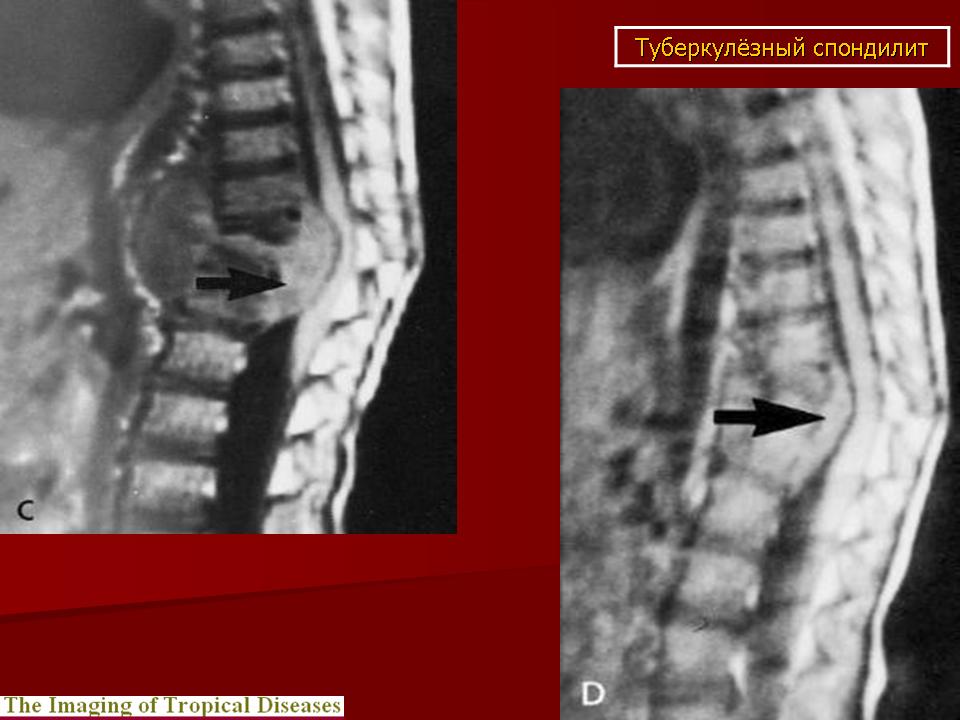 Чаще всего очаг поражения располагается в грудном и поясничном отделах позвоночника, редко в шейном. Поражение тел позвонков, а иногда дужек может возникнуть как метастаз при фурункулезе, ангине, кариесе зубов, после операций на брюшной полости, почках и органах малого таза. Местное инфицирование наблюдалось при проведении поясничной блокады позвоночника, люмбальных пункций, анестезий и операциях на дисках.
Чаще всего очаг поражения располагается в грудном и поясничном отделах позвоночника, редко в шейном. Поражение тел позвонков, а иногда дужек может возникнуть как метастаз при фурункулезе, ангине, кариесе зубов, после операций на брюшной полости, почках и органах малого таза. Местное инфицирование наблюдалось при проведении поясничной блокады позвоночника, люмбальных пункций, анестезий и операциях на дисках.
Для диагностики спондилитов используется рентгенография, компьютерная томография, магнитно-резонансная томография, сцинтиграфия, лабораторные данные.
Для радикального лечения необходима хирургическая операция – задняя внутренняя фиксация позвоночника, а при выраженных разрушениях позвонкови образовании гнойных затеков и передние операции с резекцией тел позвонков и санацией патологического очага. В дальнейшем проводится антибиотикотерапия и динамическое наблюдение. К сожалению, отказ от активной хирургической тактики лечения приводит порой к непоправимым осложнениям.
Спондилит – болезнь позвоночника | Блог ММЦ Клиника №1 Люблино, Москва
29.01.2021
Спондилит – заболевание позвоночника, при котором развивается воспаление и происходит первичное разрушение тел позвонков. Болезнь деформирует позвоночник: постепенно позвонки срастаются друг с другом или с другими частями скелета – ребрами, крестцом и даже костями таза.
При спондилите позвонков связки позвоночника окостеневают, провоцируя сильные боли и существенно снижая подвижность. Чем дольше затягивается диагностика и лечение спондилита, тем выше риск оказаться обездвиженным и в инвалидном кресле.
Причины
Спондилит возникает из-за поражения иммунной системы инфекционными заболеваниями и имеет течение аутоиммунной патологии. Иммунная система дает сбой и атакует собственные клетки, тем самым разрушая костную ткань. Организм восполняет костную массу за счет образования рубцов. Рубцы соседних костей со временем срастаются, образуя одно неподвижное соединение.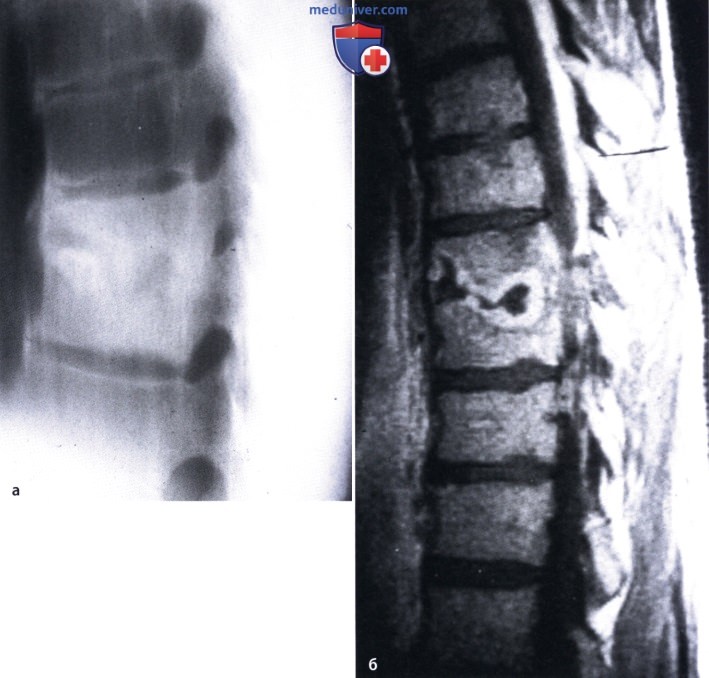
Спондилит бывает специфический и неспецифический. Специфический вызван определенным заболеванием. Неспецифический является осложнением заболевания или возникает после оперативного вмешательства и других инвазивных процедур.
Основным возбудителем специфического спондилита является золотистый стафилококк, однако заболевание может возникнуть из-за туберкулезной палочки (развивается туберкулезный спондилит), возбудителей сифилиса, гонореи и бруцеллеза, а также энтеробактерий и других патогенов.
Неспецифический гематогенный гнойный спондилит, как правило, возникает в грудном и поясничном отделах позвоночника, редко – в шейном. Может стать осложнением фурункулеза, ангины, зубного кариеса и проявиться после операций на брюшной полости, почках и органах малого таза.
Со счетов не стоит сбрасывать и генетическую предрасположенность: если в семье кто-то болел или болеет спондилитом, риск обнаружить заболевание у следующего поколения достаточно велик.
Симптомы и стадии спондилита
Спондилит проявляется в 20-30 лет и чаще от него страдают мужчины.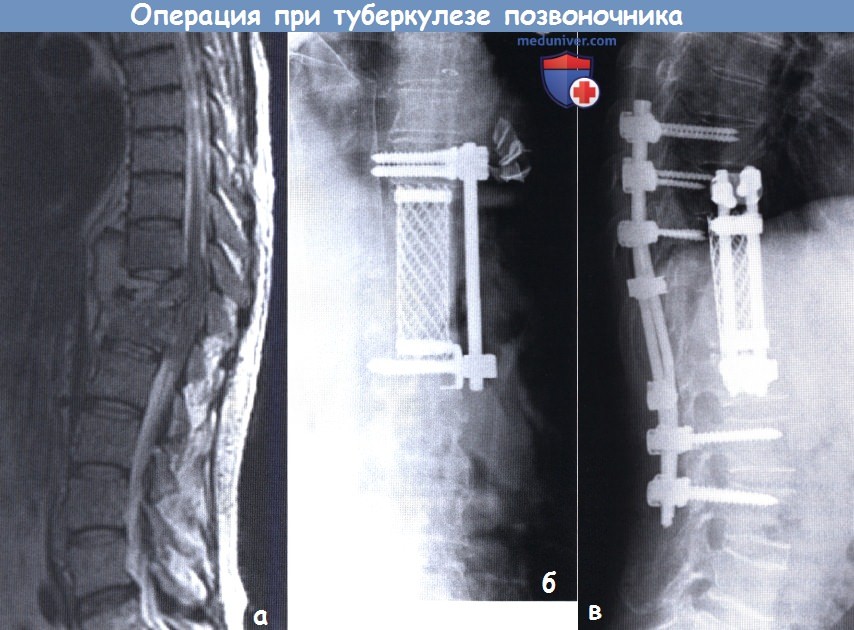
На первичной стадии наблюдаются слабые боли в спине в области поясницы. Симптомы не настолько существенны, чтобы пациент незамедлительно обратился за помощью к врачу.
Со временем боли в пояснице становятся сильнее, появляются чаще и длятся дольше. Отдых и сон облегчения не приносят. По утрам присутствует ощущение скованности, которое постепенно проходит от незначительной физической подвижности.
На вторичной стадии заболевания спондилит перемещается с поясничного отдела позвоночника на грудной и шейный. Характерные признаки: очень сильные боли в спине (не только в пояснице), которые сложно заглушить обезболивающим. Движения скованные и ограниченные из-за постоянного мышечного напряжения.
Развитие спондилита позвонков ведет к мышечной атрофии, а сращивание с ребрами ограничивает подвижность грудной клетки и приводит к проблемам с дыханием. Кроме того, при аутоиммунных заболеваниях происходит поражение любых здоровых клеток, включая клетки внутренних органов. Поэтому спондилит может стать причиной поражения сердца, почек, легких, глаз и других органов.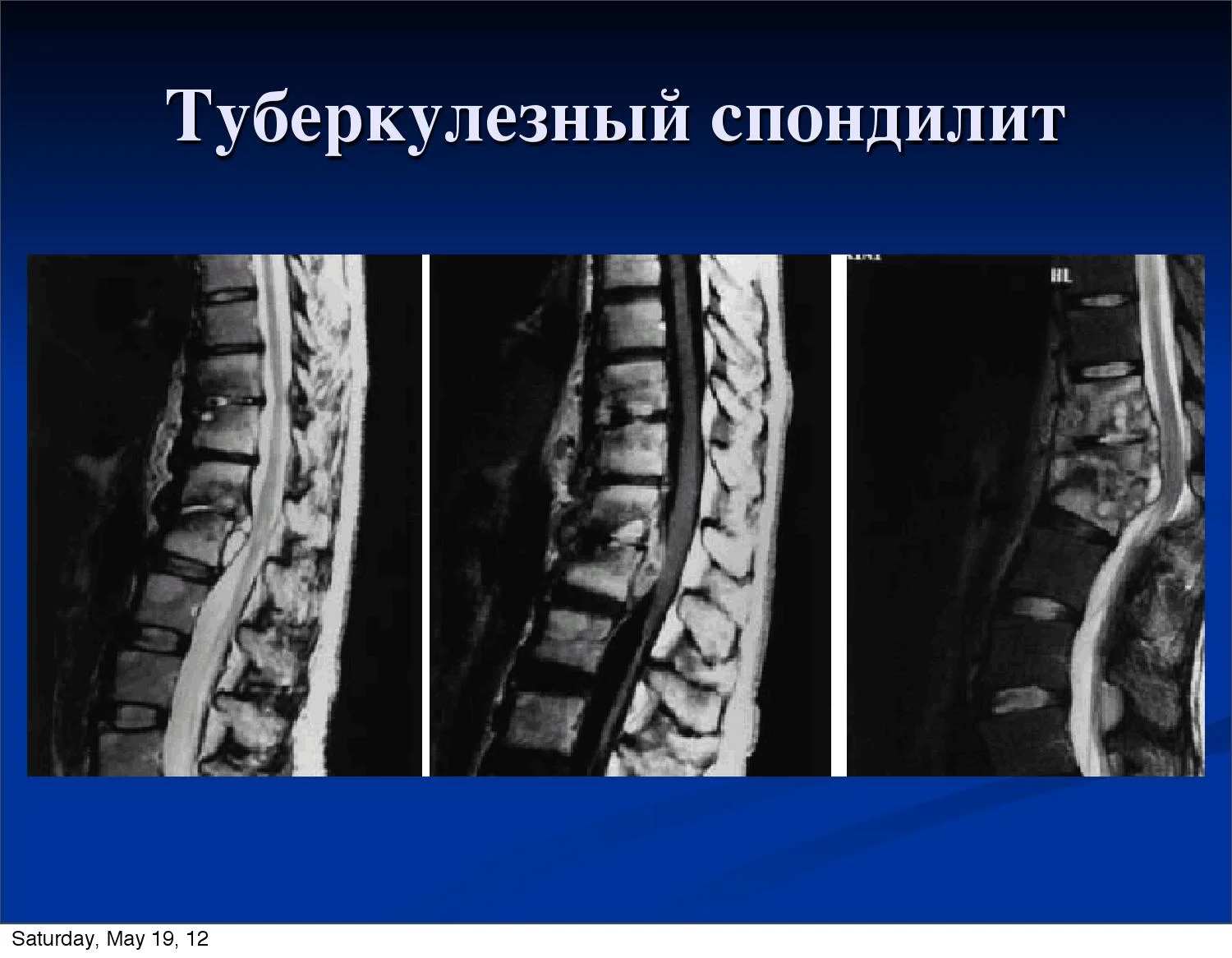
Диагностика
Спондилит любого типа и на любой стадии диагностируется с помощью рентгенографии, компьютерной томографии, магнитно-резонансной томографии, сцинтиграфии и лабораторных исследований (анализ крови, анализ мочи и другие анализы при необходимости).
Необходимые для диагностики процедуры определяет лечащий врач на основании анамнеза: первичного осмотра, жалоб больного и результатов предыдущих обследований, если такие есть.
Лечение
Лечение зависит от типа спондилита, возбудителя и стадии заболевания. На первичной стадии главная задача врача – устранить источник. Если это бактериальная инфекция назначается курс антибиотиков. Если спондилит является осложнением другого заболевания, задача врача – вылечить это заболевание и одновременно замедлить развитие спондилита. Если спондилит позвонков, – специфический или неспецифический, – запущен, требуется операция или несколько операций плюс медикаментозная терапия и длительная реабилитация.
При лечении спондилита любого типа и на любой стадии может потребоваться стабилизация позвоночника, физиотерапия, а также медикаментозная терапия. Конкретные методы лечения и лекарственные препараты подбирает лечащий врач.
Конкретные методы лечения и лекарственные препараты подбирает лечащий врач.
Спондилит нельзя вылечить полностью, но можно максимально замедлить его развитие. Поэтому своевременное обращение к врачу может предупредить появление инвалидного кресла в жизни пациента.
После курса лечения по рекомендации врача необходимо периодически делать КТ, МРТ или рентген и сдавать анализы (С-реактивный белок и СОЭ).
Фото:ru.freepik.com
Спондилит как осложнение перенесенного уросепсиса и инфекционного эндокардита (клиническое наблюдение) | Третьякова Н.А., Суханин В.С., Вдовушкина Т.А.
Введение
Спондилит — воспалительное деструктивное заболевание позвоночника и его структурных элементов (тел, межпозвонковых дисков, связочного аппарата, межпозвонковых суставов). Спондилиты подразделяются на инфекционные и неинфекционные (асептические), в свою очередь, инфекционные включают в себя неспецифические и специфические (туберкулезный, бруцеллезный, паразитарный, сифилитический).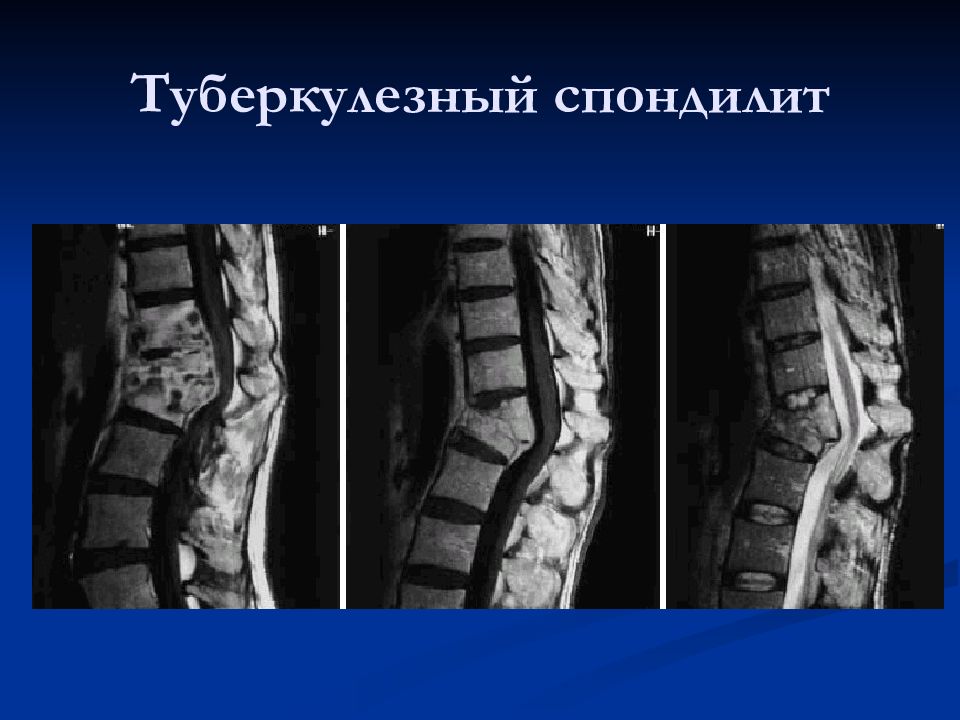 Спондилит является весьма актуальной проблемой, что объясняется увеличением частоты данного заболевания более чем в 10 раз за последние 30 лет [1, 2]. Среди гнойно-воспалительных заболеваний позвоночника инфекционный спондилит занимает 3–8% [3–5]. Локализованный в позвоночнике воспалительный процесс трудно диагностируется, сложнее вылечивается и тяжелее протекает, чем гнойно-воспалительное поражение, протекающее за пределами костной ткани. Повышение операционной активности, включая лиц пожилого возраста с наличием сопутствующих заболеваний, за последние годы привело к росту последующих осложнений, в т. ч. спондилитов.
Спондилит является весьма актуальной проблемой, что объясняется увеличением частоты данного заболевания более чем в 10 раз за последние 30 лет [1, 2]. Среди гнойно-воспалительных заболеваний позвоночника инфекционный спондилит занимает 3–8% [3–5]. Локализованный в позвоночнике воспалительный процесс трудно диагностируется, сложнее вылечивается и тяжелее протекает, чем гнойно-воспалительное поражение, протекающее за пределами костной ткани. Повышение операционной активности, включая лиц пожилого возраста с наличием сопутствующих заболеваний, за последние годы привело к росту последующих осложнений, в т. ч. спондилитов.
При инфекционном спондилите заражение чаще всего происходит гематогенным, реже — контактным путем. Возбудитель проникает в позвонок по сосудистым сообщениям между венозными сплетениями малого таза и позвоночника. Наиболее часто к инфицированию позвоночного столба приводит хроническая инфекция мочеполовой системы, холецистит, флегмоны, абсцессы, фурункулы в области позвоночника, инородные тела (последствия огнестрельных ранений, травм позвоночника).
Ключевым звеном патогенеза острого гематогенного спондилита является формирование очага острого воспаления в кости, характеризующегося комплексом стандартных сосудистых и тканевых изменений. Важной особенностью воспалительного процесса является то, что он замкнут ригидными стенками костной трубки, что приводит к сдавливанию вен и артерий. Костная гипертензия проявляется в виде болевого синдрома. Несмотря на то, что неспецифические гнойно-воспалительные поражения позвоночника относятся к довольно редким заболеваниям, смертность в этой группе пациентов остается непозволительно высокой — на уровне 1,2–8,0% [4, 6, 7]. Следует отметить, что в последнее десятилетие значительно улучшились диагностические возможности для раннего выявления неспецифических воспалительных заболеваний позвоночника, но частота диагностических ошибок остается высокой — на уровне 30–85%, а средние сроки постановки верного диагноза составляют более 2–4 мес. [4, 8–10].
Описанное далее клиническое наблюдение является примером недостаточной настороженности врачей в отношении данного заболевания, несвоевременного определения этиологии болезни, отсроченного назначения патогенетического лечения, что, в свою очередь, является решающим в исходе заболевания.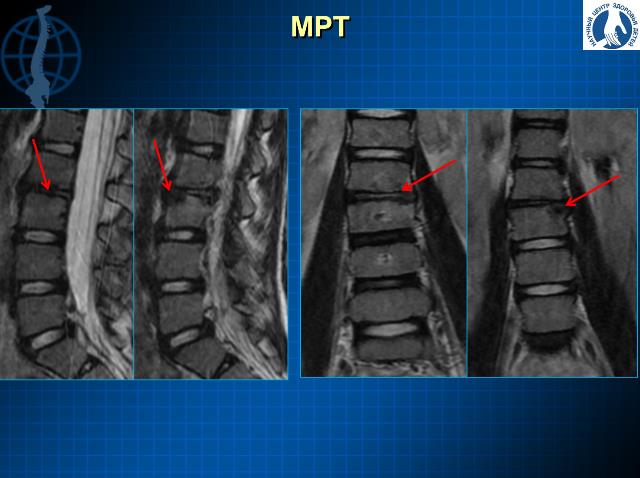 Рассматриваемый спондилит развился вследствие перенесенного уросепсиса, а затем инфекционного эндокардита (ИЭ).
Рассматриваемый спондилит развился вследствие перенесенного уросепсиса, а затем инфекционного эндокардита (ИЭ).
Проанализировано течение заболевания пациента, находившегося на лечении в неврологическом отделении ГБУЗ СО «СГБ № 4» (Самара) с 28.08.2019 по 27.09.2019.
Пациент Р., 56 лет, пенсионер, поступил в экстренном порядке в неврологическое отделение в связи с выраженным болевым синдромом в нижнегрудном и поясничном отделах позвоночника, слабостью в ногах, нарушением передвижения.
Из анамнеза известно, что пациент страдает мочекаменной болезнью; в 2017 г. перенес оперативное лечение по поводу злокачественного новообразования мочевого пузыря, полихимиотерапию. В 2011 г. имплантирован электрокардиостимулятор (ЭКС) в связи с синдромом слабости синусового узла. По причине болевого синдрома в проекции правой почки 01.06.2019 был экстренно госпитализирован в урологическое отделение, где 03.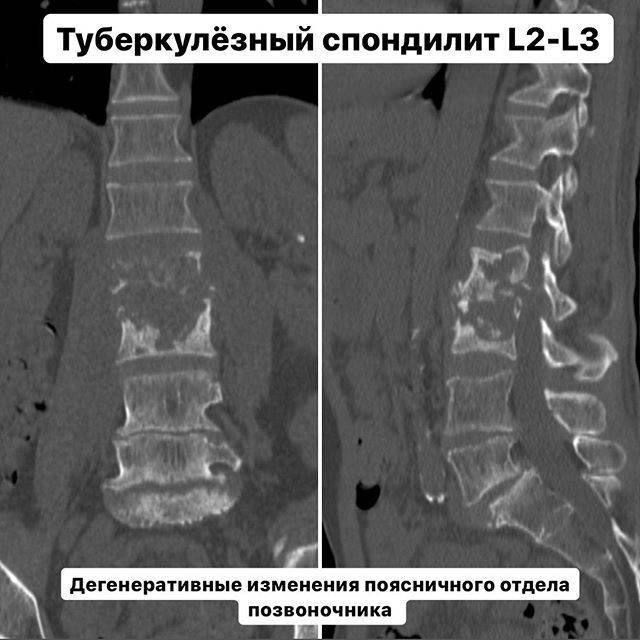
Находясь на лечении в урологическом отделении, стал отмечать боли в нижнегрудном и поясничном отделах позвоночника. Осмотрен неврологом, выполнена рентгенография, затем компьютерная томография (КТ) поясничного отдела позвоночника. Заключение от 21.06.2019: КТ-признаки межпозвонкового остеохондроза поясничного отдела позвоночника. Протрузия диска L4. Спондилоартроз. Спондилез.
К лечению был рекомендован нестероидный противовоспалительный препарат (НПВП) лорноксикам 8 мг 2 р.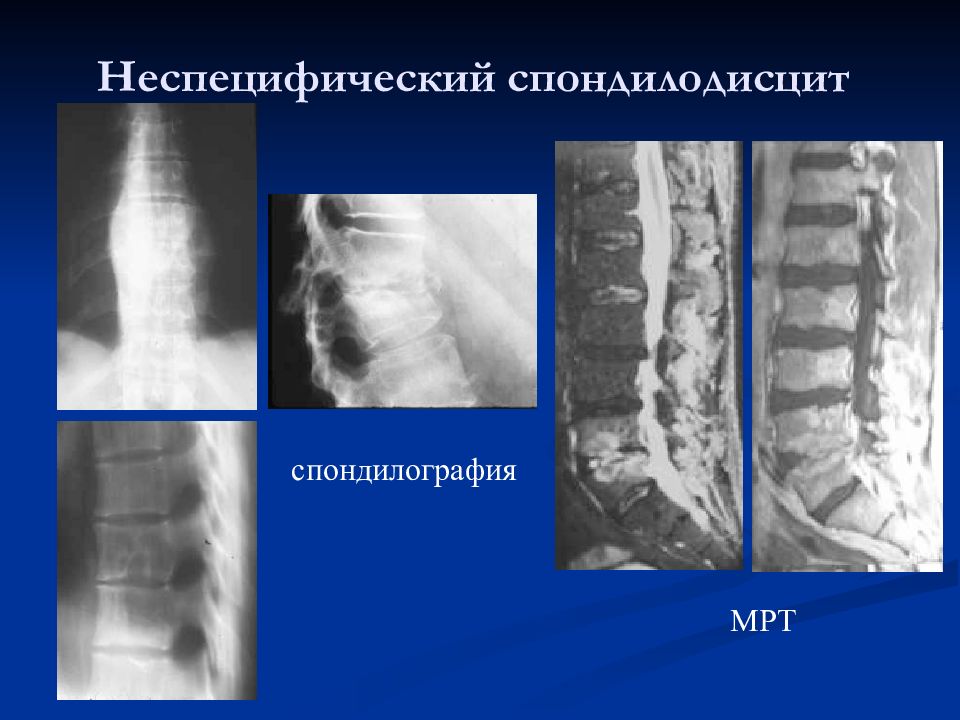 /сут в течение 7 дней. С улучшением лабораторных показателей анализов крови и мочи пациент выписан 25.06.2019 с рекомендациями: динамическое наблюдение уролога, дальнейший прием ципрофлоксацина внутрь в дозе 500 мг 2 р./сут в течение 7 дней, обильное питье.
/сут в течение 7 дней. С улучшением лабораторных показателей анализов крови и мочи пациент выписан 25.06.2019 с рекомендациями: динамическое наблюдение уролога, дальнейший прием ципрофлоксацина внутрь в дозе 500 мг 2 р./сут в течение 7 дней, обильное питье.
Дома вновь отмечал эпизоды ознобов, беспокоила общая слабость, появилась одышка при небольшой физической нагрузке, боли в спине сохранялись. В связи с изменениями на электрокардиограмме 27.06.2019 пациент направлен в областной кардиологический диспансер, госпитализирован в отделение лечения сложных нарушений ритма и электрокардиостимуляции для ревизии стимулирующей системы. При чреспищеводной Эхо-КГ выявлены большая вегетация на электроде ЭКС, недостаточность трехстворчатого клапана II–III степени. Посев крови на стерильность выполнялся трижды (29.06, 30.06, 01.07) с обеих рук. Выделен грамотрицательный микроорганизм Raoultella ornithinolytica, чувствительный к антибиотикам, а именно к противомикробному препарату из группы фторхинолонов — левофлоксацину.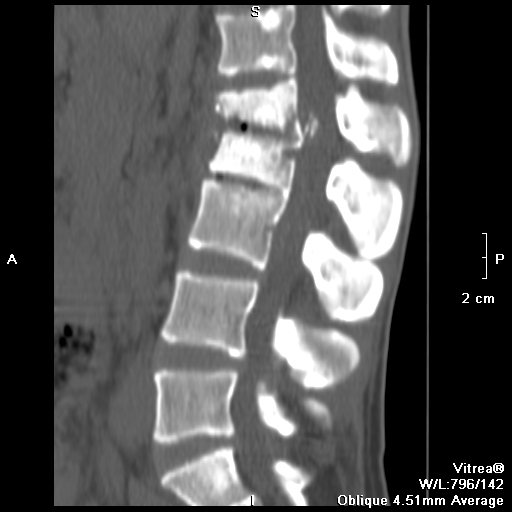
11.07.2019 выполнено оперативное лечение — пластика трехстворчатого клапана по Де Вега, удаление кардиальных электродов, имплантация ЭКС Effecta DR с эпикардиальной фасцией электродов. При проведении бактериологического анализа вегетаций с электрода (15.07.2019) выделен микроорганизм Klebsiella oxytoca, определена чувствительность к антибиотику из группы фторхинолонов (левофлоксацину). Проводилась антибактериальная терапия: ванкомицин парентерально по 1,0 г 2 р./сут в течение 10 дней; даптомицин парентерально 500 мг 1 р./сут в течение 2 нед., левофлоксацин парентерально по 500 мг 2 р./сут в течение 10 дней.
После проведения оперативного лечения, на фоне антибиотикотерапии пациент отмечал улучшение состояния в виде уменьшения слабости, нормализации температуры тела, но с сохранением болевого синдрома в спине. Повторно осматривался неврологом, рекомендовано: диклофенак натрия 25 мг/мл по 3,0 мл 1 р./сут в течение 7–10 дней, местно на поясничный отдел позвоночника пластырь с лидокаином. Выписан 20.07.2019.
Выписан 20.07.2019.
В течение последующего месяца отмечались интенсивные боли в спине, не купируемые анальгетиками, с 20.08.2019 появилась слабость в ногах. Госпитализирован в неврологическое отделение 28.08.2019. При поступлении отмечался выраженный болевой синдром в нижнегрудном и поясничном отделах позвоночника, оцениваемый по визуально-аналоговой шкале (ВАШ) на 8–9 баллов из 10, доставлен на каталке.
Неврологический статус: пациент в сознании, менингеальные знаки отрицательные, черепно-мозговые нервы без очаговой патологии. Поверхностная и глубокая чувствительность сохранена. Нижний парапарез до 3,0–3,5 балла. Сухожильные рефлексы нижних конечностей оживлены, положительный патологический рефлекс Бабинского с двух сторон. При пальпации остистых отростков позвонков выявляется резкая болезненность на уровне от Th20 до L5, напряжение паравертебральных мышц в грудном и поясничном отделах, значительно ограничен объем движений в поясничном отделе позвоночника.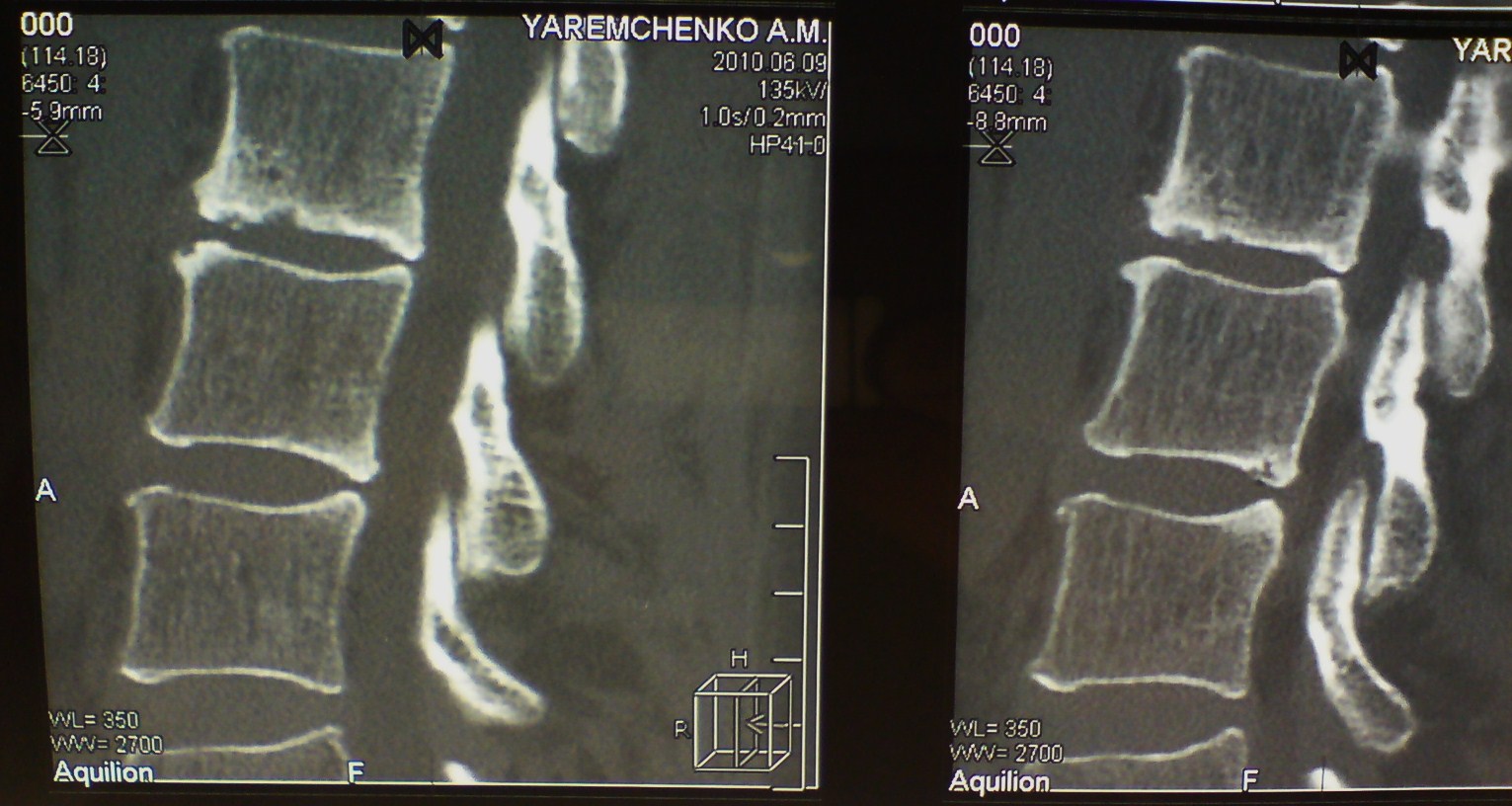 Функции тазовых органов не нарушены.
Функции тазовых органов не нарушены.
В общем анализе крови: невыраженный лейкоцитоз до 10,6×109/л с палочкоядерным сдвигом до 6%, повышение СОЭ до 28 мм/ч. В общем анализе мочи: повышенное содержание лейкоцитов до 15–20 в поле зрения при отсутствии белка и иных изменений. Биохимический анализ крови без отклонений от нормы. При поступлении С-реактивный белок (СРБ) не обнаружен.
На рисунке 1 представлена рентгенограмма грудного отдела позвоночника (боковая проекция), полученная при поступлении. Для уточнения диагноза выполнена КТ грудного отдела позвоночника (рис. 2).
Для исключения туберкулезной этиологии заболевания был выполнен Диаскинтест с отрицательным результатом. Осмотр фтизиоостеологом: данных за внелегочный туберкулез нет.
Трижды выполнялся забор крови с обеих рук на стерильность: рост микроорганизмов не выявлен.
Таким образом, пациенту был поставлен клинический диагноз: Подострый неспецифический спондилит Th22/L1, нижний парапарез с умеренными ограничениями двигательных функций. Болевой синдром.
Болевой синдром.
С учетом предыдущей антибиотикотерапии по согласованию с нейрохирургом и клиническим фармакологом пациенту были назначены: линкомицин парентерально 600 мг 2 р./сут в течение 4 нед., рифампицин 450 мг/сут на протяжении месяца, ангиопротектор диосмин 600 мг/сут, тиоктовая кислота 600 мг/сут, опиоидный анальгетик — трамадола гидрохлорид 50 мг до 2 р./сут, рекомендовано ношение жесткого грудопоясничного корсета.
Клинически отмечалась положительная динамика в виде уменьшения болевого синдрома, оценка по ВАШ — 2 балла, увеличилась сила в нижних конечностях до 4 баллов, пациент самостоятельно передвигается по отделению. Нормализовались лабораторные показатели. Пациент выписан на 31-й день с рекомендациями продолжать антибиотикотерапию: линкомицин 500 мг 2 р./сут в течение 4 нед., рифампицин 450 мг/сут в течение месяца, динамическое наблюдение невролога и нейрохирурга в течение 6 мес. Заключение по данным КТ (19.09.2019): признаки спондилодисцита Th22/L1, патологический компрессионный перелом тела Th22.
Согласно литературным данным проведение КТ/МРТ-контроля эффективности лечения нецелесообразно ввиду несоответствия клинического улучшения и картины нейровизуализации, что мы и наблюдали. Выполнение КТ/МРТ-контроля показано при неэффективности терапии, отсутствии клинического улучшения, продолжающейся отрицательной динамики со стороны лабораторных показателей [3, 6].
Проведен также динамический контроль после курса амбулаторного лечения. В октябре 2019 г. проведено оперативное лечение — чрескожная вертебропластика Th22 позвонка под лучевым контролем. Рентгенограмма от 28.10.2019 представлена на рисунке 3. Отмечено улучшение самочувствия, уменьшение боли, пациент может самостоятельно передвигаться. Неврологический статус: парезы отсутствуют.
Описанное клиническое наблюдение является примером развития подострого гематогенного остеомиелита на фоне перенесенных уросепсиса и ИЭ.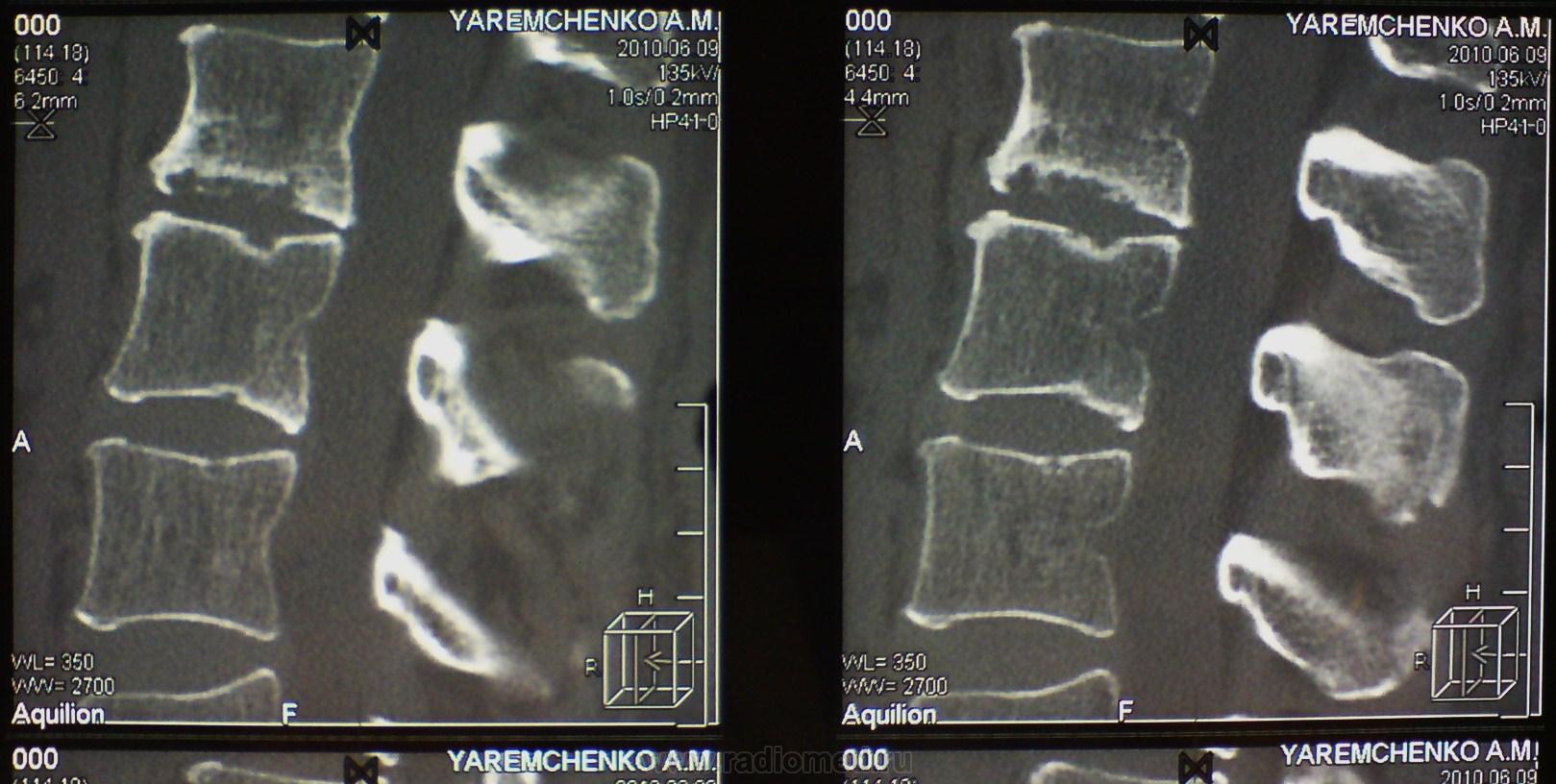 Боли в спине, возникшие еще на этапе лечения в урологическом отделении, вероятно, маскировались основным заболеванием — мочекаменной болезнью, а также состоянием после установки и удаления стента, обтурационным пиелонефритом. Рентгенография поясничного отдела позвоночника, выполненная в течение первых двух недель заболевания, как правило, не обнаруживает каких-либо изменений [11], что нашло подтверждение у нашего пациента. КТ может помочь в диагностике, согласно литературным данным, не раньше 2–4-й нед. заболевания [9, 12, 13]. У данного пациента нейровизуализационное исследование, выполненное на 3-й нед. заболевания, не выявило воспалительного характера процесса, что может быть связано с определенными трудностями диагностики, особенно на фоне уже проводимой антибактериальной терапии.
Боли в спине, возникшие еще на этапе лечения в урологическом отделении, вероятно, маскировались основным заболеванием — мочекаменной болезнью, а также состоянием после установки и удаления стента, обтурационным пиелонефритом. Рентгенография поясничного отдела позвоночника, выполненная в течение первых двух недель заболевания, как правило, не обнаруживает каких-либо изменений [11], что нашло подтверждение у нашего пациента. КТ может помочь в диагностике, согласно литературным данным, не раньше 2–4-й нед. заболевания [9, 12, 13]. У данного пациента нейровизуализационное исследование, выполненное на 3-й нед. заболевания, не выявило воспалительного характера процесса, что может быть связано с определенными трудностями диагностики, особенно на фоне уже проводимой антибактериальной терапии.
Следует отметить, что МРТ является методом выбора для диагностики воспалительных процессов в позвоночнике на ранней стадии [10, 15], более чувствительным, чем рентгенография, и более специфичным, чем КТ.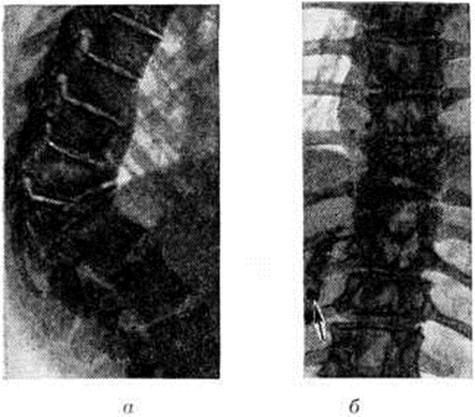 У нашего пациента противопоказанием к проведению МРТ было наличие имплантированного ЭКС.
У нашего пациента противопоказанием к проведению МРТ было наличие имплантированного ЭКС.
В последующем у пациента развился подострый ИЭ с клинической картиной, включавшей периоды субфебрилитета вперемежку с лихорадкой, нарастающую общую слабость, признаки сердечной недостаточности. На втором этапе госпитализации большое значение для диагностики и выбора лечения имели чреспищеводная Эхо-КГ, исследование крови на гемокультуру с последующим определением чувствительности выделенного возбудителя к антибиотикам. Посев крови на стерильность выявил рост достаточно редкого грамотрицательного микроорганизма Raoultella ornithinolytica, принадлежащего к семейству энтеробактерий. Антибиотикограмма продемонстрировала восприимчивость к левофлоксацину. Выделенная на электродах ЭКС Klebsiella oxytoca относится к условно патогенным аэробным грамотрицательным микроорганизмам, чувствительным к антибиотикам из группы фторхинолонов. Таким образом, проведенная терапия при выявленном ИЭ (ванкомицин, даптомицин и левофлоксацин) была адекватной.
Согласно литературным данным симптомы поражения опорно-двигательного аппарата при ИЭ встречаются примерно в 60% случаев и включают миалгии, артралгии, миозиты, тендиниты, энтезопатии, бактериальные дисциты и позвонковый остеомиелит [5, 14]. В рекомендациях Европейского общества кардиологов (2015) рекомендовано назначать всем пациентам, перенесшим ИЭ, выполнение позитронно-эмиссионной томографии, КТ тела, КТ/МРТ позвоночника при наличии боли в спине или костях, что не было выполнено в данном клиническом случае и не позволило установить неспецифическое воспалительное заболевание позвоночника на ранней стадии.
Следует отметить, что диагноз неспецифического воспалительного поражения позвоночника был поставлен отсроченно, через 3 мес. от момента перенесенного уросепсиса, и требовалось повторно направить пациента на КТ позвоночника с учетом сохраняющихся жалоб на боли в спине и отсутствия эффекта от анальгетиков. Можно согласиться, что пациент получал адекватную антибиотикотерапию, но пожилой возраст, отягощенный анамнез по онкозаболеванию, перенесенные повторные оперативные вмешательства, сепсис — все это послужило факторами, способствующими персистированию инфекции и подострому течению заболевания.
Несмотря на поздний диагноз неспецифического воспалительного заболевания позвоночника, исход у пациента благоприятный благодаря адекватной терапии и положительному ответу на лечение.
ЗаключениеПроведенный анализ клинического случая указывает, что практикующие врачи недостаточно настороженны в отношении воспалительных заболеваний позвоночника и в начале заболевания лечат его как дегенеративный процесс. Следует проводить более детальный сбор жалоб, анамнеза для более точного определения общего и неврологического статуса. Диагноз спондилита сложен и требует применения множества стратегий с включением серологических, рентгенологических, микробиологических диагностических исследований. Обзорная рентгенография позвоночника не обладает достаточной чувствительностью для ранней диагностики спондилита.
Опираясь на собственный опыт, данные литературных обзоров, можно выделить ключевые моменты, позволяющие врачу усомниться в предварительном диагнозе «остеохондроз» и провести дополнительное КТ/МРТ-исследование позвоночника:
длительная боль в спине у пациентов старше 50 лет, которая не поддается коррекции анальгетиками и НПВП;
лихорадка (в большинстве случаев неправильного типа), а у пациентов пожилого возраста и истощенных — длительный период субфебрилитета;
сопутствующие заболевания: сахарный диабет; инфекции мочеполовой системы; недавно перенесенные травмы, ранения; стоматологические, хирургические, урогинекологические, гастроэнтерологические и другие медицинские манипуляции; наличие внутрисердечного устройства, клапанных протезов; наркомания, токсикомания, алкоголизм; ВИЧ-инфекция; онкопатология; дистрофии; переохлаждения;
состояния, сопровождающиеся снижением иммунитета, — лечение иммунодепрессантами, пожилой возраст;
перенесенный ИЭ;
длительный болевой синдром в области шеи или спины, сопровождающийся повышением СОЭ или уровня СРБ.
.
Лечение спондилита
Спондилит – воспалительное заболевание позвоночника, протекающее в хронической форме. Причиной заболевания чаще всего служит туберкулезная инфекция, реже – остеомиелит позвоночника, сифилис, и другие болезни. Выделяют специфические и неспецифические спондилиты. К специфическим относят туберкулезный, бруцеллезный, гонорейный, актиномикотический, сифилитический и тифозный. К неспецифическим – гнойные поражения позвоночника, асептический спондилит, ревматоидный (Бехтерева болезнь) и анкилозирующий спондилиты.
Спондилит характеризуется разрушением костной ткани позвонков и деформацией позвоночника. В результате может образоваться горб. Болезнь может сопровождаться повышением температуры тела, недомоганием, болями в спине в области позвоночника и окружающих мышц, вялостью, похуданием. При анкилозирующем спондилите – хроническом воспалении позвоночника – суставы как бы «цементируются», что приводит к значительному ограничению их подвижности. Туберкулезный спондилит сегодня встречается реже, чем неспецифический спондилит при котором поражаются обычно два смежных позвонка, а также межпозвоночный диск, расположенный между ними.
Туберкулезный спондилит сегодня встречается реже, чем неспецифический спондилит при котором поражаются обычно два смежных позвонка, а также межпозвоночный диск, расположенный между ними.
Успешное лечение туберкулезного спондилита возможно только в условиях хирургических стационаров либо в костно-туберкулезных санаториях. В наших клиниках созданы все условия для успешного лечения спондилита .
При консервативном лечении используют иммобилизацию при помощи гипсовых кроваток, применяют противотуберкулезные препараты, массаж, ЛФК, аэро-, дието-, гелио-, и физиотерапию. Часто после окончания предварительного курса консервативного лечения спондилита больные нуждаются и в оперативном вмешательстве с целью костно-пластической стабилизации позвоночника и санации деструктивных фокусов. Обычно длительность постельного режима составляет несколько месяцев. Затем осуществляется восстановительное лечение.
Неспецифический спондилит как осложнение после лазерной вапоризации межпозвонкового диска
Введение.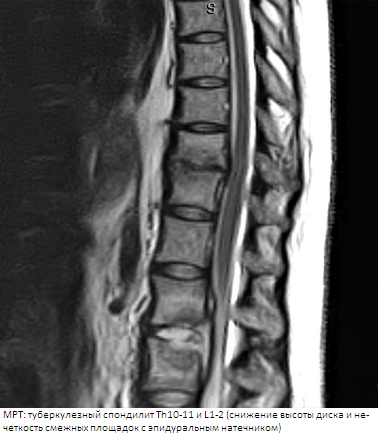
Распространенность поясничных болей настолько высока, что 80% всех людей хотя бы раз испытывают приступ острой боли в спине за свою жизнь [2, 3, 4, 5, 6, 7]. Наиболее частыми причинами возникновения хронической поясничной боли и радикулярных болей являются грыжи межпозвонковых дисков, стеноз позвоночного канала, дегенерация межпозвонкового диска без грыжевого выпячивания и синдром оперированного позвоночника, которые приводят к значительным экономическим, социальным и медицинским затратам [1].
Магнитно-резонансная томография позволяет выявить различные патологические изменения позвоночника и оценить степень деформации позвоночного канала. Назначение постельного режима, миорелаксантов, нестероидных противовоспалительных средств, витаминов группы В, антихолинестеразных препаратов, а иногда глюкокортикостероидов, а также физиотерапевтических процедур купируют ишиолюмбалгию в большинстве случаев. Стойкие боли в пояснице и нижних конечностях купируются эпидуральными и паравертебральными инъекциями глюкокортиокстероидов. Неэффективность консервативной терапии является показанием к оперативному вмешательству.
Неэффективность консервативной терапии является показанием к оперативному вмешательству.
Развитие хирургии дегенеративных заболеваний позвоночника идет по пути разработки малоинвазивных методов лечения, для снижения травматичности операции и сокращения осложнений [8, 9, 10, 11].
Одним из малоинвазивных методов лечения грыж межпозвонковых дисков является метод перкутанной лазерной вапоризации. Энергия лазера переносится в пульпозное ядро посредством волокна. Волокно помещается через тонкую иглу через заднелатеральный чрезкожный доступ под местной анестезией. Поглощение энергии лазера приводит к вапоризации воды внутри пульпозного ядра и изменению структуры его белков, что приводит к уменьшению объема и снижению внутридискового давления и как следствие к декомпрессии компримированного нервного корешка. Первая операция лазерной декомпрессии диска произведена в Европе Choy и коллегами в 1986 году.
На сегодняшний день накоплен достаточный опыт применения лазерной декомпрессии межпозвонковых дисков и в литературе описываются случаи асептических и инфицированных дисцитов после данной процедуры. Мы хотели доложить о случае из нашей практики развития спондилита двух смежных позвонков после лазерной вапоризации межпозвонкового диска VL4-5.
Мы хотели доложить о случае из нашей практики развития спондилита двух смежных позвонков после лазерной вапоризации межпозвонкового диска VL4-5.
Случай из практики
Больной А.Б. 50 лет, обратился в РСНПМЦ Ф и П с жалобами на резкие боли в поясничном отделе позвоночника, распространение болей в нижние конечности, усиление болей при движении, ограничение движений.
Из анамнеза считает себя больным в течение 8 месяцев. Заболевание началось с болей в поясничном отделе позвоночника. Лечился консервативно с диагнозом: Остеохондроз поясничного отдела позвоночника. Грыжа межпозвонкового диска VL4-5 размером 6 мм. Вторичный стеноз позвоночного канала, радикулярный синдром, принимал НПВС, физиолечение, эпидуральные блокады глюкортикоидами, без эффекта. Общий анализ крови из сопроводительных документов: Нв-117 г/л; эрит-3,5; Цвет.пок.-0,9; лейкоц-5,5; Пал.яд.-1; Сег.яд-60; Эоз.-4; лимф.-34; Мон.-5; СОЭ-5 мм/ч. Через 3 недели неэффективной терапии произведена лазерная вапоризация межпозвонкового диска VL4-5 под местной анестезией, в послеоперационном периоде назначен цефазолин 1,0 в/м 2 раза в день в течение 10 дней.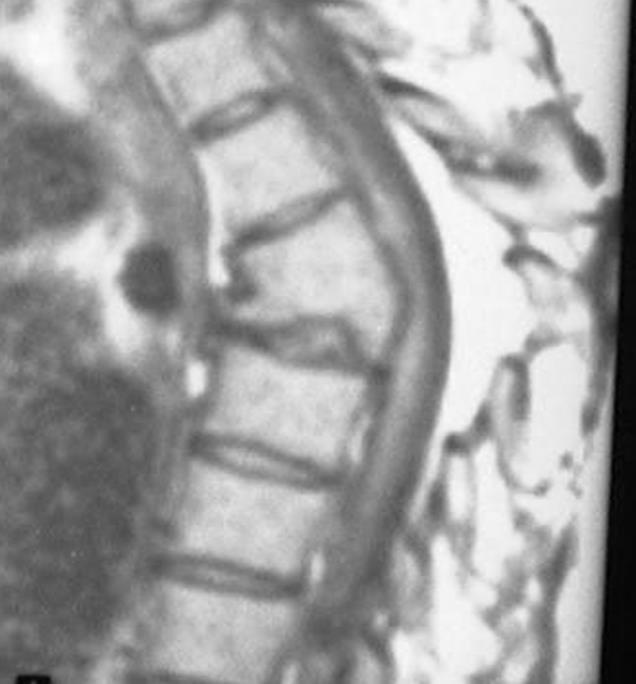 После проведенного вмешательства отмечалось клиническое улучшение. Однако уже через 2 месяца у больного стали отмечаться боли в поясничном отделе позвоночника, повышение температуры тела до 38 градусов, больному проведен курс антибиотикотерапии: антибиотиками широкого спектра действия и НПВС в течение 20 дней, температура нормализовалась и больной выписан на реабилитационное лечение. Спустя 2 месяца больной обращается к нам с вышеуказанными жалобами.
После проведенного вмешательства отмечалось клиническое улучшение. Однако уже через 2 месяца у больного стали отмечаться боли в поясничном отделе позвоночника, повышение температуры тела до 38 градусов, больному проведен курс антибиотикотерапии: антибиотиками широкого спектра действия и НПВС в течение 20 дней, температура нормализовалась и больной выписан на реабилитационное лечение. Спустя 2 месяца больной обращается к нам с вышеуказанными жалобами.
Больной вырос в удовлетворительных социальных условиях. Женат, имеет троих детей. Наследственных заболеваний нет. Наличие хронических заболеваний отрицает. Постоянно принимаемых препаратов нет. Контакт с туберкулезным больным отрицает. 1 рубец БЦЖ 5 мм. Инфекционными заболеваниями не болел и в контакте с таковыми не состоял, кровь и препараты крови не получал, у стоматолога не был. Аллергии на лекарства и пищевые продукты не отмечал. Работает слесарем.
Общее состояние больного относительно удовлетворительное. Сознание ясное, адекватное. Зрачки равновеликие, реакция на свет сохранена. Со стороны черепно-мозговых нервов без патологии. Менингиальных симптомов нет. Кожа и видимые слизистые чистые. Периферические лимфоузлы не увеличены. Подкожно-жировая клетчатка выражена умерено. Грудная клетка астенического типа. Дыхание через нос 20 в мин. Перкуторно легочный звук над всей поверхностью легких. Границы легких в пределах нормы. Аускультативно везикулярное дыхание в обоих легких. Тоны сердца ритмичные, приглушены. А/Д – 120/80 мм рт.ст., пульс – 88 уд. в 1 мин., удовлетворительного наполнения и напряжения. Язык влажный, чистый. Живот мягкий, безболезненный. Печень и селезенка не пальпируются, стул регулярный. Симптом Пастернацкого отрицательный с обеих сторон. Диурез регулярный, свободный.
Зрачки равновеликие, реакция на свет сохранена. Со стороны черепно-мозговых нервов без патологии. Менингиальных симптомов нет. Кожа и видимые слизистые чистые. Периферические лимфоузлы не увеличены. Подкожно-жировая клетчатка выражена умерено. Грудная клетка астенического типа. Дыхание через нос 20 в мин. Перкуторно легочный звук над всей поверхностью легких. Границы легких в пределах нормы. Аускультативно везикулярное дыхание в обоих легких. Тоны сердца ритмичные, приглушены. А/Д – 120/80 мм рт.ст., пульс – 88 уд. в 1 мин., удовлетворительного наполнения и напряжения. Язык влажный, чистый. Живот мягкий, безболезненный. Печень и селезенка не пальпируются, стул регулярный. Симптом Пастернацкого отрицательный с обеих сторон. Диурез регулярный, свободный.
Локальный статус. Больной передвигаться самостоятельно не может из-за боли в поясничном отделе позвоночника. Оси конечностей правильны. Активные и пассивные движения в суставах свободные. Позвоночник ровный, поясничный лордоз сглажен, паравертебральные мышцы рефлекторно напряжены. Симптом Ласега положителен с обеих сторон при 30 градусах. Симптом Вассермана положительный с обеих сторон. При глубокой пальпации резкая боль в проекции VL4-5 позвонков, боли распространяются в нижние конечности, больше влево. Отмечается парастезия в проксимальных отделах нижних конечностей. Чувствительность кожи, периферическая пульсация и мышечная сила сохранены.
Симптом Ласега положителен с обеих сторон при 30 градусах. Симптом Вассермана положительный с обеих сторон. При глубокой пальпации резкая боль в проекции VL4-5 позвонков, боли распространяются в нижние конечности, больше влево. Отмечается парастезия в проксимальных отделах нижних конечностей. Чувствительность кожи, периферическая пульсация и мышечная сила сохранены.
При поступлении общий анализ крови гемоглобин – 140 г/л; эритроциты – 3,8 × 1012; цветной показатель – 0,9; лейкоциты – 5,0× 109; палочкоядерные – 1; сегментоядерные – 59; эозинофилы – 4; лимфоциты – 32; моноциты – 4; СОЭ – 17 мм/ч. Общий анализ мочи: цвет – желтый; прозрачность – слабомутная; реакция – кислая; белка нет; эпителиальные клетки – 0-1 в поле зрения; лейкоциты – 2-3 в поле зрения; эритроциты – 0-1 в поле зрения, соли – оксалаты. Биохимический анализ: АСТ-0,36 ммоль/л; АЛТ-0,50 ммоль/л, общий билирубин – 10,5 ммоль/л; мочевина – 5,7; креатинин-78 мкмоль/л; сахар в крови – 6,2 ммоль/л. Коагулограмма: гематокрит – 50%; тромботест – VI; протромбин индекси – 84%; фибриноген – 4,25; рекальцификация – 1’55‘‘; ретракция сгустка – 53%; активность фибриногена – 15%. Диаскинтест отрицательный. На ЭКГ: синусовый ритм 88 в мин., ЭОС горизонтальная, дистрофические изменения в миокарде желудочков. На УЗИ брюшной полости и забрюшинного пространства без эхопатологии.
Коагулограмма: гематокрит – 50%; тромботест – VI; протромбин индекси – 84%; фибриноген – 4,25; рекальцификация – 1’55‘‘; ретракция сгустка – 53%; активность фибриногена – 15%. Диаскинтест отрицательный. На ЭКГ: синусовый ритм 88 в мин., ЭОС горизонтальная, дистрофические изменения в миокарде желудочков. На УЗИ брюшной полости и забрюшинного пространства без эхопатологии.
На МРТ в телах VL4-5 сигнал неоднородно снижен. Межтеловая щель сужена. Суставные поверхности неровные с узурацией, с краевыми остеофитами. Мягкие ткани вокруг инфильтрированы, утолщены, абсцессов нет. Спинномозговой канал сужен. За счет протрузии дисков VL4-5, VL5-S1 позвонков. Повышенный сигнал от тел остальных поясничных позвонков.
На рентгенограмме грудной клетки: легочные поля без инфильтративных теней. Корни легких структурны. Синусы свободны. Купола диафрагмы обычной формы. Тень сердца без особенностей.
Больному назначены НПВС, противовоспалительное, противоотечное и дезинтоксикационное лечение: Диклофенак натрия 75 мг в/м 1 раз в день №7; NaCl 0,9% – 200,0 + CaCl 10% – 10,0 в/в 1 раз в день №10; Глюкоза 5% – 200,0+ Вит С 6,0 в/в 1 раз в день №10; фуросемид 1,0 в/м 1 раз в день №10, Витамин В6 1,0 в/м 1 раз в день №10.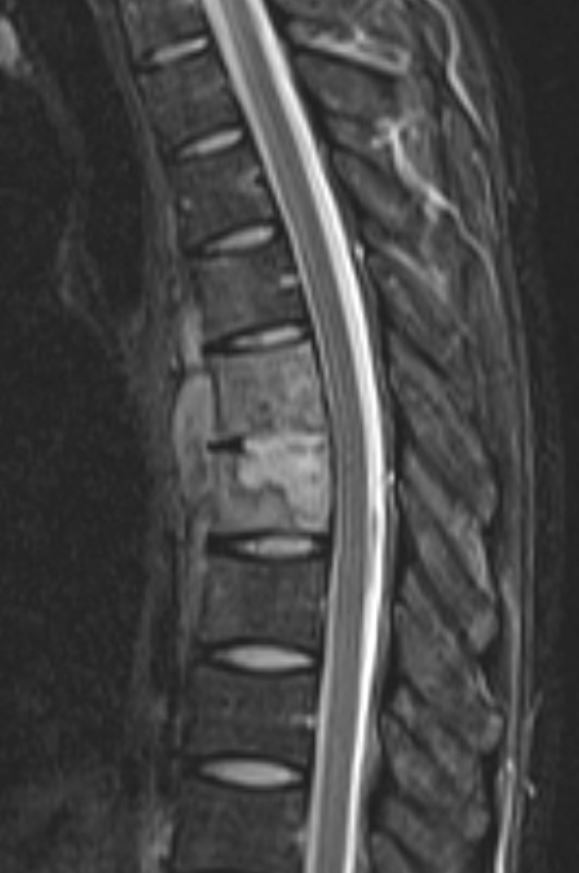 Левофлоксацин в дозе 750 мг ежедневно №20.
Левофлоксацин в дозе 750 мг ежедневно №20.
В динамике общий анализ крови гемоглобин – 140 г/л; эритроциты – 4,0 × 1012; цветной показатель – 0,9; лейкоциты – 5,6× 109; СОЭ-15 мм/ч, остальные анализа без особенностей. На МРТ в динамике через 3 недели инфильтрация уменьшилась, но сохраняется, патологический сигнал от тел VL4-5 сохраняется. Клинически резка боль при движении в поясничном отделе позвоночника с распространением болей в нижние конечности, нестабильность позвоночника.
Больному произведена операция некрэктомия VL4-5, со вскрытием спинномозгового канала, спондилодез титановым сетчатым кейджем из левостороннего переднебокового доступа. При операции отмечается: нестабильность сегмента VL4-5, деструкция и секвестрация костной ткани. Гистологическое заключение операционного материала – спондилит неспецифического характера.
В послеоперационном периоде назначены антибиотики широкого спектра в течение 10 дней для профилактики развития вторичной инфекции.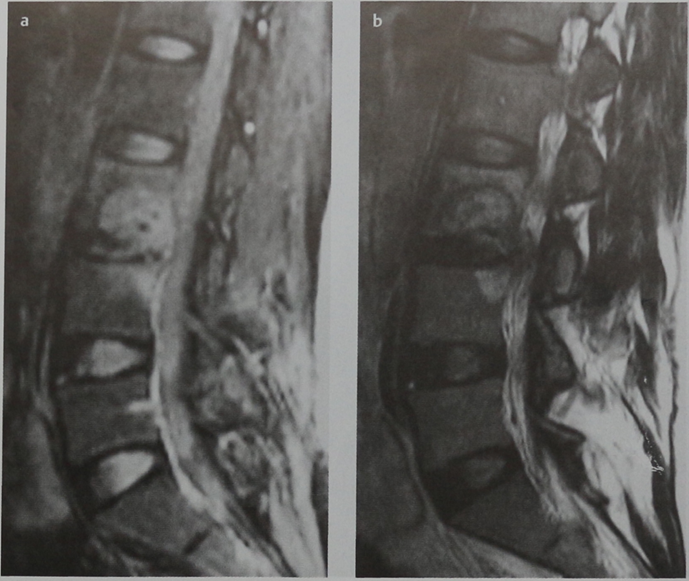 Послеоперационная рана зажила первично.
Послеоперационная рана зажила первично.
Больной активизирован в корсете через 3 недели после операции и в удовлетворительном состоянии выписан домой.
Установлен окончательный диагноз: Остеохондроз поясничного отдела позвоночника. Грыжа межпозвонкового диска VL4-5. Вторичный стеноз позвоночного канала, радикулярный синдром. СПО лазерной вапоризации межпозвонкового диска VL4-5. Осл.: спондилит VL4-5 позвонков неспецифического характера.
Рис. 1. МРТ до операции лазерной вапоризации межпозвонкового диска VL4-5 | |
Рис. 2. МРТ при поступлении | |
Рис. | |||
Обсуждение
При чрезкожной лазерной декомпрессии межпозвонкового диска, энергия лазера используется для снижения внутридискового давления путем вапоризации небольшого по объему пульпозного ядра, что уменьшает давление между пульпозным ядром и фиброзным кольцом, таким образом, приводя к ретракции грыжевого выпячивания и освобождая нервный корешок.
Vijay S. et al, 2013 сообщает, что in vitro, повышение внутридискового объема на 1 мл приводит к повышению внутридискового давления на 312 кПа или 2340 mmHg. С другой стороны, уменьшение внутридискового давления приводит к значительному уменьшение внутридискового давления, что по принципу отрицательного давления устремляет грыжевое выпячивание к центру межпозвонкового диска, декомпрессии нервного корешка и избавлению от корешковой боли. Кроме того, вапоризация воды приводит к денатурации белка пульпозного ядра, что не дает в последующем накапливать воду [12].
Считается, что чрезкожная декомпрессия межпозвонкового диска не приводит к серьезным осложнениям, кроме того факта, что последние исследования указывают на минимальный риск если процедура выполняется опытным хирургом. Потенциальные осложнения включают: инфекцию, кровотечение, повреждение нерва, усиление боли, рецидив грыжи, паралич, идиосинкразия, анафилактический шок и смертельный исход. Повреждение нервного корешка может проявиться во время погружения канюли. Опытный хирург проводит процедуру под контролем визуализации в режиме реального времени и при полном сознании пациента для того чтобы это осложнение не имело место. Повреждение кровеносных сосудов может проявиться, если артерия или вена контактирует с устройством, особенно если используется тепловая энергия, что приводит к некрозу стенки сосуда. Также надо быть осторожным, чтобы не погрузить устройство в переднюю часть фиброзного кольца.
В соответствии с данными литературы уровень осложнений после лазерной вапоризации межпозвонкового диска составляет 0. 5%. В исследовании Choy и соавт., 1998 [14], у 4 из 518 пациентов процедура осложнялась дисцитом, что составило менее 1%. Farrar и соавт., 1998 [15] сообщает о случае остеомиелита у 50 летнего мужчины после лазерной декомпрессии межпозвонкового диска по поводу грыжи диска VL4-5. В исследовании с наблюдением за больными в течение 3 месяцев после лазерной вапоризации McMillan и соавт., 2004 г. [16], указывает на усиление и рецидив болей в пояснице в 63%. Однако, сообщается, что случаев инфекции, повреждения нервов или клинически значимого кровотечения не отмечалось [13].
5%. В исследовании Choy и соавт., 1998 [14], у 4 из 518 пациентов процедура осложнялась дисцитом, что составило менее 1%. Farrar и соавт., 1998 [15] сообщает о случае остеомиелита у 50 летнего мужчины после лазерной декомпрессии межпозвонкового диска по поводу грыжи диска VL4-5. В исследовании с наблюдением за больными в течение 3 месяцев после лазерной вапоризации McMillan и соавт., 2004 г. [16], указывает на усиление и рецидив болей в пояснице в 63%. Однако, сообщается, что случаев инфекции, повреждения нервов или клинически значимого кровотечения не отмечалось [13].
Заключение: Использование энергии лазера и другой тепловой энергии, может привести к термической травме не только хрящевых структур, но и костных структур и питающих сосудов, что проявляется их некротизацией и проявляется клинически спустя месяцы после операции.
Литература:
- Васильев А. Ю., Казначеев В. М. «Пункционная лазерная вапоризация дегенерированных межпозвонковых дисков».
 М., 2005.С. 128.
М., 2005.С. 128. - Boswell M. V. et al. «Interventional techniques in the management of chronic spinal pain: Evidence-based practice guidelines». Pain Physician 2005; 8:1-47.
- Bressler H. B. et al. «The prevalence of low back pain in the elderly. A systemic review of the literature». Spine 1999; 24:1813-1819.
- Lawrence R.C. «Estimates of the prevalence of arthritis and selected musculoskeletal disorders in the United States». Arthritis Rheum 1998; 41:778-799.
- Cassidy J.D. et al. «The prevalence of low back pain and related disability in Saskatchewan Adults». Spine 1998; 23:1860-1867.
- Walker B.F. et al. «Low back pain in Australian adults: Prevalence and associated disability». J Manipulative Physiol Ther 2004; 27:238-244.
- Guo H.R. et al. «Back pain prevalence in US industry and estimates of lost workdays». Am J Public Health 1999; 89:1029-1035.
- Wang JC et al. «The effect of uniform heat- ing on the biomechanical properties of the intervertebral disc in a porcine model».
 Spine J 2005; 5:64-70.
Spine J 2005; 5:64-70. - Welch WC et al. «Alternative strategies for lumbar discectomy: Intradiscal electrothermy and nucleoplasty». Neurosurg Focus 2002; 13:E7.
- Helm S et al., «Effectiveness of thermal annular procedures in treating discogenic low back pain». Pain Physician 2012; 15:E279-E304.
- Magalhaes FN et al. «Ozone therapy as a treatment for low back pain secondary to herniated disc: A systematic review and meta-analysis of randomized controlled trials». Pain Physician 2012; 15:E115-E129.
- Vijay S. et al. «Percutaneous Lumbar Laser Disc Decompression: An Update of Current Evidence» Pain Physician 2013; 16:229-260.
- Vijay S. et al. «Percutaneous Lumbar Laser Disc Decompression: An Update of Current Evidence» Pain Physician. 2006; 9:139-146.
- Choy DS. «Percutaneous laser disc decompression (PLDD): twelve years’ experience with 752 procedures in 518 patients». J Clin Laser Med Surg 1998; 16: 325-331.
- Farrar MJ.
 «Possible salmonella osteomyelitis of spine following laser disc decompression». Eur Spine J 1998; 7:509-511.
«Possible salmonella osteomyelitis of spine following laser disc decompression». Eur Spine J 1998; 7:509-511. - McMillan MR et al. «Percutaneous laser disc decompression for the treatment of discogenic lumbar pain and sciatica: a preliminary report with 3-month follow-up in a general pain clinic population». Photomed Laser Surg 2004; 22:434-438.
Основные термины (генерируются автоматически): межпозвонковый диск, поясничный отдел позвоночника, лазерная вапоризация, боль, больной, позвоночный канал, грыжевое выпячивание, лазерная декомпрессия, нервный корешок, общий анализ крови.
диагностика и лечение в Москве
Это воспалительно-инфекционное заболевание позвоночника провоцирует деформацию позвоночного столба. В зависимости от причины возникновения, выделяют несколько видов спондилита. Без лечения заболевание может привести к серьезным негативным последствиям для работы опорно-двигательного аппарата.
В зависимости от причины возникновения, выделяют несколько видов спондилита. Без лечения заболевание может привести к серьезным негативным последствиям для работы опорно-двигательного аппарата.
Причины развития и виды патологии
На основании факторов, вызвавших спондилит, заболевание классифицируют на:
- специфический — в группу входят туберкулезный, сифилитический, гонорейный и грибковый виды патологии;
- неспецифический — гнойный и анкилозирующий (болезнь Бехтерева) спондилит.
Причины возникновения – вредные микроорганизмы и/или аутоимунные факторы.
Симптомы
Основное проявление заболевания — боль в спине. Как правило, характерные неприятные ощущения возникают в области между лопаток и беспокоят постоянно, периодически усиливаясь. На фоне спондилита могут зажиматься нервные окончания, о чем свидетельствуют резкие боли. При локализации заболевания в шейном отделе или пояснице болевые ощущения концентрируются в пораженной области.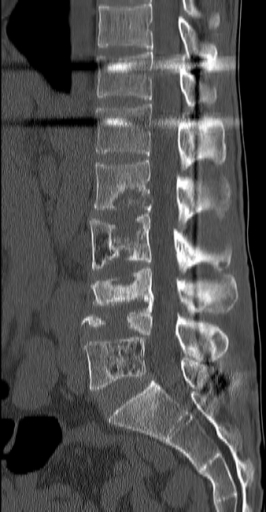 Повышение температуры, озноб, слабость говорят об осложнениях спондилита.
Повышение температуры, озноб, слабость говорят об осложнениях спондилита.
Диагностика и лечение
Для выявления заболевания назначают:
- рентгенографию;
- КТ, МРТ позвоночника;
- общий и биохимический анализ крови;
- ревмопробы;
- цитологический анализ;
- и другие диагностические процедуры (по решению врача).
Причины спондилита определяют специфику терапии. Основные цели курса лечения — устранение возбудителя, снятие болевых синдромов и возвращение подвижности. Пациенту могут назначить:
- медикаментозное лечение;
- физиотерапию;
- в тяжелых случаях — оперативное вмешательство.
На консультацию по вопросам диагностики и лечения различных заболеваний позвоночника, в том числе спондилита, к профильным специалистам «Эммаклиник» запись ведется по телефону +7 (495) 652-11-11 или через форму заявки на сайте.
Запись на прием (доступна видеоконсультация)
Ваше сообщение отправлено
Благодарим за обращение в Многопрофильный медицинский центр «Эммаклиник»!
Ваше сообщение будет обработано в ближайшее время и мы свяжемся с вами для уточнения деталей.
Будьте здоровы!
Присединяйтесь к нам в социальных сетях!
Актуальные новости, акции, полезная информация.
КОМОРБИДНОСТЬ И ПРОГНОЗИРОВАНИЕ РИСКА ВОЗНИКНОВЕНИЯ ПОСЛЕОПЕРАЦИОННЫХ ИНФЕКЦИОННЫХ ОСЛОЖНЕНИЙ У БОЛЬНЫХ ТУБЕРКУЛЕЗНЫМ СПОНДИЛИТОМ | Бурлаков
1. Бурлаков С. В., Олейник В. В., Вишневский А. А. Влияние длительности заболевания туберкулезным спондилитом на развитие осложнений // Травматология и ортопедия России. – 2013. – № 1. – С. 61-66.
2. Голка Г. Г., Танцура А. В., Кононыхин А. В. Оперативное лечение осложненных форм туберкулезного спондилита // Актуальные вопросы современной хирургии инфекционных поражений скелета: сб. тезисов II Конгресса Национальной ассоциации фтизиатров. – СПб., 2013. – С. 214-215.
тезисов II Конгресса Национальной ассоциации фтизиатров. – СПб., 2013. – С. 214-215.
3. Гончаров М. Ю., Соколович В. П., Данилов Е. П. и др. Ближайшие результаты лечения гнойных неспецифических заболеваний позвоночника // Хирургия позвоночника. – 2005. – № 2. – C. 70-72.
4. Зозуля Ю. А., Цымбалюк В. И., Ткачик И. П. Нозокомиальные инфекции в нейрохирургии: проблемы и поиски решений. Профилактика нозокомиальной инфекции с позиции доказательной медицины // Украiнский нейрохiрургiчний журнал. – 2008. – № 1. – С. 9-16.
5. Петров Н. В. Диагностика имплант-ассоциированных инфекций в ортопедии с позиции доказательной медицины // Хирургия позвоночника. – 2012. – № 1. – С. 74-83.
6. Фахртдинов А. Р. Клинико-лучевая картина туберкулезного спондилита на современном этапе // Травматология и ортопедия России. – 2006. – № 2. – С. 16-20.
Фахртдинов А. Р. Клинико-лучевая картина туберкулезного спондилита на современном этапе // Травматология и ортопедия России. – 2006. – № 2. – С. 16-20.
7. Arrigo R. T., Kalanithi P., Cheng I. et al. Charlson score is a robust predictor of 30-day complications following spinal metastasis surgery [Text] // Spine. – 2011. – Vol. 36. – P. E274-Е280.
8. Banco S. P., Vaccaro, A. R., Blam O. et al. Spine infection [Text] // Spine. – 2002. – Vol. 27, № 9. – P. 962-965.
9. Deyo R. A., Cherkin D. C., Ciol M. A. Adapting a clinical comorbidity index for use with ICD-9-CM-administrative databases [Text] // J. Clin. Epidemiol. – 1992. – Vol. 45. – P. 613-619.
10. di Paola C. P., Saravanja D. D., Boriani L. et al. Postoperative infection treatment score for the spine (PITSS): construction and validation of a predictive model to define need for a single versus multiple irrigation and debridement for spinal surgical site infection [Text] // Spine J. – 2012. – № 3. – P. 218-230.
D., Boriani L. et al. Postoperative infection treatment score for the spine (PITSS): construction and validation of a predictive model to define need for a single versus multiple irrigation and debridement for spinal surgical site infection [Text] // Spine J. – 2012. – № 3. – P. 218-230.
11. Fu K. M., Smith J. C., Sansur S. A., Shaffrey C. I. Standartized measures of healhth status and and disability and the decision to pursue operative treatment in elderly patient with degenerative scoliosis [Text] // Neurosugery. – 2010. – Vol. 66. – P. 42-47.
12. Govender S. The autcome of allografts and anterior instrumentation in spinal tuberculosis // Clin. Orthop. – 2002. – № 398. – P. 60-66.
13. Munoz E., Rosner F., Friedman R. et al. Financial risk, hospital cost, complications and comorbidities in medical non-complications and comorbidity-stratified diagnosis-related groups [Text] // Am. J. Med. – 1988. – Vol. 84, № 5. – Р. 933-939.
J. Med. – 1988. – Vol. 84, № 5. – Р. 933-939.
14. Narotam P. K., van Dellen J. R., du Trevou M. D. et al. Operative sepsis in neurosurgery: a method of classifying surgical cases [Text] // Neurosurgery. – 1994. – Vol. 34, № 3. – P. 409-415.
15. Nasser R., Yadla S., Maltenfort M. G. et al. Complications in spine surgery [Text] // J. Neurosurgery Spine. – 2010. – Vol. 13. – P. 144-150.
16. Pateder D. B., Gonzales R. A., Kebaish K. M. et al. Short term mortality and its association with independent rick factors in adult spinal deformity surgery [Text] // Spine. – 2008. – Vol. 33. – P. 1224-1228.
17. Patel N., Bagan B., Vadera S. et al. Obesity and spine surgery: relation to operative complication [Text] // J. Neurosurg Spine. – 2007. – Vol.6. – P. 291-297.
Neurosurg Spine. – 2007. – Vol.6. – P. 291-297.
18. Ratliff J. K., Lebude B., Albert T. et al. Complication in spinal surgery: comparative survey of spine surgeons and patients who underwent spinal surgery [Text] // J. Neurosurg spine. – 2009. – Vol. 10. – P. 578-584.
19. Shen Y., Silverstein J. C., Roth S. In hospital complications and mortality after effective spinal fusion surgery in Unated States: a study of the nationwide inpatient sample from 2001 to 2005 // J. Neurosurg. Anesthesiol. – 2009. – Vol. 21. – P. 21-30.
20. Taylor E. W. Surgical infection: current concerns // Eur. J. Surg. – 1997. – Suppl., 578. – P. 5-9.
21. Wang M. Y., Green B. A., Shah S. et al. Complication associated with lumbar stenosis surgery in patients older than 75 years of age [Text] // Neurosurg Focus-2003. – Vol. 14. – Р. E7.
– Vol. 14. – Р. E7.
22. Whitmore R. G., Stephen J. H., Vernick C. et al. ASA grade and charlson comorbidity index of spinal surgery patients: correlation with complication and societal cost [Text] // Spine Journal. – 2014. – Vol. 14. – P. 31-38.
Недифференцированные спондилоартропатии | Сидарс-Синай
Не то, что вы ищете?Обзор
Когда у человека наблюдаются различные симптомы, которые нельзя классифицировать как конкретное ревматоидное заболевание, считается, что у него недифференцированная спондилоартропатия.
Некоторые врачи не считают это официальным диагнозом. Некоторые считают, что это связано с анкилозирующим спондилитом, псориатическим артритом, спондилитом, связанным с воспалительным заболеванием кишечника или болезнью Крона, и реактивным артритом.
Поскольку симптомы обычно носят общий характер, человеку может быть ошибочно поставлен диагноз тревожного состояния, депрессии или фибромиалгии.
Симптомы
Иногда единственным признаком недифференцированной спондилоартропатии является боль. Другие симптомы, которые испытывают люди с недифференцированной спондилоартропатией, включают:
- Длительная, продолжающаяся боль в пояснице, которая возникает постепенно (обычно иррадиирует от ягодиц) в возрасте до 45 лет
- Общая жесткость тела, которая усиливается при пробуждении и улучшается после упражнений
- Отек в ступнях и руках в анамнезе, особенно боль в пятке.
- Общее отсутствие абдоминальных симптомов, хотя до трети пациентов имеют короткие эпизоды диареи или испражняются более двух раз в день.
- Воспаление кишечника, которое можно выявить только при илеоколоноскопии. Симптомы могут напоминать воспалительное заболевание кишечника или бактериальное поражение.
 При постоянном мониторинге кажется, что существует сильная взаимосвязь между воспалением кишечника и суставов.
При постоянном мониторинге кажется, что существует сильная взаимосвязь между воспалением кишечника и суставов. - Боль в суставах, поражающая как мелкие, так и крупные суставы, в основном в ногах и ступнях.Однако эта боль в суставах может повлиять на одну сторону тела больше, чем на другую.
Воспаление глаза - Бугристая красная сыпь, которая часто возникает при повышении температуры и болях в суставах, которые приходят и уходят
- Симптомы, влияющие на мочевыводящие пути и половые органы
Причины и факторы риска
Как и при реактивном артрите, многие люди с недифференцированными спондилоартропатиями имеют генетический маркер HLA-B27, который предполагает наличие унаследованного элемента этого заболевания.Семейные исследования показывают легкое воспаление кишечника или болезнь Крона.
Некоторые данные свидетельствуют о том, что воспаление кишечника может вызывать другие ревматические симптомы, такие как боль в суставах при этом состоянии.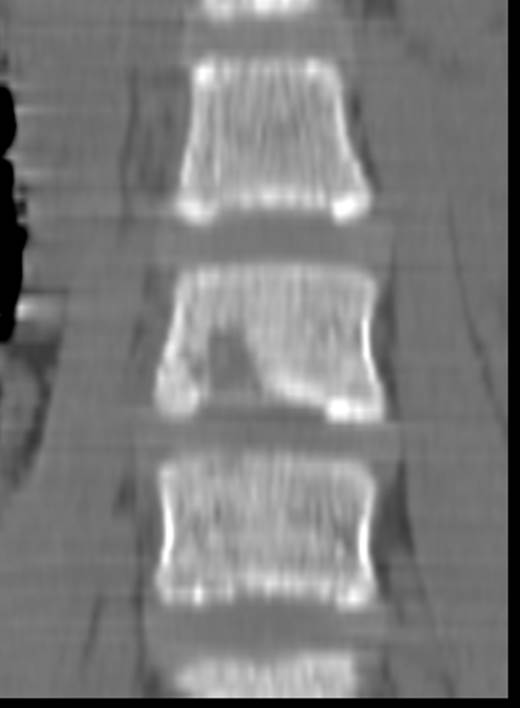 Это также может быть вирус, бактерия или микроб.
Это также может быть вирус, бактерия или микроб.
Диагностика
Природа симптомов недифференцированных спондилоартропатий позволяет легко принять их за другие состояния. Это не так часто, как другие виды ревматоидных заболеваний.Наличие квалифицированного врача, имеющего опыт лечения ревматических состояний, важно для точного диагноза и соответствующего лечения.
Не все врачи осознают, насколько распространена эта проблема, особенно среди женщин. Учитывая, что его часто упускают из виду, становится еще более важным делать домашнюю работу самостоятельно.
Врач проведет физический осмотр и изучит симптомы пациента. Он или она сделает тесты, чтобы исключить инфекции пищеварительной системы. Другие тесты, которые врач может назначить для подтверждения диагноза недифференцированной спондилоартропатии, включают:
- Илеоколоноскопия для определения воспаления в кишечнике
- Анализы крови на различные факторы, включая антитела или реакции иммунной системы
- Тест на ген HLA-B27.
 Этот тест помогает исключить анкилозирующий спондилит. Этот ген есть у более 95% людей с анкилозирующим спондилитом, тогда как у гораздо меньшего числа людей с недифференцированной спондилоартропатией он есть. (Наличие гена не обязательно означает, что у человека разовьется анкилозирующий спондилит.)
Этот тест помогает исключить анкилозирующий спондилит. Этот ген есть у более 95% людей с анкилозирующим спондилитом, тогда как у гораздо меньшего числа людей с недифференцированной спондилоартропатией он есть. (Наличие гена не обязательно означает, что у человека разовьется анкилозирующий спондилит.) - Может проявляться эрозия суставов кистей и стоп или бедра. Они могут напоминать повреждения суставов, которые часто наблюдаются при ревматоидном артрите
Лечение
Недифференцированные спондилоартропатии, как и связанные с ними ревматические заболевания, являются хроническим заболеванием, которое требует активного участия пациента, а также врача.
Лечение может включать:
- Лекарства – от нестероидных противовоспалительных препаратов, отпускаемых без рецепта, таких как аспирин или ибупрофен, до более сильных обезболивающих и кортикостероидов. Другие препараты, которые могут быть назначены, аналогичны тем, которые используются для лечения симптомов анкилозирующего спондилита, включая альфа-блокатор фактора некроза опухоли
- Тепло для жесткости, включая горячие ванны и теплый душ
- Лед для набухания
- Упражнение
- УЗИ
- Нежный массаж
- Электростимуляторы боли (блоки TENS или TNS)
- Снижение веса для уменьшения нагрузки на суставы
- Улучшение осанки
- Хирургия, в отдельных случаях
© 2000-2021 Компания StayWell, LLC. Все права защищены. Эта информация не предназначена для замены профессиональной медицинской помощи. Всегда следуйте инструкциям лечащего врача.
Все права защищены. Эта информация не предназначена для замены профессиональной медицинской помощи. Всегда следуйте инструкциям лечащего врача.
Спондилоартропатии – Американский семейный врач
1. Гладман Д.Д. Псориатический артрит. Rheum Dis Clin North Am . 1998; 24: 829–44 ….
2. Де Кейсер Ф., Elewaut D, Де Вос М, Де Влам К, Кувелье С, Миеланц Н, и другие.Воспаление кишечника и спондилоартропатии. Rheum Dis Clin North Am . 1998; 24: 785–813, ix – x.
3. Гладман Д. Спондилоартропатии. В: Лахита Р., Вайнштейн А., ред. Учебно-обзорное пособие по ревматологии. 2-е изд. rev. Нью-Йорк: Касл Коннолли, выпускник медицинского факультета, 2002: 1-26.
4. Van der Linden S, ван дер Хейде Д. Анкилозирующий спондилоартрит. Клинические признаки. Rheum Dis Clin North Am . 1998; 24: 663–76.vii.
5.Ван дер Линден С., Ван дер Хейде Д. Анкилозирующий спондилит. В: Ruddy S, Harris ED Jr, Sledge CB, ред. Учебник ревматологии Келли. 6-е изд. Филадельфия: Сондерс, 2001: 1039–54.
6. Калин А, Porta J, Картофель фри JF, Шурман DJ. Клинический анамнез как скрининговый тест на анкилозирующий спондилит. ЯМА . 1977; 237: 2613–4.
7. Зипер Дж., Браун Дж, Рудвалейт М, Боонен А, Цинк А. Анкилозирующий спондилит: обзор. Энн Рум Дис . 2002; 61 (приложение 3): iii8–18.
8. Дугадос М, Дийкманс Б, Хан М, Максимович З, ван дер Линден С, Брандт Дж. Обычные методы лечения анкилозирующего спондилита. Энн Рум Дис . 2002; 61 (приложение 3): iii40–50.
9. Ферраз МБ, Тагвелл П., Голдсмит CH, Атра Э. Мета-анализ сульфасалазина при анкилозирующем спондилите. Дж. Ревматол. . 1990; 17: 1482–6.
10. Дугадос М, ван дер Линден С, Лейрисало-Репо М, Huitfeldt B, Джухлин Р, Вейс Э, и другие. Сульфасалазин в лечении спондилоартропатии. Рандомизированное многоцентровое двойное слепое плацебо-контролируемое исследование. Революционный артрит . 1995; 38: 618–27.
11. Clegg DO, Реда DJ, Weisman MH, Блэкберн WD, Куш Джей Джей, Пушка GW, и другие. Сравнение сульфасалазина и плацебо при лечении анкилозирующего спондилита.Совместное исследование Департамента по делам ветеранов. Революционный артрит . 1996; 39: 2004–12.
12. Sampaio-Barros PD, Costallat LT, Бертоло МБ, Нето JF, Самара AM. Метотрексат в лечении анкилозирующего спондилита. Scand J Rheumatol . 2000; 29: 160–2.
13. Максимович В.П., Джангри Г.С., Фитцджеральд А.А., LeClercq S, Чиу П, Ян А, и другие. Шестимесячное рандомизированное контролируемое двойное слепое сравнение доза-эффект внутривенного введения памидроната (60 мг против 10 мг) при лечении нестероидного противовоспалительного лекарственно-рефрактерного анкилозирующего спондилита. Революционный артрит . 2002; 46: 766–73.
14. Горман Дж. Д., Мешок КЕ, Дэвис Дж. С. Мл. Лечение анкилозирующего спондилита путем подавления фактора некроза опухоли альфа. N Engl J Med . 2002; 346: 1349–56.
15. Дэвис Дж. С. Младший, ван дер Хейде Д, Браун Дж, Дугадос М, Куш Дж, Клегг Д.О., и другие. Рекомбинантный рецептор фактора некроза опухоли человека (этанерцепт) для лечения анкилозирующего спондилита: рандомизированное контролируемое исследование. Революционный артрит . 2003. 48: 3230–6.
16. Браун Дж., Брандт Дж. Листинг J, Цинк А, Альтен Р, Голдер В, и другие. Лечение активного анкилозирующего спондилита инфликсимабом: рандомизированное контролируемое многоцентровое исследование. Ланцет . 2002; 359: 1187–93.
17. Браун Дж., Sieper J, Бребан М, Коллантес-Эстевес Э, Дэвис Дж, Инман Р, и другие.Альфа-терапия противоопухолевым фактором некроза анкилозирующего спондилита: международный опыт. Энн Рум Дис . 2002; 61 (приложение 3): iii51–60.
18. Браун Дж., Фам Т, Sieper J, Дэвис Дж, ван дер Линден С, Дугадос М, и другие. Заявление о консенсусе в международном сообществе ASAS по использованию агентов противоопухолевого фактора некроза у пациентов с анкилозирующим спондилитом. Энн Рум Дис . 2003; 62: 817–24.
19. Амор Б. Синдром Рейтера. Диагностика и клиника. Rheum Dis Clin North Am . 1998; 24: 677–95, vii.
20. Ю Д.Т., Пэн Т.Ф. Синдром Рейтера. В: Ruddy S, Harris ED Jr, Sledge CB, ред. Учебник ревматологии Келли. 6-е изд. Филадельфия: Сондерс, 2001: 1055–70.
21. Лау CS, Бургос-Варгас Р, Louthrenoo W, МОК МОЙ, Вордсворт П., Цзэн QY. Особенности спондилоартропатий во всем мире. Rheum Dis Clin North Am . 1998. 24: 753–70.
22. Клегг Д.О., Реда DJ, Weisman MH, Куш Джей Джей, Васей ФБ, Шумахер HR-младший, и другие. Сравнение сульфасалазина и плацебо при лечении реактивного артрита (синдрома Рейтера). Совместное исследование Департамента по делам ветеранов. Революционный артрит . 1996; 39: 2021–207.
23. Yli-Kerttula T, Лууккайнен Р, Юли-Керттула, Моттонен Т, Хакола М, Корпела М, и другие.Влияние трехмесячного курса ципрофлоксацина на исход реактивного артрита. Энн Рум Дис . 2000; 59: 565–70.
24. Лейрисало-Репо М. Прогноз, течение болезни и лечение спондилоартропатий. Rheum Dis Clin North Am . 1998; 24: 737–51, viii.
25. Мидзиява М., Онианкитан О, Хан М.А. Спондилоартропатии в Африке к югу от Сахары. Curr Opin Rheumatol . 2000; 12: 281–6.
26. Гладман Д.Д., Пахман П. Псориатический артрит. В: Ruddy S, Harris ED Jr, Sledge CB, ред. Учебник ревматологии Келли. 6-е изд. Филадельфия: Сондерс, 2001: 1071–80.
27. Молл Ю.М., Райт В. Псориатический артрит. Сывороточный артрит . 1973; 3: 55–78.
28. Комб Б, Гупиль П, Кунц JL, Тебиб Ж, Лиоте Ф, Брегеон К. Сульфасалазин при псориатическом артрите: рандомизированное многоцентровое плацебо-контролируемое исследование. Br J Ревматол . 1996; 35: 664–8.
29. Спадаро А, Риччери V, Сили-Скавалли А, Сенси Ф, Таккари Э, Зоппини А. Сравнение циклоспорина А и метотрексата при лечении псориатического артрита: годичное проспективное исследование. Clin Exp Rheumatol . 1995; 13: 589–93.
30. Ори П, Sharp JJ, Салонен Д, Рубинштейн J, Mease PJ, Кивиц А.Дж., и другие.Этанерцепт (ENBREL) подавляет рентгенологическое прогрессирование у пациентов с псориатическим артритом [Резюме]. Тезисы 66-го ежегодного собрания Американского колледжа ревматологов и 37-го ежегодного собрания Ассоциации специалистов-ревматологов. 24–29 октября 2002 г. Новый Орлеан, Луизиана, США. Революционный артрит . 2002; 46 (9 доп.): S196.
31. Де Вос М, Миеланц Н, Кувелье С, Elewaut A, Вейс Э. Долгосрочная эволюция воспаления кишечника у пациентов со спондилоартропатией. Гастроэнтерология . 1996; 110: 1696–703.
Спондилит – обзор | ScienceDirect Topics
4 Клинические проявления
Спондилит, симметричный полиартрит, асимметричный олигоартрит, дистальный межфаланговый артрит и мутильный артрит – это пять клинических подгрупп ПсА (Moll and Wright, 1973), которые со временем могут меняться, а поражение периферических суставов может меняться. накладываются на осевое заболевание (Jones et al., 1994). Кроме того, ПсА может также возникать при отсутствии клинически очевидного псориаза, но при наличии в семейном анамнезе псориаза (подгруппа «синусоидального псориаза») (Taylor et al., 2006).
Пациенты с ПсА испытывают сердечно-сосудистые события, такие как ишемическая болезнь сердца (стенокардия и инфаркт миокарда), чаще, чем население в целом (Husted et al., 2011; Gladman et al., 2009), из-за одновременного присутствия традиционных факторов риска сердечно-сосудистых заболеваний. и хроническое воспаление (Eder and Gladman, 2015). Тяжелый псориаз связан с повышенным бременем сердечно-сосудистого риска, а наличие активного артрита может быть важным предиктором сердечно-сосудистого заболевания (Gelfand et al., 2007; Wong et al., 1997; Гладман и др., 2009; Eder et al., 2015a). Кроме того, необходимо исследовать наличие классических факторов риска – гиперхолестеринемии, гиперлипидемии, СД, гипертонии и ожирения у пациентов с ПсА, которые могут увеличивать бремя сопутствующих сердечно-сосудистых заболеваний (Gladman et al., 2009; Yeung et al., 2013; Eder et al., 2015a; Atzeni et al., 2011a; Tobin et al., 2010), а артериальная гипертензия и сахарный диабет, в частности, могут прогнозировать серьезные сердечно-сосудистые события (Eder et al., 2015a).
Хотя некоторые исследования показали, что цереброваскулярные заболевания и сердечная недостаточность не более распространены у пациентов с ПсА, чем в общей популяции (Gladman et al., 2009), были сообщения о более высокой распространенности сердечной недостаточности (ОР: 1,5) и цереброваскулярных заболеваний (ОР: 1,3) среди пациентов с ПсА с сопутствующим диабетом, гиперлипидемией и гипертонией (Han et al., 2006).
Учитывая высокую распространенность МетС и его компонентов у пациентов с ПсА (Mok et al., 2011; Raychaudhuri et al., 2010), окружность талии, артериальное давление и триглицериды сыворотки, холестерин липопротеинов высокой плотности (HDL) и голодание уровни глюкозы следует регулярно оценивать.Также следует иметь в виду, что изменяемые факторы риска, такие как физическая активность и курение, могут иметь решающее значение для снижения риска сердечно-сосудистых событий.
ПсА сам по себе является потенциальным фактором риска сердечно-сосудистых заболеваний, поэтому пациентов также следует обследовать на предмет субклинического поражения сердечно-сосудистых заболеваний (Khraishi et al., 2014). Возможные индикаторы субклинического атеросклероза и артериальной жесткости были четко продемонстрированы у пациентов с ПсА, и было бы особенно полезно исследовать их даже при отсутствии клинически очевидного сердечно-сосудистого заболевания (Costa et al., 2012; Ямницкий и др., 2013; Atzeni et al., 2011b). В частности, инструментальные исследования показали высокую распространенность макрососудистых заболеваний, эндотелиальной дисфункции, жесткости артерий и диастолической дисфункции левого желудочка у пациентов с ПсА без каких-либо клинически очевидных признаков атеросклероза или его осложнений (Gonzalez-Juanatey et al., 2007a, 2007b; Коста и др., 2012; Миланюк и др., 2015). По этой причине может быть полезно поискать субклиническое присутствие факторов риска сердечно-сосудистых заболеваний.
Анкилозирующий спондилит: обзор и многое другое
Анкилозирующий спондилит – это тип артрита, характеризующийся хроническим воспалением, которое в первую очередь поражает спину и шею (то есть позвоночник).
В тяжелых случаях кости позвоночника могут срастаться (это также называется анкилозом), в результате чего позвоночник становится жестким и негибким. Следствием этого может быть неправильная осанка. Могут быть поражены и другие суставы, включая бедра, колени, лодыжки или плечи. Заболевание также может быть связано с системными эффектами, поражающими различные органы тела.
Что такое анкилозирующий спондилит?
Классификация
Анкилозирующий спондилит относится к группе состояний, известных как спондилоартропатии. К другим спондилоартропатиям относятся:
Спондилоартропатии подразделяются на аксиальные и периферические, в зависимости от того, какие суставы поражены. Осевой относится к вовлечению позвоночника. Периферический относится к другим суставам за пределами позвоночника.
Анкилозирующий спондилит – это аксиальная спондилоартропатия.
По данным CDC (исследования NHANES Центров по контролю и профилактике заболеваний), по меньшей мере 2,7 миллиона взрослых в США страдают осевым спондилоартритом.
Симптомы анкилозирующего спондилита
Самыми ранними симптомами анкилозирующего спондилита обычно являются боль и скованность в нижней части спины. Симптомы обычно появляются в возрасте до 45 лет. Боль и скованность развиваются и перерастают в хронические симптомы. Как правило, боль при анкилозирующем спондилите усиливается после отдыха или бездействия и улучшается при физической активности.Это может вызвать утреннюю скованность, которая сохраняется более 30 минут.
Боль и скованность со временем могут прогрессировать от позвоночника к шее. Кости позвоночника и шеи могут срастаться, что приводит к ограничению диапазона движений и снижению гибкости позвоночника. Как уже упоминалось, могут быть вовлечены плечи, бедра и другие суставы.
Боль в бедре довольно часто встречается при анкилозирующем спондилите и может быть связана с болью в паху или ягодицах, а также с трудностями при ходьбе.Если поражена грудная клетка, ненормальное расширение грудной клетки может вызвать затруднение дыхания. Могут быть поражены сухожилия и связки (например, поражение пятки при ахилловом тендините и подошвенном фасциите).
Анкилозирующий спондилит также является системным заболеванием, что означает, что у людей может развиться лихорадка, усталость, воспаление глаз или кишечника. Поражение сердца или легких встречается редко, но возможно.
Заболевание в первую очередь поражает мужчин. Заболевание заболевает в два-три раза чаще мужчин, чем женщин.Однако у любого человека может развиться анкилозирующий спондилит. Обычно болезнь возникает в возрасте от 17 до 35 лет.
Причины
Причина заболевания неизвестна, но генетический маркер HLA-B27 присутствует у 90% людей с этим заболеванием, что свидетельствует о генетической связи. Однако важно отметить, что не все, у кого есть HLA-B27. маркер развивает анкилозирующий спондилит.
По данным Американской ассоциации спондилитов, существует более шестидесяти других генов / генетических маркеров, влияющих на предрасположенность к анкилозирующему спондилиту.Исследователи полагают, что причиной развития болезни является триггерное событие окружающей среды в сочетании с восприимчивостью.
Диагностика
Диагноз в основном основывается на симптомах, физикальном осмотре, анализах крови и визуализирующих исследованиях. Ранние симптомы анкилозирующего спондилита могут имитировать другие состояния, поэтому диагностические тесты используются для исключения других ревматических заболеваний. Отсутствие ревматоидного фактора и ревматоидных узелков помогает отличить его от ревматоидного артрита.
Хотя не существует единого анализа крови, который мог бы окончательно диагностировать анкилозирующий спондилит, тест HLA-B27 дает важный диагностический ключ, особенно для определенных групп людей.
Например, анкилозирующий спондилит – маловероятный диагноз для белого человека европейского происхождения и отрицательный на HLA-B27. Тесты на неспецифическое воспаление (скорость оседания и CRP) полезны для определения клинической картины, но не диагностический.
Визуализирующие исследования часто показывают характерные изменения в костях крестцово-подвздошных суставов.Хотя изменения можно увидеть на рентгеновских снимках, после появления симптомов могут пройти годы, прежде чем они станут заметны. МРТ также можно использовать для поиска характерных изменений крестцово-подвздошных суставов, часто обнаруживая их раньше, чем на рентгеновских снимках. Рентген также используется для оценки признаков повреждения позвоночника.
Лечение
Лечение этого состояния в первую очередь направлено на уменьшение боли, скованности и воспаления. Целями лечения также являются предотвращение деформации, поддержание функции и осанки.
Лекарства, используемые для лечения анкилозирующего спондилита, включают следующее:
- Нестероидные противовоспалительные препараты (НПВП) – первая линия фармакологического лечения. Многие люди используют только лекарства от НПВП, чтобы справиться с этим.
- Анальгетики или обезболивающие можно использовать, если боль не купируется только НПВП.
- Блокаторы TNF (Хумира (адалимумаб), Ремикейд (инфликсимаб), Энбрел (этанерцепт), Цимзия (цертолизумаб пегол) и Симпони (голимумаб)) одобрены для лечения анкилозирующего спондилита и показали значительное улучшение активности заболевания.
- Cosentyx (секукинумаб), ингибитор IL-17, был одобрен в январе 2016 года для лечения этого состояния.
- DMARD (противоревматические препараты, модифицирующие заболевание) могут использоваться для замедления прогрессирования заболевания. Обычно сульфасалазин применяется у пациентов с анкилозирующим спондилитом и периферическим артритом, которые не могут использовать блокаторы TNF. Некоторым людям может помочь только метотрексат, но в целом он не считается эффективным при анкилозирующем спондилите. Другой DMARD, арава (лефлуномид), считается малоэффективным.
- Пероральные кортикостероиды используются редко, но когда они принимаются, они должны быть краткосрочными, а не долгосрочными.
Физическая терапия и упражнения являются важной частью любого плана лечения анкилозирующего спондилита. Невозможно переоценить важность физических упражнений как части борьбы с заболеванием и сохранения подвижности и функций.
Прогноз
Некоторые люди с этим заболеванием имеют легкое течение болезни и могут нормально работать и функционировать.У других развивается тяжелое заболевание, и они живут со значительными ограничениями из-за осевого заболевания. У некоторых людей с анкилозирующим спондилитом развиваются опасные для жизни внесуставные осложнения, но в большинстве случаев это не так.
Как правило, индивидуальный пациент имеет дело с колеблющейся активностью заболевания, с которой по большей части можно справиться. Меньшая часть людей с этим заболеванием действительно достигает стадии, когда симптомы ослабевают, и они считаются находящимися в стадии ремиссии.
Если у вас есть вопросы или опасения, поговорите со своим лечащим врачом.Предлагаемые ими стратегии лечения, преодоления трудностей и хорошей жизни могут улучшить ваше самочувствие и ваш общий результат.
Справочник врача по анкилозирующему спондилиту
Получите наше руководство для печати к следующему визиту к врачу, которое поможет вам задать правильные вопросы.
Отправить руководство по электронной почтеОтправить себе или близкому человеку.
Зарегистрироваться
Это руководство для обсуждения с доктором отправлено на адрес {{form.email}}.
Произошла ошибка. Пожалуйста, попробуйте еще раз.
Жилой колодец
Сращенный или менее гибкий позвоночник более подвержен переломам. Тем не менее, вы должны помнить о дополнительном риске и принимать меры предосторожности. Вам следует поговорить со своим лечащим врачом об ограничении или избегании поведения, которое может увеличить риск падения. Это может включать что угодно, от ограничения количества потребляемого алкоголя до установки поручней и сбора ковриков в доме. Избегайте деятельности с высокой ударной нагрузкой. В основном, руководствуйтесь здравым смыслом и берегите свой позвоночник.
Подумайте об использовании подушки, которая обеспечивает хорошее выравнивание шеи и спины во время отдыха или сна. Всегда пристегивайтесь ремнем безопасности во время вождения или в качестве пассажира в транспортном средстве. Кроме того, курящим людям с анкилозирующим спондилитом рекомендуется бросить курить, чтобы снизить риск проблем с дыханием. И не забывайте о важности участия в программе упражнений для укрепления позвоночника и улучшения общего состояния суставов.
Слово Verywell
Если симптомы, вызываемые анкилозирующим спондилитом, влияют на вашу повседневную жизнь, знайте, что существуют варианты лечения.Поговорите со своим лечащим врачом о том, какие лекарства или терапевтические программы подходят вам. Помимо лекарств, многие люди считают, что простая растяжка и физиотерапия имеют большое значение для улучшения самочувствия их тела. Начните медленно и исследуйте ходы, которые подходят именно вам. Это может занять некоторое время, но вы можете обнаружить что-нибудь полезное.
Поражение легких при анкилозирующем спондилите
Dunham CL, Kautz FG (1941) Spondylarthritis ankylopoietica: обзор и отчет о двадцати случаях.Am J Med Sci 201: 232–250
Статья Google Scholar
Campbell AH, McDonald CB (1965) Фиброз верхних долей, связанный с анкилозирующим спондилитом. Br J Dis Chest 59: 90–101
Артикул PubMed CAS Google Scholar
Rosenow EC III, Strimlan CV, Muhm JR, Ferguson RH (1977) Плевролегочные проявления анкилозирующего спондилита. Mayo Clin Proc 52: 641–649
PubMed CAS Google Scholar
Дэвис Д. (1972) Анкилозирующий спондилит и фиброз легких. Q J Med 41: 395–417
PubMed CAS Google Scholar
Boushea DK, Sundstrom WR (1989) Плевропульмональные проявления анкилозирующего спондилита. Semin Arthritis Rheum 18: 277–281
Статья PubMed CAS Google Scholar
Паркин А., Робинсон П.Дж., Хиклинг П. (1982) Региональная вентиляция легких при анкилозирующем спондилите.Br J Radiol 55: 833–836
PubMed CAS Статья Google Scholar
Farquhar DRE, Чемберлен MJ, McCain GA, Morgan WK (1989) Удаление вдыхаемых частиц при анкилозирующем спондилите. Ann Rheum Dis 48: 974–977
PubMed CAS Google Scholar
Hillerdal G (1983) Анкилозирующий спондилит – заболевание легких – недиагностированное заболевание? Eur J Respir Dis 64: 437–441
PubMed CAS Google Scholar
Eulry F, Mayaudon H, Sirvin-Bordier L, Perier E, Guillemot C, Lechevalier D et al (1998) HLA-B27 и вовлечение дыхательных путей при аксиальных спондилоартропатиях: ретроспективное исследование с участием 107 пациентов мужского пола. Rev Rhum Engl Ed 65: 560–566
PubMed CAS Google Scholar
Feltelius N, Hedenstrom H, Hillerdal G, Hallgren R (1986) Поражение легких при анкилозирующем спондилите. Ann Rheum Dis 45: 736–740
PubMed CAS Google Scholar
Franssen MJAM, Van Herwaarden CLA, Van de Putte LBA, Gribnau FWJ (1986) Функция легких у пациентов с анкилозирующим спондилитом. Изучение влияния активности заболевания и лечения нестероидными противовоспалительными препаратами. J Rheumatol 13: 936–940
PubMed CAS Google Scholar
Vanderschueren D, Decramer M, Van den Daele P, Dequeker J (1989) Функция легких и максимальное давление дыхания при анкилозирующем спондилите.Ann Rheum Dis 48: 632–635
PubMed CAS Google Scholar
Eulry F, Marotel C, Lechevalier D, Haguenauer D, Crozes P, Magnin J (1994) Поражение легких при анкилозирующем спондилите: взаимосвязь с фенотипами альфа-1-антитрипсина и курением. Rev Rhum Engl Ed 61: 349–358
Google Scholar
Wendling D, Dalphin JC, Toson B, Depierre A, Guidet M (1990) Бронхоальвеолярный лаваж при анкилозирующем спондилите.Ann Rheum Dis 49: 325–326
PubMed CAS Google Scholar
Кчир М.М., Мтимет С., Кочбати С., Зуари Р., Айед М., Гарби Т. и др. (1992) Бронхоальвеолярный лаваж и трансбронхиальная биопсия при спондилоартропатиях. J Rheumatol 19: 913–916
PubMed CAS Google Scholar
Jeandel P, Bonnet D, Chouc PY, Molinier S, Raphenon G, Martet G et al (1994) Mise en proof d’une alveolite pulmonaire infraclinique au cours des spondyloarthropathies.Rev Rhum Ed Fr 61: 301–309
PubMed CAS Google Scholar
Fenlon HM, Casserly I, Sant SM, Breatnach E (1997) Простые рентгенограммы и КТ грудной клетки высокого разрешения у пациентов с анкилозирующим спондилитом. AJR Am J Roentgenol 168: 1067–1072
PubMed CAS Google Scholar
Турецчек К., Эбнер В., Флейшманн Д., Вундербалдингер П., Эрлахер Л., Зонтисич Т. и др. (2000) Раннее поражение легких при анкилозирующем спондилите: оценка с помощью КТ тонких срезов.Clin Radiol 53: 632–636
Артикул Google Scholar
Senocak O, Manisali M, Ozaksoy D, Sevinc C, Akalin E (2003) Изменения паренхимы легких при анкилозирующем спондилите: демонстрация с помощью КТ высокого разрешения и корреляция с длительностью заболевания. Eur J Radiol 45: 117–122
Статья PubMed Google Scholar
Кирис А., Озгокмен С., Кокакок Э., Ардикоглу А., Огур Э. (2003) Результаты компьютерной томографии легких с высоким разрешением при раннем анкилозирующем спондилите.Eur J Radiol 47: 71–76
Статья PubMed Google Scholar
Эль Маграуи А., Чауир С., Абид А., Бецза А., Табач Ф, Ахемиал Л. и др. (2004) Результаты исследования легких при компьютерной томографии грудной клетки с высоким разрешением у пациентов с анкилозирующим спондилитом. Корреляция с длительностью заболевания, клиническими данными и результатами исследования функции легких. Clin Rheumatol 23: 123–128
Статья PubMed Google Scholar
Соуза А.С. Младший, Мюллер Н.Л., Маркиори Э., Соарес-Соуза Л.В., Соуза Роча М. (2004) Легочные аномалии при анкилозирующем спондилите: результаты КТ высокого разрешения на вдохе и выдохе у 17 пациентов. J Thorac Imaging 19: 259–263
Статья PubMed Google Scholar
Алтин А.Р., Оздолап С., Савранлар А., Сарикая С., Тор М., Карт Л. и др. (2005) Сравнение ранних и поздних плевропульмональных результатов анкилозирующего спондилита с помощью компьютерной томографии высокого разрешения и влияния на повседневное жизнь.Clin Rheumatol 24: 22–28
Статья PubMed Google Scholar
Grenier P, Chevret S, Beigelman C, Brauner MW, Chastang C, Valeyre D (1994) Хроническое диффузное инфильтративное заболевание легких: определение диагностической ценности клинических данных, рентгенографии грудной клетки и КТ с байесовским анализом. Радиология 191: 383–390
PubMed CAS Google Scholar
Van der Linden S, Valkenburg HA, Cats A (1984) Оценка диагностических критериев анкилозирующего спондилита: предложение по модификации критериев Нью-Йорка. Arthritis Rheum 27: 361–368
PubMed Google Scholar
Consenso Brasileiro de Tuberculose (Бразильский консенсус по туберкулезу) (1997) J Pneumol 23: 294–342
Google Scholar
Браун Дж., Сипер Дж., Бребан М., Коллантес-Эстевес Э., Дэвис Дж., Инман Р. и др. (2002) Терапия альфа-фактором некроза опухолей при анкилозирующем спондилите: международный опыт.Ann Rheum Dis 61 (Дополнение III): 51–60
Google Scholar
Keat A, Barkham N, Bhalla A, Gaffney K, Marzo Ortega H, Paul S. et al, BSR Standards, Guidelines and Audit Working Group (2005) BSR Рекомендации по назначению блокаторов TNF-α у взрослых с анкилозирующей болезнью спондилит. Ревматология 44: 939–947
Статья PubMed CAS Google Scholar
Кин Дж. (2005) ФНО-блокирующие агенты и туберкулез: новые препараты проливают свет на старую тему.Ревматология 44: 714–720
Статья PubMed CAS Google Scholar
Furst DE, Cush J, Kaufmann S, Siegel J, Kurth R (2002) Предварительные рекомендации по диагностике и лечению туберкулеза у пациентов с ревматоидным артритом в иммуносупрессивных испытаниях или на лечении биологическими агентами. Ann Rheum Dis 61 (Дополнение II): 62–63
Статья PubMed Google Scholar
Стюарт Р.М., Ридьярд Дж. Б., Пирсон Дж. Д. (1976) Региональная функция легких при анкилозирующем спондилите. Торакс 31: 433–437
PubMed CAS Статья Google Scholar
Van Noord JA, Cuberghs M, Van de Woestijne KP, Demedts M (1991) Общее респираторное сопротивление и реактивность при анкилозирующем спондилите и кифосколиозе. Eur Respir J 4: 945–951
PubMed Google Scholar
Aggarwal NA, Gupta D, Wanchu A, Jindal SK (2001) Использование статической механики легких для выявления раннего легочного поражения у пациентов с анкилозирующим спондилитом. J Postgrad Med 47: 89–94
PubMed CAS Google Scholar
Cerrahoglu L, Unlu Z, Can M, Goktan C, Celik P (2002) Жесткость поясницы, но не рентгенологические изменения грудной клетки, связаны с изменением тестов функции легких при анкилозирующем спондилите. Clin Rheumatol 21: 275–279
Статья PubMed CAS Google Scholar
Camiciottoli G, Trapani S, Ermini M, Falcini F, Pistolesi M (1999) Функция легких у детей, страдающих ювенильной спондилоартропатией. J Rheumatol 26: 1382–1386
PubMed CAS Google Scholar
Carter R, Riantawan P, Banham SW, Sturrock RD (1999) Исследование факторов, ограничивающих аэробные способности у пациентов с анкилозирующим спондилитом. Respir Med 93: 700–708
Артикул PubMed CAS Google Scholar
Fisher LR, Cawley MID, Holgate ST (1990) Связь между расширением грудной клетки, легочной функцией и толерантностью к физической нагрузке у пациентов с анкилозирующим спондилитом. Ann Rheum Dis 49: 921–925
PubMed CAS Статья Google Scholar
Сечкин Ю., Болукбаши Н., Гурсель Г., Эроз С., Сепичи В., Эким Н. (2000) Взаимосвязь между функцией легких и толерантностью к физической нагрузке у пациентов с анкилозирующим спондилитом. Clin Exp Rheumatol 18: 503–506
PubMed Google Scholar
Remy-Jardin M, Remy J, Gosselin B, Becette V, Edme JL (1993) Паренхиматозные изменения легких, вторичные по отношению к курению сигарет: корреляции патологического и CT. Радиология 186: 643–651
PubMed CAS Google Scholar
Remy-Jardin M, Edme JL, Boulenguez C, Remy J, Mastora I, Sobaszek A (2002) Продолжительное последующее исследование легких курильщика с помощью КТ тонких срезов в корреляции с тестами функции легких. Радиология 222: 261–270
PubMed Google Scholar
Sampaio-Barros PD, Bértolo MB, Kraemer MHS, Marques-Neto JF, Samara AM (2001) Первичный анкилозирующий спондилит: модели заболевания в бразильской популяции из 147 пациентов. J Rheumatol 28: 560–565
PubMed CAS Google Scholar
Conde RA, Sampaio-Barros PD, Donadi EA, Kraemer MHS, Persoli L, Coimbra IB et al (2003) Частота аллелей HLA-B27 у бразильских пациентов с анкилозирующим спондилитом. J Rheumatol 30: 2511–2512
PubMed Google Scholar
Sampaio-Barros PD, Conde RA, Donadi EA, Kraemer MHS, Persoli L, Coimbra IB et al (2003) Недифференцированные спондилоартропатии у бразильцев: важность аллелей HLA-B27 и B7-CREG в характеристике и прогрессировании заболевания. J Rheumatol 30: 2632–2637
PubMed CAS Google Scholar
Связанный с HLA-B27 путь опосредует образование синдесмофитов в AS
Анкилозирующий спондилит (АС) характеризуется образованием синдесмофитов и чаще встречается у людей с HLA-B27 + , но неясно, связаны ли эти два явления.Согласно результатам нового исследования, неправильная укладка HLA-B27 напрямую связана с образованием синдесмофитов через тканеспецифическую щелочную фосфатазу (TNAP) в процессе, который может быть целевым терапевтическим.
Предоставлено: Springer Nature Limited
«Мы извлекли мезенхимальные стволовые клетки (МСК) из энтезов пациентов с СА, чтобы устранить какие-либо отклонения в МСК, полученных от СА», – объясняет соавтор-корреспондент Куо-И Линь. «Мы не обнаружили каких-либо существенных различий в продукции цитокинов или хемокинов, которые мы тестировали в MSC, полученных из AS, по сравнению с контрольными MSC, но MSC, полученные из AS, действительно показали ускоренную минерализацию при остеогенной индукции.
Исследователи были удивлены, обнаружив, что эта усиленная минерализация не регулируется фактором транскрипции RUNX2, который обычно связан с этим процессом, а вместо этого регулируется TNAP через фактор транскрипции RARβ. Дальнейшие исследования in vitro показали, что развернутый HLA-B27 вызывает повышающую регуляцию TNAP в AS-производных MSCs посредством пути IRE1α-sXBP1 ответа развернутого белка. Важно отметить, что сывороточные концентрации костно-специфического TNAP были увеличены у пациентов с AS по сравнению со здоровыми людьми из двух разных когорт и коррелировали с прогрессированием заболевания.
«Мы также имплантировали полученные из AS MSC возле механически разрушенного позвоночника мышей NOD-SCID, чтобы проверить, демонстрируют ли они усиленное костеобразование in vivo», – говорит соавтор-корреспондент Shih-Chieh Hung. «Эта новая модель на животных, кажется, имитирует развитие новых костных отростков у пациентов».
«развернутый HLA-B27 вызывает повышенную регуляцию TNAP в MSC, производных от AS»
Интересно, что лечение этих мышей ингибиторами TNAP левамизолом (противоглистным препаратом) или памидронатом (бисфосфонатом) существенно снижало образование синдесмофитов.«В будущем мы надеемся выявить новые лекарственные препараты-кандидаты, поскольку доступные в настоящее время ингибиторы TNAP могут иметь некоторые побочные эффекты», – заключает Линь.
Информация об авторе
Принадлежность
Nature Reviews Ревматология
Джоанна Кларк
Автор, ответственный за переписку
Для корреспонденции Джоанна Кларк.
Об этой статье
Цитируйте эту статью
Clarke, J.Связанный с HLA-B27 путь опосредует образование синдесмофитов при AS. Nat Rev Rheumatol 16, 3 (2020). https://doi.org/10.1038/s41584-019-0343-2
Скачать цитату
Ребенок с туберкулезным спондилитом одного третьего шейного позвонка: история болезни | Journal of Medical Case Reports
Недавнее глобальное возрождение туберкулеза привело к достижению цели 6 в области развития, сформулированной в Декларации тысячелетия Организации Объединенных Наций, направленной на сокращение вдвое показателей распространенности туберкулеза и смертности от него к 2015 году.Несмотря на то, что эта цель выполняется, наблюдается относительное увеличение внелегочных заболеваний, которые являются более сложными с диагностической точки зрения [4, 5]. Позвоночник является наиболее частым очагом скелетного туберкулеза, и при поражении шейных позвонков высок риск тяжелой инвалидности.
Классическая клиническая картина туберкулеза позвоночника – местная боль, болезненность, жесткость и мышечный спазм продолжительностью несколько недель. У нашего пациента было такое представление, но он жаловался на боль в шее, а не на боль в спине, которая встречается гораздо чаще при туберкулезе поясничного или грудного отдела позвоночника [6].Тщательный анамнез выявил два других симптома, характерных для туберкулеза позвоночника: «плач во сне» и «беспокойный сон». Лихорадка, потеря веса и анорексия отсутствовали у нашего пациента и отсутствуют у большинства пациентов с туберкулезом позвоночника. Рентгенография грудной клетки также оказалась бесполезной, как сообщалось в предыдущих случаях туберкулеза позвоночника [6]. Кроме того, диагноз был затруднен из-за отрицательной кожной пробы на туберкулин и анализа высвобождения гамма-интерферона, которые могут давать ложноотрицательные результаты у детей [7].
Демонстрация микобактерий туберкулеза в поражении скелета является золотым стандартом диагностики туберкулеза [8].Однако в предыдущих отчетах утверждается, что ни одна серия не могла сделать это во всех случаях, и при подозрении на туберкулез позвоночника рекомендуется эмпирическое лечение [9, 10].
Нам не удалось получить биопсию кости или материал для мазка и посева из-за сложной траектории, необходимой для игольной биопсии под визуальным контролем, не разрешенной ее родителями. Хирургическое вмешательство не проводилось, поскольку часто встречаются ложноотрицательные результаты биопсии, отрицательный мазок на кислотоустойчивые бациллы и невозможность посева Mycobacterium tuberculosis .
Богатая сосудистая сеть губчатой кости тел позвонков вызывает гематогенное распространение M. tuberculosis и туберкулезный спондилит. Артериальное кровоснабжение позвонков осуществляется из передней и задней спинных артерий, при этом сегментарные артерии разветвляются для снабжения верхней и нижней половин соседних позвонков. Это вызывает характерные проявления туберкулеза позвоночника: разрушение тел смежных позвонков и поражение межпозвонковых дисков.
Одиночное заболевание позвонка без поражения диска, наблюдаемое у нашего пациента, очень необычно.Это было описано у нескольких взрослых [10]. Механизм, с помощью которого туберкулезные палочки откладывались в одном теле позвонка без вовлечения соседних позвонков или диска, остается неясным, и ранняя стадия заболевания является вероятным объяснением. Кроме того, туберкулез шейки матки встречается только в 0,3–2,2% случаев туберкулеза позвоночника [6, 11, 12].
При дифференциальной диагностике учитывались два состояния: инфекционный процесс или эозинофильная гранулема кости (унифокальный гистиоцитоз из клеток Лангергана, LCH, кости).Отсутствие склероза делало гнойный спондилит маловероятным.
Unifocal LCH – редкое заболевание, которое может проявляться коллапсом одного шейного позвонка у ребенка [3, 13]. Диагноз унифокального LCH может быть подтвержден только гистологическим исследованием. Нормальный костный мозг, отсутствие остеолитических поражений в других костях и отсутствие ультразвуковых свидетельств поражения печени или селезенки исключили мультисистемный гистиоцитоз.
Случайное обнаружение очагового кальцинированного узелка в ее печени еще раз подтвердило туберкулез.Туберкулез является наиболее вероятной причиной бессимптомных кальцифицированных узлов в печени в Шри-Ланке, поскольку паразитарные инфекции, такие как шистосомоз или висцеральный лейшманиоз, чрезвычайно редки. Биопсия узелка печени не проводилась из-за отсутствия показаний, необходимых для исключения основного заболевания печени или диагностики излечимой паразитарной инфекции.
Противотуберкулезное лечение в четырехкратном режиме проводилось до разрешения превертебрального сбора мягких тканей. Хотя печень является необычным местом для кальцинированного туберкулезного узелка, ее исчезновение после противотуберкулезного лечения было значительным.Полный курс лечения продолжительностью 12 месяцев завершился клиническими и рентгенологическими свидетельствами заживления без неврологического дефицита или деформации [14].


 3. МРТ после 20 дней терапии Левофлоксацином
3. МРТ после 20 дней терапии Левофлоксацином М., 2005.С. 128.
М., 2005.С. 128. Spine J 2005; 5:64-70.
Spine J 2005; 5:64-70.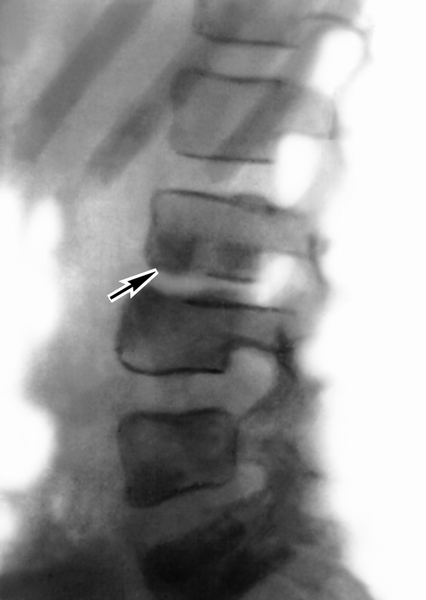 «Possible salmonella osteomyelitis of spine following laser disc decompression». Eur Spine J 1998; 7:509-511.
«Possible salmonella osteomyelitis of spine following laser disc decompression». Eur Spine J 1998; 7:509-511. При постоянном мониторинге кажется, что существует сильная взаимосвязь между воспалением кишечника и суставов.
При постоянном мониторинге кажется, что существует сильная взаимосвязь между воспалением кишечника и суставов. Этот тест помогает исключить анкилозирующий спондилит. Этот ген есть у более 95% людей с анкилозирующим спондилитом, тогда как у гораздо меньшего числа людей с недифференцированной спондилоартропатией он есть. (Наличие гена не обязательно означает, что у человека разовьется анкилозирующий спондилит.)
Этот тест помогает исключить анкилозирующий спондилит. Этот ген есть у более 95% людей с анкилозирующим спондилитом, тогда как у гораздо меньшего числа людей с недифференцированной спондилоартропатией он есть. (Наличие гена не обязательно означает, что у человека разовьется анкилозирующий спондилит.)