Диафизарные переломы – Вопрос 40. Диафизарные переломы костей голени. Диагноз. Классификация. Протокол оказания помощи на этапах эвакуации в мирное время.
Диафизарные переломы костей голени – БолезньИнформ
Патогенез (что происходит?) во время Диафизарного перелома костей голени
Большеберцовая кость является основной опорной костью, от целости которой в основном зависит функции голени. Кость расположена эксцентрично и соединена с малоберцовой костью плотной межкостной мембраной, играющей существенную роль в характере смещения отломков.
Мышцы расположены по задней и наружной поверхностям и прикрепляются на уровне верхней и средней третей голени, на нижней трети прикрепления мышц нет. Переднее-внутренняя поверхность голени мышц не имеет.
Смещение отломков по ширине при переломе обеих конечностей зависит от направления внешней силы. Смещение в сторону в зависимости от механизма его возникновения не может быть типичным, однако вследствие эластической ретракции мышц при прочих равных условиях периферический отломок имеет тенденцию к смещению кпереди и внутрь.
Ретракция мышц вызывает угловое смещение, а при наличии бокового смещения — и по длине. Угловое смещение вследствие эластической ретракции мышц и силы тяжести чаще всего наблюдается под углом, открытым кнаружи. Смещение отломков при косых и винтообразных переломах зависит от направления плоскости излома.
(по А. И. Казьмину)
Начало искривления
позвоночного столба – это эпифизеолиз
межпозвонковых дисков.
Смещение дисков
при эпифизеолизе ведет к смещению
пульпозного ядра в одну из сторон.
Позвоночник искривляется в сторону
отсутствия ядра и искривление его в
другую сторону невозможно (рис. 140).
Вертикальное положение больного при
этом так же невозможно.
Установлено,
что стабилизация дуги искривления не
зависит от степени развития болезни, а
зависит от степени смещения пульпозного
вершинах первичных искривлений.
Пока
пульпозное ядро не имело признаков
дегенерации, сохранялась асимметрия
дисков. С началом дегенерации ядра эта
асимметрия начинала исчезать и появлялась
клиновидная деформация тел позвонков.
Нарушение роста тел позвонков наступает
только после дегенерации дисков и
является вторичным процессом, связанным
с состоянием дисков и в частности –
пульпозных ядер. Это подтверждает
выявляемый эпифизеолиз дисков.
Что
способствует его появлению? Извращение
обменных процессов? Вертикальное
положение тела человека? Установить
это пока не возможно. Прежде всего, для
выяснения этого вопроса необходимы
больные с начальными стадиями развития
болезни, а ортопед, чаще всего, впервые
видит больного уже со сформировавшейся
дугой искривления.
Смещение
пульпозного ядра приводит к дисбалансу
на высоте искривления напряжены мышцы
выпуклой стороны, в нижней части –
напряжены мышцы вогнутой стороны (рис.
141).
Дисбаланс мышц
при искривлении ведет к торсии позвонков.
Смещение пульпозного ядра приводит к
неправильной нагрузке на тело нижележащего
позвонка, что способствует развитию
остеохондроза и формированию клиновидного
позвонка на вершине искривления.
Переломы голени возможны от прямого воздействия, при этом возникают поперечные и оскольчатые переломы одной или обеих костей. От непрямого воздействия при вращении тела с фиксированной стопой возникают винтообразные переломы обеих костей голени, реже — одной большеберцовой.
Диафизарные переломы голени часто сопровождаются смещением отломков (80% случаев). Отломки вправляются с трудом, после вправления нередко наступает вторичное смещение.
Особенности диагностики опухолей у детей
Диагностика
опухолей у детей представляет собой
одну из трудных задач современной
ортопедии, рентгенологии и патологической
анатомии. Это связано не только с
разнообразием заболеваний, но и
характерным начальным течением ряда
заболеваний без проявления ясных
симптомов.
Нередко распознают их поздно,
при явно выраженном проявлении болезни.
Болезненный очаг, как правило, залегает
в глубине костной коробки, при этом
ребенок в отличие от взрослого не всегда
в состоянии оценить свои ощущения и
сформулировать свои жалобы.
Ранняя
диагностика опухолей затруднена
необычайным сходством отдельных
новообразований. Как клиницист не может
клинические данные, так и рентгенолог
не может быть уверенным в наличии
определенного заболевания на основании
описания только рентгенограммы.
Таким
образом, диагностика заболеваний скелета
– трудное и ответственное дело, Здесь
необходимо комплексное использование
существующих методов распознавания
костных опухолей.
На ранних стадиях
многие костные заболевания не имеют
специфической симптоматики. В связи с
этим необходимо пользоваться отдельными,
даже незначительными данными, которые
в сумме определяют «трудно рождающийся
диагноз».
К ним относятся анамнез, первые
жалобы, длительность болезни и
сопоставление соответствия размеров
опухоли с давностью заболевания,
результаты внешнего осмотра, общего
состояния больного, его возраст, пол,
локализация новообразования.
Трудности
диагностики костных поражений опухолевым
возникают у детей лишь тогда, когда
болезненный очаг либо достигает больших
размеров и сдавливает рядом находящиеся
нервные стволы, либо, выходя за границы
кости до надкостницы, вовлекают ее в
процесс и проявляются болями.
Выяснение
характера боли – существенная часть
трудного диагноза. Чаще всего боли
являются первыми симптомами злокачественных
опухолей, так как в процесс вовлекается
надкостница. Вначале боли носят
непостоянный характер.
Позже больной
ребенок уточняет их локализацию. Сначала
боли периодические, затем становятся
постоянными, наблюдаются в покое, даже
при иммобилизации больной конечности
гипсовой шиной боли не стихают ни днем,
ни ночью.
Иногда боли не соответствуют
локализации опухоли. В этих случаях
необходимо думать об иррадиации болей
по нервным стволам. Так, при локализации
могут локализоваться в коленном суставе,
иррадиируя по бедренному нерву. Весьма
характерны ночные боли, в значительной
степени изнуряющие больного.
При отдельных
злокачественных новообразованиях боли
появляются раньше, чем очаг выявляется
на обычной рентгенограмме. В этих случаях
необходимо прибегать к современным
методам обследования больного:
компьютерной и ядерномагнитнорезонансной
томографии, которые позволяю выявить
очаг размером около 2мм.
Доброкачественные
опухоли почти всегда безболезненны.
Боли в этих случаях чаще вторичные, за
счет механического давления большой
опухолью рядом расположенных нервных
стволов. Только остеоид-остома (рис.
125) проявляет себя сильным болевым
синдромом, обусловленным увеличенным
внутрикостным давлением в «гнезде
опухоли». Кроме того, эти боли хорошо
снимаются аспирином, а при злокачественных
снимается на непродолжительное время
только наркотическими веществами.
Некоторые
опухоли костей, расположенные эндостально
(рис. 126), впервые проявляют себя
патологическим переломом (остеобластокластома,
хондрома). Существует мнение, что такие
переломы, срастаясь, могут привести к
«самоизлечению», что вызывает определенные
сомнения.
https://www.youtube.com/watch?v=JPtZk60Wr7w
Уточняя
анамнез заболевания, выясните, прежде
всего, первые симптомы заболевания.
Дети и родители нередко обращают внимание
на предшествующую травму, хотя установлено,
что травма не имеет никакого отношения
к появлению опухолевого роста.
При
обычном травматическом повреждении
боль, припухлость, нарушение функции
появляются сразу же после травмы, а при
опухолях эти клинические симптомы
появляются спустя некоторое время,
Поинтересуйтесь, применялось ли больному
физиотерапевтическое лечение, особенно
тепловые процедуры, и его эффективность.
Больные с опухолями отмечают, что
применение тепла усиливает боли и
увеличивает пораженный сегмент. ФТЛ
при опухолях противопоказано, так как
стимулирует опухолевый рост.
Общее состояние
больного при опухолях костей не страдает.
При доброкачественных опухолях оно
вообще не меняется, исключая остеоид-остеому.
Злокачественные опухоли, особенно у
маленьких детей, могут начинаться как
острый воспалительный процесс и,
например, начало саркомы Юинга нередко
«протекает» под диагнозом «Остеомиелит»
(рис. 124).
Хороший внешний
вид ребенка не исключает наличия у него
злокачественного новообразования, так
как кахексия развивается только в
терминальной стадии процесса. Дети
просто не доживают до ракового истощения,
Внешний
вид органа, пораженного костной опухолью,
припухлостью, которая пальпаторно
отличается плотной консистенцией. Призлокачественных опухолях боль
предшествует припухлостии появление
припухлости при злокачественных опухолях
– поздний симптом.
Только при
остеобластокластомах со значительным
истончением кортикального слоя в месте
опухоли при пальпации можно ощутить
костный хруст (крепитацию), появляющийся
из-за повреждения тонкого кортикального
слоя при пальпации.
Метастатические
опухоли никогда не пальпируются, а
остеолитические формы чаще всего
проявляются патологическим переломом.
В области
определяющейся деформации, над
доброкачественной опухолью кожные
покровы не изменяются. При злокачественных
– кожа бледная, истонченная, с
просвечивающимися венозными сосудами
(«мраморная кожа»), тяжело смещается
распадающихся опухолях возможно их
изязвление (рис. 124).
Нарушение функции
конечности зависит от локализации
очага по отношению к суставу: остеогенная
саркома, локализующаяся в эпиметафизе
бедра, вызывает болевую контрактуру, а
гигантома (ОБК) даже при прорыве опухоли
в сустав не нарушает функцию конечности
(сустава), т.к.
безболезненна. Ограничение
движений нередко связаны с патологическим
переломом, который может стать первым
признаком опухоли, а при злокачественных
новообразованиях свидетельствует об
инкурабельности
опухоли и дает резкий толчок к
метастазированию.
Возраст
больного имеет существенное значение
для решения вопроса о характере опухоли.
Для детского возраста характерны
первичные опухоли, метастатические
крайне редки, а у взрослых наоборот —
метастатические встречаются в 20 раз
чаще.
Так, на каждого больного с первичной
опухолью приходится 2-3 метастатических.
Возраст ребенка имеет существенное
значение в возникновении некоторых
видов опухолей. Так, эозинофильная
гранулема чаще выявляется у детей
дошкольного возраста, фиброзная дисплазия
характерна для детей 10-12 лет, а для детей
5 лет – саркома Юинга, для детей старше
8 лет и подростков – остеогенная саркома.
Локализация
опухоли очень характерна. Некоторые
опухоли имеют свою излюбленную
локализацию, что может быть одним из
диагностических симптомов. Так, хондромы
локализуются в мелких костях кисти
(рис.
127), гигантома (ОБК) у детей – в
проксимальном метадиафизе плеча (рис.
128), а у взрослых – в проксимальном
метаэпифизе большеберцовой кости.
Остеогенная саркома локализуется в
дистальном метафизе бедра (рис.
Лабораторные
данные. Общий анализ крови выполняется
всем больным. При доброкачественных
опухолях в нем изменений не выявляется.
Практически, только у больных с саркомой
Юинга в общем анализе крови определяются
изменения по типу воспалительного
синдрома: высокая СОЭ, нейтрофильный
лейкоцитоз со сдвигом формулы влево.
Биохимические
исследования. Биохимические исследования
в настоящее время играют огромную роль
в определении характера и стадии
патологического процесса в кости.
Значительное увеличение белка сыворотки
крови выявляется при миеломной болезни.
Наряду с этим в моче появляются тельца
Бенс-Джойса, которые в норме отсутствуют.
Вопрос 40. Диафизарные переломы костей голени. Диагноз. Классификация. Протокол оказания помощи на этапах эвакуации в мирное время.
Диафизарные переломы голени составляют 11-13% от числа всех переломов. Лечение таких переломов костей голени остается одной из важнейших проблем травматологии. Диафизарные переломы голени часто сопровождаются смещением отломков (80% случаев). Отломки вправляются с трудом, после вправления нередко наступает вторичное смещение.
Классификация по АО:
А1 — спиральный перелом, А2 — косой перелом, A3 — поперечный перелом.
В1 — клиновидный спиральный перелом, В2 — клиновидный сгибательный перелом, ВЗ – клиновидный фрагментированный перелом.
С1 — сложный спиральный перелом, С2 — сложный сегментарный перелом, СЗ – сложный иррегулярный перелом.
Диагностика диафизарных переломов костей голени несложна – всегда есть явная деформация, укорочение и всегда легко пропальпировать нарушение непрерывности переднего гребня большеберцовой кости. При переломах верхнего конца большеберцовой кости может быть повреждена и тромбирована подколенная артерия, поэтому при этих переломах особо внимательно надо ощупать стопы ( нет ли разницы в температуры ) и изучить пульсацию тыльной артерии. Если у фельдшера или врача районной больницы возникает подозрение о нарушении магистрального артериального кровотока, то транспортировка больного на этап специализированной ангиотравматологической помощи должна быть незамедлительной. О своем подозрении фельдшер непременно должен сообщить хирургу районной больницы, чтобы он еще до прибытия больного изучил возможности скорейшей помощи ему ангиохирургом. Если перелом костей голени открытый, то фельдшер вводит обезболивающие препараты (2%-ный раствор промедола 2 мл или 50%- ный раствор анальгина 2 мл и 2 мл 1%-ного раствора димедрола, антибиотики- 2 млн. Ед пенициллина внутримышечно) и осуществляет транспортную иммобилизацию перелома тремя большими лестничными шинами.
На этапах специализированной помощи. Лечение изолированных переломов большеберцовой кости без смещения отломков осуществляется циркулярной гипсовой повязкой в течение 2-4 месяцев. При выраженном отеке голени – вскрывается дорожка по передней поверхности. После спадения отека повязка превращается в глухую циркулярную. Изолированные переломы большеберцовой кости со смещением лечат оперативно в связи с тем, что они относятся к невправимым из-за целой малоберцовой кости. Гипсовой повязкой лечат переломы без смещения, а также репонируемые и легко удерживаемые переломы. Гипсовая повязка не предупреждает вторичного смещения, поэтому она не должна применяться при косых и винтообразных переломах. При переломах в верхней трети голени гипсовая повязка накладывается от ягодичной складки, при средней трети – от середины бедра до кончиков пальцев стопы. При наличии отека голени гипсовую повязку рассекают по передней поверхности.
Лечение методом постоянного скелетного вытяжения является основным при закрытых переломах обеих костей голени любой локализации. Спица для вытяжения проводится либо за надлодыжечную область, либо – за пяточную кость. Нога укладывается на шину Белера. Первоначальный вправляющий груз по оси голени – 10% от массы пострадавшего. Затем по контрольной рентгенограмме, которая производятся не раньше чем через 24-48 часов, подбирают индивидуальный груз. Продолжительность постельного режима – 4 недели. Достоверным клиническим критерием достаточности срока лечения является отсутствие патологической подвижности в зоне перелома, что и является показанием для очередного рентгенологического исследования места перелома. После демонтажа скелетного вытяжения конечность фиксируют гонитной гипсовой повязкой на 2-3 месяца. Трудоспособность восстанавливается через 4-6 месяцев со дня травмы.
Оперативное лечение закрытых диафизарных переломов показано при интерпозиции мягких тканей в зоне перелома, открытых и осложненных переломах, нерепонируемых переломах. При переломах диафизов обеих костей проводят остеосинтез только большеберцовой кости.
20)Диафизарные переломы бедренной кости. Диагноз. Протокол лечения.
Диафизарный перелом бедра – тяжелая травма, сопровождающаяся болевым шоком и значительной кровопотерей. Переломы бедра возникают в результате прямой травмы (падение, удар). Возможен перелом бедра при непрямой травме (скручивании, сгибании). Причиной повреждения может стать падение с высоты, автомобильная авария, производственная или спортивная травма. Чаще страдают люди молодого и среднего возраста.
При прямой травме возникают поперечные, косые и оскольчатые переломы бедра, при непрямой – винтообразные.
При переломе бедра на отломки воздействует большое количество мышц, прикрепляющихся к бедренной кости. Мышцы тянут отломки в стороны, вызывая их смещение. Направление смещения зависит от уровня перелома.
Симптомы
Пациент с переломом бедра предъявляет жалобы на сильную боль в месте повреждения. В области перелома наблюдается отечность, кровоизлияние, деформация конечности и патологическая подвижность. Нога, как правило, укорочена.
Перелом бедра может сопровождаться повреждением нерва или крупного сосуда. Возможно развитие травматического шока, обусловленного резкой болью и выраженной кровопотерей.
Первая помощь
Поврежденную конечность необходимо зафиксировать, наложив шину Дитерикса или шины Крамера. Пациенту вводят обезболивающее. Затем его накрывают одеялом и транспортируют в стационар.
Лечение
При переломе бедра существует опасность развития травматического шока. Профилактические противошоковые мероприятия включают в себя адекватное обезболивание. При значительной кровопотере проводится переливание крови и кровезаменителей.
Гипсовая повязка на начальном этапе лечения не применяется, поскольку с ее помощью невозможно удержать отломки в правильном положении. В качестве основных методов лечения используется скелетное вытяжение, аппараты внешней фиксации и операция (остеосинтез).
Противопоказанием к оперативному лечению при переломе бедра являются тяжелые сопутствующие заболевания, инфицированные раны и общее тяжелое состояние больного в результате сочетанной травмы. При наличии противопоказаний к операции показано скелетное вытяжение сроком на 6-12 недель.
Спица для скелетного вытяжения проводится через мыщелки бедра или бугристость большеберцовой кости. Больного укладывают на щит, поврежденную ногу кладут на шину Белера. Величина груза при переломе бедра определяется уровнем перелома характером смещения.
Груз может быть увеличен у молодых пациентов с хорошо развитыми мышцами. Средняя величина груза в начале лечения – около 10 кг. По мере устранения смещения груз уменьшают. После снятия вытяжения на поврежденную конечность накладывают гипсовую повязку на срок до 4 месяцев.
При консервативном лечении коленный и тазобедренный сустав долгое время остаются неподвижными. Оперативное лечение позволяет увеличить подвижность пациента и предупредить развитие контрактур.
Операцию проводят после нормализации состояния больного. Остеосинтез выполняют, используя пластины, штифты и стержни.
ОТКРЫТЫЕ ДИАФИЗАРНЫЕ И МЕТАФИЗАРНЫЕ ПЕРЕЛОМЫ, ОСЛОЖНЕННЫЕ ИНФЕКЦИЕЙ
ГЛАВА IV
Клиническое течение открытых переломов зависит от общего состояния больного, его возраста, состояния нервной и сердечно-сосудистой систем, реактивности и приспособительно-компенсаторных возможностей организма.
У больных, перенесших тяжелый шок, при большой кровопотере, а также у пожилых людей повышен риск развития инфекции и других осложнений. Опасность осложнений при открытых переломах с обширными и загрязненными ранами большая, чем при открытых переломах с небольшими и средней величины ранами. По данным А. В. Каплана и О. Н. Марковой, при открытом переломе типа IA осложнений не наблюдалось; количество их возрастало соответственно тяжести травмы: IБ – 2%, IIБ – 4,9%, IIВ –
18,3%, IIIБ – 42,4%, IIIB – 50,9%, IV – 63,9%. Течение открытых переломов во многом зависит от локализации повреждений. По-разному протекают открытые диафизарные, околосуставные и внутрисуставные переломы бедра, голени, плеча и предплечья.
Открытые переломы костей верхней конечности протекают обычно более гладко и с меньшим числом осложнений, чем открытые переломы нижних конечностей, что в первую очередь связано с лучшими условиями кровообращения плеча и предплечья по сравнению с бедром и голенью, меньшим микробным загрязнением кожи верхних конечностей.
Особенно пристального наблюдения требуют больные с открытыми переломами в первые 5-10 дней после травмы, когда имеется угроза развития аэробной и анаэробной инфекции.
Мы (А. В. Каплан, О. Н. Маркова, 1975) различаем следующие виды клинического течения открытых переломов.
Асептическое течение по типу закрытых переломов. Для развития инфекции в кости в зависимости от разных условий требуется от 2 до 8 нед. «Травматический остеомиелит» обычно с самого начала, а иногда после подострой стадии принимает хроническую форму. Из всех тканей человеческого организма кость наиболее подвержена хронической инфекции при открытой травме.
Благодаря комплексному лечению в настоящее время у преобладающего большинства больных с открытыми переломами инфекция не развивается и процесс сращения протекает без осложнений или со сравнительно легкими осложнениями. Так протекают переломы с заживлением раны первичным натяжением, сюда могут быть отнесены открытые переломы с ограниченным поверхностным нагноением или краевым некрозом кожи, которые чаще наблюдаются на передней поверхности голени. Участок некротизированной ткани не следует насильно удалять,- обычно он сам медленно, в течение 2-4 нед, отторгается. За этот срок под сухим некрозом кожи образуется грануляционная ткань, которая часто служит хорошим барьером проникновению инфекции в зону перелома. Рана постепенно эпителизируется с краев; при задержке эпителизации следует прибегать к свободной пересадке кожи. Кожная пластика должна производиться в ранние сроки после отторжения некроза кожи. У некоторых больных нагноительный процесс носит поверхностный характер или ограничивается пределами мягких тканей; обычно такая рана скоро закрывается.
Псевдоасептическое течение со скрытым периодом развития инфекционного осложнения. Вначале (первые дни) перелом протекает по типу закрытого. В дальнейшем, иногда в ближайшие дни или в более позднем периоде, отмечается прогрессирующее нарастание симптомов, указывающих на ухудшение состояния: нарушаются аппетит и
сон, повышается температура, увеличиваются лейкоцитоз, СОЭ; местно определяется отек. При снятии швов и раздвигании краев раны из глубины выделяется гной, видны серые участки некротизированной ткани. В обоих случаях при раннем выявлении развивающейся инфекции и принятии необходимых мер удается вскоре купировать процесс и изменить его течение в благоприятном направлении. В других случаях, особенно при запоздалой диагностике, процесс прогрессирует, иногда протекает бурно и стихание его происходит лишь в более поздний период.
Острое течение с бурным развитием в первые дни воспалительного процесса в области открытого перелома. Состояние сразу становится тяжелым. Больной жалуется на боли в поврежденной конечности, слабость, плохой аппетит и сон. Отмечаются бледность кожных покровов, анемия, повышение температуры тела и интоксикация. Необходимо своевременно широко раскрыть рану, рассечь отечные ткани, вскрыть гнойные затеки и карманы, удалить некротизированные ткани и создать условия для постоянного оттока отделяемого из ран. В крайне тяжелых случаях приходится даже ампутировать конечность. Нужно принять меры, направленные на улучшение общего состояния больного, поднятие реактивности и иммунологических свойств организма, усилить борьбу с инфекцией и интоксикацией путем внутривенного введения раствора глюкозы, раствора Рингера, изотонического раствора хлорида натрия с добавлением гемодеза, полиглюкина, реополиглюкина, антибактериальной сыворотки, переливания крови, соответствующих антибиотиков и другие меры.
При глубоком нагноении обычно развивается остеомиелит. Спешить с удалением металлического стержня или другого фиксатора в остром периоде следует не всегда, так как неподвижность отломков после удаления фиксаторов нарушается, что ведет к лишней травматизации тканей и распространению инфекции. Однако чрезмерно длительное оставление обнаженных фиксаторов в гнойной ране также имеет свои пределы. При значительной интоксикации могут возникнуть показания к более широкому раскрытию раны, вскрытию гнойных затеков, срочному, удалению металлических конструкций и созданию условий для свободного оттока гноя. В большинстве случаев для обездвижения отломков следует наложить гипсовую повязку или компрессионный аппарат и удалить металлический фиксатор.
Ухудшение состояния, интоксикация, высокая температура, частый пульс, боли, в особенности распирающего характера, нарастание отека, краснота, соответствующие изменения крови и другие симптомы должны вызвать опасение за жизнь больного, мысль о развитии анаэробной инфекции, сепсисе и других тяжелых осложнениях. В этих случаях не следует ограничиваться только пассивным наблюдением и протоколированием в истории болезни картины нарастающего ухудшения состояния больного. Когда стоит вопрос о сохранении жизни и этого нельзя достичь щадящими методами (рассечение ран, некрэктомия, вскрытие затеков и др.), нужно пожертвовать конечностью и своевременно произвести вторичную ампутацию.
Подострое или хроническое течение инфекционного осложненного открытого перелома с выраженной клинической картиной тяжелой интоксикации (токсемия, сепсис, септикопиемия, раневое истощение), развившейся постепенно или после острого инфекционного осложнения (гнойное, гнилостное, анаэробное).
Состояние больного обычно тяжелое или очень тяжелое. В таких случаях речь идет о спасении жизни и нужно своевременно ампутировать конечность.
Хроническое течение с самого начала, медленно развивающееся или стабилизировавшееся после остро или подостро протекающего инфекционного процесса. У части больных имеются свищи, секвестры и концевой остеомиелит. Общее состояние обычно удовлетворительное, явления интоксикации не выражены. Только раннее выявление и последующее рациональное лечение позволяют купировать инфекционный процесс в ранних стадиях и предотвращают возникновение тяжелых осложнений, угрожающих жизни, приводящих к ампутации конечности или инвалидизации в связи с
тяжелыми инфекционными, трофическими, ишемическими и иными поражениями конечности.
Помимо инфекционных осложнений, связанных с травмой, недостаточностью первичной обработки и обездвижения отломков, инфекция может развиться в результате вторичного инфицирования, которое в значительной степени обусловлено существующей
внастоящее время проблемой госпитализма. Вторичное инфицирование раны происходит при перевязках в результате попадания в нее микробов из воздуха, с рук и из носоглотки медицинского персонала, от больных с инфекционными осложнениями, с больничного белья и одежды. Основным источником госпитальной инфекции являются больные с гнойными ранами, свищами и другими открытыми очагами инфекции. Происходит постоянный обмен, особенно антибиотикоустойчивыми штаммами микробов, между больными, обслуживающим персоналом и окружающими предметами (В. И. Мельникова, 1970).
Борьба с госпитализмом в настоящее время является исключительно актуальной и сложной, поэтому она должна проводиться решительно и постоянно. Прежде всего следует безукоризненно соблюдать правила хирургической асептики не только в операционных, но и в перевязочных и палатах.
Выбор рационального, эффективного лечения и правильное прогнозирование при инфицированных открытых переломах в большей степени зависит от правильной оценки вида инфекционного осложнения, определения распространенности процесса, особенности течения его и учета общего состояния больного.
Заживление открытых переломов с небольшими поверхностными ранами и незначительным отделяемым, а также переломов, осложненных ограниченным некрозом кожи на небольшом участке, мало отличается от заживления неосложненных открытых переломов.
При открытых диафизарных переломах с большими гранулирующими ранами производят в ранние сроки после травмы отсроченную или вторичную кожную пластику. Наличие гнойного отделяемого и патогенной микрофлоры в ране является противопоказанием к кожной пластике, если пересадка аутокожи произведена мелкими лоскутами по методу Тирша или Янович-Чаинского. Обширные раны, как правило, заживают в течение 3-4 нед после пластики.
При обширных инфицированных ранах с наличием некротизированных тканей, гнойных затеков и прогрессировании патологического процесса у больных, находящихся
втяжелом состоянии, конечности угрожает ампутация уже в ранние сроки после травмы в связи с развитием тяжелой гнойной, гнилостной или анаэробной инфекции. Чаще это больные с открытыми переломами типа IIB, IIIB или IV.
При осложнениях открытых диафизарных переломов тяжелыми инфекционными процессами необходимо на основании клинических, лабораторных и рентгенологических данных в максимально короткий срок оценить общее состояние больного, уточнить характер и тяжесть осложнения и определить прогноз в смысле возможности сохранить жизнь и конечность. В зависимости от этого следует наметить наиболее рациональный план лечения больного.
Хирургический метод лечения. Основываясь на опыте Великой Отечественной войны, А. В. Каплан (1948), И. Л. Крупко (1954, 1956), А. Н. Беркутов (1960) и др. для предупреждения тяжелого течения открытых инфицированных переломов при наличии в ране мертвых тканей рекомендуют производить позднюю и повторную хирургическую обработку раны. Она заключается в широком раскрытии раны, тщательном иссечении и удалении всех мертвых тканей и свободных костных отломков. Если ранее был произведен остеосинтез – фиксатор не удаляется (Н. Е. Махсон, 1977). При смещенных отломках их репонируют и производят остеосинтез спицами, реже другими фиксаторами. Рану промывают антисептиками и подвергают вакуумированию. Местно вводят антибиотики и протеолитические ферменты. Отток раневого отделяемого обеспечивают
дренированием и контрапертурами. При гладком течении накладывают отсроченные швы. Если условия позволяют, рану можно сразу зашивать и установить длительное (постоянное или прерывистое) промывание антисептиками с отсасыванием жидкости тонкими полиэтиленовыми трубками, проведенными вглубь раны через узкие отверстия в коже, которые плотно охватывают трубки. Можно использовать отсасывающие аппараты. Иммобилизация конечности осуществляется обычными способами. Своевременное применение этого метода может прервать нагноительный процесс.
Вторичная ампутация конечности. Благодаря современным методам лечения открытых переломов (первичная хирургическая обработка раны, хорошая репозиция и фиксация отломков, антибиотикотерапия) вторичные ампутации производятся в исключительных случаях. Лишь при тяжелой токсемии от распространения инфекции, вторичном кровотечении из своевременно нераспознанного повреждения магистрального сосуда, гангрене конечности в результате тромбоза сосудов и тяжелых формах газовой гангрены для спасения жизни показана вторичная ампутация конечности.
Развитие инфекции в кости имеет свои особенности, обусловленные специфической структурой ее, наличием минерального компонента, образующегося на коллагеновой основе, в которой заключены живые элементы кости (остеоциты, сосуды и др.). Наряду с этим структурное строение в различных областях трубчатой кости неодинаково. Так, строение диафиза существенно отличается от метаэпифизарной части. Сами элементы кости отличаются не только своей структурой, но и особенностями кровоснабжения, сопротивляемости механическим, инфекционным, токсическим и иным воздействиям, реактивностью и потенциальной возможностью к репаративной регенерации.
При воспалительном процессе сдавливаются и тромбируются внутрикостные сосуды, нарушается жизнеспособность костных клеток и лишенная кровоснабжения зона кости некротизируется.
Ограниченные небольшие участки некротизированной кости часто незаметно выделяются вместе с гноем либо частично или полностью распадаются, рассасываются. Более значительные секвестры, образующиеся в диафизе вследствие незначительной васкуляризации из периоста, приходится удалять хирургическим путем.
Вметафизах губчатой кости секвестры образуются медленно, в течение долгого времени четко не отграничиваются, и поэтому операция требует большой тщательности и осторожности.
Внастоящее время возбудителем травматического остеомиелита обычно является стафилококк, а не стрептококк. В ряде случаев возбудителями оказываются и другие микроорганизмы (синегнойная палочка, протей, кишечная палочка и др., рассматривавшиеся ранее как непатогенные или условно-патогенные микробы), часто мультирезистентные к антибиотикам, а также анаэробы.
На основании клинического опыта мы (А. В. Каплан, О. Н. Маркова, 1967) выделяем следующие формы диафизарного и метаэпифизарного травматического остеомиелита как осложнения после открытых диафизарных переломов длинных трубчатых костей: 1) остеомиелит со свободно лежащими осколками кости (первично нежизнеспособные мелкие секвестры), правильнее – первичный некроз кости; 2) ограниченный краевой (пристеночный) остеомиелит без секвестров; 3) концевой остеомиелит фрагментов поврежденной кости на ограниченном участке; 4) концевой остеомиелит одного из фрагментов с возникновением крупных полуцилиндрических или цилиндрических секвестров; 5) концевой остеомиелит обоих отломков кости на ограниченном участке, 6) остеомиелит концов обоих отломков с образованием массивных секвестров; 7) остеомиелит на значительном протяжении кости (диафиза и метафиза) с образованием вторичных секвестров за счет распространения воспалительного процесса.
Возникновение особенно тяжелых и обширных остеомиелитов при открытых диафизарных переломах длинных трубчатых костей с размозжением мягких тканей наблюдается чаще после остеосинтеза погружными металлическими конструкциями,
произведенного в момент первичной хирургической обработки. Металлические штифты и пластинки обеспечивают большую или меньшую неподвижность отломков, но применение их во время первичной хирургической обработки открытого перелома ухудшает условия гемодинамики на его уровне, так как при этом методе, помимо травматического повреждения питающих кость сосудов, кровообращение кости еще больше ухудшается за счет повреждения сосудов при отслойке надкостницы или разрушении костного мозга при остеосинтезе.
Хронический инфекционный процесс в кости, даже в виде ограниченного остеомиелитического очага, трудно поддается лечению, требует много времени и усилий, чтобы избежать инвалидности и возвратить больного к труду.
Лечение. Лечение остеомиелита должно проводиться комплексно. Секвестрэктомия является типичной операцией при лечении хронического остеомиелита. Она включат не только удаление секвестров, но и полную санацию секвестральной полости с удалением всех грануляций, обработкой стенок и дна полости растворами антисептиков (спирт, фурацилин, 10% спиртовой раствор йода и др.). Операцию можно считать успешно законченной только тогда, когда санированная, со здоровыми жизнеспособными стенками секвестральная полость превращена в отлогий желоб, который полностью заполнен пластическим материалом (мышца на питающей ножке, в соответствующих случаях – измельченный консервированный аллохрящ, реже измельченная аутоили, еще реже, консервированная аллокость или другие биологические ткани, которые имеют определенные преимущества по сравнению с небиологическими материалами).
В. А. Чернавский и Б. М. Миразимов (1967), Н. М. Шаматов, Ш. Ш. Хамраев и Т. И. Кретова (1967) при операциях по поводу подострого и хронического остеомиелита стали использовать вакуум-аппарат и производить пломбировку секвестральной полости измельченным консервированным хрящом. Вакуумирование способствует удалению всех некротических тканей из костной полости, что создает неблагоприятные условия для жизнедеятельности микрофлоры и значительно уменьшает микробную загрязненность раны. Вакуумирование также позволяет хорошо очистить свищевые ходы, размягчает рубцовую ткань, улучшает кровоснабжение тканей. После вакуумирования рану зашивают наглухо.
Успех операции секвестрэктомии во многом зависит также от раннего и полного закрытия кожной раны. Для закрытия значительных дефектов кожи можно рекомендовать кожную аутопластику мостовидным лоскутом с двумя питающими ножками; при отсутствии условий для ее проведения возможна пластика свободным полнослойным перфорированным лоскутом аутокожи. А. К. Тычинкина (1962) рекомендовала заготовить лоскут на противоположной конечности и закрыть им после операции кожный дефект.
Н. М. Шаматов, Ш. Ш. Хамраев и Т. И. Кретова (1967) дефект кожи после секвестрэктомии закрывали лоскутами консервированной аллокожи. Мы по предложению С. С. Фейгельмана (1973) временно закрываем обнаженную кость формалинизированной кожей, под которой кость покрывается грануляциями.
Для гладкого заживления раны после секвестрэктомии имеет большое значение свободный отток отделяемого из глубины раны. Закрывая полностью операционную рану с целью профилактики вторичного инфицирования кости, следует делать контрапертуры на задней или боковой поверхности конечности.
Иммобилизацию конечности при открытых инфицированных переломах лучше всего осуществить компрессионно-дистракционным аппаратом (рис. 11). Если имеются общие противопоказания или местные условия (затеки, локализация перелома и ран, обширность их, сильное гноетечение и т. д.), неблагоприятные для наложения аппарата, временно или для постоянного лечения накладывают гипсовую повязку (мостовидная или лонгетноциркулярная с окнами). Гипсовая повязка используется также для лечения переломов без смещений или при устойчивых, хорошо репонированных переломах.
Общее лечение инфицированных открытых переломов при соответствующих показаниях следует сочетать с направленной антибиотикотерапией, проводимой после определения чувствительности микрофлоры ран к ряду антибиотиков.
При наличии стойкой устойчивости ассоциаций микробов к отдельным антибиотикам следует прибегать к комбинированному лечению несколькими синергично действующими антибиотиками, комбинируя различные пути введения (местно и внутримышечно; парентерально и перорально), сочетая антибиотики с сульфаниламидами (главным образом продленного действия) и нитрофуранами. При выборе сочетаний антибиотиков надо исходить из механизма их действия и комбинировать только те антибиотики, действие которых при таком применении усиливается и создается синертический эффект.
Наиболее эффективными являются следующие сочетания: пенициллины (включая полисинтетические) + мовомицин, певициллин + стрептомицин, пенициллин + канамицин, мономицин + олеандомицин, тетрациклины + эритромицин, тетрациклины + олеандомицин, тетрациклины + новобиоцин, линкомицин + мономицин, линкомицин + тетрациклины и многие другие. Хорошо зарекомендовал себя гентамицин.
Необходимо сохранение резерва антибиотиков (антибиотики «запаса»), к которым микрофлора даже гнойных ран продолжает оставаться более чувствительной.
При стафилококковой инфекции мягких тканей и стафилококковом сепсисе весьма Эффективны (при чувствительности к ним стафилококков) полусинтетические пенициллины, макролиды и ристомицин.
Антибиотики широкого спектра действия, такие, как мономицин, морфоциклин, гликоциклин и некоторые комплексные антибиотики типа тетраолеана, следует оставлять для лечения больных со смешанной инфекцией.
По данным В. М. Мельниковой и О. Н. Марковой (1975), при подостром остеомиелите монокультура стафилококка встречается только у 1/3 больных: у 2/3 – появляются ассоциации из двух и трех микробов.
При хроническом остеомиелите в состав ассоциаций, как правило, входит уже 4-5 видов микробов. В ассоциациях появляются кишечная палочка, энтерококк, протей, синегнойная «палочка и другие микробы, причем добиться исчезновения из ассоциаций протея и синегнойной палочки весьма трудно. Основным микробом костной раны, естественно, является стафилококк. Если в ранний период остеомиелита микрофлора ран и свищей чувствительна ко многим антибиотикам, то в хронический период из глубины свищевых ходов высеваются ассоциации микробов, устойчивые почти ко всем применяемым антибиотикам.
О. Н. Маркова и В. М. Мельникова (1975) рекомендуют применение линкомицина как при острой, так и при хронической стафилококковой инфекции костной ткани. Если микрофлора чувствительна к пенициллину или тетрациклину, начинать лечение надо с этих антибиотиков, а затем назначать макролиды или полусинтетические пенициллины (метициллин, оксациллин) и только при устойчивости стафилококка к этим препаратам применять линкомицин.
Учитывая способность линкомицина действовать внутри костной ткани, целесообразно ограничить его применение в других случаях, оставив его в резерве как наиболее ценный препарат для лечения стафилококковых поражений костей и суставов. Однако и при инфекции костей и суставов не следует назначать линкомицин без особых показаний, чтобы как можно дольше сохранить чувствительность микрофлоры к этому ценному антибиотику.

Рис. 11. Открытый косой перелом в нижней трети правой голени, осложненный остеомиелитом (свищевая форма).
а – через 3 мес после травмы – положение отломков в гипсовой повязке после лечения; б – лечение аппаратом Илизарова; в – через 5 мес консолидация: состояние после
снятия аппарата.
Показанием к проведению регионарной перфузии могут быть только крайне тяжелые, не поддающиеся лечению другими методами острые и хронические свищевые формы остеомиелита. И. Л. Крупко (1965) считает, что особенно показана перфузия больным, у которых безуспешно проводились многократные оперативные вмешательства, но свищевые ходы с нечувствительной к антибиотикам флорой не поддаются ни оперативному, ни консервативному лечению. Перфузия позволяет создать в конечности с изолированным кровообращением сверхвысокую концентрацию антибиотиков при высоком насыщении крови кислородом, витаминами, гормонами и антикоагулянтами.
Клинические наблюдения (П. А. Куприянов, И. Л. Крупко, М. Н. Фаршатов, 1959, 1962, 1965), показали, что перфузия редко может быть использована как самостоятельный лечебный метод. Чаще она должна сочетаться с оперативными вмешательствами, главным образом радикальной секвестрэктомией.
Метод перфузии нельзя относить к числу простых и безопасных, поэтому он применяется при наиболее тяжелых формах остеомиелита и только в высококвалифицированных научно-исследовательских учреждениях. В тяжелых случаях применяют внутриаортальное введение через тонкий постоянный катетер антибиотиков и антисептических средств (Н. Е. Махсон, 1978).
У больных с повышенной чувствительностью к антибиотикам вместе с антибиотиками следует назначать антигистаминные препараты (димедрол, супрастин, пипольфен и др.), а в случае необходимости полностью отменить антибиотики и перейти к лечению сульфаниламидами или нитрофурановыми препаратами. У ослабленных больных при длительном лечении антибиотиками профилактически следует применять противогрибковые препараты – нистатин, леворин и др. (О. Н. Маркова, В. М. Мельникова, 1975).
Для повышения эффективности терапии, особенно у ослабленных больных, введение антибиотиков следует сочетать со средствами, стимулирующими реактивность организма и способствующими борьбе с инфекцией, а именно: дробные переливания крови, витаминотерапия (А, В, С, D), введение продигиозана, вакцин, сывороток, стафилококкового анатоксина, антистафилококковой плазмы, алоэ, стекловидного тела, АТФ и других препаратов. При антибиотикотерапии инфекций, особенно септического характера, когда в организме создается дефицит гамма-глобулина, следует вводить гаммаглобулин (по 0,5-2 мл/кг, желательно внутривенно однократно или несколько раз). Назначают также внутривенное вливание изотонического раствора хлорида натрия, глюкозы, а также проводят противоинтоксикационную терапию (гемодез и др.).
На современном этапе местное лечение гнойно-некротических ран немыслимо без применения протеолитических ферментов, представляющих собой биологически активные препараты. В. И. Стручков (1967), много лет изучавший действие протеолитических ферментов, рекомендует использовать их при лечении нагноившихся ран, флегмон мягких тканей и остеомиелита. Для лечения гнойно-воспалительных заболеваний конечностей применяют в настоящее время следующие протеолитические ферменты: трипсин, химотрипсин, химопсин, плазмин, стрептокиназу, бактериальную дезоксирибонуклеазу и другие ферменты, в том числе комбинированные препараты. Основное терапевтическое действие ферментных препаратов основано на их протеолитическом, противовоспалительном, антикоагуляционном и детидратационном свойствах. Ферменты могут также расщеплять пенициллиназу и некоторые бактериальные токсины. При этом они не тормозят рост грануляций и эпителизацию ран (Н. Ф. Камаев, 1962; В. И. Стручков и др., 1970).
Комплексное использование стафилококкового анатоксина с антибиотиками, разработанное И. В. Руфановым с сотр. (1964), применяемое с лечебной целью при инфицированных стафилококком открытых переломах И. А. Мовшовичем и соавт. (1969), оказалось также весьма эффективным даже у тяжелобольных. Стафилококковый анатоксин следует комбинировать с теми антибиотиками, к которым выявлена наибольшая чувствительность микробов, что не только позволяет повысить иммунитет и снизить сенсибилизацию организма, но и надежно подавляет развитие возбудителя инфекции.
Несмотря на определенные достижения, лечение травматических остеомиелитов до настоящего времени представляет исключительно большие трудности. Некоторые больные многократно и безуспешно подвергаются операции и комплексному лечению, а процесс в кости рецидивирует.
Диафизарные переломы костей голени
Лечение диафизарных переломов костей голени остается одной из важнейших проблем травматологии. По данным НИИСП им. Н. В. Склифосовского, они составляют до 14% от всех травм опорно-двигательного аппарата.Временная нетрудоспособность пострадавших с диафизарными переломами голени колеблется в широких пределах: от 3—4 мес при изолированных переломах больше-берцовой кости без смещения до 5—7 мес при переломах со смещением, иногда достигает 9—10 мес. Процент первичного выхода на инвалидность в результате диафизарных переломов голени составляет от 5,1 до 39,9. В структуре инвалидности переломы голени также занимают ведущее место и составляют от 7 до 37,6% от всех травм опорно-двигательного аппарата.
Длительная нетрудоспособность и высокий процент первичного выхода на инвалидность можно объяснить большим количеством осложнений, которые встречаются как при оперативном лечении, так и при классических консервативных способах. Все это в значительной мере обусловлено анатомическими особенностями голени. Большеберцовая кость является основной опорной костью, от целости которой в основном зависит функции голени. Кость расположена эксцентрично и соединена с малоберцовой костью плотной межкостной мембраной, играющей существенную роль в характере смещения отломков. Мышцы расположены по задней и наружной поверхностям и прикрепляются на уровне верхней и средней третей голени, на нижней трети прикрепления мышц нет. Передневнутренняя поверхность голени мышц не имеет. Отсутствием мышечного футляра можно объяснить сравнительно большее количество отломков, переломов со смещением в нижней трети по сравнению с переломами в верхней трети.
По данным НИИСП им. Н. В. Склифосовского, переломы в средней трети голени составили 55,7%, в нижней трети — 38,9%, в верхней трети — 4,5%, двойные — 0,9%. Смещение отломков по ширине при переломе обеих конечностей зависит от направления внешней силы. Смещение в сторону в зависимости от механизма его возникновения не может быть типичным, однако вследствие эластической ретракции мышц при прочих равных условиях периферический отломок имеет тенденцию к смещению кпереди и внутрь. Ретракция мышц вызывает угловое смещение, а при наличии бокового смещения — и по длине. Угловое смещение вследствие эластической ретракции мышц и силы тяжести 368 чаще всего наблюдается под углом, открытым кнаружи. Смещение отломков при косых и винтообразных переломах зависит от направления плоскости излома.
Переломы голени возможны от прямого воздействия, при этом возникают поперечные и оскольчатые переломы одной или обеих костей. От непрямого воздействия при вращении тела с фиксированной стопой возникают винтообразные переломы обеих костей голени, реже — одной большеберцовой. Винтообразные переломы являются наиболее распространенными и составляют в среднем 40% от числа других видов переломов голени.
Диафизарные переломы голени часто сопровождаются смещением отломков (80% случаев). Отломки вправляются с трудом, после вправления нередко наступает вторичное смещение.
Диагностика переломов обеих костей голени или только большеберцовой не представляет трудностей. Болыпеберцовая кость на всем протяжении по передневнутренней поверхности покрыта кожей без мышц и легко может быть пальпирована. При пальпации следует выявить локальную болезненность, а при внимательном осмотре иногда можно определить и характер линии перелома. В случае переломов обеих костей голени четко определяются деформация, крепитация, подвижность костных отломков.
Изолированный перелом малоберцовой кости для диагностики труден, особенно в верхней трети, где много мышц. Единственным признаком перелома является болезненность при пальпации. Если диагноз вызывает сомнение, то при оказании первой помощи надо поступать, как при переломе.
Для уточнения диагноза необходимо получить рентгеновский снимок в двух проекциях. При наличии винтообразного перелома большеберцовой кости в нижней трети следует проверить состояние малоберцовой кости в средней и нижней третях и убедиться в отсутствии перелома ее, поэтому надо сделать рентгенограмму всего сегмента голени.
Лечение диафизарных переломов обеих костей голени независимо от локализации не имеет принципиальных различий. Эти переломы всегда сопровождаются смещением костных отломков, поэтому при поступлении больного в стационар целесообразно применить постоянно скелетное вытяжение.
Постоянное вытяжение может быть самостоятельным методом лечения или комбинированным с последующим применением гипсовой повязки или оперативного лечения. В период лечения больного на вытяжении надо убедиться в возможности репозиции перелома, интерпозиции тканей, состоянии кожи мягких тканей поврежденной конечности, оценить общее состояние больного для определения последующей тактики лечения. В зависимости от опыта врача можно, минуя постоянное вытяжение, применить тот или иной метод консервативного или оперативного лечения.
Постоянное вытяжение осуществляют на стандартной шине. Предварительно проводят анестезию места перелома: вводят в гематому 20—25 см3 2% раствора новокаина. В пяточную кость вводят спицу и натягивают скобой. Большое значение для репозиции перелома имеет создание ложа на шине для голени и бедра. Для этого на шину должны быть надеты два гамачка с тесемками: один для голени, другой для бедра. Натягивать гамачок надо нетуго, чтобы создать ложе по форме икроножной мышцы. Изменяя натяжение гамачка, можно придать различное положение костным отломкам. В практике укоренилось бинтование шины марлевыми бинтами с целью создания ложа. Это неверно и недопустимо, так как теряется смысл возможности репозиции костных отломков с помощью гамачков.
Ногу укладывают на шину, стопу укрепляют в вертикальном положении: приклеивают клеолом на стопе бинт или надевают на подошву чулок-гамачок. Для вытяжения голени вешают груз 6—8 кг и через 20—30 мин репонируют перелом с учетом имеющегося смещения отломков. Продольная тяга осуществляется грузом за скобу, что ликвидирует смещение по длине и под углом. При поперечных переломах часто остается неликвидированным вальгусное положение, что в случае срастания перелома резко нарушает функцию суставов. В норме голень имеет некоторое искривление кнутри, т. е. варусное положение. Для ликвидации вальгусного положения применяют боковые тяги с помощью мягких колец или прибинтовывают пелот. Вальгусное положение можно исправить поворотом стопы кнутри и зафиксировать в этом положении стопу на специальной шине. Смещение костных отломков кпереди и кзади достигается натяжением гамачка.
После репозиции перелома уменьшают груз до 3—5 кг, что достаточно для удержания отломков в правильном положении. Затем делают контрольный рентгеновский снимок. В течение первых 3 нед необходимо ежедневно контролировать положение ноги на шине и возможность возникновения вторичных смещений костных отломков. Контроль осуществляет весь медицинский персонал, имеющий отношение к лечению больного, и сам больной. Если больной не может контролировать положение ноги на скелетном вытяжении, то лечение этим методом бессмысленно.
Клиническим контролем срастания голени является возможность активно поднять голень при снятом грузе, при этом больной не должен ощущать болей в области перелома. Перелом голени срастается при нормальном течении репаративного процесса через 1,5— 2 мес. Этот срок является сроком клинического срастания, когда образуется только периостальная мозоль, достаточная, чтобы больной ходил с костылями, осуществляя дозированную нагрузку на ногу. После того как снято вытяжение, больной ходит с костылями еще 1,5—2 мес, касаясь пола поврежденной ногой и постепенно увеличивая нагрузку. Затем такой же срок ходит с палочкой. Лечение перелома костей голени постоянным вытяжением занимает 5—6 мес. Постоянное вытяжение необходимо с первых дней сочетать с лечебной гимнастикой, которая заключается в активных движениях стопой, пальцами и напряжением мышц.
Метод постоянного вытяжения должен соответствовать следующим требованиям: обеспечить раннюю и удовлетворительную репозицию отломков, оптимальную тягу мышц, исключить ретракцию мышц в патологическом положении костных отломков, своевременно предупредить и устранить ущемление мягких тканей между отломками, обеспечить надежную консолидацию костных отломков, сохранить физиологический тонус мышц поврежденной конечности и функцию близлежащих суставов, поддержать тонус всего организма.
Сложности в выполнении указанных требований скелетного вытяжения связаны прежде всего с несовершенством используемого оборудования — единственной выпускаемой промышленностью стандартной шины Белера для лечения переломов голени. Эта шина выпускается одного размера с постоянными тазобедренным и коленным углами, что не позволяет во многих случаях обеспечить положение покоя и расслабления мышц. Роликовые блоки, которыми оснащена шина Белера, плохо вращаются, из-за чего теряется часть тяги. Увеличивают массу груза, требуемого для репозиции отломков, и применяемые для его подвески матерчатые шнуры вместо капроновой лески. Использование детально разработанной системы демпферного скелетного вытяжения позволяет уменьшить груз для репозиции. Отпала необходимость подъема ножного конца кровати для противотяги, что привело к снижению летальности в группе пожилых больных от обострения сопутствующих сердечно-легочных заболеваний.
Многие авторы подчеркивают, что стандартная шина Белера имеет весьма ограниченные возможности репозиции отломков и их стабилизации в процессе лечения.
Для устранения смещений под углом во фронтальной плоскости, как и для устранения смещений по ширине, стандартная шина Белера приспособлений не имеет. Наиболее часто для устранения этих видов смещения применяют ватно-марлевые петли с грузами, прижимные пелоты и т. д. Эти способы репозиции нефизиологичны, так как в результате длительного давления петель и пелотов на голень нарушается местное кровообращение, развивается отек конечности с явлениями хронической венозной недостаточности, постоянное давление на мягкие ткани, сосуды, нервы может привести к их повреждению. Более совершенным способом устранения смещений по ширине и варусно-вальгусных деформаций является боковое демпферированное скелетное вытяжение. Оно осуществляется двумя штыкообразно изогнутыми спицами, проведенными навстречу друг другу вблизи места перелома; за эти спицы через демпферные пружины производится скелетное вытяжение.
Отрицательными сторонами метода следует считать дополнительную травматизацию мягких тканей и потенциальную возможность инфицирования области перелома. Для устранил ротационного смещения периферического отломка болыпеберцовой кости и его стабилизации на шине Белера существует множество приспособлений, большая часть которых сводится к подвешиванию натянутой в скобе спицы к поперечной перекладине шины Белера или ее модификаций. Для этой цели используют полоски бинта, пружины, капроновые нити и т. д., снабженные тем или иным механизмом для регулирования их длины и, следовательно, коррекции ротационного смещения. Можно устранять ротационное смещение прикреплением к стопе специального подстопника, который в свою очередь подвешивается к поперечной перекладине шины Белера.
Наиболее совершенной для репозиции и стабилизации отломков в достигнутом положении является созданная в НИЙСП им. Н. В. Склифосовского специальная шина для лечения переломов голени. Эта шина позволяет устранить укорочение, угловые и ротационные смещения, а также стабилизировать дистальный отломок в достигнутом положении.
Лечение переломов костей голени на шине осуществляется следующим образом. После обезболивания области перелома, проведения спицы через пяточную кость и натяжения ее в скобе конечность укладывают на шину, предварительно затянутую гамачком. Спицу, натянутую в скобе, закрепляют в фиксаторах стоек, что придает дистальному костному отломку устойчивость при вытяжении. К скобе присоединяют демпферную пружину и шнур, который перекидывают через блок и на нем подвешивают необходимый для скелетного вытяжения груз. Уложив голень на шину, моделируют гамачок под голенью, причем гамачок должен заканчиваться на 2—3 см дистальнее области перелома голени. Такое положение конечности на шине обеспечивает возможность свободной манипуляции с периферическим отломком голени при репозиции.
Репозицию осуществляют следующим образом. Смещение по длине устраняют путем подбора груза на скелетном вытяжении. Опосредованное крепление периферического отломка голени на подвижной каретке, передвигающейся на шарикоподшипниках по направляющим, обеспечивает постоянство направления и плавность вытяжения отломков костей.
Устранение смещения отломков под углом в сагиттальной плоскости достигается регулировкой высоты штока: вращением гайки высоту штока увеличивают (для устранения угла, открытого кзади) или уменьшают (для устранения угла, открытого кпереди). Угловые смещения отломков во фронтальной плоскости устраняют приведением или отведением периферического отломка. Для этого изменяют положение поперечного стержня в горизонтальной плоскости. Изменением положения этого же стержня в вертикальной плоскости устраняют ротационные смещения периферического отломка.
Правильность положения отломков костей голени после репозиции контролируют по рентгенограммам. При необходимости устраняют остающиеся виды смещений.
Скелетное вытяжение осуществляют до образования первичной костной мозоли, после чего накладывают гипсовую повязку. Отрицательной чертой постоянного вытяжения при лечении переломов голени является длительный срок пребывания больного в лежачем положении. Для сокращения постельного режима возможно сочетание вытяжения с гипсовой иммобилизацией. Через 3—4 нед с момента травмы больного можно освободить от скелетного вытяжения и перевести на гипсовую повязку. К этому времени образуется первичная костная мозоль, т. е. происходит клиническое срастание перелома, и можно не опасаться вторичного смещения отломков.
Гипсовые повязки, наложенные на голень, могут быть классическими — от средней трети бедра до кончиков пальцев и укороченными, оставляющими свободным от фиксации смежный коленный сустав. Эти повязки получили название функциональных. Консервативное лечение проводят по следующим показаниям: при косых, оскольчатых, винтообразных и поперечных переломах голени, если в остром периоде устранены угловое, ротационное смещение и укорочение, смещение по ширине не превышает х/3 диаметра болыпеберцовой кости. Допустимы угловые смещения до 5°: при переломах без смещения; при закрытых и переведенных в закрытые открытых переломах голени со смещением и без смещения; при переломах на уровне нижней, средней и верхней третьей диафиза, а также при переломах дистального метаэпифиза.
Противопоказаниями являются: неустранимость углового, ротационного смещений, укорочения, полное смещение по ширине; интерпозиция мягких тканей; отсутствие контакта с больным. Угловые, ротационные смещения и укорочение обычно легко устраняются консервативными способами. Смещение по ширине трудно устранить полностью без операции. При условии, что перелом сросся, такое смещение не нарушает ни функции, ни косметики. Это же относится и к небольшим угловым деформациям. Следует подчеркнуть, что и в функциональном, и в косметическом отношении небольшой варус предпочтительнее вальгуса, а угол, открытый кпереди, — углу, открытому кзади.
Весь курс функционального лечения переломов голени можно разделить на 4 этапа.
I этап — период с момента поступления больного в стационар.
Первичная иммобилизация в остром периоде ничем не отличается от общепринятой методики.
При поступлении после рентгенографии производят анестезию места перелома 20—30 мл 2% раствора новокаина. Если перелом со смещением, то под местной анестезией проводят спицу через пяточную кость и налаживают скелетное вытяжение на стандартной шине.
При переломах без смещения после анестезии накладывают заднюю глубокую гипсовую лонгету до средней трети бедра, конечность укладывают в возвышенном положении. Иммобилизация гипсовой лонгетой может быть произведена и при стабильных переломах без укорочения после одномоментного устранения угловых и ротационных смещений.
Очень важно, чтобы ранний посттравматический отек полностью прошел. Если циркулярную повязку накладывают на отечную ногу, то через несколько дней неизбежно теряется плотность ее подгонки, между кожей голени и гипсом появляется пустота и отломки смещаются.
Недопустимо наложение циркулярной гипсовой повязки непосредственно после травмы. Нарастающий отек и гематома могут вызвать сдавление и некроз мягких тканей.
При переломах без смещения первичная иммобилизация проводится в течение 3—14 дней, при переломах со смещением — от 2 до 4 нед.
II этап — фиксация перелома циркулярной гипсовой повязкой.
1. Циркулярная гипсовая повязка с каблуком. На ногу от пальцев до нижней трети бедра надевают тонкий хлопчатобумажный чулок промышленного образца. Под среднюю треть бедра устанавливают упор и осуществляют продольную тягу за спицу со скобой с помощью ассистента или груза с силой, исключающей образование угла, открытого кпереди. Больному рекомендуют полностью расслабить мышцы голени и бедра, этому же способствует полусогнутое до 130—140° положение колена. Затем накладывают глубокую заднюю гипсовую лонгету толщиной в 8—10 слоев от конца пальцев до уровня бугристости большеберцовой кости. Спереди края лонгеты должны перекрыться. Повязку укрепляют циркулярными турами 2—3 гипсовых бинтов средней величины. При переломах нижней и средней третей голени верхний край повязки спереди заканчивается у нижнего полюса надколенника и полого спускается по бокам кзади до уровня бугристости большеберцовой кости, позволяя полный объем движений в коленном суставе.
До застывания гипса необходимо удерживать стопу под углом 90°, тщательно отмоделировать повязку над сводом стопы, областью- мыщелков большеберцовой кости и головки малоберцовой, областью лодыжек, передневнутренней поверхности большеберцовой кости. В верхней и средней третях голени повязку моделируют таким образом, чтобы ее поперечный срез приблизился по форме к треугольнику. Для этого нужно убрать упор из-под бедра, выпрямить колено и прижать влажную еще повязку к поверхности стола, поглаживая ладонями передние внутреннюю и наружную поверхности повязки на уровне верхней и средней третей; задняя поверхность повязки станет уплощенной. Такое моделирование создает большую ротационную стабильность. При переломах верхней трети голени повязку наращивают проксимально циркулярными турами гипсового бинта до уровня верхнего полюса надколенника (коленный сустав согут под углом 170°). Положение отломков контролируется рентгенологически. Затем удаляют скобу и спицу и к повязке пригипсовывают каблук с точкой опоры чуть кпереди от продольной оси большеберцовой кости. Когда гипс подсохнет, через 1—2 сут верхний край повязки, наложенной на голень, моделируют.
При лечении скелетным вытяжением часто не удается полностью устранить вальгусные деформации только тягой по оси. Целесообразность использования боковой тяги пелотом сомнительна, так как постоянное локальное давление может привести к некрозу мягких тканей. Можно рекомендовать одномоментную коррекцию оставшихся угловых смещений в момент наложения гипсовой повязки. После этого производят рентгенографию; повязка сохнет в течение 2 сут. В эти дни больной привыкает к вертикальному положению, сидит, свесив ноги, при отсутствии головокружения начинает ходить с костылями, не наступая на сломанную ногу.
Как только гипсовая повязка полностью высохнет, больному рекомендуют ходить при помощи двух костылей с дозированной нагрузкой на ногу. Величина нагрузки контролируется самим больным: он должен ориентироваться на болевые ощущения. Нагрузку увеличивают постепенно до болевого синдрома.
Через 3—5 дней ходьбы с нагрузкой следует сделать контрольную рентгенографию для выявления возможных вторичных смещений. Если появилось угловое смещение, то его можно исправить в этой же гипсовой повязке. Для этого гипс рассекают поперечно на уровне перелома на 3А периметра со стороны, куда открыт угол. Производят коррекцию деформации и в образовавшуюся щель вставляют гипсовый клин. Дополнительно повязку укрепляют циркулярными турами одного гипсового бинта. Повторяют рентгенографический контроль. После суточного перерыва осевая нагрузка возобновляется. Больного можно выписать из стационара сразу после наложения циркулярной гипсовой повязки с каблуком, если есть уверенность в том, что он самостоятельно выполнит нагрузочный режим. Пациент приходит на осмотр через неделю с контрольными рентгенограммами. В противном случае лучше обучить больного навыками ходьбы в стационаре.
При низких метафизарных и эпиметафизарных переломах циркулярная повязка с каблуком остается на весь период иммобилизации, в среднем до 2,5 мес со дня травмы. При прочих переломах повязку заменяют на «гильзу».
2. Циркулярная гипсовая повязка «гильза». На ногу надевают чулок и устанавливают подбедренный упор, как описано ранее. Пятка опирается на стол. На стопу от основания пальцев до уровня на 3—4 см выше суставной щели голеностопного сустава накладывают цинк-желатиновую повязку толщиной в 3—5 слоев мягкого марлевого бинта и в течение нескольких минут ей дают подсохнуть. Раскатывают гипсовую лонгету в форме усеченного конуса длиной от верхушки наружной лодыжки до нижнего полюса надколенника. На нижней узкой стороне лонгеты делают Т-образный разрез и накладывают ее на переднюю поверхность диафиза голени. Спереди край повязки (горизонтальная часть Т-образного разреза) располагается на 1,0—1,5 см выше уровня щели голеностопного сустава. Из боковых частей лонгеты формируют плотно прилегающие к лодыжкам накладки. Задний край повязки по уровню соответствует переднему. Лонгету фиксируют циркулярными турами 2—3 гипсовых бинтов средней величины. На область голеностопного сустава накладывают 8-образую повязку из мягкого марлевого бинта для точного моделирования нижнего края повязки по форме лодыжек и высыхания гипса в таком положении. Через 1—2 сут мягкий бинт снимают.
Гипсовая повязка «гильза» позволяет полный объем движений в коленном и голеностопном суставах. Эластичная цинк-желатиновая повязка, практически не затрудняя движений голеностопного сустава, сдерживает отек стопы. Кроме того, склеиваясь с гипсом, такая повязка в некоторой мере увеличивает стабильность положения «гильзы» на диафизе голени. При отсутствии пасты Уна эта часть повязки может быть выполнена из эластичного наголеностопника промышленного образца.
III этап — наложение циркулярной повязки «гильза» и ходьба с полной нагрузкой на ногу.
Повязку накладывают после того, как больной начал ходить в циркулярной повязке с каблуком с полной нагрузкой, не испытывая при этом болей в месте перелома. Такой навык больные приобретают обычно ко 2-му месяцу со дня травмы. Смена повязки возможна как в стационаре, так и в амбулаторных условиях. После снятия гипса проводится клинико-рентгенологический контроль сращения и положения отломков. Обычно к этому моменту патологической подвижности в месте перелома уже нет. Если выявляется ограниченная тугая подвижность, то после наложения «гильзы» следует повторить рентгенографию для оценки оси голени. При наличии выраженной безболезненной подвижности в месте перелома необходимо решать вопрос об оперативном лечении. Ходьбу с полной нагрузкой на ногу возобновляют через 1—2 дня, т. е. после высыхания повязки. Первые дни больному рекомендуют ходить осторожно, даже с костылями, чтобы дать возможность голеностопному суставу адаптироваться к внезапно возвращенной подвижности. После приобретения достаточных навыков и уверенности больные могут начать приступать на пятку и носок.
При косых, винтообразных и оскольчатых закрытых переломах иммобилизация продолжается в среднем до 2,5 мес со дня травмы. Сроки увеличивают на 2—3 нед при поперечных и открытых переломах, а также в случае, если при смене гипсовой повязки в месте перелома определялась подвижность и если больной длительное время ходил с костылями, не полностью нагружая ногу. Иммобилизация прекращается по достижении клинического сращения перелома: отсутствие патологической подвижности и болей при осевой и угловых нагрузках. На рентгенограммах линия перелома еще прослеживается. В целом при использовании повязки «гильза» врач не ограничен в сроках иммобилизации боязнью развития контрактур суставов. Больным она доставляет гораздо меньше неудобств, они могут ходить в обычной обуви. Чрезмерно затягивать иммобилизацию не рекомендуется, так как повязка, жестко ограничивая мышцы голени, препятствует окончательному восстановлению их массы и силы, не позволяет полностью разработать движения в голеностопном суставе.
В ряде случаев повязку «гильза» можно наложить сразу после периода первичной иммобилизации, минуя циркулярную гипсовую повязку с каблуком: при переломах верхней и средней третей без смещения, трещинах, стабильных изолированных переломах большеберцовой кости. Обычно 2-й период иммобилизации необходим. Исключение движений голеностопного сустава и, следовательно, движений мышц и сухожилий в зоне перелома создает большой комфорт, уменьшает болевые ощущения и больной может быстрее достигуть полной нагрузки на ногу при ходьбе.
IV этап — период окончательной реабилитации.
После снятия гипса проводится клинико-рентгенологический контроль. Если иммобилизация проведена без смены гипсовой повязки, то после ее снятия реабилитационные мероприятия направлены в основном на разработку движений в голеностопном суставе. Больным рекомендуют перейти на ходьбу при помощи костылей на 1—2 нед для адаптации сустава к подвижности, нагрузку на ногу при этом следует сохранить. Проводятся активная лечебная гимнастика, массаж, физиопроцедуры.
После прекращения иммобилизации «гильзой» объем движений голеностопного сустава составляет 70—80% от объема движений сустава интактной конечности. Больные могут ходить без дополнительной внешней опоры, часть из них практически не хромает и по сути не нуждается в какой-либо специальной реабилитации. Лица умственного, легкого физического труда и учащиеся иногда могут быть сразу выписаны на работу. У других больных реабилитация направлена прежде всего на восстановление силы мышц голени.
Функциональный метод лечения перелома голени укороченной гипсовой повязкой высокоэффективен и позволяет добиться выздоровления в среднем за 5 мес. Функциональная активность не препятствует, а, наоборот, способствует консолидации перелома. Ранняя осевая нагрузка, активные движения в коленном суставе улучшают кровообращение, практически исключают атрофию мышц и остеопороз, стойкие контрактуры суставов. Окончательная реабилитация не вызывает затруднений. Позднее введение осевой нагрузки, наоборот, ухудшает функциональные результаты.
Оперативное лечение
Показания для операции при переломах голени следующие: 1) консервативно невправимые переломы; 2) двойные переломы большеберцовой кости с большим смещением; 3) интерпозиция тканей; 4) опасность нарушения целости кожи костными отломками, сдавление периферических нервов и кровеносных сосудов; 5) открытые переломы.
Операцию при переломах обеих костей голени надо проводить только на большеберцовой кости, так как при восстановлении ее целости малоберцовая кость, как правило, срастается. Оперативное вправление отломков без дополнительной их фиксации на современном этапе недопустимо.
При диафизарных переломах голени в отличие от диафизарных переломов других локализаций остеосинтез большеберцовой кости с успехом можно выполнять всеми существующими в настоящее время фиксаторами: экстрамедуллярными (винты, болты, пластины), интрамедуллярными (стержни, штифты), в неочаговыми аппаратами (Илизарова, Калнберза, Волкова—Оганесяна и др.). Этому способствуют простота оперативных доступов и относительная легкость вправления костных отломков благодаря отсутствию мышечного слоя на передневнутренней поверхности большеберцовой кости. В литературе существует много мнений, доказывающих преимущество одного вида остеосинтеза перед другим. Спор этот беспредметный, поскольку при правильно проведенном остеосинтезе и отсутствии послеоперационных осложнений все методы позволяют восстановить нормальную функцию голени не ранее 4—5 мес. Результаты лечения зависят не только от метода остеосинтеза, но и от профессиональных навыков и умения врача.
Преимущество надо отдавать тому виду остеосинтеза, который, во-первых, является менее травматичным, а также удобным для больного в послеоперационном периоде; во-вторых, дает возможность оставить больного в послеоперационном периоде без внешней гипсовой фиксации, начать раннюю нагрузку на конечность и обеспечить движения в крупных суставах.
Остеосинтез большеберцовой кости металлическими винтами или болтами удобен при винтообразных переломах с длинной линией излома. Метод прост, позволяет достигнуть хорошего сопоставления костных отломков и неподвижности их. В послеоперационном периоде следует накладывать гипсовую повязку на голень на срок не менее 2 мес.
Остеосинтез большеберцовой кости пластинкой можно применять при всех видах переломов. Лучше пользоваться прочной металлической пластинкой на 8—12 винтах. Такой вид остеосинтеза не требует гипсовой повязки. Пластинки надо фиксировать на наружной поверхности большеберцовой кости, где имеется мышечный слой. Укладывать массивные пластинки по внутренней поверхности большеберцовой кости проще, но опасно из-за возможности развития некроза кожи. Интрамедуллярный остеосинтез большеберцовой кости стержнем типа Богданова нецелесообразен даже при поперечных переломах, так как он требует полноценной гипсовой иммобилизации на весь период срастания перелома.
Прочность фиксации перелома зависит от диаметра интрамедуллярно введенного штифта. Рассверливание костномозгового канала дает возможность применить более прочные штифты, которые обеспечивают хорошую фиксацию отломков и не требуют в послеоперационном периоде дополнительной фиксации. Рассверливание следует производить при локализации перелома дистальнее или проксимальнее суженной части костномозгового канала большеберцовой кости. При остеосинтезе большеберцовой кости прочную фиксацию можно обеспечить штифтами диаметром 9—12 мм.
Остеосинтез большеберцовой кости может быть выполнен после открытой и закрытой репозиции. При закрытой репозиции штифты вводят в костномозговой канал через проксимальный метафиз, не обнажая место перелома. Преимущество его перед открытым методом в сохранении периостальных тканей у концов отломка, меньшей опасности инфицирования перелома, меньших травматичности и кровопотери.
Массивный металлический штифт вводят в костномозговой канал большеберцовой кости, как при открытой, так и при закрытой репозиции, антеградно.
Разрез кожи около 4 см производят по передней поверхности голени над местом перелома большеберцовой кости. После обнажения отломков через операционную рану сверлами расширяют костномозговой канал до необходимого размера. Затем ногу сгибают в коленном суставе под углом 90°, поставив стопу на операционный стол, и производят разрез кожи от середины надколенника до проксимального эпифиза большеберцовой кости по внутреннему краю собственной связки надколенника. Далее разрезом длиной около 2 см вскрывают фиброзную капсулу коленного сустава (синовиальную оболочку повреждать не следует). При этом на эпифизе большеберцовой кости можно пальпировать внесуставную площадку, являющуюся местом введения штифта.
При закрытой репозиции отломков через проксимальный метафиз вводят иаправитель диаметром 3—4 мм, продвигают его в костномозговой канал дистального отломка и по нему под контролем рентгенографии вводят штифт.
Компрессионно-дистракционный остеосинтез голени может быть применен при любом характере перелома большеберцовой кости. Голень, как никакой другой сегмент, по своему анатомическому строению удобна для лечения компрессионно-дистракционными аппаратами. К чрескостному остеосинтезу голени следует прибегать в том случае, если неэффективны консервативные методы. Компрессионно-дистракционные аппараты применяют с целью надежной фиксации большеберцовой кости и репозиции отломков. К достоинствам метода следует отнести малую травматичность по сравнению с погружным остеосинтезом, а к недостаткам — неудобство нахождения больного в быту с громоздким аппаратом. Хорошая фиксация отломков голени может быть обеспечена аппаратом на 4 кольцах, причем через каждое кольцо или полукольцо должно быть проведено не менее 2 спиц. Два кольца должны быть расположены в проксимальном и 2 — в дистальном отломках. При винтообразных или косых переломах с длинной плоскостью излома можно применять встречно-боковую компрессию спицами с упорной площадкой или штыкообразно изогнутыми. Натяжение спиц, закрепленных в кольцах, плотно сдавливает костные отломки по плоскостям излома. Непременные условия лечения переломов голени компрессионно-дистракционным методом — ходьба с нагрузкой и движения в коленном и голеностопном суставах, так как они способствуют восстановлению кровоснабжения.
Лечение изолированных переломов диафиза большеберцовой кости имеет определенные особенности. Это объясняется тем, что неповрежденная малоберцовая кость затрудняет репозицию перело379 ма при наличии смещения отломков болыпеберцовой кости, а при отсутствии смещения является «распоркой», препятствующей сопоставлению костных отломков и срастанию их.
Изолированные переломы болыпеберцовой кости, особенно поперечные (даже без смещения), довольно часто не срастаются, поэтому в подобных случаях целесообразно оперативное вмешательство. Лечение гипсовыми повязками или постоянным вытяжением проводится по тому же принципу, что и при переломе обеих костей голени. Лечение изолированного перелома диафиза малоберцовой кости не представляет трудностей, так как переломы малоберцовой кости со смещением и без смещения не нарушают функции и, как правило, всегда срастаются. Смещение костных отломков всегда бывает незначительным, главным образом в сторону, так как неповрежденная болыпеберцовая кость является «распоркой» и препятствует смещению отломков по длине. Первые 2—5 дней следует ограничить ходьбу, а после ликвидации болевого синдрома можно ходить с нагрузкой на ногу без внешней фиксации.
Переломы головки малоберцовой кости могут сопровождаться повреждением малоберцового нерва. Обычно повреждение нерва вызвано ушибом его и подлежит консервативному лечению. В случае полного повреждения нерва показано сшивание его. Малоберцовый нерв трудно восстанавливается даже после оперативного вмешательства. Результатом повреждения нерва является отвисание стопы. При необратимой потере функции малоберцового нерва следует производить ортопедические операции на стопе.
Открытые повреждения диафиза голени
Из всех открытых диафизарных переломов костей подобные переломы голени стоят на первом месте. На.долю голени приходится 35% от всех диафизарных открытых переломов. Наиболее опасны из-за возможности гнойных осложнений открытые переломы нижней трети голени.
Ведущее значение в лечении пострадавших с открытыми переломами голени придают заживлению раны мягких тканей, поскольку это означает ликвидацию опасности инфекции. Поэтому в практической работе надо ориентироваться не на анатомический тип переломов, а на степень и характер повреждения мягких тканей.
Различают 4 вида ран при открытых переломах:
1) раны с малой зоной повреждения, края которых можно ушить без натяжения;
2) раны со средней зоной повреждения, отслоением мягких тканей, когда для закрытия отломков требуются послабляющие разрезы;
3) размозженные раны с большой зоной повреждения и обширным отслоением мягких тканей, лечение которых невозможно без пересадки кожи;
4) раны с массивными повреждениями мягких тканей, магистральных сосудов, нервов, угрожающие жизнеспособности конечности, травматические ампутации.
Такая дифференцировка ран позволяет определить тактику и объем лечебных мероприятий и правильно оценить результаты лечения.
Первичная хирургическая обработка состоит в удалении из раны нежизнеспособных тканей, инородных тел и загрязнений. Иссечение ушибленных и нежизнеспособных тканей производят постепенно до дна раны, а для очищения раневой поверхности применяют вакуумпирование.
При ранах с малой зоной повреждения в момент первичной хирургической обработки остеосинтез производить нецелесообразно, так как эти раны обычно заживают первичным натяжением, а любая операция остеосинтеза вызывает дополнительную травму, что может способствовать развитию нагноения. Таким больным при поступлении фиксируют перелом гипсовой повязкой или скелетным вытяжением в зависимости от положения костных отломков. После заживления раны показания к лечению перелома такие же, как и при закрытом переломе. При ранах со средней зоной повреждения мягких тканей после репозиции отломки следует фиксировать компрессионно-дистракционным аппаратом, причем фиксирующие спицы проводят вдали от раны с целью профилактики нагноения мягких тканей вокруг спиц. Аппарат дает возможность прочно фиксировать костные отломки, производить активные движения в крупных суставах, что способствует улучшению кровообращения, позволяет оставить рану открытой для динамического контроля.
При ранах с большой зоной повреждения мягких тканей целесообразно накладывать стержневой аппарат внешней фиксации для временной стабилизации отломков. После заживления раны возможен перемонтаж аппарата.
После обработки раны, репозиции и фиксации отломков тактика лечения сводится к следующему. Последовательно сшивают поврежденные нервы, сухожилия, послойно — мягкие ткани. При ранах с малой зоной повреждения это удается сравнительно легко; при ранах со средней зоной повреждения необходима пластика местными тканями с помощью послабляющих разрезов. Послабляющие «лампасные» разрезы на голени делают с латеральной стороны, после чего выкроенный кожно-фасциальный лоскут перемещают и закрывают им оголенные костные отломки, а образовавшийся дефект кожи закрывают расщепленным лоскутом кожи. С успехом можно пользоваться также многочисленными мелкими послабляющими разрезами (насечками) через всю толщу кожи, располагая их в шахматном порядке по окружности раны. Это позволяет ослабить натяжение кожных краев, предупреждает формирование избыточной гематомы и уменьшает посттравматический отек в области перелома. При ранах с большой зоной повреждения и обширным отлоением мягких тканей приходится прибегать к более сложным пластическим операциям.
Обширные кожные дефекты требуют пересадки формалинизированной кожи, которая также предотвращает плазмопотерю, обладает антисептическими свойствами и способствует росту грануляций. При ранах с массивными повреждениями мягких тканей и травматических ампутациях надо произвести первичную хирургическую обработку, оставив рану незашитой, хорошо дренировать ее марлевыми салфетками.
Травматология и ортопедия
Под редакцией члена-корр. РАМН
Ю. Г. Шапошникова
Опубликовал Константин Моканов
ОТКРЫТЫЕ ДИАФИЗАРНЫЕ И МЕТАФИЗАРНЫЕ ПЕРЕЛОМЫ, ОСЛОЖНЕННЫЕ ИНФЕКЦИЕЙ

ГЛАВА IV
Клиническое течение открытых переломов зависит от общего состояния больного, его возраста, состояния нервной и сердечно-сосудистой систем, реактивности и приспособительно-компенсаторных возможностей организма.
У больных, перенесших тяжелый шок, при большой кровопотере, а также у пожилых людей повышен риск развития инфекции и других осложнений. Опасность осложнений при открытых переломах с обширными и загрязненными ранами большая, чем при открытых переломах с небольшими и средней величины ранами. По данным А. В. Каплана и О. Н. Марковой, при открытом переломе типа IA осложнений не наблюдалось; количество их возрастало соответственно тяжести травмы: IБ – 2%, IIБ – 4,9%, IIВ –
18,3%, IIIБ – 42,4%, IIIB – 50,9%, IV – 63,9%. Течение открытых переломов во многом зависит от локализации повреждений. По-разному протекают открытые диафизарные, околосуставные и внутрисуставные переломы бедра, голени, плеча и предплечья.
Открытые переломы костей верхней конечности протекают обычно более гладко и с меньшим числом осложнений, чем открытые переломы нижних конечностей, что в первую очередь связано с лучшими условиями кровообращения плеча и предплечья по сравнению с бедром и голенью, меньшим микробным загрязнением кожи верхних конечностей.
Особенно пристального наблюдения требуют больные с открытыми переломами в первые 5-10 дней после травмы, когда имеется угроза развития аэробной и анаэробной инфекции.
Мы (А. В. Каплан, О. Н. Маркова, 1975) различаем следующие виды клинического течения открытых переломов.
Асептическое течение по типу закрытых переломов. Для развития инфекции в кости в зависимости от разных условий требуется от 2 до 8 нед. «Травматический остеомиелит» обычно с самого начала, а иногда после подострой стадии принимает хроническую форму. Из всех тканей человеческого организма кость наиболее подвержена хронической инфекции при открытой травме.
Благодаря комплексному лечению в настоящее время у преобладающего большинства больных с открытыми переломами инфекция не развивается и процесс сращения протекает без осложнений или со сравнительно легкими осложнениями. Так протекают переломы с заживлением раны первичным натяжением, сюда могут быть отнесены открытые переломы с ограниченным поверхностным нагноением или краевым некрозом кожи, которые чаще наблюдаются на передней поверхности голени. Участок некротизированной ткани не следует насильно удалять,- обычно он сам медленно, в течение 2-4 нед, отторгается. За этот срок под сухим некрозом кожи образуется грануляционная ткань, которая часто служит хорошим барьером проникновению инфекции в зону перелома. Рана постепенно эпителизируется с краев; при задержке эпителизации следует прибегать к свободной пересадке кожи. Кожная пластика должна производиться в ранние сроки после отторжения некроза кожи. У некоторых больных нагноительный процесс носит поверхностный характер или ограничивается пределами мягких тканей; обычно такая рана скоро закрывается.
Псевдоасептическое течение со скрытым периодом развития инфекционного осложнения. Вначале (первые дни) перелом протекает по типу закрытого. В дальнейшем, иногда в ближайшие дни или в более позднем периоде, отмечается прогрессирующее нарастание симптомов, указывающих на ухудшение состояния: нарушаются аппетит и

сон, повышается температура, увеличиваются лейкоцитоз, СОЭ; местно определяется отек. При снятии швов и раздвигании краев раны из глубины выделяется гной, видны серые участки некротизированной ткани. В обоих случаях при раннем выявлении развивающейся инфекции и принятии необходимых мер удается вскоре купировать процесс и изменить его течение в благоприятном направлении. В других случаях, особенно при запоздалой диагностике, процесс прогрессирует, иногда протекает бурно и стихание его происходит лишь в более поздний период.
Острое течение с бурным развитием в первые дни воспалительного процесса в области открытого перелома. Состояние сразу становится тяжелым. Больной жалуется на боли в поврежденной конечности, слабость, плохой аппетит и сон. Отмечаются бледность кожных покровов, анемия, повышение температуры тела и интоксикация. Необходимо своевременно широко раскрыть рану, рассечь отечные ткани, вскрыть гнойные затеки и карманы, удалить некротизированные ткани и создать условия для постоянного оттока отделяемого из ран. В крайне тяжелых случаях приходится даже ампутировать конечность. Нужно принять меры, направленные на улучшение общего состояния больного, поднятие реактивности и иммунологических свойств организма, усилить борьбу с инфекцией и интоксикацией путем внутривенного введения раствора глюкозы, раствора Рингера, изотонического раствора хлорида натрия с добавлением гемодеза, полиглюкина, реополиглюкина, антибактериальной сыворотки, переливания крови, соответствующих антибиотиков и другие меры.
При глубоком нагноении обычно развивается остеомиелит. Спешить с удалением металлического стержня или другого фиксатора в остром периоде следует не всегда, так как неподвижность отломков после удаления фиксаторов нарушается, что ведет к лишней травматизации тканей и распространению инфекции. Однако чрезмерно длительное оставление обнаженных фиксаторов в гнойной ране также имеет свои пределы. При значительной интоксикации могут возникнуть показания к более широкому раскрытию раны, вскрытию гнойных затеков, срочному, удалению металлических конструкций и созданию условий для свободного оттока гноя. В большинстве случаев для обездвижения отломков следует наложить гипсовую повязку или компрессионный аппарат и удалить металлический фиксатор.
Ухудшение состояния, интоксикация, высокая температура, частый пульс, боли, в особенности распирающего характера, нарастание отека, краснота, соответствующие изменения крови и другие симптомы должны вызвать опасение за жизнь больного, мысль о развитии анаэробной инфекции, сепсисе и других тяжелых осложнениях. В этих случаях не следует ограничиваться только пассивным наблюдением и протоколированием в истории болезни картины нарастающего ухудшения состояния больного. Когда стоит вопрос о сохранении жизни и этого нельзя достичь щадящими методами (рассечение ран, некрэктомия, вскрытие затеков и др.), нужно пожертвовать конечностью и своевременно произвести вторичную ампутацию.
Подострое или хроническое течение инфекционного осложненного открытого перелома с выраженной клинической картиной тяжелой интоксикации (токсемия, сепсис, септикопиемия, раневое истощение), развившейся постепенно или после острого инфекционного осложнения (гнойное, гнилостное, анаэробное).
Состояние больного обычно тяжелое или очень тяжелое. В таких случаях речь идет о спасении жизни и нужно своевременно ампутировать конечность.
Хроническое течение с самого начала, медленно развивающееся или стабилизировавшееся после остро или подостро протекающего инфекционного процесса. У части больных имеются свищи, секвестры и концевой остеомиелит. Общее состояние обычно удовлетворительное, явления интоксикации не выражены. Только раннее выявление и последующее рациональное лечение позволяют купировать инфекционный процесс в ранних стадиях и предотвращают возникновение тяжелых осложнений, угрожающих жизни, приводящих к ампутации конечности или инвалидизации в связи с

тяжелыми инфекционными, трофическими, ишемическими и иными поражениями конечности.
Помимо инфекционных осложнений, связанных с травмой, недостаточностью первичной обработки и обездвижения отломков, инфекция может развиться в результате вторичного инфицирования, которое в значительной степени обусловлено существующей
внастоящее время проблемой госпитализма. Вторичное инфицирование раны происходит при перевязках в результате попадания в нее микробов из воздуха, с рук и из носоглотки медицинского персонала, от больных с инфекционными осложнениями, с больничного белья и одежды. Основным источником госпитальной инфекции являются больные с гнойными ранами, свищами и другими открытыми очагами инфекции. Происходит постоянный обмен, особенно антибиотикоустойчивыми штаммами микробов, между больными, обслуживающим персоналом и окружающими предметами (В. И. Мельникова, 1970).
Борьба с госпитализмом в настоящее время является исключительно актуальной и сложной, поэтому она должна проводиться решительно и постоянно. Прежде всего следует безукоризненно соблюдать правила хирургической асептики не только в операционных, но и в перевязочных и палатах.
Выбор рационального, эффективного лечения и правильное прогнозирование при инфицированных открытых переломах в большей степени зависит от правильной оценки вида инфекционного осложнения, определения распространенности процесса, особенности течения его и учета общего состояния больного.
Заживление открытых переломов с небольшими поверхностными ранами и незначительным отделяемым, а также переломов, осложненных ограниченным некрозом кожи на небольшом участке, мало отличается от заживления неосложненных открытых переломов.
При открытых диафизарных переломах с большими гранулирующими ранами производят в ранние сроки после травмы отсроченную или вторичную кожную пластику. Наличие гнойного отделяемого и патогенной микрофлоры в ране является противопоказанием к кожной пластике, если пересадка аутокожи произведена мелкими лоскутами по методу Тирша или Янович-Чаинского. Обширные раны, как правило, заживают в течение 3-4 нед после пластики.
При обширных инфицированных ранах с наличием некротизированных тканей, гнойных затеков и прогрессировании патологического процесса у больных, находящихся
втяжелом состоянии, конечности угрожает ампутация уже в ранние сроки после травмы в связи с развитием тяжелой гнойной, гнилостной или анаэробной инфекции. Чаще это больные с открытыми переломами типа IIB, IIIB или IV.
При осложнениях открытых диафизарных переломов тяжелыми инфекционными процессами необходимо на основании клинических, лабораторных и рентгенологических данных в максимально короткий срок оценить общее состояние больного, уточнить характер и тяжесть осложнения и определить прогноз в смысле возможности сохранить жизнь и конечность. В зависимости от этого следует наметить наиболее рациональный план лечения больного.
Хирургический метод лечения. Основываясь на опыте Великой Отечественной войны, А. В. Каплан (1948), И. Л. Крупко (1954, 1956), А. Н. Беркутов (1960) и др. для предупреждения тяжелого течения открытых инфицированных переломов при наличии в ране мертвых тканей рекомендуют производить позднюю и повторную хирургическую обработку раны. Она заключается в широком раскрытии раны, тщательном иссечении и удалении всех мертвых тканей и свободных костных отломков. Если ранее был произведен остеосинтез – фиксатор не удаляется (Н. Е. Махсон, 1977). При смещенных отломках их репонируют и производят остеосинтез спицами, реже другими фиксаторами. Рану промывают антисептиками и подвергают вакуумированию. Местно вводят антибиотики и протеолитические ферменты. Отток раневого отделяемого обеспечивают

дренированием и контрапертурами. При гладком течении накладывают отсроченные швы. Если условия позволяют, рану можно сразу зашивать и установить длительное (постоянное или прерывистое) промывание антисептиками с отсасыванием жидкости тонкими полиэтиленовыми трубками, проведенными вглубь раны через узкие отверстия в коже, которые плотно охватывают трубки. Можно использовать отсасывающие аппараты. Иммобилизация конечности осуществляется обычными способами. Своевременное применение этого метода может прервать нагноительный процесс.
Вторичная ампутация конечности. Благодаря современным методам лечения открытых переломов (первичная хирургическая обработка раны, хорошая репозиция и фиксация отломков, антибиотикотерапия) вторичные ампутации производятся в исключительных случаях. Лишь при тяжелой токсемии от распространения инфекции, вторичном кровотечении из своевременно нераспознанного повреждения магистрального сосуда, гангрене конечности в результате тромбоза сосудов и тяжелых формах газовой гангрены для спасения жизни показана вторичная ампутация конечности.
Развитие инфекции в кости имеет свои особенности, обусловленные специфической структурой ее, наличием минерального компонента, образующегося на коллагеновой основе, в которой заключены живые элементы кости (остеоциты, сосуды и др.). Наряду с этим структурное строение в различных областях трубчатой кости неодинаково. Так, строение диафиза существенно отличается от метаэпифизарной части. Сами элементы кости отличаются не только своей структурой, но и особенностями кровоснабжения, сопротивляемости механическим, инфекционным, токсическим и иным воздействиям, реактивностью и потенциальной возможностью к репаративной регенерации.
При воспалительном процессе сдавливаются и тромбируются внутрикостные сосуды, нарушается жизнеспособность костных клеток и лишенная кровоснабжения зона кости некротизируется.
Ограниченные небольшие участки некротизированной кости часто незаметно выделяются вместе с гноем либо частично или полностью распадаются, рассасываются. Более значительные секвестры, образующиеся в диафизе вследствие незначительной васкуляризации из периоста, приходится удалять хирургическим путем.
Вметафизах губчатой кости секвестры образуются медленно, в течение долгого времени четко не отграничиваются, и поэтому операция требует большой тщательности и осторожности.
Внастоящее время возбудителем травматического остеомиелита обычно является стафилококк, а не стрептококк. В ряде случаев возбудителями оказываются и другие микроорганизмы (синегнойная палочка, протей, кишечная палочка и др., рассматривавшиеся ранее как непатогенные или условно-патогенные микробы), часто мультирезистентные к антибиотикам, а также анаэробы.
На основании клинического опыта мы (А. В. Каплан, О. Н. Маркова, 1967) выделяем следующие формы диафизарного и метаэпифизарного травматического остеомиелита как осложнения после открытых диафизарных переломов длинных трубчатых костей: 1) остеомиелит со свободно лежащими осколками кости (первично нежизнеспособные мелкие секвестры), правильнее – первичный некроз кости; 2) ограниченный краевой (пристеночный) остеомиелит без секвестров; 3) концевой остеомиелит фрагментов поврежденной кости на ограниченном участке; 4) концевой остеомиелит одного из фрагментов с возникновением крупных полуцилиндрических или цилиндрических секвестров; 5) концевой остеомиелит обоих отломков кости на ограниченном участке, 6) остеомиелит концов обоих отломков с образованием массивных секвестров; 7) остеомиелит на значительном протяжении кости (диафиза и метафиза) с образованием вторичных секвестров за счет распространения воспалительного процесса.
Возникновение особенно тяжелых и обширных остеомиелитов при открытых диафизарных переломах длинных трубчатых костей с размозжением мягких тканей наблюдается чаще после остеосинтеза погружными металлическими конструкциями,

произведенного в момент первичной хирургической обработки. Металлические штифты и пластинки обеспечивают большую или меньшую неподвижность отломков, но применение их во время первичной хирургической обработки открытого перелома ухудшает условия гемодинамики на его уровне, так как при этом методе, помимо травматического повреждения питающих кость сосудов, кровообращение кости еще больше ухудшается за счет повреждения сосудов при отслойке надкостницы или разрушении костного мозга при остеосинтезе.
Хронический инфекционный процесс в кости, даже в виде ограниченного остеомиелитического очага, трудно поддается лечению, требует много времени и усилий, чтобы избежать инвалидности и возвратить больного к труду.
Лечение. Лечение остеомиелита должно проводиться комплексно. Секвестрэктомия является типичной операцией при лечении хронического остеомиелита. Она включат не только удаление секвестров, но и полную санацию секвестральной полости с удалением всех грануляций, обработкой стенок и дна полости растворами антисептиков (спирт, фурацилин, 10% спиртовой раствор йода и др.). Операцию можно считать успешно законченной только тогда, когда санированная, со здоровыми жизнеспособными стенками секвестральная полость превращена в отлогий желоб, который полностью заполнен пластическим материалом (мышца на питающей ножке, в соответствующих случаях – измельченный консервированный аллохрящ, реже измельченная аутоили, еще реже, консервированная аллокость или другие биологические ткани, которые имеют определенные преимущества по сравнению с небиологическими материалами).
В. А. Чернавский и Б. М. Миразимов (1967), Н. М. Шаматов, Ш. Ш. Хамраев и Т. И. Кретова (1967) при операциях по поводу подострого и хронического остеомиелита стали использовать вакуум-аппарат и производить пломбировку секвестральной полости измельченным консервированным хрящом. Вакуумирование способствует удалению всех некротических тканей из костной полости, что создает неблагоприятные условия для жизнедеятельности микрофлоры и значительно уменьшает микробную загрязненность раны. Вакуумирование также позволяет хорошо очистить свищевые ходы, размягчает рубцовую ткань, улучшает кровоснабжение тканей. После вакуумирования рану зашивают наглухо.
Успех операции секвестрэктомии во многом зависит также от раннего и полного закрытия кожной раны. Для закрытия значительных дефектов кожи можно рекомендовать кожную аутопластику мостовидным лоскутом с двумя питающими ножками; при отсутствии условий для ее проведения возможна пластика свободным полнослойным перфорированным лоскутом аутокожи. А. К. Тычинкина (1962) рекомендовала заготовить лоскут на противоположной конечности и закрыть им после операции кожный дефект.
Н. М. Шаматов, Ш. Ш. Хамраев и Т. И. Кретова (1967) дефект кожи после секвестрэктомии закрывали лоскутами консервированной аллокожи. Мы по предложению С. С. Фейгельмана (1973) временно закрываем обнаженную кость формалинизированной кожей, под которой кость покрывается грануляциями.
Для гладкого заживления раны после секвестрэктомии имеет большое значение свободный отток отделяемого из глубины раны. Закрывая полностью операционную рану с целью профилактики вторичного инфицирования кости, следует делать контрапертуры на задней или боковой поверхности конечности.
Иммобилизацию конечности при открытых инфицированных переломах лучше всего осуществить компрессионно-дистракционным аппаратом (рис. 11). Если имеются общие противопоказания или местные условия (затеки, локализация перелома и ран, обширность их, сильное гноетечение и т. д.), неблагоприятные для наложения аппарата, временно или для постоянного лечения накладывают гипсовую повязку (мостовидная или лонгетноциркулярная с окнами). Гипсовая повязка используется также для лечения переломов без смещений или при устойчивых, хорошо репонированных переломах.

Общее лечение инфицированных открытых переломов при соответствующих показаниях следует сочетать с направленной антибиотикотерапией, проводимой после определения чувствительности микрофлоры ран к ряду антибиотиков.
При наличии стойкой устойчивости ассоциаций микробов к отдельным антибиотикам следует прибегать к комбинированному лечению несколькими синергично действующими антибиотиками, комбинируя различные пути введения (местно и внутримышечно; парентерально и перорально), сочетая антибиотики с сульфаниламидами (главным образом продленного действия) и нитрофуранами. При выборе сочетаний антибиотиков надо исходить из механизма их действия и комбинировать только те антибиотики, действие которых при таком применении усиливается и создается синертический эффект.
Наиболее эффективными являются следующие сочетания: пенициллины (включая полисинтетические) + мовомицин, певициллин + стрептомицин, пенициллин + канамицин, мономицин + олеандомицин, тетрациклины + эритромицин, тетрациклины + олеандомицин, тетрациклины + новобиоцин, линкомицин + мономицин, линкомицин + тетрациклины и многие другие. Хорошо зарекомендовал себя гентамицин.
Необходимо сохранение резерва антибиотиков (антибиотики «запаса»), к которым микрофлора даже гнойных ран продолжает оставаться более чувствительной.
При стафилококковой инфекции мягких тканей и стафилококковом сепсисе весьма Эффективны (при чувствительности к ним стафилококков) полусинтетические пенициллины, макролиды и ристомицин.
Антибиотики широкого спектра действия, такие, как мономицин, морфоциклин, гликоциклин и некоторые комплексные антибиотики типа тетраолеана, следует оставлять для лечения больных со смешанной инфекцией.
По данным В. М. Мельниковой и О. Н. Марковой (1975), при подостром остеомиелите монокультура стафилококка встречается только у 1/3 больных: у 2/3 – появляются ассоциации из двух и трех микробов.
При хроническом остеомиелите в состав ассоциаций, как правило, входит уже 4-5 видов микробов. В ассоциациях появляются кишечная палочка, энтерококк, протей, синегнойная «палочка и другие микробы, причем добиться исчезновения из ассоциаций протея и синегнойной палочки весьма трудно. Основным микробом костной раны, естественно, является стафилококк. Если в ранний период остеомиелита микрофлора ран и свищей чувствительна ко многим антибиотикам, то в хронический период из глубины свищевых ходов высеваются ассоциации микробов, устойчивые почти ко всем применяемым антибиотикам.
О. Н. Маркова и В. М. Мельникова (1975) рекомендуют применение линкомицина как при острой, так и при хронической стафилококковой инфекции костной ткани. Если микрофлора чувствительна к пенициллину или тетрациклину, начинать лечение надо с этих антибиотиков, а затем назначать макролиды или полусинтетические пенициллины (метициллин, оксациллин) и только при устойчивости стафилококка к этим препаратам применять линкомицин.
Учитывая способность линкомицина действовать внутри костной ткани, целесообразно ограничить его применение в других случаях, оставив его в резерве как наиболее ценный препарат для лечения стафилококковых поражений костей и суставов. Однако и при инфекции костей и суставов не следует назначать линкомицин без особых показаний, чтобы как можно дольше сохранить чувствительность микрофлоры к этому ценному антибиотику.
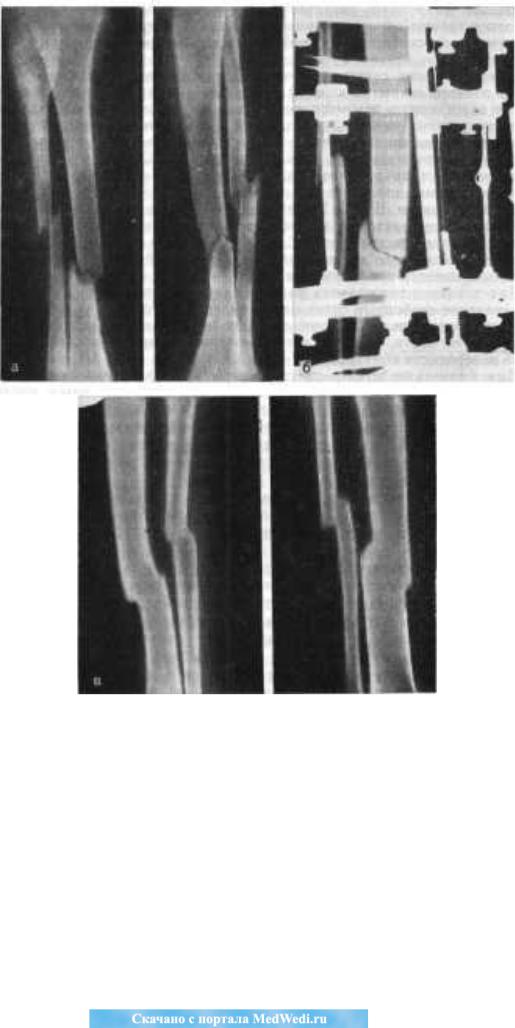
Рис. 11. Открытый косой перелом в нижней трети правой голени, осложненный остеомиелитом (свищевая форма).
а – через 3 мес после травмы – положение отломков в гипсовой повязке после лечения; б – лечение аппаратом Илизарова; в – через 5 мес консолидация: состояние после
снятия аппарата.
Показанием к проведению регионарной перфузии могут быть только крайне тяжелые, не поддающиеся лечению другими методами острые и хронические свищевые формы остеомиелита. И. Л. Крупко (1965) считает, что особенно показана перфузия больным, у которых безуспешно проводились многократные оперативные вмешательства, но свищевые ходы с нечувствительной к антибиотикам флорой не поддаются ни оперативному, ни консервативному лечению. Перфузия позволяет создать в конечности с изолированным кровообращением сверхвысокую концентрацию антибиотиков при высоком насыщении крови кислородом, витаминами, гормонами и антикоагулянтами.

Клинические наблюдения (П. А. Куприянов, И. Л. Крупко, М. Н. Фаршатов, 1959, 1962, 1965), показали, что перфузия редко может быть использована как самостоятельный лечебный метод. Чаще она должна сочетаться с оперативными вмешательствами, главным образом радикальной секвестрэктомией.
Метод перфузии нельзя относить к числу простых и безопасных, поэтому он применяется при наиболее тяжелых формах остеомиелита и только в высококвалифицированных научно-исследовательских учреждениях. В тяжелых случаях применяют внутриаортальное введение через тонкий постоянный катетер антибиотиков и антисептических средств (Н. Е. Махсон, 1978).
У больных с повышенной чувствительностью к антибиотикам вместе с антибиотиками следует назначать антигистаминные препараты (димедрол, супрастин, пипольфен и др.), а в случае необходимости полностью отменить антибиотики и перейти к лечению сульфаниламидами или нитрофурановыми препаратами. У ослабленных больных при длительном лечении антибиотиками профилактически следует применять противогрибковые препараты – нистатин, леворин и др. (О. Н. Маркова, В. М. Мельникова, 1975).
Для повышения эффективности терапии, особенно у ослабленных больных, введение антибиотиков следует сочетать со средствами, стимулирующими реактивность организма и способствующими борьбе с инфекцией, а именно: дробные переливания крови, витаминотерапия (А, В, С, D), введение продигиозана, вакцин, сывороток, стафилококкового анатоксина, антистафилококковой плазмы, алоэ, стекловидного тела, АТФ и других препаратов. При антибиотикотерапии инфекций, особенно септического характера, когда в организме создается дефицит гамма-глобулина, следует вводить гаммаглобулин (по 0,5-2 мл/кг, желательно внутривенно однократно или несколько раз). Назначают также внутривенное вливание изотонического раствора хлорида натрия, глюкозы, а также проводят противоинтоксикационную терапию (гемодез и др.).
На современном этапе местное лечение гнойно-некротических ран немыслимо без применения протеолитических ферментов, представляющих собой биологически активные препараты. В. И. Стручков (1967), много лет изучавший действие протеолитических ферментов, рекомендует использовать их при лечении нагноившихся ран, флегмон мягких тканей и остеомиелита. Для лечения гнойно-воспалительных заболеваний конечностей применяют в настоящее время следующие протеолитические ферменты: трипсин, химотрипсин, химопсин, плазмин, стрептокиназу, бактериальную дезоксирибонуклеазу и другие ферменты, в том числе комбинированные препараты. Основное терапевтическое действие ферментных препаратов основано на их протеолитическом, противовоспалительном, антикоагуляционном и детидратационном свойствах. Ферменты могут также расщеплять пенициллиназу и некоторые бактериальные токсины. При этом они не тормозят рост грануляций и эпителизацию ран (Н. Ф. Камаев, 1962; В. И. Стручков и др., 1970).
Комплексное использование стафилококкового анатоксина с антибиотиками, разработанное И. В. Руфановым с сотр. (1964), применяемое с лечебной целью при инфицированных стафилококком открытых переломах И. А. Мовшовичем и соавт. (1969), оказалось также весьма эффективным даже у тяжелобольных. Стафилококковый анатоксин следует комбинировать с теми антибиотиками, к которым выявлена наибольшая чувствительность микробов, что не только позволяет повысить иммунитет и снизить сенсибилизацию организма, но и надежно подавляет развитие возбудителя инфекции.
Несмотря на определенные достижения, лечение травматических остеомиелитов до настоящего времени представляет исключительно большие трудности. Некоторые больные многократно и безуспешно подвергаются операции и комплексному лечению, а процесс в кости рецидивирует.
причины, симптомы и методы диагностики

Диафизарный перелом femur – сложная и опасная травма.
Такая разновидность травм, как диафизарные переломы бедра (femur) встречаются примерно у каждого 15-го пациента травматологии и у каждого 5-го человека с повреждениями нижних конечностей. Они относятся к категории опасных травм, так как могут стать причиной летального исхода при неоказании своевременной медицинской помощи. Рассмотрим их особенности и классификацию более подробно.
Содержание статьи
Локализация и виды
Переломами диафиза femur считаются повреждения костной ткани на участке от подвертельной сверху и до надмыщелковой зоны снизу. По сути, это тело бедра, его прямой участок.

Диафизальным переломомом считается повреждение кости от подвертельной зоны сверху и до надмыщелковой снизу.
Переломы диафиза классифицируются на такие виды:
- верхней, средней и нижней трети;
- поперечные, косые, винтообразные;
- открытые и закрытые;
- оскольчатые;
- двойные;
- клинообразные, сегментарные, мультифрагментарные;
- неполные;
- простые и сложные;
- сочетанные травмы;
- со смещение и без.
Чаще всего отломки femur подвергаются смещению, что может спровоцировать сопутствующие повреждения тканей. Определить точное расположение и тип перелома, а также степень его тяжести и стратегию дальнейшего лечения может только врач. В любом случае необходимо как можно скорее обратиться за профессиональной медицинской помощью.
Причины и последствия
Переломы диафиза бедра чаще всего встречаются у пациентов младшей возрастной категории: дети, подростки и молодые люди.
Причинами таких повреждений могут стать:
- прямой или непрямой удар;
- падение;
- сдавление;
- неестественная ротация конечности;
- сгибание кости;
- огнестрельное ранение;
- авария;
- спортивная травма.
Подобные переломы опасны своими последствиями, так как цена многих из них затрагивает жизнь человека. В результате повреждения бедра могут затрагиваться нервные пучки, крупные кровеносные сосуды, мышечные связки.
Наиболее опасными последствиями являются:
- изменение длины и формы конечности, и, как результат, хромота;
- значительная потеря крови;
- травматический шок;
- нарушение чувствительности конечности;
- нарушение двигательной способности;
- жировая эмболия;
- застойная пневмония.
Как видим, при переломах бедра не исключается наступление инвалидности и даже летального исхода.
Симптомы
Для того чтобы определить наличие повреждения бедра при подобной локализации, человеку необязательно владеть профессиональными знаниями и навыками. Диагностировать диафизарный перелом достаточно просто благодаря проявлению специфических признаков.
Основными симптомами травмы являются:
- сильная боль в ноге;
- выраженная отечность в месте перелома;
- кровоподтеки;
- при наличии раны – сильное кровотечение;
- нарушение двигательной способности;
- неспособность двигать конечностью;
- при напряжении мышц возникает сильная боль;
- аномальная подвижность бедра;
- костная крепитация;
- достаточно выраженная деформация ноги, ее укорочение;
- ротация конечности, стопа чаще всего смотрит наружу;
- побледнение кожных покровов;
- нарушение чувствительности на участке, расположенным ниже поврежденной области.
Сильнейшие боли и интенсивная кровопотеря могут привести к потере сознания и развитию у пострадавшего травматического шока, что является непосредственной угрозой для его жизни.
Характер смещения отломков
Отдельно следует отметить, что такие травмы практически всегда сопровождаются выраженным смещением костных фрагментов. Это обусловлено тем, что на этом участке ноги хорошо развиты мышцы, а они, в свою очередь, крепятся к femur.
При образовании перелома мышечные пучки оттягивают костные отломки в определенном направлении. По характеру смещения в определенной степени можно судить о локализации травмы.
Рассмотрим особенности смещения кости, в зависимости от расположения точки разлома:
- Верхняя треть. Верхний отломок подвергается воздействию ягодичных и подвздошно-поясничной мышц, что смещает его наружу и вперед. В свою очередь нижний конец диафиза оттягивается приводящими мышцами бедра и смещается во внутреннем направлении.
- Средняя треть. Ягодичные мышцы оттягивают верхний фрагмент кнаружи и кпереди, но не столь выраженно, как при переломах верхней трети. Нижний отломок тянется назад к середине. Таким образом, происходит смещение костей по длине.
- Нижняя треть. Приводящие мышцы удерживают верхнюю часть кости и провоцируют внутреннее смещение. Нижний фрагмент подвергается воздействию икроножных мышц, что способствует его натяжению и смещению в направлении кзади.
Первая помощь
Так как перелом диафиза бедра является опасной травмой, особое значение приобретает правильность и своевременность оказания первой помощи. Грамотные действия способны спасти жизнь пострадавшему.
Инструкция по оказанию первой доврачебной помощи представлена в таблице ниже:
| Действие и фото | Краткое описание |
Остановить кровотечение  Чтобы остановить кровотечения выше места травмы накладывается жгут или его аналог из подручных средств. | Выше места ранения накладывается жгут, обязательно указывается точное время его наложения, рана закрывается бинтом или тканью. Можно использовать в качестве жгута ремень, отрезок ткани, шнур и т. д. |
Дать обезболивающее  Чтобы не было болевого шока, пострадавшему дают (или колят) обезболивающее. | Для предотвращения болевого шока обязательно дайте пострадавшему любой обезболивающий препарат. |
Приложить лед  Если есть возможность, то к травмированной конечности стоит приложить холод. | Холод поможет снизить болевые ощущения, отечность и частично сократить кровопотери за счет сужения сосудов. |
Помочь занять удобное положение  Перед или для транспортировки больного необходимо уложить в наиболее удобное положение при травме бедра. | Лучше всего уложить больного на спину, а под колено подложить валик из одежды или подушку. |
Зафиксировать поврежденную конечность  Травмированную конечность необходимо зафиксировать. | На ногу накладывается шина. Можно использовать любые подручные материалы, обеспечивающие жесткость фиксации для голеностопа, колена и тазобедренного сустава. В крайнем случае, примотайте поврежденную ногу к здоровой, стараясь не спровоцировать смещение кости. |
Реанимирующие мероприятия  При необходимости проводят реанимационные мероприятия. | Если человек начинает терять сознание, а его жизненные показатели ухудшаются, необходимо произвести реанимирующие мероприятия: освободить дыхательные пути и сделать искусственное дыхание, а также непрямой массаж сердца. |
Вызвать «скорую помощь»  К травмированному человеку как можно скорее необходимо вызвать «скорую». | Врачи скорой помощи обеспечат пострадавшему необходимую транспортную иммобилизацию и доставят его в медучреждение. При необходимости медики вводят более сильное обезболивающее, производят переливание крови и искусственную вентиляцию легких. |
Оказание психологической поддержки  Пострадавшего надо поддерживать морально. | Больного необходимо поддерживать морально, отвлекать от болевых ощущений и стрессового напряжения, с помощью разговора предотвращать потерю сознания. |
Особенности лечения
Для предотвращения негативных последствий необходимо как можно скорее доставить пострадавшего в больницу. Диагностика производится травматологом посредством осмотра и прощупывания поврежденной конечности. Для более точного определения типа и степени сложности перелома назначается рентгенологическое обследование, а в некоторых случаях – и томография.
Такие травмы требуют продолжительного комплексного лечения. Консервативная терапия применяется в тех случаях, когда состояние здоровья пациента не позволяет производить хирургические вмешательства либо при несложных повреждениях.
На первых этапах лечения при отсутствии смещения, например, при неполном переломе, накладывается гипсовая повязка. Если имеется смещение, для восстановления правильной формы и длины конечности требуется скелетное вытяжение.
Его суть заключается в фиксации специальными спицами отломка бедра, чаще в области над мыщелком и бугристости большеберцовой кости. Конечность укладывается на шину Белера, а к фиксаторам подводятся утяжелители. В среднем их вес составляет 8 — 12 кг.
По мере сращивания кости можно сокращать силу противодействия для мышц конечности, уменьшая вес груза. Через несколько недель пациента переводят на кожное вытяжение и надевают на ногу ортез или гипсовую повязку.
Также на протяжении курса лечения пациенту назначается прием обезболивающих и противовоспалительных препаратов, антибиотиков и витаминов. Точный перечень медикаментов назначается лечащим врачом.
Хирургические методы
Так как перелом диафиза часто сопровождается осложнениями и смещениями, может потребоваться проведение операции. Целью хирургического вмешательства является остеосинтез с параллельным восстановлением целостности сосудов и мягких тканей.
Для соединения диафизарных фрагментов могут применяться костные фиксаторы (штифт, пластины, гвозди и винты), а также наружные приспособления. Довольно часто применяется интрамедуллярный ретроградный метод остеосинтеза с внутрикостным введением штифта, который остается навсегда в конечности пациента. Его вбивают в заранее подготовленное отверстие в костномозговом канале, а конец со стороны введения в вертельную ямку фиксируется винтами.
После завершения репозиции и остеосинтеза рану зашивают, соединяя послойно мягкие ткани и сосуды. Дополнительно устанавливается дренаж, минимум на 1 сутки. Дальнейшее лечение производится в стационаре, пока состояние пациента не стабилизируется.
Реабилитация и прогноз
Реабилитационный период длится около полугода. На начальном этапе необходимо принимать антибиотики и НПВС с обезболивающими. Рана ежедневно обрабатывается антисептиками. Находясь в постели. Больной должен выполнять дыхательные упражнения для профилактики пневмонии.
Когда скелетное вытяжение будет завершено, а перелом консолидируется, можно приступать к простым физическим упражнениям и понемногу вставать с постели. Дополнительно рекомендуются физиопроцедуры и массаж.
При успешном лечении и восстановлении нога полностью восстановит свои функции. Больше информации о диафизарных переломах бедра вы можете получить, посмотрев видео в этой статье.

