Метотрексат гормональный препарат или нет – МЕТОТРЕКСАТ таблетки – инструкция по применению, отзывы, состав, аналоги, форма выпуска, побочные эффекты, противопоказания
Метотрексат гормональный препарат или нет — Все про суставы
Source: LekMed.ru
Читайте также
Страница 2 из 2 Метотрексат — Methotrexatlim. Фармакологические свойства и противоопухолевое действие. Метотрексат относится к довольно токсичным препаратам. Высокие дозы препарата вызывают у различных животных общую слабость, потерю аппетита, адинамию, диспепсические расстройства, стоматит, угнетение кроветворения, снижение массы тела, общее истощение. У павших животных обнаруживают дегенеративные изменения слизистой оболочки кишок, значительную гипоплазию костного мозга и атрофию лимфоидной ткани. Одним из наиболее характерных побочных действий метотрексата является нарушение деятельности органов системы пищеварения, выражающееся у животных рвотой, диареей, деструктивными изменениями в тонкой кишке. Под влиянием токсических доз у животных происходят заметные нарушения функций печени — снижается содержание белка и белковых фракций в сыворотке крови, возникает их дисбаланс, нарушается антитоксическая, экскреторная и пигментная функции, замедляется желчевыделение. В печеночной паренхиме выявляются дегенеративные морфологические изменения. После частичной гепатэктомии метотрексат тормозит регенераторные процессы в печени животных. У больных в процессе лечения метотрексатом также нередко возникают изменения отдельных функций печени, вплоть до развития желтухи. Метотрексат, как и другие цитостатики, угнетает гемопоэз. После однократного применения препарата наблюдается выраженный миелодепрессивный эффект: резкая лейкопения и уменьшение числа миелоидных элементов в костном мозге, что проявляется нарушением не только дифференцировки клеток — предшественников миелоидных элементов, но и их созревания. На этом фоне наблюдаются снижение весовых коэффициентов лимфоидных органов (селезенки, вилочковой железы, лимфоузлов), обеднение их цитологической картины, уменьшение количества властных клеток, а также деструктивные изменения в элементах лимфопоэза. В лимфоузлах и селезенке уменьшаются количество и размеры фолликулов, в больших лимфоцитах появляются пикнотизированные ядра, снижается число митозов и плазматических клеток. После применения метотрексата происходят изменения со стороны почек — у животных нарушается диурез, снижается клиренс, развиваются дистрофические процессы в клубочковом аппарате и канальцах почек. Препарат может оказывать тератогенное и антикоагулянтное действие (вызывать нарушение свертываемости крови). Механизм действия. По современным представлениям, противоопухолевая активность метотрексата связана с блокированием в опухолевых клетках биосинтеза ДНК, РНК и белка. На пути биосинтеза этих жизненно важных компонентов клетки метотрексат вызывает множественные метаболические блоки. Одной из наиболее важных сторон механизма цитотоксического действия метотрексата является то, что он, как и другие аналоги фолиевой кислоты, препятствует превращению последней в ее биологически активные производные, играющие важную роль в биосинтезе пуринов и тимина нуклеиновых кислот de novo. В отличие от других антиметаболитов, Биологические эффекты метотрексата дозозависимы: малые дозы препарата нарушают синтез ДНК и РНК и вызывают дегенеративные изменения клеток в S-фазе, а большие нарушают синтез белка и вызывают изменения клеток в G1-фазе. На неделящиеся клетки метотрексат не влияет, что свидетельствует о его фазоспецифичности. В клинике обнаружено, что быстро пролиферирующие лимфомы более чувствительны к препарату, чем медленно растущие. У животных с опухолями уменьшены сроки выявления препарата и снижена его концентрация почти во всех органах, в том числе в печени и почках. Исключение составляет селезенка — в ее ткани уровень метотрексата и сроки его обнаружения значительно возрастают. В ткани опухоли преимущественного накопления препарата не выявлено, в то же время значительно замедлен его транспорт из опухолевых клеток. Проникает препарат в опухолевую клетку путем активного транспорта, а при высоких концентрациях — путем пассивной диффузии. В клетках он специфически связывается с ДГФК-редуктазой до полного насыщения, а также присутствует в свободном виде. Через 3 ч после введения невысоких доз метотрексата устанавливается динамическое равновесие, т.е. эквивалентная концентрация внутри и вне клетки. Обратный выход препарата из клетки затруднен. Проницаемость мембран опухолевых и лейкозных клеток для метотрексата выше, чем нормальных, а снижение концентрации в последних происходит быстрее, чем в опухолевых и лейкозных. Препарат выводится с мочой и калом. С мочой выводится до 70% Н-метотрексата, а 27% выводимых веществ являются метаболитами. В кале это соотношение составляет 19 и 72% На протяжении 12—14 ч выводится до 24%, а в течение 30 ч — более 90% препарата преимущественно в неизмененной форме. Лишь после введения высоких доз до 33% выделяется в виде 7-оксиметотрексата. Обнаружено, что у больных до 20% метотрексата связывается белками сыворотки крови. Снижение содержания препарата в крови трехфазное. Период полувыведения его из крови после внутривенного введения составляет более 40 ч. После приема внутрь препарат быстро всасываете» и достигает максимального уровня в крови через 1,5 ч. Плазматический клиренс составляет 80 мл/мин, а период полувыведения — 44 ч. Из пищеварительного канала всасывается 80—88% метотрексата. После местного применения 0,5% спиртового раствора, 0,2% мази или после внутрикожной инъекции 0,1 мл 0,5% раствора препарат в крови не обнаруживается. У детей после внутривенной шестичасовой инфузии период полувыведения метотрексата значительно сокращается и составляет в среднем 3—6 ч; за 72 ч с мочой выделяется более 70% препарата. У взрослых больных с мочой экскретируется 86—88% метотрексата, © фекалиями — 1,1—4,6%. За сутки после внутривенного введения выделяется до 96% метотрексата и 3—6% метаболитов, а через двое суток — 59,5% препарата и 40,5% таких метаболитов, как 7-оксиметотрексат и 4-амино-4- дезокси-10-метилптероиновая кислота. После перорального введения препарата этих же малоактивных продуктов биотрансформации выделяется больше — через сутки с мочой выводится 62,6% метотрексата и 37,4% метаболитов, а через двое суток — лишь 4,3% препарата и 95,7% метаболитов. В клинике обнаружено, что при прерывистом режиме введения высоких доз препарата под защитой лейковорина метотрексат более длительно и значительно в больших количествах находится в организме, чем при более частом применении его в малых дозах. При этом снижаются токсические проявления. После длительной инфузии больших доз препарата на фоне высокой концентрации его в плазме крови элиминация происходит в 2 фазы — периоды полувыведения 2 и 10 ч. Через сутки после окончания инфузии в моче обнаруживается до 50% введенной дозы препарата, при этом максимальный; уровень в моче более чем в 10 раз превышает его содержание в плазме крови. С помощью препарата, меченного тритием, показано, что в организме, человека и большинства экспериментальных животных он не дезаминируется и выделяется в основном в неизмененном виде. Однако в организме кроликов и морских свинок метотрексат может превращаться в 7- оксиметотрексат (ОМТ). Через 10 ч после введения препарата концентрация ОМТ и метотрексата в плазме крови больных одинакова. По мере повышения концентрации ОМТ внутриклеточное содержание метотрексата, как и уровень его в плазме крови, снижается. При этом значительно возрастает уровень 5-фосфорибозил-пирофосфата в лейкозных клетках, тогда как активность L-синтетазы значительно не изменяется. В моче и фекалиях грызунов обнаружено 3 нестабильных метаболита метотрексата. Основным является 4-амино-10-метилптероиновая кислота. Частичное превращение метотрексата в организме; мышей и крыс происходит под действием ферментов кишечных бактерий. 44- Амино-1 0-метилптероиновая кислота менее токсична и менее активна, чем метотрексат, поэтому такой путь метаболизма можно рассматривать как его. детоксикацию. Благодаря высокой Степени ионизации и слабой липофильности препарат на 50% связывается с белками плазмы крови, но все же проникает через гематоэнцефалический барьер — полости рта, раке пищевода и желудка, при лимфомах, остеогенной саркоме, саркоме Юинга, саркомах мягких тканей, медуллобластоме у детей. В отдельных случаях объективные ремиссии наблюдаются при опухолях яичника, печени, раке шейки матки, грибовидном микозе, лимфогранулематозе. Метотрексат оказался одним из наиболее эффективных средств лечения хориокарциномы матки. В ранних стадиях заболевания и невысоком титре хорионического гонадотропина полной регрессии опухоли после проведения курса химиотерапии можно достичь у 90% больных. В запущенных случаях с диссеминацией процесса предпочтительна комбинация метотрексата с дактиномицином, рубомицином и хлорбутином, в результате полная регрессия наступает у 70—80% больных. Особенно ценным представляется тот факт, что после успешного курса лечения хорионэпителиомы у многих женщин сохраняется детородная функция. При остром лейкозе лечение метотрексатом в ряде случаев приводит к продлению жизни больных до двух лет. Наряду с клинической наступает и гематологическая ремиссия. Лучшие результаты получены при опухолевой форме острого лейкоза, особенно при сочетании препарата с другими цитостатиками. Немаловажно то, что метотрексат является единственным препаратом, применяющимся для профилактики поражений ЦНС при остром лимфобластном лейкозе. Способ применения. Препарат вводят внутривенно, внутримышечно, перорально и интралюмбально. Детям, больным острым лейкозом, метотрексат предпочтительнее давать внутрь. Режим применения его зависит от формы заболевания, переносимости препарата и чувствительности к нему опухоли. Перорально препарат назначают ежедневно по 2,5—5 или 10 мг либо через день по 25 мг. Иногда его вводят по 20—25 мг ежедневно в течение 5 дней либо в той же дозе 2 раза в неделю. При интенсивной терапии метотрексат дают в высокой дозе — 30—40 мг 1 раз в 5 дней. При указанных режимах курсовая доза препарата в среднем составляет 200—300 мг. Повторные курсы лечения обычно проводят через 2—4 нед (в зависимости от сроков исчезновения Признаков токсичности). В последнее время за рубежом с успехом используют высокие и сверхвысокие дозы метотрексата под защитой антидота лейковорина. В этих случаях в течение 4—24 ч внутривенно капельно вводят от 50 До 500 мг/кг (в среднем 7,52 г/м2) препарата. Для предупреждения почечной токсичности за 12 ч до инъекции метотрексата производят гипергидратацию, которую продолжают еще в течение суток после начала его введения. Препарат начинают вводить, когда pH мочи достигает 7,0 и выше. Если pH мочи ниже 7,0, дополнительно назначают гидрокарбонат натрия. Через 2 ч после окончания инфузии метотрексата внутривенно вводят лейковорин в дозе 15 мг/м2, инъекции повторяют через каждые 6 ч (всего 8 введений). Лейковорин можно назначать и внутримышечно по 15 мг каждые ч либо по 9 мг каждые 6 ч с последующим пероральным его приемом через каждые 6 ч (всего 4 раза). Показана целесообразность перорального приема лейковорина. В качестве антидота могут быть также использованы тимидин и фермент карбоксипептидаза. Побочное действие. В период лечения метотрексатом у больных могут возникать нарушения со стороны органов пищеварения. Диспепсический синдром проявляется в виде тошноты, рвоты, диареи, стоматита, гастроэнтероколита, может возникать местное раздражение слизистой оболочки полости рта, пищевода и кишок, развиваются гингивиты, глосситы, эзофагиты, язвенные поражения слизистой оболочки кишок. Препарат обладает мйелодепрессивным действием, поэтому у больных нередко развиваются умеренные лейкопения, анемия и тромбоцитопения. Иногда возникают гепатопатии, а при длительном применении препарата возможно развитие фиброза и даже цирроза печени. При наличии у больных хронической патологии почек возможно проявление нейротоксичности, возникновение нефрита и цистита. У некоторых бальных появляются конъюнктивиты, изредка — ректиты, дерматиты, гиперпигментация кожи, алопеция. Описаны случаи аллергического пульмонита. При интратекальном введении нередко наблюдаются нейропатии — судороги, головокружения, головная боль, трофические расстройства. Многие возникающие нарушения обратимы и после удлинения интервала между введениями или снижения дозы метотрексата проходят без дополнительной терапии. Антидотом метотрексата является лейковорин. Поэтому в тяжелых случаях передозировки препарата больному необходимо сразу же ввести 3—6 г лейковорина. Одновременно назначать лейковорин и метотрексат не рекомендуется. Противопоказания. Беременность, заболевания печени и почек, угнетение костномозгового кроветворения. При высоких показателях мочевины и креатинина даже малые дозы метотрексата могут вызвать тяжелую интоксикацию. Форма выпуска и хранение. Для перорального применения метотрексат выпускают в таблетках, покрытых оболочкой, содержащих по 0,0023 г (2,3 мг) препарата; в упаковке по 30 таблеток. Для инъекций выпускают в Ампулах по 0,005 г (3 мг). Растворы готовят непосредственно перед введением. Хранят препарат в сухом, защищенном от света месте при невысокой температуре (+5 .. +10 °С) по списку Б. Выпускают препарат транснациональная корпорация «Фармация и Апджон», фирма «Lederie» (США) — основной поставщик, Россия и Украина. Экспортерами также являются Чехия, Бельгия, Австрия, Франция, Литва, Финляндия, Швеция, Индия. | ||||
Метотрексат это гормональный препарат или нет — Все про суставы
Source: LekMed.ru
Читайте также
Страница 2 из 2 Метотрексат — Methotrexatlim. Фармакологические свойства и противоопухолевое действие. Метотрексат относится к довольно токсичным препаратам. Высокие дозы препарата вызывают у различных животных общую слабость, потерю аппетита, адинамию, диспепсические расстройства, стоматит, угнетение кроветворения, снижение массы тела, общее истощение. У павших животных обнаруживают дегенеративные изменения слизистой оболочки кишок, значительную гипоплазию костного мозга и атрофию лимфоидной ткани. Биологические эффекты метотрексата дозозависимы: малые дозы препарата нарушают синтез ДНК и РНК и вызывают дегенеративные изменения клеток в S-фазе, а большие нарушают синтез белка и вызывают изменения клеток в G1-фазе. На неделящиеся клетки метотрексат не влияет, что свидетельствует о его фазоспецифичности. В клинике обнаружено, что быстро пролиферирующие лимфомы более чувствительны к препарату, чем медленно растущие. | ||||
Метотрексат в ревматологии: особенности приема, побочные деймтвия
Метотрексат – один из важнейших и эффективных медикаментов в терапии ревматоидного артрита, он относится к базисным препаратам.
По старым стандартам метотрексат следовало назначать после предварительного лечения нестероидными противовоспалительными средствами и гормонами в течение хотя бы двух недель, но последние исследования ученых и клинические наблюдения за больными говорят о необходимости его более раннего применения.

В дозах, используемых для лечения ревматоидного артрита, метотрексат увеличивает количество аденозина (естественного противовоспалительного фактора, вырабатываемого организмом) в очаге активного воспаления, который преимущественно накапливается в синовиальной ткани, что обеспечивает быстрый и хороший клинический эффект. Поддаются терапии даже злокачественно протекающие и запущенные случаи, в среднем заметное улучшение состояние больных, уменьшение припухлости и других местных признаков воспаления, исчезновение болей и улучшение двигательной функции наступает через 3-6 недель от начала приема метотрексата.
Препарат замедляет и частично предотвращает развитие необратимых деструктивных изменений в хрящевой ткани, что подтверждается результатами рентгенологического обследования, тем самым сохраняется правильное анатомическое строение сустава и его подвижность.
По данным врачей-ревматологов, около 80% больных получают именно метотрексат в качестве основного лекарства. Это возможно из-за заметного клинического влияния и относительно небольшого процента возникновения серьезных побочных эффектов при средних терапевтических дозах. Кроме того, хорошая отдача от применения этого вещества позволяют значительно снизить дозу или даже полностью отменить нестероидные противовоспалительные и гормональные препараты. Понятно, что это уменьшает негативное влияние на печень, почки и другие органы пациента.
Назначение метотрексата при артрите
Первоначально взрослому человеку при ревматоидном артрите назначается 7,5 мг метотрексата один раз в неделю, в виде таблеток или инъекций, внутривенных или внутримышечных. Если же ожидаемого эффекта нет более 1,5-2 месяцев, начинают постепенно увеличивать дозу, на 2,5 мг в неделю. Добившись стойкого улучшения, подбирают оптимальное количество препарата, которое больной будет принимать длительное время. Резкое прекращение приема вызывает обострение, которое с трудом удается купировать, так что снижать дозу нужно осторожно и постепенно.
Наиболее распространенное побочное действие метотрексата – влияние на желудочно-кишечный тракт: снижается аппетит, беспокоят тошнота, рвота, похудание. При сильно выраженном их проявлении прием препарата можно разбить на 2-3 или заменить инъекциями.
Более серьезное, но, к счастью, достаточно редкое осложнение при приеме метотрексата – внезапное появление одышки, сопровождаемой кашлем и повышением температуры, говорящие о развитии интерстициального пневмонита. Повреждение печени чаще всего бывает у пациентов, не способных отказаться от алкоголя во время лечения.
Для своевременного обнаружения токсического влияния на костный мозг больным ежемесячно проводят общий анализ крови, необходимы также биохимические анализы для контроля над функциями почек и печени.
Метотрексат противопоказан при беременности из-за значительного отрицательного влияния на плод, назначение его кормящей матери требует прекращения грудного вскармливания. А планировать беременность можно лишь через месяц прекращения приема препаратов женщиной и три месяца – мужчиной.
Метотрексат — Википедия
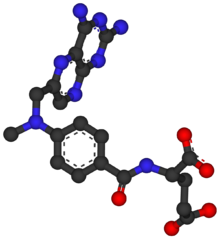
Метотрексат — цитостатический препарат из группы антиметаболитов, антагонистов фолиевой кислоты. Оказывает выраженное иммуносупрессивное действие даже в относительно низких дозах, не обладающих заметной гематологической токсичностью. Благодаря этому метотрексат шире, чем другие цитостатики с иммуносупрессивной активностью, применяется в качестве подавляющего иммунитет препарата. Синтезирован в 1940-х годах сотрудником Лаборатории Ледерле (ныне часть «Pfizer») Йеллапрагадой Суббарао.
Действует в S-фазу клеточного цикла. Механизм действия связан с ингибированием синтеза пуриновых нуклеотидов и тимидилата в результате необратимого связывания с дигидрофолатредуктазой, что препятствует восстановлению дигидрофолата в активный тетрагидрофолат. Более активен в отношении быстро растущих клеток.
В значительной степени проникает через ГЭБ (в зависимости от применяемой дозы). При интратекальном введении в значительном количестве поступает в системный кровоток. Связывание с белками (преимущественно с альбумином) плазмы около 50 %. Биотрансформируется в печени. Выводится почками (в неизменённом виде) и с желчью (менее 10 %). T1/2 зависит от применяемой дозы и имеет существенные индивидуальные различия. При повторном введении накапливается в тканях в виде метаболитов.
Острый лимфолейкоз, трофобластическая болезнь, рак кожи, рак шейки матки и вульвы, рак пищевода, плоскоклеточный рак головы и шеи, рак почечной лоханки и мочеточников, остеогенная и мягкоклеточная саркома, саркома Юинга, рак легкого, рак молочной железы, герминогенные опухоли яичка и яичников, рак печени, рак почки, ретинобластома, медуллобластома, рак полового члена, лимфогранулематоз, апластическая анемия. Псориаз, воспалительные заболевания кишечника (язвенный колит, болезнь Крона), ревматоидный артрит, ряд других аутоиммунных заболеваний в адекватных дозах. Инъекции метотрексата — приемлемая форма лечения больных с внематочной беременностью без признаков разрыва маточных труб, гемодинамической нестабильности и гемоперитонеума.
Принимают внутрь, вводят в/в, в/м, интралюмбально. Устанавливают индивидуально, в зависимости от показаний и стадии заболевания, состояния системы кроветворения, схемы противоопухолевой терапии. При лечении больных активной формой болезни Крона применяется в дозе 25 мг в\м 1 раз в неделю, что позволяет уменьшить дозу КС. В последующем, для поддержания ремиссии вводится по 15 мг в\м 1 раз в неделю.
Со стороны пищеварительной системы: возможны язвенный стоматит, анорексия, гингивит, фарингит, тошнота; редко — диарея, мелена, энтерит, панкреатит; в отдельных случаях (при длительном ежедневном применении) — некроз печени, цирроз, жировая атрофия, перипортальный фиброз печени.
Со стороны системы кроветворения: лейкопения, анемия, тромбоцитопения.
Со стороны ЦНС: чувство усталости, головокружение; редко — головная боль, афазия, сонливость, судороги.
Со стороны репродуктивной системы: нарушения оогенеза и сперматогенеза, олигоспермия, нарушения менструального цикла, снижение либидо, импотенция.
Со стороны мочевыделительной системы: гематурия, цистит, выраженные нарушения функции почек.
Аллергические реакции: озноб, снижение сопротивляемости к инфекции; редко — крапивница, токсический эпидермальный некролиз, синдром Стивенса-Джонсона.
Дерматологические реакции: кожная сыпь, фотосенсибилизация, нарушения пигментации, телеангиэктазии, акне, фурункулёз.
Возможное изменение роста за определенное время.
Выраженные нарушения функции печени и/или почек, лейкопения, тромбоцитопения, беременность. Метотрексат не следует применять при иммунодефицитных состояниях.
Метотрексат противопоказан к применению при беременности. При необходимости назначения в период лактации следует прекратить грудное вскармливание.
В экспериментальных исследованиях установлено эмбриотоксическое и тератогенное действие метотрексата.
Не следует применять метотрексат при асците, плевральном выпоте, язвенной болезни желудка и двенадцатиперстной кишки, язвенном колите, подагре или нефропатии (в том числе в анамнезе).
Не рекомендуют применять у пациентов с ветряной оспой (в том числе недавно перенесённой или после контакта с заболевшими), опоясывающим герпесом и другими острыми инфекционными заболеваниями.
Перед началом терапии и на фоне проводимого лечения следует контролировать картину периферической крови, функцию печени и почек, рентгенографию грудной клетки.
При лечении ревматоидного артрита или псориаза развёрнутый общий анализ крови следует делать не реже 1 раза в месяц, а лабораторные исследования функции печени или почек — не реже 1 раза в 1-2 месяца.
При применении по поводу псориаза не следует прерывать местное лечение заболевания. При передозировке рекомендуется применение кальция фолината (но не позднее, чем через 4 ч).
При проведении комбинированной противоопухолевой терапии следует соблюдать особую осторожность при одновременном применении метотрексата в высоких дозах с препаратами, оказывающими нефротоксическое действие (например, с цисплатином).
Не рекомендуют проводить вакцинацию пациентов и членов их семей.
С осторожностью следует сочетать метотрексат (даже в низких дозах) с ацетилсалициловой кислотой. В экспериментальных исследованиях установлено канцерогенное и мутагенное действие метотрексата.
Метотрексат в форме таблеток, лиофилизированного порошка для инъекций и раствора для инъекций включён в Перечень ЖНВЛС.
При одновременном применении с витаминными препаратами, содержащими фолиевую кислоту или её производные, возможно снижение эффективности метотрексата.
Одновременное применение НПВС в высоких дозах может привести к увеличению концентрации метотрексата в плазме и к удлинению периода его выведения, а также к увеличению концентрации метотрексата, не связанного с альбуминами плазмы, что, в свою очередь, усиливает токсические эффекты метотрексата (прежде всего на ЖКТ и систему кроветворения).
При одновременном применении с пенициллинами метотрексата (даже в низких дозах) возможно усиление его токсических эффектов.
При одновременном применении с сульфаниламидами, особенно с котримоксазолом, существует риск усиления миелодепрессивного действия.
При применении азота закиси у пациентов, получающих метотрексат, возможно развитие тяжелой непредсказуемой миелодепрессии, стоматита.
При одновременном применении с метотрексатом вальпроевой кислоты возможно уменьшение её концентрации в плазме крови.
Колестирамин связывает метотрексат, уменьшает его энтерогепатическую рециркуляцию, что приводит к снижению его концентрации в плазме крови.
При одновременном применении с меркаптопурином возможно повышение его биодоступности вследствие нарушения метаболизма при первом прохождении через печень.
Неомицин и паромомицин уменьшают абсорбцию метотрексата из ЖКТ.
У пациентов, получающих омепразол, возможно повышение концентрации метотрексата в плазме крови.
При одновременном применении с пробенецидом возможно 3—4-кратное увеличение концентрации метотрексата в плазме крови вследствие уменьшения его почечной экскреции.
При одновременном применении метотрексата с ретиноидами возможно повышение риска гепатотоксического действия.
Салицилаты потенцируют действие метотрексата вследствие уменьшения его почечной экскреции.
После курса лечения тетрациклином метотрексат, применяемый даже в низких дозах, может оказывать токсическое действие.
При последовательном введении метотрексата и фторурацила возможен синергизм действия; фторурацил, введённый перед метотрексатом, может уменьшать его токсичность.
Цисплатин оказывает нефротоксическое действие и поэтому может уменьшать почечную экскрецию метотрексата, что приводит к усилению его токсичности.
Возможно повышение токсичности при применении циклоспорина у пациентов, получавших метотрексат.

