Эозинофильный фасциит фото – Диффузный (эозинофильный) фасциит – симптомы болезни, профилактика и лечение Диффузного (эозинофильного) фасциита, причины заболевания и его диагностика на EUROLAB
Диффузный эозинофильный фасциит (болезнь Шульмана)
Диффузный эозинофильный фасциит (ДЭФ) — относительно редкое системное заболевание соединительной ткани с преимущественным поражением глубокой фасции (воспаление с исходом в фиброз), подкожной клетчатки и подлежащих мышц и дермы, сопровождающееся эозинофилией и гипергаммаглобулинемией.Как самостоятельная нозологическая форма заболевание выделено в 1974 г. L. Е. Shulman из склеродермической группы болезней. ДЭФ развивается преимущественно в возрасте 25-60 лет, хотя возможно возникновение заболевания в детском и пожилом возрасте. Мужчины болеют в 2 раза чаще, чем женщины.
Этиология и патогенез
Этиология и патогенез заболевания изучены недостаточно. Среди провоцирующих факторов, способствующих развитию ДЭФ, отмечают чрезмерную или необычную для больного физическую нагрузку (физическое перенапряжение), в частности поднятие тяжестей, спортивные перетренировки. Из других предшествующих факторов следует отметить переохлаждение, травмы, операции, нервно-психическое перенапряжение и стрессы. Предполагается также роль генетической предрасположенности. В патогенезе ДЭФ центральное место занимают иммунные нарушения, что подтверждается наличием гипергаммаглобулинемии, повышением содержания иммуноглобулинов, особенно иммуноглобулина G, циркулирующих иммунных комплексов и развитием иммунного воспаления в глубокой фасции и близлежащих тканях.
Клиника
Заболевание обычно начинается остро с возникновения характерных изменений в течение первого месяца (и даже недели), хотя возможно и постепенное начало с медленным прогрессированием заболевания. Начало болезни может совпадать с физическим перенапряжением.
В клинической картине преобладает уплотнение мягких тканей верхних и нижних конечностей, главным образом в области предплечий и голеней. Кисти и стопы при этом, как правило, не поражаются. Возможно распространение процесса на туловище, редко — на шею и лицо. Характерен симптом «апельсиновой корки» в виде мягких втяжений при максимальном натяжении кожи (при максимальном разгибании конечности). Могут также наблюдаться диффузная или очаговая гиперпигментация кожи в пораженных участках, кожный зуд, сухость и явления гиперкератоза.
Пораженные ткани отечны и напряжены. Несмотря на то, что кожные покровы над ними не вовлечены в процесс, кожа в этих участках выглядит сморщенной. При эозинофильном фасциите нередко развиваются сгибательные контрактуры локтевых и коленных суставов, редко — пальцев кистей. У части больных отмечаются полиартралгии.
Вовлечение внутренних органов не наблюдается. Специфические лабораторные изменения отсутствуют. Не присуща заболеванию и сосудистая патология, лишь изредка имеют место сосудистые нарушения в виде «стертого» синдрома Рейно. Тесты на ревматоидные факторы и антинуклеарные антитела обычно отрицательны. У некоторых больных выявляется значительная эозинофилия (до 50%). Увеличение числа эозинофилов обнаруживается и в участках воспаления.
Диагностика
Из лабораторных показателей диагностическим признаком болезни считается эозинофилия (до 50%). Периферическая и тканевая эозинофилия выявляется обычно в раннем периоде заболевания, а в дальнейшем может уменьшиться или полностью исчезнуть, особенно при назначении ГКС. Могут также наблюдаться: увеличение СОЭ, наличие СРБ, гиперα2– и γ-глобулинемия, повышение содержания в сыворотке крови серомукоида, фибриногена, церулоплазмина, иммуноглобулинов G и М, ЦИК, повышение титра антинуклеарных и ревматоидного факторов. Это отражает воспалительную и иммунологическую активность заболевания.
При морфологическом исследовании патологические изменения обнаруживаются преимущественно в фасциях и прилежащих тканях. В раннем периоде ДЭФ утолщенная и отечная фасция содержит набухшие коллагеновые волокна, инфильтрирована лимфоплазмоцитарными клетками, гистиоцитами и эозинофилами. Аналогичная инфильтрация выявляется в подкожной клетчатке, нижних слоях дермы и участках мышцы, прилегающих к фасции. В поздних стадиях наблюдается преобладание склероза и гиалиноза в фасции и прилегающих тканях, уменьшение или исчезновение клеточной инфильтрации и экссудативных процессов.
Диагноз ДЭФ основывается в первую очередь на сочетании характерных клинических (уплотнение тканей преимущественно в области предплечий и голеней с нарушением объема движений и развитием сгибательных контрактур) и лабораторных (эозинофилия, гипергаммаглобулинемии) признаков болезни. При постановке диагноза следует также учитывать связь с предшествующим физическим перенапряжением, преимущественное поражение мужчин и острое начало заболевания. Диагноз ДЭФ должен быть подтвержден морфологическим исследованием биоптатов фасции и прилежащих тканей.
Лечение
Лечение ДЭФ должно быть длительным и систематическим. Терапия более эффективна в раннем периоде болезни. Прежде всего назначаются кортикостероиды, главным образом преднизолон в начальной дозе 20-40 мг в сутки. После достижения клинического эффекта доза постепенно снижается до поддерживающей — 5-10 мг в сутки. В такой дозе преднизолон может применяться в течение многих месяцев и даже лет. Лечение стероидами может комбинироваться с НПВП (мелоксикам, диклофенак и др.) и аминохинолиновыми производными. При неэффективности гормонотерапии дополнительно назначаются иммуносупрессоры, преимущественно азатиоприн по 150 мг в сутки в течение нескольких месяцев.
Показано применение при ДЭФ антифиброзных средств, в частности тиоловых соединений и димексида.
Д-пеницилламин назначается по 450-600 мг в сутки, унитиол вводится внутримышечно ежедневно по 5-10 мл 5% раствора в течение 30-40 дней или методом суперэлектрофореза с димексидом (20-25 ежедневных сеансов на курс лечения). Используются также аппликации 50% раствора димексида.
Определенный клинический эффект оказывает используемая в последние годы карбогемосорбция. При невысокой активности патологического процесса проводится массаж и лечебная физкультура.
“Ревматология”
Т.Н. Бортная
ФАСЦИИТ ЭОЗИНОФИЛЬНЫЙ – это… Что такое ФАСЦИИТ ЭОЗИНОФИЛЬНЫЙ?
Диффузный (эозинофильный) фасциитД(Э)Ф-системное заболевание соединительной ткани с преимущественным поражением глубокой фасции (воспаление с исходом в фиброз), подкожной клетчатки и подлежащих мышц и дермы, сопровождающееся эозинофилией и гипергаммаглобулинемией. ЭФ был выделен в 1975 г. L. Е. Shulman из системной склеродермии как склеродер моподобный синдром.
Д(Э)Ф не изучен изза относительной редкости заболевания. Очевидно широкое распространение заболевания, поскольку по данным литературы известно более 100 наблюдений за больными из различных стран мира. В нашей стране первое описание ЭФ относится к 1978 г., всего описано 15 случаев. Среди заболевших ЭФ преобладают мужчины среднего возраста, но болеют дети и пожилые люди.
Изучена достаточно хорошо благодаря исследованию биоптата кожи, подлежащих тканей и мышц. Эпидермис и верхние слои дермы обычно нормальные, иногда утолщены, отечны.
В глубоких слоях дермы и в подкожной клетчатке по соединительнотканным прослойкам обнаруживаются периваскулярные гистиоцитарные инфильтраты с включением отдельных эозинофилов и развитием фиброза. Особенно значительные изменения обнаруживаются в фасции — она утолщена во много раз по сравнению с нормой, инфильтрирована большим количеством лимфоцитов и гистиоцитов с примесью плазматических клеток и эозинофилов.
В фасции определяются фибрино идные изменения коллагеновых волокон вплоть до фибриноид ного некроза. В последующем в фасции развивается фиброз.
Соединительнотканные прослойки с выраженными признаками воспалительной инфильтрации; иногда наблюдаются признаки повреждения мышечных волокон. В поздних стадиях болезни, при преобладании процессов склероза в пораженных тканях, дифференциальная диагностика с ССД затруднена.
Диффузный (эозинофильный) фасциитД(Э)Ф-системное заболевание соединительной ткани с преимущественным поражением глубокой фасции (воспаление с исходом в фиброз), подкожной клетчатки и подлежащих мышц и дермы, сопровождающееся эозинофилией и гипергаммаглобулинемией. ЭФ был выделен в 1975 г. L. Е. Shulman из системной склеродермии как склеродер моподобный синдром.
Д(Э)Ф не изучен изза относительной редкости заболевания. Очевидно широкое распространение заболевания, поскольку по данным литературы известно более 100 наблюдений за больными из различных стран мира. В нашей стране первое описание ЭФ относится к 1978 г., всего описано 15 случаев. Среди заболевших ЭФ преобладают мужчины среднего возраста, но болеют дети и пожилые люди.
Изучена достаточно хорошо благодаря исследованию биоптата кожи, подлежащих тканей и мышц. Эпидермис и верхние слои дермы обычно нормальные, иногда утолщены, отечны.
В глубоких слоях дермы и в подкожной клетчатке по соединительнотканным прослойкам обнаруживаются периваскулярные гистиоцитарные инфильтраты с включением отдельных эозинофилов и развитием фиброза. Особенно значительные изменения обнаруживаются в фасции — она утолщена во много раз по сравнению с нормой, инфильтрирована большим количеством лимфоцитов и гистиоцитов с примесью плазматических клеток и эозинофилов.
В фасции определяются фибрино идные изменения коллагеновых волокон вплоть до фибриноид ного некроза. В последующем в фасции развивается фиброз.
Соединительнотканные прослойки с выраженными признаками воспалительной инфильтрации; иногда наблюдаются признаки повреждения мышечных волокон. В поздних стадиях болезни, при преобладании процессов склероза в пораженных тканях, дифференциальная диагностика с ССД затруднена.
Что провоцирует Диффузный (эозинофильный) фасциит


Этиология и патогенез заболевания изучены недостаточно. В качестве провоцирующих факторов фигурируют чрезмерное охлаждение, физическое перенапряжение, например, ношение тяжестей, спортивные перетренировки, травмы.
Реже Д(Э)Ф развивается после острой инфекции или аллергической реакции. Возможно, играет роль генетическое предрасположение.
Например, М. Thibierge отмечает в семьях больных случаи очаговой склеродермии, РА, сахарного диабета.
Среди механизмов развития Д(Э)Ф значительное внимание уделяется иммунным нарушениям, что проявляется гипергамма глобулинемией и повышением содержания иммуноглобулинов, особенно IgG, циркулирующих иммунных комплексов и развитием иммунного по своей сути воспаления в глубокой фасции и близлежащих тканях.
S. J.

Wasserman и соавт. предложили оригинальную гипотезу патогенеза ЭФ, в соответствии с которой начальным звеном является антигенная альтерация наиболее пораженных при болезни тканей, включая мышцы, в результате чрезмерной физической нагрузки или другой причины с поступлением в очаг поражения эозинофилов, возможно, обусловленным лимфокинной и иммунокомплексной или специфической эозинофильной активностью.
Привлеченные в пораженные ткани фагоциты стимулируют развитие воспаления и фиброза, представляющих основные клинические проявления болезни. Интересна также концепция G.
Solomon и соавт. в основу которой положено преимущественное нарушение клеточного иммунитета, вовлечение субпопуляции Тлимфоцитов, обладающих Н2рецепторами.
Авторы получили удовлетворительный эффект от применения циметидина, являющегося антагонистом Н2рецепторов. Следовательно, вопросы этиологии патогенеза ЭФ еще не решены, однако особенностью болезни является избыточная эозинофилотаксическая активность, определяющаяся у большинства больных, а также нарушение функции Тсупрес соров.
Различные взаимоотношения основных патогенетических процессов определяют клинические особенности течения Д(Э)Ф.
Симптомы Диффузного (эозинофильного) фасциита
Клиническая картина характериуется уплотнением мягких тканей верхних и нижних конечностей с нарушением их двигательной активности, вплоть до развития сгибательных контрактур в различных суставах, преимущественно пальцев рук.
Один из наиболее ранних признаков болезни — появление чувства стягивания кожи в области верхних и (или) нижних конечностей, ощущение набухания и плотности, реже зуда. Почти одновременно отмечается ограничение движений в руках, слабость в ногах при подъеме по лестнице.
Характерно развитие уплотнения мягких тканей предплечий и (или) голеней, распространяющегося на плечи и бедра, появляющегося на протяжении нескольких месяцев или даже дней. Крайне редко умеренное уплотнение обнаруживается на шее, лице, животе или на туловище.
Уплотнения, как правило, неболезненны, хотя изредка больные жалуются на умеренные спонтанные боли в этих участках.
Структура кожи обычно не меняегся, ни в местах уплотнений становится натянутой, блестящей, изредка гиперпигментирован ной с признаками гиперкератоза. Характерен симптом «апельсиновой корки» в виде мягких втяжений при максимальном натяжении, т.е. максимальном разгибании конечности (на внутренней поверхности плеч, бедер).
У всех больных наблюдается ограничение активных движений в суставах конечностей изза их уплотнений, вплоть до развития стойких контрактур преимущественно в пальцах рук, реже в локтевых и коленных суставах.
Суставы не изменены, артриты не выявляются, но у ряда больных могут наблюдаться полиартралгии как проявление общей активности болезни. Значительно чаще больные жалуются на полимиалгию и мышечную слабость, хотя клинически признаки миозита не обнаруживаются.
Поражений внутренних органов, сосудистых расстройств, включая синдром Рейно, какихлибо нарушений трофики не отмечается, что и отличает ЭФ от ССД. Может быть непостоянный субфебрилитет.
Среди лабораторных показателей диагностическое значение имеет эозинофилия до 10-44 %, сопровождающаяся гипергам маглобулинемией. У 50 % больных увеличена СОЭ до 20- 30 мм/ч, реже до 50 мм/ч, отмечается повышение СРБ. В острой стадии болезни повышается содержание серомукоида, фибриногена, церулоплазмина у /з больных, но незначительно.
Изменения гуморального иммунитета нехарактерны. Чаще повышается количество IgG, реже выявляются ЦИК и крайне редко АНФ.
Диагностика Диффузного (эозинофильного) фасциита
Диагноз Д(Э)Ф труден при обнаружении характерных уплотнений на верхних и нижних конечностях, симптома «апельсиновой корки», ограничения движений вплоть до развития сгибательных контрактур. Диагностическое значение имеют гиперэозинофилия и гипергаммаглобулинемия.
Диагностическое значение имеет биопсия всего комплекса пораженных при Д(Э)Ф тканей: кожи, подкожной клетчатки, фасции, мышцы. При этом характерны патоморфологические изменения в фасции — значительное утолщение с признаками воспаления и фиброза.
Причины заболевания
Этиология эозинофильного фасциита неизвестна, но некоторые исследователи связывают это расстройство с аберрантным иммунным ответом. Кроме того, токсичные, экологические факторы, некоторые препарата, также могут быть причиной развития эозинофильного фасциита у некоторых лиц.
У некоторых людей с эозинофильным фасциитом также были обнаружены Borrelia burgdorferi, которые могут быть возможным возбудителем фасциита. Тем не менее, исследователям так и не удалось указать на связь между эозинофильным фасциитом и инфекцией Borrelia.
Borrelia можно определить путем прямого микроскопического исследования образцов тканей или с помощью полимеразной цепной реакции. Положительный ответ от проведения этих тестов может подтолкнуть клинициста к правильной диагностике эозинофильного фасциита.
В пробирке, анализ фибробластов из полученных на биопсии фасций может указать на повышенное производство мРНК коллагена типов I, III, и IV, по сравнению со смежными дермальными фибробластами. Кроме того, фасциальные фибробласты могут вырабатывать трансформирующий фактор роста бета-I и фактор роста соединительной ткани, которые могут быть основной причиной фиброза.
Дегрануляции эозинофилов могут привести к активации фибробластов.
Дальнейшее изучение эозинофильного фасциита может указать на повышенные уровни трансформирующего фактора роста-бета и интерлейкина 5, которые можно нормализовать кортикостероидной терапией. Другие исследования показывает, что фасциальные воспалительные инфильтраты в основном состоят из CD8 Т-лимфоцитов, макрофагов, эозинофилов, что свидетельствует о возможной цитотоксической иммунной реакции в ответ на наличие возможных инфекционных агентов или факторов из окружающей среды.
И совсем недавно, при проведении других исследований были обнаружены повышенные сывороточные уровни супероксиддисмутазы марганца и тканевого ингибитора металлопротеиназы (ТIMP-1). Уровни TIMP-1 в сыворотке могут также служить в качестве маркера тяжести заболевания.
Этиология и патогенез заболевания пока исследованы не так хорошо, чтобы уверенно говорить о причинах, но уже собрана достаточная база для определения провоцирующих факторов:
- переохлаждение;
- чрезмерные физические нагрузки, избыточные спортивные тренировки;
- травмы;
- последствия острой инфекции или аллергического состояния;
- воздействие токсинов;
- стрессы на фоне подверженности психосоматическим явлениям;
- генетическая предрасположенность.
Иммунные нарушения имеют серьезную значимость в механизмах развития этого синдрома. Об этом говорит как существенное повышение глобулинов класса G, так и тот факт, что воспалительные явления в глубоких фасциях и близлежащих тканях чаще всего имеют иммунную природу.
В последнее время появились убедительные гипотезы, основанные на различных аспектах аномального иммунного ответа организма на патогенные факторы, но процесс изучения еще далек от завершения.

Развитие патологии наиболее часто провоцируется переохлаждением и физическим перенапряжением. В данном случае болезнь может появиться вследствие получения травмы, усердных тренировок и ношения тяжестей. К более редким причинам относятся аллергические реакции и острые инфекции.
Возможно, присутствует генетическая предрасположенность. При выявлении механизмов развития болезни значительное внимание уделяется нарушениям работы иммунной системы.
До сих пор точно не установлено, почему развивается болезнь, но получилось выявить особенность заболевания, которая присутствовала у многих больных: избыточная эозинофилотаксическая активность.
Симптомы заболевания:
- Больные жалуются на чувство распирания в тканях. Уплотнения в основном выявляются в области голеней и предплечий. Присутствуют болевые ощущения в мышцах, подвижность ног и рук человека ограничена. В некоторых случаях больной испытывает слабость, у него повышается температура.
- В области предплечий и голеней обнаруживаются двусторонние симметричные уплотнения. Патологический процесс может протекать и в других частях тела (туловище, бедра, плечи). Шею и лицо он затрагивает очень редко.
- Иногда могут быть обнаружены: утолщение ладонного апоневроза, синдром карпального канала, теносиновит. Заболевание может сопровождаться сгибательными контрактурами в области суставов (в основном плечевых и локтевых), они могут сочетаться с гиперкератозом и гиперпигментацией кожи. В этих областях с внутренней стороны отмечаются изменения, которые внешне напоминают «апельсиновую корку», когда больной отводит руку в сторону, они более выражены.
- Хотя и очень редко, но возможны нарушения функционирования некоторых внутренних органов. Для их выявления необходима тщательная диагностика.
- Абсолютно у всех людей, которые находились под наблюдением, при заболевании диффузный фасциит симптомы, касающиеся общего состояния, присутствовали одинаковые: снижение массы тела, слабость, лихорадка (в основном с субфебрильной температурой).
К сожалению, выяснить причины этого заболевания пока не удалось. Возможно есть некоторая связь с большой постоянной физической нагрузкой, травмой, инфекцией или аллергией. Но всё же точно известно, что в основе патологического процесса лежит иммунное воспаление, которое приводит к поражению фасций, мышц, подкожной клетчатки и кожи.
Этиология и патогенез заболевания изучены недостаточно. В качестве провоцирующих факторов фигурируют чрезмерное охлаждение, физическое перенапряжение, например, ношение тяжестей, спортивные перетренировки, травмы.
Реже Д(Э)Ф развивается после острой инфекции или аллергической реакции. Возможно, играет роль генетическое предрасположение.
Например, М. Thibierge отмечает в семьях больных случаи очаговой склеродермии, РА, сахарного диабета.
Среди механизмов развития Д(Э)Ф значительное внимание уделяется иммунным нарушениям, что проявляется гипергамма глобулинемией и повышением содержания иммуноглобулинов, особенно IgG, циркулирующих иммунных комплексов и развитием иммунного по своей сути воспаления в глубокой фасции и близлежащих тканях.
S. J.
Wasserman и соавт. предложили оригинальную гипотезу патогенеза ЭФ, в соответствии с которой начальным звеном является антигенная альтерация наиболее пораженных при болезни тканей, включая мышцы, в результате чрезмерной физической нагрузки или другой причины с поступлением в очаг поражения эозинофилов, возможно, обусловленным лимфокинной и иммунокомплексной или специфической эозинофильной активностью.
Привлеченные в пораженные ткани фагоциты стимулируют развитие воспаления и фиброза, представляющих основные клинические проявления болезни. Интересна также концепция G.
Solomon и соавт. в основу которой положено преимущественное нарушение клеточного иммунитета, вовлечение субпопуляции Тлимфоцитов, обладающих Н2рецепторами.
Авторы получили удовлетворительный эффект от применения циметидина, являющегося антагонистом Н2рецепторов. Следовательно, вопросы этиологии патогенеза ЭФ еще не решены, однако особенностью болезни является избыточная эозинофилотаксическая активность, определяющаяся у большинства больных, а также нарушение функции Тсупрес соров.
Различные взаимоотношения основных патогенетических процессов определяют клинические особенности течения Д(Э)Ф.
Клиническая картина
Диффузный фасциит начинается чаще всего с ощущения набухания, распирания и уплотнения в предплечьях и голенях. Иногда отмечается слабость, ограничение в движениях и повышение температуры тела.
Если пациента осмотрит врач, то он без труда обнаруживает уплотнение предплечий и голеней, которое симметрично на обеих руках и ногах. Также возможно вовлечение в процесс и других частей тела – туловища и бёдер. Что же касается лица и шеи, то здесь воспаление отмечается довольно редко.
Как правило, кисти и стопы в патологию не вовлекаются, однако у некоторых пациентов могут быть диагностированы теносиновиты и синдром карпального канала. Также отмечается утолщение ладонного апоневроза.
В области плечевых и локтевых суставов выявляются контрактуры, возможна также гиперпигментация кожи и чрезмерное утолщение рогового слоя эпидермиса. При отведении рук в стороны можно увидеть и другие изменения кожи на внутренней стороне предплечий и плеч. Здесь она больше напоминает апельсиновую корку.
Причины и симптомы болезни
Эозинофильный фасциит имеет внезапное и болезненное начало развития, с последующим отеком ног и с образованием эритематозных площадей. Это расстройства прогрессирует быстро, в течение от нескольких недель до месяцев, у пациентов может развиться жесткость и уплотнение кожи, в результате чего могут развиться характерные контрактуры в сгибательных областях с нарушением подвижности суставов.
Предплечья, ноги, бедра и туловище страдают чаще всего (в порядке убывания по частоте). Целых 50% пациентов сообщают о том, что именно тяжелая физическая тренировка непосредственно предшествует началу болезни.
Недомогание, слабость и лихорадка часто присутствуют у большинства пациентов. В одном из исследований, проведенном в 2008 году, исследователи выяснили, что усталость была наиболее распространенным симптомом.
Боль и зуд также являются частыми жалобами, но они не так распространены как усталость. Из всех опрошенных пациентов, 62% имели сразу усталость, боль и зуд.
Явный артрит встречается у 40% больных.
Физическое обследование
Клиническая картина эозинофильного фасциита проходит через 3 этапа. Некоторые этапы могут присутствовать одновременно и в разных участках тела.
Первый этап представляет собой симметричную, диффузную эритематозную болезненность конечностей, с последующим переходом в отечную стадию, при которой развиваются специфические ямочки. Последний этап включает в себя развитие ряби на коже с участками гипопигментации, уплотнений и упругости.
В пострадавших областях, кожа и подкожные ткани сильно связаны друг с другом, у таких пациентов кожа будет тяжело оттягиваться. Хотя конечности страдают чаще всего (88%), у некоторых пациентов может также пострадать туловище.
- Контрактуры в локтях, запястье, лодыжках, коленях, плечах могут быть обнаружены у 55-75% больных.
- Кистевой туннельный синдром присутствует у 20% больных.
- Воспалительный артрит присутствует у целых 40% пациентов.
- Субклинический миозит присутствует у меньшинства пациентов.
- В отличие от склеродермии, явление Рейно, аномальные капилляры ногтевого валика и склеродактилия отсутствуют.
Клиническая картина характериуется уплотнением мягких тканей верхних и нижних конечностей с нарушением их двигательной активности, вплоть до развития сгибательных контрактур в различных суставах, преимущественно пальцев рук.
Один из наиболее ранних признаков болезни — появление чувства стягивания кожи в области верхних и (или) нижних конечностей, ощущение набухания и плотности, реже зуда. Почти одновременно отмечается ограничение движений в руках, слабость в ногах при подъеме по лестнице.
Характерно развитие уплотнения мягких тканей предплечий и (или) голеней, распространяющегося на плечи и бедра, появляющегося на протяжении нескольких месяцев или даже дней. Крайне редко умеренное уплотнение обнаруживается на шее, лице, животе или на туловище.
Уплотнения, как правило, неболезненны, хотя изредка больные жалуются на умеренные спонтанные боли в этих участках.
Структура кожи обычно не меняегся, ни в местах уплотнений становится натянутой, блестящей, изредка гиперпигментирован ной с признаками гиперкератоза. Характерен симптом «апельсиновой корки» в виде мягких втяжений при максимальном натяжении, т.е. максимальном разгибании конечности (на внутренней поверхности плеч, бедер).
У всех больных наблюдается ограничение активных движений в суставах конечностей изза их уплотнений, вплоть до развития стойких контрактур преимущественно в пальцах рук, реже в локтевых и коленных суставах.
Суставы не изменены, артриты не выявляются, но у ряда больных могут наблюдаться полиартралгии как проявление общей активности болезни. Значительно чаще больные жалуются на полимиалгию и мышечную слабость, хотя клинически признаки миозита не обнаруживаются.
Поражений внутренних органов, сосудистых расстройств, включая синдром Рейно, какихлибо нарушений трофики не отмечается, что и отличает ЭФ от ССД. Может быть непостоянный субфебрилитет.
Среди лабораторных показателей диагностическое значение имеет эозинофилия до 10-44 %, сопровождающаяся гипергам маглобулинемией. У 50 % больных увеличена СОЭ до 20- 30 мм/ч, реже до 50 мм/ч, отмечается повышение СРБ. В острой стадии болезни повышается содержание серомукоида, фибриногена, церулоплазмина у /з больных, но незначительно.
Изменения гуморального иммунитета нехарактерны. Чаще повышается количество IgG, реже выявляются ЦИК и крайне редко АНФ.
Диагностика болезни Шульмана
Лабораторные анализы
Трудно поставить диагноз, если выявлены только ограниченные движения, симптом «апельсиновой корки», уплотненные участки на конечностях. Диагностика возможна при обнаружении гипергаммаглобулинемии и гиперэозинофилии.
При постановке диагноза важны результаты биопсии всех пораженных тканей. Для заболевания характерно развитие патоморфологических изменений в фасциях — воспалительного процесса со значительным утолщением тканей и фиброзом.
Поскольку не все врачи обладают достаточной квалификацией, не всегда ставится правильный диагноз. Важно уметь отличить диффузный фасциит от других болезней, симптомы которых могут совпадать.
Диагноз Д(Э)Ф труден при обнаружении характерных уплотнений на верхних и нижних конечностях, симптома «апельсиновой корки», ограничения движений вплоть до развития сгибательных контрактур. Диагностическое значение имеют гиперэозинофилия и гипергаммаглобулинемия.
Диагностическое значение имеет биопсия всего комплекса пораженных при Д(Э)Ф тканей: кожи, подкожной клетчатки, фасции, мышцы. При этом характерны патоморфологические изменения в фасции — значительное утолщение с признаками воспаления и фиброза.
Трудности своевременного распознавания болезни Шульмана связаны, прежде всего, с редкой встречаемостью данной патологии в клинической практике. Тем не менее, все пациенты с подозрением на диффузный эозинофильный фасциит для верификации диагноза должны направляться к ревматологу. С целью исключения кожных заболеваний в начальной стадии может потребоваться консультация дерматолога.
Наряду с клиническими признаками, важную роль в подтверждении болезни Шульмана играют лабораторные показатели, а именно высокая эозинофилия, гиперα2- и γ-глобулинемия, увеличение СОЭ, фибриногена, серомукоида, церулоплазмина, IgG и IgМ, наличие СРБ, ЦИК и др. В единичных случаях отмечаются положительные антинуклеарные антитела, АНФ и ревматоидный фактор.
Решающее значение в диагностике болезни Шульмана принадлежит результатам биопсии кожи, мышц и мышечной фасции. Морфологические изменения в тканях характеризуются утолщением и отеком фасции, периваскулярным скоплением лимфоцитов, гистиоцитов и эозинофилов; в поздних стадиях – преобладанием явлений склероза и гиалиноза.
Дифференциальная диагностика болезни Шульмана проводится с дерматомиозитом, системной склеродермией, склередемой Бушке, фибромиозитом, тендовагинитом, ревматоидным артритом, аллергическим дерматитом и др..
Диагностика и лечение
Многие случаи эозинофильного фасциита реагируют на кортикостероиды (88%, из них 25% достигает полного ответа), хотя в некоторых случаях может произойти спонтанное излечение. Полное восстановление может занять до 1-3 лет. Лучший ответ достигается при введении высоких доз кортикостероидов, особенно если терапия иницируется на ранних этапах болезни.
В литературе также были обнаружены сообщения, что некоторые лица вообще не отвечали на кортикостероидную терапию и таким людям назначались дополнительные терапии.
Такие дополнительные лекарства включают гидроксихлорохин, колхицин, циметидин, циклоспорин, азатиоприн, метотрексат. Также, уже сегодня доступны новые препараты, которые можно использовать в качестве добавок к кортикостероидам или в качестве монотерапевтических средств. Эти препараты включают инфликсимаб, циклофосфамид, дапсона, ретиноидоподобный UVA1 и псорален плюс UVA (PUVA).
В одном из исследований, в которых принимали участия три человека с стероид-устойчивым эозинофильным фасциитом, все пациенты показали улучшение в уплотнении кожи и в тяжести контрактур суставов после применения инфликсимаба в дозе 3 мг/кг (на протяжении 8 недель).
Хирургическое вмешательство
Хирургическая декомпрессия кистевого туннельного синдрома может потребоваться для некоторых пациентов с эозинофильным фасциитом.
Лечение всех диффузных заболеваний соединительной ткани (ДЗСТ) является длительным комплексным процессом. Эозинофильный фасциит требует такого же подхода. Важно начать лечение как можно раньше, но в связи с проблемами диагностики начало адекватной терапии бывает запоздалым. В истории медицинских наблюдений описаны случаи самопроизвольного излечения больных, но надеяться на подобный исход не стоит.
Среди препаратов, показанных при лечении синдрома Шульмана, на первом месте находятся глюкокортикостероиды, из которых более часто применяется Преднизолон. Поскольку лечение осуществляется только специалистом, он определяет точную дозировку, длительность курса и режим терапии.
Обычно суточная доза препарата составляет 20–30 мг, но может быть повышена в 2 раза. На ранних этапах болезни эффективность высоких доз кортикостероидов оказывается максимальной.
Продолжительность курса преднизолона зависит от тяжести заболевания и обычно проходит в 2 этапа:
- до наступления первых признаков снижения активной фазы болезни дозировка поддерживается неизменной;
- после отмечаемого пациентом и врачом уменьшения интенсивности симптомов и улучшения состояния дозировка значительно уменьшается.
Длительность поддерживающей стероидной терапии может превышать несколько месяцев и даже лет. Применение препаратов группы НПВС (таких, как Анальгин, Ибупрофен, Диклофенак, Мовалис и др.) обычно неоправданно ввиду малой эффективности.
Восприимчивость больных к терапии Преднизолоном весьма высока (до 90%), но в случае отсутствия прогресса при лечении медикаментозное воздействие расширяют за счет цитостатиков, чаще всего из этой группы применяют Азатиоприн.
Это мощное средство, оказывающее не только цитостатическое, но и иммуносупресивное воздействие, а подавление иммунной реакции организма имеет важное значение в лечении всех заболеваний группы ДЗСТ.
На ранней стадии развития болезни лечение, для реализации которого применяются медикаменты, может привести к получению некоторых положительных изменений. Но поскольку заболевание часто выявляется несвоевременно, лечение является запоздалым и такие методы оказываются недостаточно эффективными.
Состояние пациента требует длительного лечения, которое состоит из комплекса процедур. При выявлении болезни на последней стадии лечение может быть многолетним, и не всегда полученный результат будет положительным.
Известно, что при диффузном фасциите наиболее выражены признаки воспалительного процесса. Обнаруженное воспаление требует применения ГКС, обычно по 20-30 мг Преднизолона каждые сутки, намного реже — по 60-70 мг.
Данный метод позволяет снизить выраженность воспаления. Количество лекарственного средства постепенно снижают, применяя поддерживающую дозу в течение длительного времени (обычно от нескольких месяцев до 8 лет).
Терапия редко оказывается эффективной. Если не удалось достичь необходимого результата, больному назначают цитостатики. Наиболее часто врачи применяют Азатиоприн в дозировке 150 мг/сутки. Лечение препаратом производится на протяжении нескольких месяцев.
Может применяться местная терапия, направленная на устранение воспаления и прекращение фиброза. Если эффективность лечения снижается, пациенту назначается массаж и ЛФК. При торпидном течении болезни, когда отсутствует эффективность терапии, рекомендуется гемосорбция.
Если патологию удалось выявить на ранней стадии, показано лечение с использованием Циметидина (1000 мг в сутки) и Преднизолона (0,35-0,5 мг в сутки).
Чем раньше начато лечение, тем эффективнее оно проходит. Если болезнь выявлена своевременно, при этом пациенту было оказано систематическое лечение, за 1 год могут произойти значительные улучшения. При позднем обнаружении болезни прогноз более печальный.
Симптомы диффузного фасциита требуют длительного и систематического лечения. Самая эффективная терапия в самом начале развития заболевания. Здесь на первый план в лечении выступают кортикостероиды. Препаратом выбора становится преднизолон в первоначальной дозе 20 – 40 мг в течении суток.
После того, как нужный положительный эффект будет достигнут, дозу постепенно снижают и оставляют на уровне поддерживающей, которая составляет около 5 – 10 мг в сутки. Такая доза назначается пациенту на протяжении длительного периода – месяцы, и даже годы.
Терапия кортикостероидами может совмещаться с приёмом нестероидных противовоспалительных препаратов, например, мелоксикама, диклофенака и многих других. Также к лечению подключают аминохинолиновые производные — делагил, резохин, хингамин, плаквенил.
При отсутствии лечения, что часто наблюдается на позднем этапе заболевания, назначаются препараты из группы иммуносупрессоров. Преимущественно это азатиоприн в дозировке 150 мг в сутки. Принимается препарат на протяжении нескольких месяцев.
Среди других препаратов:
- Д-пеницилламин по 40 – 600 мг в сутки;
- Унитиол по 5 – 10 мг внутримышечно;
- Аппликации с димексидом;
- Электрофорез с димексидом и унитиолом;
В некоторых случаях хороший клинический эффект может дать процедура карбогемосорбции. При этом такой экстракорпоральный метод гемокоррекции помогает вывести из крови пациента токсические соединения, как эндогенной, так и экзогенной природы.
При начальном этапе заболевания свою эффективность доказали регулярный массаж и лечебная физкультура.
Лекарственные средства эффективны в раннем периоде болезни, однако нередко постепенное развитие процесса приводит к несвоевременному распознаванию и запоздалому лечению. Как и при других заболеваниях из группы ДБСТ, при ЭФ необходимо длительное, нередко многолетнее, комплексное лечение.
Поскольку на первое место в клинической картине болезни выступают признаки воспалительной активности, наиболее показаны ГКС, главным образом преднизолон по 20-30 мг/сут, реже больше (60-70 мг/сут). В подавляющих дозах преднизолон назначают до снижения активности процесса, уменьшения субъективных и объективных признаков болезни.
В дальнейшем дозу преднизолона постепенно снижают до поддерживающей, которую нередко приходится назначать в течение многих месяцев и даже лет (до 8 лет, по данным Н. Г.
Гусевой и соавт.
Терапия НПВП обычно неэффективна.
При неэффективности лечения ГКС дополнительно назначают цитостатики, преимущественно азатиоприн по 150 мг/сут в течение нескольких месяцев, а при развитии фиброза — Dпени цилламин до 450-600 мг/сут. Длительность приема препаратов определяется наличием воспалительных, иммунных или фиброзных изменений.
В качестве местной противовоспалительной и антифиброзирующей терапии в комплексе лечения включаются курсы аппликаций ДМСО (50 %), фонофореза трилона Б на пораженные области. При снижении активности процесса проводятся ЛФК, курсы массажа.
При торпидном течении болезни и неэффективности терапии, по данным Н. Г. Гусевой и соавт., рекомендуется гемо сорбция. Возможно, что экстракорпоральная терапия показана и в более ранние сроки болезни в связи с повышением активности эозинофилотаксического фактора.
По данным S. Herson и соавт., на ранних стадиях болезни следует назначать преднизолон по 0,35-0,6 мг/кг в сочетании с циметидином в дозе до 1000 мг/сут в качестве бло катора Н2рецепторов.
Таким образом, эффективность лечения зависит от сроков его начала. При раннем распознавании и систематическом лечении почти у всех больных к концу 1го года развивается значительное улучшение состояния или клиническая ремиссия. Однако при позднем распознавании и развитии фиброза результаты лечения намного хуже.
Терапия болезни Шульмана наиболее эффективна при раннем выявлении заболевания; при этом лечение должно быть длительным, систематическим и комплексным. С целью купирования воспалительной активности назначаются глюкокортикостероиды (преднизолон), иногда в комбинации с НПВП, блокаторами Н-рецепторов (циметидином).
Дополнительно может потребоваться лечение цитостатиками (азатиоприном), а при развитии фиброза – Д-пеницилламином. При упорном и тяжелом течении болезни Шульмана применяется гемосорбция.
Местная противовоспалительная и антифиброзирующая терапия включает аппликации димексида, ультрафонофорез динатриевой соли этилендиаминтетрауксусной кислоты. Вне обострения болезни Шульмана добавляются курсы массажа и ЛФК, диатермии, теплых лечебных ванн.
В результате своевременно начатой и патогенетически обоснованной терапии к концу первого года лечения у большинства пациентов отмечается улучшение состояния или достижение клинической ремиссии. В литературе описаны случаи спонтанной регрессии болезни Шульмана.
Однако встречаются и менее благоприятные варианты диффузного эозинофильного фасциита с упорным течением и развитием стойких остаточных контрактур.
Лечение и прогноз при болезни Шульмана
Конечная стадия фиброзного процесса приводит к развитию существенных проблем из-за склероза кожи и контрактур суставов. Кроме того, артрит, невропатии, дерматомиозит также могут присутствовать у некоторых пациентов.
У 10% пациентов может развиться миелодисплазия, например апластическая анемия, которая предвещает плохой прогноз. Однако, в некоторых случаях возможно спонтанное выздоровление, а если оно и не произойдет, то лечение кортикостероидами или другими, уже описанными агентами, сможет привести к восстановлению.
В целом, прогноз для пациентов с эозинофильным фасциитом хороший. Большинство пациентов могут ожидать на частичное или полное выздоровление.
redkie-bolezni.com
Фасциит — воспалительное заболевание соединительной ткани, окружающей мышцы, нервы и сосуды (фасции). Эозинофильный фасциит (синдром Шульмана) является одной из форм этой патологии и относится к диффузным заболеваниям соединительной ткани.
Полное название синдрома — диффузный эозинофильный фасциит. В отличие от других заболеваний этой категории он ограничивается проявлениями на руках и ногах больного.
До середины 70-х годов ХХ века не существовало отдельного описания этой патологии, пока ревматолог Л.Шульман не охарактеризовал его в качестве нового синдрома. Точных данных о распространении этого заболевания нет, но оно считается редким. Подробных описаний течения болезни существует немногим более сотни. Отмечается поражение лиц мужского пола, женщины болеют примерно в 2 раза реже.
Диффузный (эозинофильный) фасциит – описание болезни
Диффузный (эозинофильный) фасциитД(Э)Ф-системное заболевание соединительной ткани с преимущественным поражением глубокой фасции (воспаление с исходом в фиброз), подкожной клетчатки и подлежащих мышц и дермы, сопровождающееся эозинофилией и гипергаммаглобулинемией. ЭФ был выделен в 1975 г. L. Е. Shulman из системной склеродермии как склеродер моподобный синдром.
- Эпидемиология
Д(Э)Ф не изучен изза относительной редкости заболевания. Очевидно широкое распространение заболевания, поскольку по данным литературы известно более 100 наблюдений за больными из различных стран мира. В нашей стране первое описание ЭФ относится к 1978 г., всего описано 15 случаев. Среди заболевших ЭФ преобладают мужчины среднего возраста, но болеют дети и пожилые люди.
- Патоморфология
Изучена достаточно хорошо благодаря исследованию биоптата кожи, подлежащих тканей и мышц. Эпидермис и верхние слои дермы обычно нормальные, иногда утолщены, отечны. В глубоких слоях дермы и в подкожной клетчатке по соединительнотканным прослойкам обнаруживаются периваскулярные гистиоцитарные инфильтраты с включением отдельных эозинофилов и развитием фиброза. Особенно значительные изменения обнаруживаются в фасции – она утолщена во много раз по сравнению с нормой, инфильтрирована большим количеством лимфоцитов и гистиоцитов с примесью плазматических клеток и эозинофилов. В фасции определяются фибрино идные изменения коллагеновых волокон вплоть до фибриноид ного некроза. В последующем в фасции развивается фиброз. Соединительнотканные прослойки с выраженными признаками воспалительной инфильтрации; иногда наблюдаются признаки повреждения мышечных волокон. В поздних стадиях болезни, при преобладании процессов склероза в пораженных тканях, дифференциальная диагностика с ССД затруднена.
Возникновение болезни Диффузный (эозинофильный) фасциит
Этиология и патогенез заболевания изучены недостаточно. В качестве провоцирующих факторов фигурируют чрезмерное охлаждение, физическое перенапряжение, например, ношение тяжестей, спортивные перетренировки, травмы. Реже Д(Э)Ф развивается после острой инфекции или аллергической реакции. Возможно, играет роль генетическое предрасположение. Например, М. Thibierge отмечает в семьях больных случаи очаговой склеродермии, РА, сахарного диабета.
Среди механизмов развития Д(Э)Ф значительное внимание уделяется иммунным нарушениям, что проявляется гипергамма глобулинемией и повышением содержания иммуноглобулинов, особенно IgG, циркулирующих иммунных комплексов и развитием иммунного по своей сути воспаления в глубокой фасции и близлежащих тканях. S. J. Wasserman и соавт. предложили оригинальную гипотезу патогенеза ЭФ, в соответствии с которой начальным звеном является антигенная альтерация наиболее пораженных при болезни тканей, включая мышцы, в результате чрезмерной физической нагрузки или другой причины с поступлением в очаг поражения эозинофилов, возможно, обусловленным лимфокинной и иммунокомплексной или специфической эозинофильной активностью. Привлеченные в пораженные ткани фагоциты стимулируют развитие воспаления и фиброза, представляющих основные клинические проявления болезни. Интересна также концепция G. Solomon и соавт., в основу которой положено преимущественное нарушение клеточного иммунитета, вовлечение субпопуляции Тлимфоцитов, обладающих Н2рецепторами. Авторы получили удовлетворительный эффект от применения циметидина, являющегося антагонистом Н2рецепторов. Следовательно, вопросы этиологии патогенеза ЭФ еще не решены, однако особенностью болезни является избыточная эозинофилотаксическая активность, определяющаяся у большинства больных, а также нарушение функции Тсупрес соров. Различные взаимоотношения основных патогенетических процессов определяют клинические особенности течения Д(Э)Ф.
Симптомы болезни Диффузный (эозинофильный) фасциит
Клиническая картина характериуется уплотнением мягких тканей верхних и нижних конечностей с нарушением их двигательной активности, вплоть до развития сгибательных контрактур в различных суставах, преимущественно пальцев рук.
Один из наиболее ранних признаков болезни – появление чувства стягивания кожи в области верхних и (или) нижних конечностей, ощущение набухания и плотности, реже зуда. Почти одновременно отмечается ограничение движений в руках, слабость в ногах при подъеме по лестнице. Характерно развитие уплотнения мягких тканей предплечий и (или) голеней, распространяющегося на плечи и бедра, появляющегося на протяжении нескольких месяцев или даже дней. Крайне редко умеренное уплотнение обнаруживается на шее, лице, животе или на туловище. Уплотнения, как правило, неболезненны, хотя изредка больные жалуются на умеренные спонтанные боли в этих участках.
Структура кожи обычно не меняегся, ни в местах уплотнений становится натянутой, блестящей, изредка гиперпигментирован ной с признаками гиперкератоза. Характерен симптом «апельсиновой корки» в виде мягких втяжений при максимальном натяжении, т. е. максимальном разгибании конечности (на внутренней поверхности плеч, бедер). У всех больных наблюдается ограничение активных движений в суставах конечностей изза их уплотнений, вплоть до развития стойких контрактур преимущественно в пальцах рук, реже в локтевых и коленных суставах.
Суставы не изменены, артриты не выявляются, но у ряда больных могут наблюдаться полиартралгии как проявление общей активности болезни. Значительно чаще больные жалуются на полимиалгию и мышечную слабость, хотя клинически признаки миозита не обнаруживаются.
Поражений внутренних органов, сосудистых расстройств, включая синдром Рейно, какихлибо нарушений трофики не отмечается, что и отличает ЭФ от ССД. Может быть непостоянный субфебрилитет.
Среди лабораторных показателей диагностическое значение имеет эозинофилия до 10-44 %, сопровождающаяся гипергам маглобулинемией. У 50 % больных увеличена СОЭ до 20- 30 мм/ч, реже до 50 мм/ч, отмечается повышение СРБ. В острой стадии болезни повышается содержание серомукоида, фибриногена, церулоплазмина у /з больных, но незначительно.
Изменения гуморального иммунитета нехарактерны. Чаще повышается количество IgG, реже выявляются ЦИК и крайне редко АНФ.
Диагностика болезни Диффузный (эозинофильный) фасциит
Диагноз Д(Э)Ф труден при обнаружении характерных уплотнений на верхних и нижних конечностях, симптома «апельсиновой корки», ограничения движений вплоть до развития сгибательных контрактур. Диагностическое значение имеют гиперэозинофилия и гипергаммаглобулинемия.
Диагностическое значение имеет биопсия всего комплекса пораженных при Д(Э)Ф тканей: кожи, подкожной клетчатки, фасции, мышцы. При этом характерны патоморфологические изменения в фасции – значительное утолщение с признаками воспаления и фиброза.
Однако в связи с недостаточной квалификацией врачи нередко ошибочно ставят неправильный диагноз (ССД, дермато миозит или фибромиозит, тендовагинит, РА и др.). По данным Н. Г. Гусевой и соавт., только 2 из 10 больных были направлены в клинику с правильным диагнозом Д(Э)Ф. Таким образом, в первую очередь Д(Э)Ф следует дифференцировать с ССД и склеродермоподобными синдромами.
ССД отличается от Д(Э)Ф наличием синдрома Рейно, плотным отеком пальцев рук и кистей, дилатацией пищевода, поражением легких по типу базального пневмофиброза и развитием других висцеритов. В то же время нужно иметь в виду возможность сочетания ССД и Д(Э)Ф.
Склеродерма Бушке отличается от Д(Э)Ф развитием плотного отека верхней части туловища и проксимальных отделов конечностей, отсутствием характерных для ЭФ морфологических изменений фасции в области поражения.
Отсутствие миозита, дерматита и артрита позволяет отличить Д(Э)Ф от дерматомиозита и РА. Для тендовагинита характерно локальное несимметричное поражение того или иного сухожилия, в то время как при ЭФ процесс всегда симметричный с присущими ему внешними изменениями тканей и эозинофи лией.
Наличие плотного симметричного отека и характерного био птата позволяет отличить ЭФ от гиперэозинофилии различного происхождения.
Лечение болезни Диффузный (эозинофильный) фасциит
Лекарственные средства эффективны в раннем периоде болезни, однако нередко постепенное развитие процесса приводит к несвоевременному распознаванию и запоздалому лечению. Как и при других заболеваниях из группы ДБСТ, при ЭФ необходимо длительное, нередко многолетнее, комплексное лечение.
Поскольку на первое место в клинической картине болезни выступают признаки воспалительной активности, наиболее показаны ГКС, главным образом преднизолон по 20-30 мг/сут, реже больше (60-70 мг/сут). В подавляющих дозах преднизолон назначают до снижения активности процесса, уменьшения субъективных и объективных признаков болезни. В дальнейшем дозу преднизолона постепенно снижают до поддерживающей, которую нередко приходится назначать в течение многих месяцев и даже лет (до 8 лет, по данным Н. Г. Гусевой и соавт.
Терапия НПВП обычно неэффективна.
При неэффективности лечения ГКС дополнительно назначают цитостатики, преимущественно азатиоприн по 150 мг/сут в течение нескольких месяцев, а при развитии фиброза – Dпени цилламин до 450-600 мг/сут. Длительность приема препаратов определяется наличием воспалительных, иммунных или фиброзных изменений.
В качестве местной противовоспалительной и антифиброзирующей терапии в комплексе лечения включаются курсы аппликаций ДМСО (50 %), фонофореза трилона Б на пораженные области. При снижении активности процесса проводятся ЛФК, курсы массажа.
При торпидном течении болезни и неэффективности терапии, по данным Н. Г. Гусевой и соавт., рекомендуется гемо сорбция. Возможно, что экстракорпоральная терапия показана и в более ранние сроки болезни в связи с повышением активности эозинофилотаксического фактора.
По данным S. Herson и соавт., на ранних стадиях болезни следует назначать преднизолон по 0,35-0,6 мг/кг в сочетании с циметидином в дозе до 1000 мг/сут в качестве бло катора Н2рецепторов.
Таким образом, эффективность лечения зависит от сроков его начала. При раннем распознавании и систематическом лечении почти у всех больных к концу 1го года развивается значительное улучшение состояния или клиническая ремиссия. Однако при позднем распознавании и развитии фиброза результаты лечения намного хуже.
Профилактика болезни Диффузный (эозинофильный) фасциит
Первичная профилактика не разработана. Вторичная профилактика обострении связана с систематичностью проводимой комплексной терапии.
К каким докторам следует обращаться при болезни Диффузный (эозинофильный) фасциит
Ревматолог
Диффузный фасциит: симптомы и лечение
При заболевании диффузный фасциит симптомы и признаки, выявленные в ходе врачебного осмотра, позволяют подобрать наиболее эффективные методы лечения. Диффузный (эозинофильный) фасциит – редкая болезнь, затрагивающая соединительную ткань. В данный процесс вовлекается преимущественно подкожная жировая клетчатка и околомышечные фасции.

Обычно заболевание развивается после тяжелой физической нагрузки, которой человек был подвержен за несколько недель, дней или часов до нарушения состояния здоровья.
Развитию диффузного фасциита подвержены люди разного возраста.
Эпидемиология и патоморфология заболевания
Эпидемиология мало изучена по той причине, что болезнь принадлежит к редко возникающим заболеваниям. Данные медицинской литературы свидетельствуют о том, что под наблюдением врачей находилось больше 100 человек, проживающих в разных странах.
Первые описания болезни в нашей стране (15 случаев) были произведены в 1978 году. Среди больных были разные люди, но в основном мужчины среднего возраста.
 Патоморфологию удалось изучить достаточно хорошо. Для получения информации был исследован биоптат мышц, кожи и подлежащих тканей. Эпидермис и верхние слои дермы обычно находились в нормальном состоянии, иногда наблюдалась незначительная отечность и небольшое утолщение.
Патоморфологию удалось изучить достаточно хорошо. Для получения информации был исследован биоптат мышц, кожи и подлежащих тканей. Эпидермис и верхние слои дермы обычно находились в нормальном состоянии, иногда наблюдалась незначительная отечность и небольшое утолщение.
В соединительных участках подкожной клетчатки и дермы, расположенной более глубоко, присутствовали периваскулярные гистиоцитарные инфильтраты, включающие отдельные эозинофилы.
Кроме того, отмечалось развитие фиброза. Больше изменений было обнаружено именно в фасции. Разрушение коллагеновых волокон приводило к фибриноидному некрозу и фиброзу.
У некоторых больных были повреждены мышечные волокна. Диагностика заболевания на поздних стадиях, когда в пораженных тканях развились процессы склероза, затруднена.
Вернуться к оглавлению
Причины и симптомы болезни
Развитие патологии наиболее часто провоцируется переохлаждением и физическим перенапряжением. В данном случае болезнь может появиться вследствие получения травмы, усердных тренировок и ношения тяжестей. К более редким причинам относятся аллергические реакции и острые инфекции.
Возможно, присутствует генетическая предрасположенность. При выявлении механизмов развития болезни значительное внимание уделяется нарушениям работы иммунной системы.

Симптомы заболевания:
- Больные жалуются на чувство распирания в тканях. Уплотнения в основном выявляются в области голеней и предплечий. Присутствуют болевые ощущения в мышцах, подвижность ног и рук человека ограничена. В некоторых случаях больной испытывает слабость, у него повышается температура.
- В области предплечий и голеней обнаруживаются двусторонние симметричные уплотнения. Патологический процесс может протекать и в других частях тела (туловище, бедра, плечи). Шею и лицо он затрагивает очень редко.
- Иногда могут быть обнаружены: утолщение ладонного апоневроза, синдром карпального канала, теносиновит. Заболевание может сопровождаться сгибательными контрактурами в области суставов (в основном плечевых и локтевых), они могут сочетаться с гиперкератозом и гиперпигментацией кожи. В этих областях с внутренней стороны отмечаются изменения, которые внешне напоминают «апельсиновую корку», когда больной отводит руку в сторону, они более выражены.
- Хотя и очень редко, но возможны нарушения функционирования некоторых внутренних органов. Для их выявления необходима тщательная диагностика.
- Абсолютно у всех людей, которые находились под наблюдением, при заболевании диффузный фасциит симптомы, касающиеся общего состояния, присутствовали одинаковые: снижение массы тела, слабость, лихорадка (в основном с субфебрильной температурой).
Вернуться к оглавлению
Диагностика и лечение
 Трудно поставить диагноз, если выявлены только ограниченные движения, симптом «апельсиновой корки», уплотненные участки на конечностях. Диагностика возможна при обнаружении гипергаммаглобулинемии и гиперэозинофилии.
Трудно поставить диагноз, если выявлены только ограниченные движения, симптом «апельсиновой корки», уплотненные участки на конечностях. Диагностика возможна при обнаружении гипергаммаглобулинемии и гиперэозинофилии.
При постановке диагноза важны результаты биопсии всех пораженных тканей. Для заболевания характерно развитие патоморфологических изменений в фасциях – воспалительного процесса со значительным утолщением тканей и фиброзом.
Поскольку не все врачи обладают достаточной квалификацией, не всегда ставится правильный диагноз. Важно уметь отличить диффузный фасциит от других болезней, симптомы которых могут совпадать.
Вернуться к оглавлению
Лечение заболевания
На ранней стадии развития болезни лечение, для реализации которого применяются медикаменты, может привести к получению некоторых положительных изменений. Но поскольку заболевание часто выявляется несвоевременно, лечение является запоздалым и такие методы оказываются недостаточно эффективными.
Состояние пациента требует длительного лечения, которое состоит из комплекса процедур. При выявлении болезни на последней стадии лечение может быть многолетним, и не всегда полученный результат будет положительным.
 Известно, что при диффузном фасциите наиболее выражены признаки воспалительного процесса. Обнаруженное воспаление требует применения ГКС, обычно по 20-30 мг Преднизолона каждые сутки, намного реже – по 60-70 мг.
Известно, что при диффузном фасциите наиболее выражены признаки воспалительного процесса. Обнаруженное воспаление требует применения ГКС, обычно по 20-30 мг Преднизолона каждые сутки, намного реже – по 60-70 мг.
Данный метод позволяет снизить выраженность воспаления. Количество лекарственного средства постепенно снижают, применяя поддерживающую дозу в течение длительного времени (обычно от нескольких месяцев до 8 лет).
Терапия редко оказывается эффективной. Если не удалось достичь необходимого результата, больному назначают цитостатики. Наиболее часто врачи применяют Азатиоприн в дозировке 150 мг/сутки. Лечение препаратом производится на протяжении нескольких месяцев.
Может применяться местная терапия, направленная на устранение воспаления и прекращение фиброза. Если эффективность лечения снижается, пациенту назначается массаж и ЛФК. При торпидном течении болезни, когда отсутствует эффективность терапии, рекомендуется гемосорбция.
Если патологию удалось выявить на ранней стадии, показано лечение с использованием Циметидина (1000 мг в сутки) и Преднизолона (0,35-0,5 мг в сутки).
Чем раньше начато лечение, тем эффективнее оно проходит. Если болезнь выявлена своевременно, при этом пациенту было оказано систематическое лечение, за 1 год могут произойти значительные улучшения. При позднем обнаружении болезни прогноз более печальный.
Диффузный эозинофильный фасциит – ФГБНУ НИИР им. В.А. Насоновой
Диффузный эозинофильный фасциит
Что такое диффузный эозинофильный фасциит?
Диффузный эозинофильный фасциит (ДЭФ), или болезнь Шульмана, склеродермоподобное заболевание, характеризующееся уплотнением верхних и нижних конечностей, преимущественно предплечий и голеней, часто сопровождающееся увеличением эозинофилов в периферической крови (эозинофилия).
ДЭФ встречается чаще у мужчин, в возрасте 26-60 лет. Выявлена четкая связь с чрезмерной или необычной физической нагрузкой.
В Институт ревматологии имени В.А. Насоновой обеспечивается системный подход к диагностике и терапии данного заболевания, накоплен большой опыт дифференциальной диагностики с другими заболеваниями склеродермической группы.
Симптомы
Основными признаками ДЭФ являются:
-
Связь с предшествующим физическим перенапряжением.
-
Острое начало с двусторонним симметричным уплотнением тканей преимущественно в области предплечий и голеней, а иногда и всех конечностей, исключая кисти, с ограничением движений; может уплотняться живот.
-
Развитие сгибательных контрактур, преимущественно локтевых и голеностопных суставов, иногда и суставов кистей.
-
Поражение кожи по типу «апельсиновой корки».
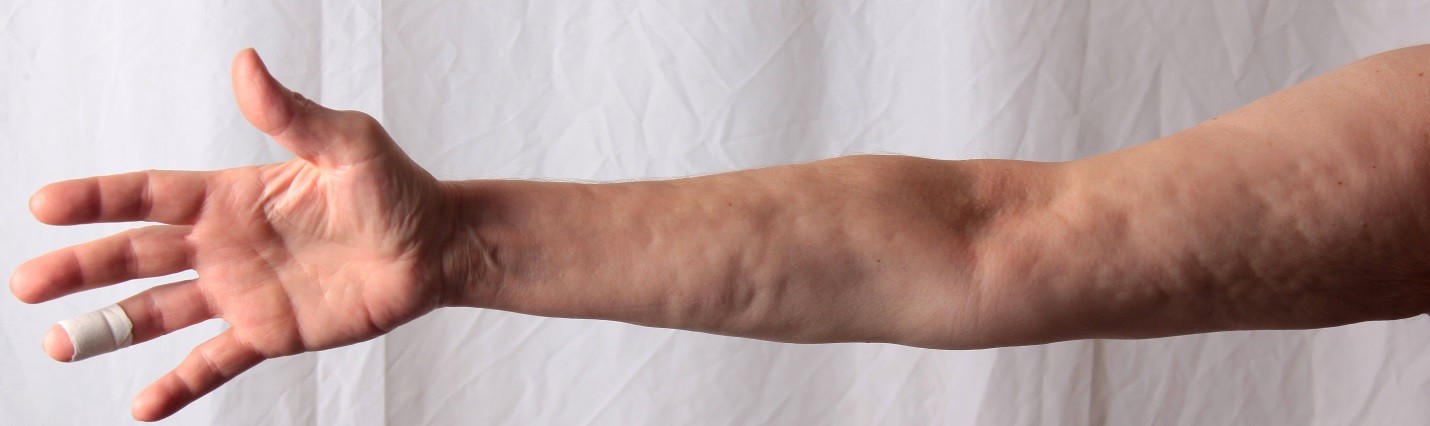
Зачем нужна консультация ревматолога?
Несмотря на четкую клинико-лабораторную картину заболевания, диагноз ДЭФ устанавливается поздно и нередко ошибочно, что ухудшает его прогноз.
Во время приема врач-ревматолог тщательно соберет анамнез заболевания, изучит имеющуюся медицинскую документацию, проведёт осмотр и ответит на все вопросы, касающиеся данного заболевания, назначит дополнительные лабораторные и инструментальные обследования, а при необходимости – биопсию фасции поврежденной области. После подтверждения диагноза врач обсудит с вами доступные возможности терапии.
Насколько эффективно лечение ДЭФ?
При своевременной диагностике и рано начатой терапии ДЭФ успешно лечится глюкокортикоидами и антифиброзными препаратами вплоть до полного исчезновения патологической симптоматики. Терапия должна быть длительной (не менее года), осуществляться под наблюдением врача-ревматолога.
Специалисты, занимающиеся диагностикой и лечением в институте: сотрудники лаборатории микроциркуляции и воспаления
Запишитесь на приём к специалисту по телефону +7 495 109-29-10 доб. 1, 2; +7 495 109-39-99
Диффузный эозинофильный фасциит — Боли в ногах
Рђ Р‘ Р’ Р“ Р” Р– Р— Р™ Рљ Р› Рњ Рќ Рћ Рџ Р РЎ Рў РЈ Р¤ РҐ Р¦ Р§ РЁ Р Р® РЇ
- Что такое Диффузный (эозинофильный) фасциит
- Что провоцирует Диффузный (эозинофильный) фасциит
- Симптомы Диффузного (эозинофильного) фасциита
- Диагностика Диффузного (эозинофильного) фасциита
- Лечение Диффузного (эозинофильного) фасциита
- Профилактика Диффузного (эозинофильного) фасциита
- К каким докторам следует обращаться если у Вас Диффузный (эозинофильный) фасциит
Что такое Диффузный (эозинофильный) фасциит
Диффузный (эозинофильный) фасциитД(Э)Ф-системное заболевание соединительной ткани с преимущественным поражением глубокой фасции (воспаление с исходом в фиброз), подкожной клетчатки и подлежащих мышц и дермы, сопровождающееся эозинофилией и гипергаммаглобулинемией. ЭФ был выделен в 1975 г. L. Е. Shulman из системной склеродермии как склеродер моподобный синдром.
- Эпидемиология
Д(Э)Ф не изучен изза относительной редкости заболевания. Очевидно широкое распространение заболевания, поскольку по данным литературы известно более 100 наблюдений за больными из различных стран мира. В нашей стране первое описание ЭФ относится к 1978 г., всего описано 15 случаев. Среди заболевших ЭФ преобладают мужчины среднего возраста, но болеют дети и пожилые люди.
- Патоморфология
Изучена достаточно хорошо благодаря исследованию биоптата кожи, подлежащих тканей и мышц. Эпидермис и верхние слои дермы обычно нормальные, иногда утолщены, отечны. В глубоких слоях дермы и в подкожной клетчатке по соединительнотканным прослойкам обнаруживаются периваскулярные гистиоцитарные инфильтраты с включением отдельных эозинофилов и развитием фиброза. Особенно значительные изменения обнаруживаются в фасции — она утолщена во много раз по сравнению с нормой, инфильтрирована большим количеством лимфоцитов и гистиоцитов с примесью плазматических клеток и эозинофилов. В фасции определяются фибрино идные изменения коллагеновых волокон вплоть до фибриноид ного некроза. В последующем в фасции развивается фиброз. Соединительнотканные прослойки с выраженными признаками воспалительной инфильтрации; иногда наблюдаются признаки повреждения мышечных волокон. В поздних стадиях болезни, при преобладании процессов склероза в пораженных тканях, дифференциальная диагностика с ССД затруднена.
Что провоцирует Диффузный (эозинофильный) фасциит
Этиология и патогенез заболевания изучены недостаточно. В качестве провоцирующих факторов фигурируют чрезмерное охлаждение, физическое перенапряжение, например, ношение тяжестей, спортивные перетренировки, травмы. Реже Д(Э)Ф развивается после острой инфекции или аллергической реакции. Возможно, играет роль генетическое предрасположение. Например, М. Thibierge отмечает в семьях больных случаи очаговой склеродермии, РА, сахарного диабета.
Среди механизмов развития Д(Э)Ф значительное внимание уделяется иммунным нарушениям, что проявляется гипергамма глобулинемией и повышением содержания иммуноглобулинов, особенно IgG, циркулирующих иммунных комплексов и развитием иммунного по своей сути воспаления в глубокой фасции и близлежащих тканях. S. J. Wasserman и соавт. предложили оригинальную гипотезу патогенеза ЭФ, в соответствии с которой начальным звеном является антигенная альтерация наиболее пораженных при болезни тканей, включая мышцы, в результате чрезмерной физической нагрузки или другой причины с поступлением в очаг поражения эозинофилов, возможно, обусловленным лимфокинной и иммунокомплексной или специфической эозинофильной активностью. Привлеченные в пораженные ткани фагоциты стимулируют развитие воспаления и фиброза, представляющих основные клинические проявления болезни. Интересна также концепция G. Solomon и соавт., в основу которой положено преимущественное нарушение клеточного иммунитета, вовлечение субпопуляции Тлимфоцитов, обладающих Н2рецепторами.
торы получили удовлетворительный эффект от применения циметидина, являющегося антагонистом Н2рецепторов. Следовательно, вопросы этиологии патогенеза ЭФ еще не решены, однако особенностью болезни является избыточная эозинофилотаксическая активность, определяющаяся у большинства больных, а также нарушение функции Тсупрес соров. Различные взаимоотношения основных патогенетических процессов определяют клинические особенности течения Д(Э)Ф.
Симптомы Диффузного (эозинофильного) фасциита
Клиническая картина характериуется уплотнением мягких тканей верхних и нижних конечностей с нарушением их двигательной активности, вплоть до развития сгибательных контрактур в различных суставах, преимущественно пальцев рук.
Один из наиболее ранних признак
Диффузный (эозинофильный) фасциит
Краткое описание
Диффузный фасциит – патология соединительной ткани с поражением кожи, подкожной клетчатки, мышц. Протекает на фоне эозинофилии (повышение числа эозинов в крови), гипергаммаглобулинемии (повышение в крови гамма-глобулина).
Болезнь названа по имени американского врача, исследователя ревматизма Шульмана, учёный в 1970-х годах выделил заболевание в отдельную форму. Редкость заболевания поразительна: отечественная наука сталкивалась лишь с несколькими случаями.
Болеют преимущественно мужчины в возрасте от 25 до 60 лет. У женщин болезнь Шульмана встречается приблизительно в два раза реже. Начинается заболевание с общих симптомов, многие пациенты не подозревают развитие диффузного фасциита. Специфические симптомы появляются постепенно. Многие терапевты склонны считать, что у пациента развивается системная склеродермия либо прочее аутоиммунное заболевание.
Причины заболевания
Причины эозинофильного фасциита изучены недостаточно ввиду редкости. Недостаточно изучены основные факторы риска заболевания. Известно, что эозинофильный фасциит развивается в результате действия перечисленных факторов.
Этиология и патогенез заболевания пока исследованы не так хорошо, чтобы уверенно говорить о причинах, но уже собрана достаточная база для определения провоцирующих факторов:
- переохлаждение;
- чрезмерные физические нагрузки, избыточные спортивные тренировки;
- травмы;
- последствия острой инфекции или аллергического состояния;
- воздействие токсинов;
- стрессы на фоне подверженности психосоматическим явлениям;
- генетическая предрасположенность.
Иммунные нарушения имеют серьезную значимость в механизмах развития этого синдрома. Об этом говорит как существенное повышение глобулинов класса G, так и тот факт, что воспалительные явления в глубоких фасциях и близлежащих тканях чаще всего имеют иммунную природу.
В последнее время появились убедительные гипотезы, основанные на различных аспектах аномального иммунного ответа организма на патогенные факторы, но процесс изучения еще далек от завершения.
Этиология
Этиологические факторы патологического процесса до настоящего времени окончательно не изучены. Ученые установили, что до первичного проявления зачастую предшествуют:
- излишние физнагрузки;
- оперативные вмешательства;
- травмирования;
- аллергии;
- острые инфекционные процессы в организме;
- воздействия длительных низких температур;
- психо-эмоциональное перенапряжение.
Признаки диффузного фасциита
Картина симптомов болезни характерна наличием уплотнения мягких тканей рук и ног. Нарушается их двигательная активность.
Развиваются сгибательные контрактуры в суставах пальцев. Сгибательная контрактура приобретает вид нарушения разгибания сустава в отличие от разгибательной контрактуры, когда сустав сложно сгибать.
Диффузный фасциит прогрессирует остро — через несколько дней после действия провоцирующих факторов.
Сначала больного беспокоит общее недомогание, повышенная температура, боль в суставах и мышцах. На неблагоприятном фоне развивается болезненный отёк дистального отдела конечностей. Поражаются стопы, голени, бёдра, туловище. Редко отёк распространяется на пальцы, шею, туловище. Одновременно появляется ощущение стягивания кожи, зуд.
Симптомы заболевания
ДЭФ начинается остро либо подостро вследствие действия провоцирующих факторов. Первоначально проявляются неспецифические признаки: недомогание, небольшое повышение температуры, боли в мышцах и суставах.
Далее постепенно либо резко формируется плотный болезненный «подушкоподобная» отечность дермы дистальных частей рук и ног. Редко отечность переходит на лицевую и шейную поверхность, пальцы, бедренную область и туловище.
Очаги имеют симметричное либо ассиметричное расположение, бывают одиночными либо многочисленными. В зоне уплотнений кожа натягивается, имеет лоснящийся вид, во время разгибания конечностей и натягивания кожного покрова появляется симптом «апельсиновой корочки».
Клиническая картина характериуется уплотнением мягких тканей верхних и нижних конечностей с нарушением их двигательной активности, вплоть до развития сгибательных контрактур в различных суставах, преимущественно пальцев рук.
Один из наиболее ранних признаков болезни — появление чувства стягивания кожи в области верхних и (или) нижних конечностей, ощущение набухания и плотности, реже зуда. Почти одновременно отмечается ограничение движений в руках, слабость в ногах при подъеме по лестнице.
Характерно развитие уплотнения мягких тканей предплечий и (или) голеней, распространяющегося на плечи и бедра, появляющегося на протяжении нескольких месяцев или даже дней. Крайне редко умеренное уплотнение обнаруживается на шее, лице, животе или на туловище.
Уплотнения, как правило, неболезненны, хотя изредка больные жалуются на умеренные спонтанные боли в этих участках.
Структура кожи обычно не меняегся, ни в местах уплотнений становится натянутой, блестящей, изредка гиперпигментирован ной с признаками гиперкератоза. Характерен симптом «апельсиновой корки» в виде мягких втяжений при максимальном натяжении, т.е. максимальном разгибании конечности (на внутренней поверхности плеч, бедер).
У всех больных наблюдается ограничение активных движений в суставах конечностей изза их уплотнений, вплоть до развития стойких контрактур преимущественно в пальцах рук, реже в локтевых и коленных суставах.
Суставы не изменены, артриты не выявляются, но у ряда больных могут наблюдаться полиартралгии как проявление общей активности болезни. Значительно чаще больные жалуются на полимиалгию и мышечную слабость, хотя клинически признаки миозита не обнаруживаются.
Поражений внутренних органов, сосудистых расстройств, включая синдром Рейно, какихлибо нарушений трофики не отмечается, что и отличает ЭФ от ССД. Может быть непостоянный субфебрилитет.
Среди лабораторных показателей диагностическое значение имеет эозинофилия до 10-44 %, сопровождающаяся гипергам маглобулинемией. У 50 % больных увеличена СОЭ до 20- 30 мм/ч, реже до 50 мм/ч, отмечается повышение СРБ. В острой стадии болезни повышается содержание серомукоида, фибриногена, церулоплазмина у /з больных, но незначительно.
Изменения гуморального иммунитета нехарактерны. Чаще повышается количество IgG, реже выявляются ЦИК и крайне редко АНФ.
Особенности диагностики болезни
Диагноз Д(Э)Ф труден при обнаружении характерных уплотнений на верхних и нижних конечностях, симптома «апельсиновой корки», ограничения движений вплоть до развития сгибательных контрактур. Диагностическое значение имеют гиперэозинофилия и гипергаммаглобулинемия.
Диагностическое значение имеет биопсия всего комплекса пораженных при Д(Э)Ф тканей: кожи, подкожной клетчатки, фасции, мышцы. При этом характерны патоморфологические изменения в фасции — значительное утолщение с признаками воспаления и фиброза.
Своевременное распознавание заболевания затруднено ввиду редкости болезни. Однако больные с подозрением на эозинофильный фасциит направляются к ревматологу для углубленного анализа. Иногда требуется осмотр дерматолога для исключения заболеваний кожи.
Большое значение имеет наличие апельсиновой корки на коже, ограничение двигательной активности. Диагностическое значение показывает биохимический анализ кожи с верификацией данных гамма-глобулина, СОЭ, фибриногена. Положительный ревматоидный фактор заставляет думать о наличии болезни Шульмана.
Иногда пациенту ошибочно ставится диагноз «системная склеродермия», «тендовагинит» или «ревматоидный артрит». Это связано с недостаточной квалификацией врача и недостаточной изученностью заболевания. Поэтому важна дифференциальная диагностика: болезнь требуется отличать от системной склеродермии, подобных синдромов. Главные отличительные черты болезни Шульмана:
- Отсутствие синдрома Рейно;
- Отсутствие плотного отёка пальцев рук и кистей;
- При системной склеродермии у больного поражаются лёгкие и пищевод;
- При склеродермии Бушке развивается плотный отёк верхней части туловища. Характерное для эозинофильного фасциита поражение фасций отсутствует;
- При тендовагините поражение сустава несимметричное, в отличие от эозинофильного фасциита.
Решающее значение для диагностики имеет биопсия кожи, мышц, мышечных фасций.
Лабораторные данные • Периферическая эозинофилия (в 60% случаев) • Гипергаммаглобулинемия (в 35%) • Повышение СОЭ (в 30%) • АНАТ и РФ не обнаруживают (важно для дифференциальной диагностики).
Инструментальные данные • Биопсия кожи с захватом подкожной клетчатки и фасции •• Значительное утолщение фасции •• Периваскулярная аккумуляция лимфоцитов и эозинофилов •• Гомогенизация коллагена •• Отёк тканей.
Дифференциальная диагностика • Сходную клиническую картину с эозинофильным фасциитом прежде имели синдром эозинофилии — миалгии и токсический масляный синдром. Синдром эозинофилии — миалгии исчез вместе с устранением с рынка L — триптофана, токсический масляный синдром — после уничтожения партии токсичного оливкового масла, содержащего олеоанилин • Системная склеродермия.
Особенности лечения
Лекарственные средства эффективны в раннем периоде болезни, однако нередко постепенное развитие процесса приводит к несвоевременному распознаванию и запоздалому лечению. Как и при других заболеваниях из группы ДБСТ, при ЭФ необходимо длительное, нередко многолетнее, комплексное лечение.
Поскольку на первое место в клинической картине болезни выступают признаки воспалительной активности, наиболее показаны ГКС, главным образом преднизолон по 20-30 мг/сут, реже больше (60-70 мг/сут). В подавляющих дозах преднизолон назначают до снижения активности процесса, уменьшения субъективных и объективных признаков болезни.
В дальнейшем дозу преднизолона постепенно снижают до поддерживающей, которую нередко приходится назначать в течение многих месяцев и даже лет (до 8 лет, по данным Н. Г.
Гусевой и соавт.
Терапия НПВП обычно неэффективна.
При неэффективности лечения ГКС дополнительно назначают цитостатики, преимущественно азатиоприн по 150 мг/сут в течение нескольких месяцев, а при развитии фиброза — Dпени цилламин до 450-600 мг/сут. Длительность приема препаратов определяется наличием воспалительных, иммунных или фиброзных изменений.
В качестве местной противовоспалительной и антифиброзирующей терапии в комплексе лечения включаются курсы аппликаций ДМСО (50 %), фонофореза трилона Б на пораженные области. При снижении активности процесса проводятся ЛФК, курсы массажа.
При торпидном течении болезни и неэффективности терапии, по данным Н. Г. Гусевой и соавт., рекомендуется гемо сорбция. Возможно, что экстракорпоральная терапия показана и в более ранние сроки болезни в связи с повышением активности эозинофилотаксического фактора.
По данным S. Herson и соавт., на ранних стадиях болезни следует назначать преднизолон по 0,35-0,6 мг/кг в сочетании с циметидином в дозе до 1000 мг/сут в качестве бло катора Н2рецепторов.
Таким образом, эффективность лечения зависит от сроков его начала. При раннем распознавании и систематическом лечении почти у всех больных к концу 1го года развивается значительное улучшение состояния или клиническая ремиссия. Однако при позднем распознавании и развитии фиброза результаты лечения намного хуже.
Диффузный фасциит лечится особенно эффективно на ранних стадиях. Важно своевременно обнаружить болезнь. Запоздалое лечение менее эффективно. Однако возможно добиться стойкого эффекта благодаря длительному, комплексному лечению.
В терапии диффузного фасциита ведущее место имеет применение глюкокортикостероидов. В первую очередь, Преднизолон.
В редких случаях назначаются большие (60 мг и больше) дозы препарата. Назначение Преднизолона – длительное, до снижения активности патологического процесса.
Препарат полагается принимать до снижения объективных и субъективных признаков болезни. Известны случаи приёма Преднизолона длительно – до восьми лет.
Применение нестероидных противовоспалительных препаратов не даёт необходимой эффективности, в большинстве случаев не назначаются. Иногда препараты назначают в комбинации с Преднизолоном.
Наиболее эффективный препарат группы – Циметидин. Дополнительно назначаются цитостатики (Азатиоприн).
При выраженном фиброзе назначают D-пеницилламин. Дозировка цитостатиков – до 150 миллиграммов в сутки, а Д-пенициллин назначается до 600 мг в сутки.
При корректном назначении терапевтических мер, правильном выполнении больным рекомендаций врача патологические симптомы пропадают. Пациенты чувствуют облегчение состояния и заметное улучшение активных движений в суставах.
Показана местная противовоспалительная и противофиброзирующая терапия. Используют аппликации диметилсульфоксида, фонофорез Трилона Б. При условии, что активность патологического процесса снижена, применяют лечебную физкультуру и массаж. Лечебные теплые ванны способствуют улучшению состояния пациентов.
Лечение всех диффузных заболеваний соединительной ткани (ДЗСТ) является длительным комплексным процессом. Эозинофильный фасциит требует такого же подхода. Важно начать лечение как можно раньше, но в связи с проблемами диагностики начало адекватной терапии бывает запоздалым. В истории медицинских наблюдений описаны случаи самопроизвольного излечения больных, но надеяться на подобный исход не стоит.
Среди препаратов, показанных при лечении синдрома Шульмана, на первом месте находятся глюкокортикостероиды, из которых более часто применяется Преднизолон. Поскольку лечение осуществляется только специалистом, он определяет точную дозировку, длительность курса и режим терапии.
Обычно суточная доза препарата составляет 20–30 мг, но может быть повышена в 2 раза. На ранних этапах болезни эффективность высоких доз кортикостероидов оказывается максимальной.
Продолжительность курса преднизолона зависит от тяжести заболевания и обычно проходит в 2 этапа:
- до наступления первых признаков снижения активной фазы болезни дозировка поддерживается неизменной;
- после отмечаемого пациентом и врачом уменьшения интенсивности симптомов и улучшения состояния дозировка значительно уменьшается.
https://www.youtube.com/watch?v=sbMyYJhDVPE
Длительность поддерживающей стероидной терапии может превышать несколько месяцев и даже лет. Применение препаратов группы НПВС (таких, как Анальгин, Ибупрофен, Диклофенак, Мовалис и др.) обычно неоправданно ввиду малой эффективности.
Восприимчивость больных к терапии Преднизолоном весьма высока (до 90%), но в случае отсутствия прогресса при лечении медикаментозное воздействие расширяют за счет цитостатиков, чаще всего из этой группы применяют Азатиоприн.
Это мощное средство, оказывающее не только цитостатическое, но и иммуносупресивное воздействие, а подавление иммунной реакции организма имеет важное значение в лечении всех заболеваний группы ДЗСТ.
Лекарственное лечение • Иммунодепрессивная терапия •• ГК: преднизолон 40–60 мг/сут — при наличии воспалительной и иммунологической активности (высокая СОЭ, гипергаммаглобулинемия). По мере подавления активности дозу преднизолона снижают до поддерживающей (5–10 мг/сут) на последующие годы •• Противомалярийные препараты: гидроксихлорохин 200–400 мг/сут в дополнение к преднизолону или без него (при отсутствии признаков активности) • Местная противовоспалительная терапия — аппликации диметил сульфоксида (см.
Склеродермия системная).
Прогноз. Описаны случаи спонтанного выздоровления по истечении 3 лет болезни, но остаются резидуальные контрактуры.
МКБ-10 • M35.4 Диффузный (эозинофильный) фасциит
Приложение. Фасциит некротизирующий — быстро прогрессирующее воспаление фасций, сопровождаемое развитием сосудистого тромбоза и, как следствие, обширным некрозом вовлечённых в патологический процесс тканей, тяжёлой интоксикацией.
Кожные покровы над зоной поражения могут оставаться неизменёнными, что может привести к недооценке тяжести процесса. Может развиться после колотых и огнестрельных ранений, оперативных вмешательств.
Клиническая картина • наличие пузырей с серозно — геморрагическим экссудатом, пастозность и покраснение кожи либо подкожная крепитация; возможно полное отсутствие каких — либо изменений кожи • появление признаков прогрессирующей интоксикации (лихорадка, тахикардия), локальная болезненность в области раны • некротическая рана с зловонным серозно — гнойным отделяемым.
Диагностика: бактериоскопическое и бактериологическое исследования Прогноз — серьёзный, эффективность лечения зависит от своевременности хирургического вмешательства и хорошо спланированной комплексной интенсивной терапии.

