Болят ли метастазы – Как определяют метастазы в организме. Причины, стадии, признаки и симптомы метастаз.
Боль при метастазах
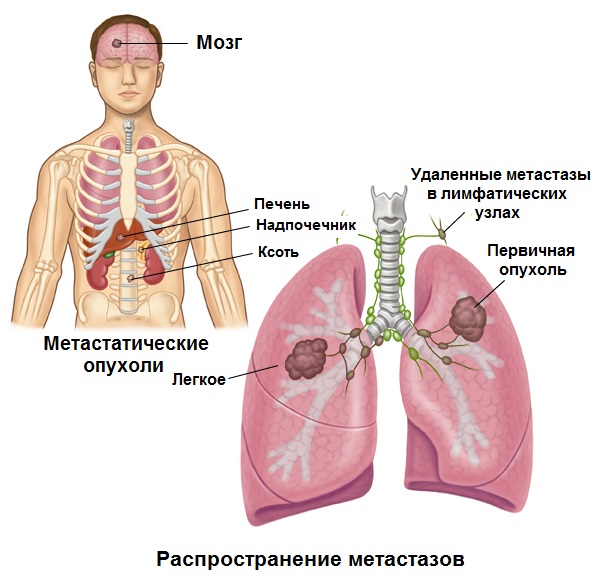
Очень часто метастазы образовываются в области нервов, и это приводи к болевым ощущениям. Все дело в том, что образование сдавливает нерв. Образования можно наблюдать в области спинного или головного мозга, что причиняет сильные болевые ощущения.
Еще одна причина, когда человек чувствует боль при метастазах – химиотерапия. Для такой процедуры используют различные препараты, которые провоцируют сильную боль в стопах и кистях.
Как уменьшить болевые ощущения?
Чтобы уменьшить страдания пациента врачи применяют несколько методов лечения:
• стероидные препараты;• лучевая терапия;
• чрескожные электростимуляторы.
Стероидные лекарства применяют в первую очередь. Они снимают отек и уменьшают давление опухоли на ближайшие ткани и нервы. Это пациенту не стало легче, используется лучевая терапия.
Чрескожный электростимулятор – специальные аппарат, который выделяет слабые электрические сигналы. Он стимулирует метастазы и уменьшает боль.
Если пациента мучает боль, связанная с давлением на нервы врачи могут применять эпидуральную анестезию. Данные препарат является сильным обезболивающим, который блокирует проведение нервного импульса от нерва к мозгу, что приводит к исчезновению неприятных ощущений. Данный препарат вводят в спинной мозг. Несмотря на сильные болевые ощущения во время введения анестезии, такой укол использую очень часто, ведь он надолго снимает боль при метастазах.
Болевые ощущения в животе
Причиной такого неприятного явления могут стать вздутие и запор. А вот причиной запора чаще всего является неподвижность пациента или частое введение обезболивающих препаратов.
Если больного беспокоят боли в середине живота, это, скорее всего, говорит об увеличении лимфоузлов, что сдавливают нервы и органы. Также лимфатическая ткань может прорастать в нервы.
При наблюдении болевых ощущений в правой стороне живота врачи приходят к мнению, что метастазы поразили печень. Если образования наблюдаются в нескольких местах и имеют небольшой размер, врачи используют лучевую терапию. Если метастазы занимают большое пространство, лучевое лечение не используется, так как это грозит серьезными последствиями.
Метастазы в костной системе
Очень часто злокачественные образования поражают кости человека. Если такое явление наблюдается в нескольких областях тела, лучшим методом избавления от боли является лучевое лечение. Данный метод помогает в 80% случаев, что и делает его таким популярным в области онкологии.
Для лучшего эффекта врачи назначают различный спектр противовоспалительных и стероидных лекарств. В этом случае неплохой результат может принести и химиотерапия, гормональное лечение. В тяжелых случаях эти методы сочетают вместе.
В современной медицине при болевых очищениях в области метастазов назначают внутривенные инъекции, которые действуют именно в область опухоли.
Если человека беспокоит боль при метастазах в конечностях, неплохо помогает обездвиживание этой части тела. Для этого пациенту накладывают плотную повязку и приписывают постельный режим.
Боль в мышечной ткани
Болевые ощущения в мышцах – довольно неприятное явление, которое распространяется по всему телу пациента. Все это плохо влияет на самочувствие человека – он быстро утомляется и практически не может двигаться. В этом случае медики используют специальные антидепрессанты, массаж и другие препараты для расслабления.
При мышечных болях лучевую терапию не используют, так как она может привести к уплотнению грудной мышцы. Ко всему этому пациент должен много времени проводить на свежем воздухе и гулять.
Если метастазы поразили область нервов, у пациентов наблюдается защитная реакция в виде тех самых болевых ощущений. В некоторых случаях пациентам нужен покой, а иногда и физические нагрузки – все зависит от области, которую затронули метастазы. Также отличным вариантом для снижения мышечной боли является применения тепла и холода. Для такой процедуры необходимо две грелки – с холодной и горячей водой. Их по очереди прикладывают к пораженным мышцам на 20-30 секунд. Такие манипуляции снимают отек и отлично расслабляют.
Стоит сказать, что самостоятельно назначать себе препараты нельзя. Только врач после полной диагностики может сказать, в каком лечении нуждается пациент.
метастазы в костях, лимфоузлах, симптомы, куда идут метастазы?

Рак молочной железы лечится даже в запущенной стадии, но эффективность противоопухолевой терапии с течением времени изменяется не в лучшую сторону, начинается распространение метастазов, отличающихся от материнской опухоли чувствительностью к лекарственным препаратам.
Особенности метастазирования
Рак молочной железы дает метастазы куда угодно, но чаще всего в подмышечные лимфоузлы, лёгкие, кости и печень. Исследование удаленной опухоли под микроскопом позволяет выявить индивидуальные клеточные — гистологические факторы вероятности метастазирования в будущем, тем не менее невозможно предсказать, где и когда появятся вторичные очаги рака и появятся ли вообще.
Сомнительно операбельный рак после длительного лечения может никогда не осложниться метастазами, но радикальное удаление молочной железы с сантиметровым раком не гарантирует излечения, через несколько лет возможно метастазирование.
Гетерогенный клеточный состав карциномы обуславливает разную чувствительность метастазов к лекарствам, даже в одном органе узлы по-разному отзываются на химиотерапию: одни уменьшаются, вторые — увеличиваются, а третьи замирают на долгий срок.
Популяция злокачественных клеток, ставшая родоначальницей рака молочной железы, и её отдалённое клеточное потомство неодинаковы — рак молочной железы и его метастазы абсолютно разные по особенностям развития и по реагированию на противоопухолевые лекарства.
Все это стало основанием для проведения профилактической химиотерапии или гормонотерапии всем женщинам, страдающим раком молочной железы, начиная с 1 стадии. Дополнительное послеоперационное лечение не проводится при опухоли менее полсантиметра и без единого критерия неблагоприятного прогноза. Но и после полноценного и качественного лечения нельзя надеяться на извлечение, метастазы могут появиться и через десятилетия, поэтому всю жизнь женщине предстоит наблюдение онколога с регулярными обследованиями.
Куда метастазирует рак молочной железы
 Первый барьер на пути распространения раковых клеток — лимфатические узлы подмышечной области, собирающие лимфу от всей молочной железы. Сначала в лимфоузлах появляются скопления раковых клеток, в дальнейшем происходит их полное замещение опухолевой тканью. Метастазы в подмышечном лимфоколлекторе не считаются отдаленными, но их состояние характеризует степень диссеминации рака по организму, если лимфоузлы чисты, то отсутствуют и отдалённые метастазы. При большинстве морфологических вариантов рака молочной железы прогноз зависит от объёма повреждения регионального лимфоколлектора. Но при тройном негативном раке, особенно большого размера, такая корреляция не обязательна, благо, что этот молекулярно-биологический вариант нетипичен для российских женщин.
Первый барьер на пути распространения раковых клеток — лимфатические узлы подмышечной области, собирающие лимфу от всей молочной железы. Сначала в лимфоузлах появляются скопления раковых клеток, в дальнейшем происходит их полное замещение опухолевой тканью. Метастазы в подмышечном лимфоколлекторе не считаются отдаленными, но их состояние характеризует степень диссеминации рака по организму, если лимфоузлы чисты, то отсутствуют и отдалённые метастазы. При большинстве морфологических вариантов рака молочной железы прогноз зависит от объёма повреждения регионального лимфоколлектора. Но при тройном негативном раке, особенно большого размера, такая корреляция не обязательна, благо, что этот молекулярно-биологический вариант нетипичен для российских женщин.
Головной мозг практически не поражается метастазами в первую волну диссеминации раковых клеток, как правило, появление в нем очагов опухоли манифестирует давнюю болезнь и случается после множества курсов химиотерапии, часто обозначая выход заболевания из-под терапевтического контроля.
Распространение опухоли в легкие может происходить изолированно или вместе с появлением вторичных очагов в других органах. Способствует образованию в легочной ткани раковых отсевов отличное кровоснабжение и анатомическая близость к молочной железе. Клетки рака попадают в легочные альвеолы с током крови и с лимфой.
Метастазы в кости также типичны для рака молочной железы, причем наиболее часто отсевы случаются при гормонально зависимой карциноме. Они возникают как изолированно — только в скелете, так последовательно и параллельно с очагами рака в других органах и тканях. Метастазы в костях сложно лечатся, но прогноз достаточно благоприятный — продолжительность жизни существенно дольше, чем при других локализациях. Если очаги единичны, то можно рассчитывать больше чем на 5 лет жизни.
Печеночные метастазы в большинстве случаев свидетельствуют о давнем раковом процессе, изначальное метастазирование в печень случается довольно редко, но давнее заболевание с поражением других органов или скелета, как правило, сопровождается и образованием очагов в ткани печени.
Запись на консультацию круглосуточно
Симптомы
Клинические проявления опухоли могут отсутствовать довольно продолжительное время, пока опухолевая масса не начнёт нарушать функционирование органа, попутно отправляя организм продуктами жизнедеятельности.
- Симптомы при метастазах рака молочной железы в лёгких
- Метастазы в кости проявляются болями, но не всегда, зачастую на начальном этапе развития и даже в период «расцвета» метастазирования может вообще не быть никаких симптомов.
- Признаки печеночного поражения появляются при выключении из функционирования более половины органа, это тошнота с эпизодами рвоты, сильнейшая слабость, нарушение питания, в терминальной стадии печеночной недостаточности развивается желтуха, асцит и кровотечение из вен пищевода.
- Метастатическое поражение головного мозга сопровождается головными болями, изменениями зрения, головокружением и рвотой при поворотах головы.
Диагностика метастаз при раке молочной железы
Множественное метастатическое поражение можно заподозрить на основании жалоб при осмотре пациентки, но нередко вторичные узлы находят только при обследовании. Поражение подмышечных лимфоузлов обнаруживается уже при первичном УЗИ, маммографии, МРТ. Уточняющая морфологическая диагностика — биопсия во время операции.

Для обследования легких и брюшной полости лучше выбрать КТ, головного мозга — МРТ.
Очаги в костях выявляют при остеосцинтиграфии, затем по очагам накопления проводится уточняющая КТ-диагностика.
Крупноочаговое метастазирование в печень можно выявить при УЗИ, мелкие очаги лучше выявляются при КТ или МРТ.
ПЭТ-КТ обнаружит метастазирование в любом органе и ткани.
Лечение
Генерализация рака молочной железы лечится только лекарствами — химиотерапией и гормонами. Только опухолевое поражение подмышечных лимфоузлов радикально лечат удалением — лимфаденэктомией. При сочетании с метастазированием в другие органы операция бессмысленна. При поражении головного мозга и костей возможна лучевая терапия.
Прогноз
Метастатическая стадия лечится, но прогноз в отношении жизни неблагоприятен. Средняя продолжительность жизни при поражении внутренних органов редко превышает 2-3 года, при изолированных метастазах рака молочной железы в кости — до 5 лет и более. С очаговым поражением печени или головного мозга продолжительность жизни без лечения не превышает нескольких месяцев.
Возможные осложнения
Рост и распространение метастазов рака молочной железы ухудшает функционирование органа вплоть до развития его недостаточности. Декомпенсации функции приводит к существенному ухудшению состояния больной и ограничивает возможности противоопухолевой терапии.
В Европейской клинике не только умеют лечить злокачественное заболевание, но для каждой пациентки разрабатывается программа поддерживающего и восстановительного лечения, что помогает лучше переносить терапию и сдерживать развитие устойчивости к лекарственным препаратам.
Запись на консультацию круглосуточно
Список литературы:
- Стенина М.Б., Жукова Л.Г., Королева И.А., и др./ Практические рекомендации по лекарственному лечению инвазивного рака молочной железы// Злокачественные опухоли; 2016, № 4, Спецвыпуск 2.
- Howard-Anderson J., Ganz P.A., Bower J.E., Stanton A.L./ Quality of life, fertility concerns, and behavioral health outcomes in younger breast cancer survivors: a systematic review// J Natl Cancer Inst.; 2012, Mar 7;104(5).
- Joyce D.P., Manning A., Carter M., et al./ Meta-analysis to determine the clinical impact of axillary lymph node dissection in the treatment of invasive breast cancer// Breast Cancer Res Treat.; 2015 Sep; 153(2)
причины, симптомы, диагностика и лечение, прогноз

Метастазы – вторичные злокачественные опухоли различных органов и тканей, возникшие в результате гематогенного, лимфогенного или имплантационного распространения злокачественных клеток первичного новообразования. Могут обнаруживаться в любом органе. На ранних стадиях протекают бессимптомно. В последующем клинические проявления зависят от локализации метастаза. Диагноз устанавливается с учетом анамнеза, жалоб, данных объективного осмотра, результатов анализов и инструментальных исследований. Лечение – химиотерапия, радиотерапия, хирургические вмешательства.
Общие сведения
Метастазы – отдаленные очаги онкологического процесса, возникшие при перемещении злокачественных клеток по организму. Выявляются у лиц любых возрастов, однако наибольшее количество поражений обнаруживаются у пациентов старше 50 лет. Могут появляться при большинстве злокачественных опухолей и поражать любые органы. Чаще всего злокачественные новообразования метастазируют в лимфатические узлы, легкие и печень. Несколько реже встречаются метастазы в кости, надпочечники, почки и центральную нервную систему. Редко диагностируются метастатические поражения поджелудочной железы, селезенки, кожи, скелетных мышц и сердечной мышцы.
Нарушения функции различных органов, обусловленные ростом метастазов, являются ведущей причиной смертности при онкологических заболеваниях. Появление вторичных очагов ухудшает прогноз и делает невозможным радикальное лечение злокачественной опухоли либо создает существенные ограничения при выборе методов терапии. Диагностику и лечение метастазов осуществляют специалисты в области онкологии и других специальностей (в зависимости от локализации вторичного очага).

Метастазы
Этиология и патологическая анатомия метастазов
Без соответствующего лечения со временем метастазы возникают почти при всех злокачественных опухолях, однако сроки их появления могут существенно варьировать. Иногда метастазы обнаруживаются через несколько лет после развития первичного процесса, иногда – через несколько месяцев, а иногда и вовсе становятся первым проявлением онкологического заболевания, поэтому временной интервал между развитием первичной опухоли и возникновением метастазов не удается установить даже приблизительно.
Специалисты считают, что в некоторых случаях злокачественные клетки могут мигрировать в различные органы, образовывая «спящие очаги», которые в последующем активизируются и начинают быстро расти. Однако причины, по которым метастазы при одном и том же заболевании появляются и развиваются с разной скоростью, пока не установлены. Можно лишь перечислить ряд факторов, способствующих быстрому возникновению и прогрессированию вторичных образований.
В числе таких факторов – большое количество мелких сосудов вокруг первичного новообразования, особенности расположения и гистологического строения первичного очага, иммунные расстройства и возраст пациентов (у молодых метастазы возникают и прогрессируют быстрее, чем у пожилых). Большое значение имеет противоопухолевая терапия – после такой терапии трудно прогнозировать вероятность и возможное время появления метастазов. Иногда вторичные очаги возникают спустя несколько лет после прохождения курса лечения, на фоне изменения каких-то жизненных условий или без всяких видимых причин.
Клетки первичной опухоли могут распространяться по организму тремя путями: лимфогенным (по лимфатическим сосудам), гематогенным (по кровеносным сосудам) и имплантационным. Имплантационное метастазирование становится возможным после разрушения капсулы органа и выхода злокачественных клеток в ту или иную естественную полость. Например, клетки рака яичника через брюшную полость могут мигрировать на поверхность печени, а клетки первичного рака легких через плевральную полость – на поверхность плевры.
Преобладающий путь метастазирования определяется происхождением и степенью злокачественности опухоли. Клетки соединительнотканных и эпителиальных новообразований чаще мигрируют по лимфатическим путям. При опухолях высокой степени злокачественности преобладает гематогенное распространение. В большинстве случаев лимфогенные метастазы появляются раньше гематогенных. В первую очередь страдают регионарные лимфоузлы. Затем злокачественные клетки могут распространяться дальше по лимфатической системе.
Знание особенностей лимфотока в той или иной анатомической зоне позволяет определять возможные пути метастазирования и выявлять вторичные скопления злокачественных клеток (за исключением случаев микрометастазирования). Гематогенные метастазы возникают на значительном удалении от органа, пораженного первичным процессом, поэтому для их обнаружения приходится проводить комплексное обследование с учетом наиболее вероятных областей метастазирования.
Разные виды рака с различной частотой метастазируют в те или иные органы. Так, рак молочной железы, рак почек, рак предстательной железы и рак щитовидной железы чаще всего дают метастазы в легкие, кости и печень. При раке желудка, раке яичников, раке толстой кишки, раке тела матки и раке поджелудочной железы поражаются печень, брюшина и легкие. Рак прямой кишки и рак легкого распространяются в печень, надпочечники и легкие (при раке легкого страдает второе легкое). Меланома дает метастазы в печень, легкие, кожу и мышцы.
Среди вторичных новообразований преобладают солидные узловые формы, реже встречаются язвенные поверхности (например, при поражении кожи), слизеобразующие объемные образования (метастазы Крукенберга) и другие типы опухолей. Размер метастазов может варьировать от нескольких миллиметров до 20 и более сантиметров. Возможно одиночное поражение определенного органа, множественное поражение определенного органа, а также одиночные или множественные вторичные очаги в нескольких органах. Отдельно стоит упомянуть так называемые «пылевые» метастазы – множественные мелкие очаги в брюшной полости, провоцирующие развитие асцита.
По своей гистологической структуре вторичные новообразования обычно соответствуют первичной опухоли. Вместе с тем, в отдельных случаях метастазы могут иметь гистологическое строение, отличающееся от строения первичного рака. Обычно такие отличия выявляются при метастазировании опухоли полого органа в паренхиматозный орган (например, при метастатическом раке печени, возникшем вследствие первичного рака толстой кишки). Иногда из-за различия в структуре первичного и вторичного очагов возникают сложности при дифференцировке метастазов и множественного рака.
Симптомы метастазов
На начальных стадиях метастазы обычно протекают бессимптомно. В последующем клинические проявления зависят от локализации вторичного новообразования. Местная симптоматика сочетается с общими признаками онкологического заболевания: гипертермией, потерей аппетита, уменьшением массы тела вплоть до раковой кахексии, общей слабостью и анемией. При метастазах в лимфатические узлы наблюдается увеличение их размера, определяемое при пальпации или в процессе визуального осмотра.
Узлы обычно безболезненные, мягко-эластической консистенции. Чаще всего метастазы локализуются в шейных, паховых, подмышечных и надключичных лимфоузлах. При достаточно большом размере такие очаги могут быть обнаружены уже на этапе обычного осмотра. Выявление метастазов в некоторых лимфатических узлах (забрюшинных, парааортальных, узлах брюшной полости, узлах средостения) возможно только при проведении инструментальных исследований, поскольку эти анатомические образования недоступны для объективного обследования. Подозрение на наличие таких метастазов может возникнуть при их значительном увеличении, вызывающем сдавление близлежащих анатомических образований.
Проявления гематогенных метастазов определяются их локализацией. При вторичных очагах в головном мозге возникают головокружения, распирающие головные боли, тошнота, рвота и очаговые неврологические расстройства. При метастазировании в спинной мозг появляются боли, быстрая утомляемость при физической нагрузке, нарушения деятельности тазовых органов, прогрессирующие расстройства движений и чувствительности. При метастазах в легких наблюдаются частые рецидивы воспалительных заболеваний (бронхита, пневмонии, гриппа, ОРВИ), в последующем присоединяется одышка и кашель с примесью крови в мокроте.
Метастазы в печень проявляются тяжестью и болями в правом подреберье, нарушением печеночных функций, увеличением и бугристостью печени. На поздних стадиях выявляются желтуха, асцит и прогрессирующая печеночная недостаточность. Вторичные новообразования в костях вызывают мучительные боли, гиперкальциемию и патологические переломы. Возможно сдавление спинного мозга, нервных и сосудистых стволов. При метастазах в брюшину возникает асцит, обусловленный нарушением регуляции процесса выделения и всасывания жидкости тканями брюшины.
Метастазы в кожу представляют собой плотные, быстро растущие одиночные или множественные узлы телесного, синеватого или розоватого цвета. В последующем наблюдается их распад и изъязвление. При некоторых первичных новообразованиях (например, при карциноме молочной железы, раке толстого кишечника, раке яичника и раке мочевого пузыря) симптомы вторичных кожных опухолей могут имитировать клиническую картину рожистого воспаления. Реже (обычно – при опухолях молочной железы) выявляются склеродермоподобные метастазы.
Диагностика метастазов
Диагноз устанавливается на основании клинических данных и результатов дополнительных исследований. Из-за высокой склонности к развитию метастазов любое злокачественное новообразование является показанием для расширенного обследования (даже если признаки поражения других органов отсутствуют). Больным с подозрением на метастазы назначают общий анализ крови, биохимический анализ крови и анализ крови на маркеры рака. Пациентов направляют на рентгенографию грудной клетки, УЗИ органов брюшной полости, УЗИ органов малого таза, КТ и МРТ головного мозга, КТ и МРТ спинного мозга, сцинтиграфию костей скелета, рентгенографию костей скелета и другие исследования.
Наличие метастазов окончательно подтверждают при проведении гистологического либо цитологического исследования измененной ткани. Забор гистологического материала из мягких тканей осуществляют путем инцизионной, сердцевинной или щипковой биопсии. При поверхностном расположении метастазов используют скарификационную биопсию, при поражении костей – трепан-биопсию. Материал для цитологического исследования получают путем взятия обычных отпечатков или мазков-отпечатков. Для забора жидкости проводят аспирационную биопсию.
Дифференциальную диагностику метастазов осуществляют с первичными новообразованиями и с множественным раком (при одновременном или почти одновременном обнаружении нескольких очагов в одном или разных органах). В некоторых случаях требуется дифференцировка с дегенеративно-дистрофическими и воспалительными процессами. Так, симптоматическую пневмонию при метастазах в легких необходимо дифференцировать с обычной пневмонией, мелкие метастазы в позвоночник на фоне предшествующего остеопороза – с возрастными изменениями позвоночника и т. д.
Лечение метастазов
Тактика лечения определяется индивидуально с учетом вида рака, состояния первичной опухоли, общего состояния больного, чувствительности клеток к тому или иному типу лечебного воздействия, количества, локализации и размера метастазов. Возможно использование радиотерапии, химиотерапии, иммунохимиотерапии, гормонотерапии, классических хирургических вмешательств, радиохирургии, криохирургии и эмболизации питающих артерий. Как правило, при метастазах применяется комбинация нескольких методов лечения (например, химиотерапии и лучевой терапии, химиотерапии и иммунотерапии, лучевой терапии и хирургического вмешательства и т. д.). Показания к оперативному лечению и объем вмешательства также зависят от количества и локализации метастазов.
При метастазах в регионарные лимфатические узлы обычно проводят лимфаденэктомию в сочетании с удалением первичного новообразования. При контролируемых первичных опухолях и одиночных метастазах в отдаленные органы в некоторых случаях возможно радикальное иссечение вторичных очагов. При множественных метастазах хирургическое вмешательство, как правило, не показано. Исключением являются ситуации, когда паллиативная операция может отсрочить летальный исход или улучшить качество жизни больного (например, краниотомия для снижения опасного внутричерепного давления, вызванного метастатической опухолью мозга).
Прогноз при метастазах
До недавнего времени наличие метастазов рассматривалось, как свидетельство скорой гибели пациента. Сейчас ситуация постепенно меняется, хотя наличие вторичных опухолей по-прежнему рассматривается, как крайне неблагоприятный прогностический признак. Использование новых методов диагностики и лечения в ряде случаев позволяет увеличить среднюю продолжительность жизни больных. При определенных условиях стало возможным радикальное лечение метастазов некоторых локализаций, например, одиночных очагов метастатического рака печени или метастатического рака головного мозга.
В целом прогноз при метастазах определяется степенью запущенности онкологического процесса, возможностями конкретного лечебного учреждения (некоторые лечебные и диагностические методики доступны только в крупных центрах), видом, локализацией и стадией первичной опухоли, возрастом больного, состоянием его иммунной системы, степенью истощения, уровнем нарушения функций различных органов и пр. Средняя продолжительность жизни при метастатическом раке печени составляет около полугода, поражении головного мозга – несколько недель, при метастазах в кости – несколько лет, при вторичных новообразованиях в почках – 1-3 года.
фото, симптомы, лечение, прогноз, видео
Каждый день в человеческом организме появляются тысячи аномальных клеточных структур, способных в дальнейшем приобрести злокачественный статус. Благодаря иммунитету эти клетки своевременно уничтожаются.
Но если иммунная защита по определенным причинам пропускает эти клетки, то они беспрепятственно размножаются, формируясь в опухоль ракового характера.
Что такое метастазы при раке?
Злокачественные клетки из очагов первичной локализации посредством крово- и лимфотока распространяются в другие органические структуры, формируя метастазные очаги, которые фактически являются вторичными локализациями рака.
Итак, метастазы – это раковые клетки, которые распространяются по организму из основного очага опухолевого процесса.
Когда рак расползается в соседние ткани, говорят о регионарном метастазировании. Если же злокачественные клеточные структуры с кровотоком или лимфатической жидкостью проникли в периферические ткани, то возникает отдаленное метастазирование.
Причины распространения
В целом метастазирование обуславливается определенными факторами онкологического роста, которые стимулируют формирование капиллярных и сосудистых сетей вокруг опухолевого образования.
В результате создается благоприятная среда для злокачественных структур, которая обеспечивает их необходимым питанием. По такому сценарию происходит метастазирование по всему телу.
В целом распространение злокачественных клеток может происходить по различным путям:
- С кровотоком – злокачественные клетки гематогенно по венам, капиллярным структурам и сосудам распространяются по организму;
- С током лимфы. Лимфоузлы выступают защитным барьером для злокачественных структур и в них происходит частичное их уничтожение. Но когда измененных клеток слишком много, то макрофаги не могут с ними справиться;
- Имплантационно или по оболочке серозной ткани.
Метастазы лимфогенного происхождения наиболее свойственны раку маточной шейки и желудка, гортани и толстой кишки, саркомам и меланомам.
Гематогенные пути метастазирования обычно наблюдаются при поздних стадиях хорионэпителиом и сарком, малотазовых и брюшных опухолях, гипернефромах и пр.
На какой стадии появляются и как быстро распространяются?
Если онкопациент не получает необходимого лечения, то метастазы со временем возникнут при любом раковом процессе, но срок появления не всегда однозначен.
При одних онкопатологиях метастазирование возникает уже через несколько месяцев после образования первичного опухолевого очага, а при других выявляются лишь через по прошествии нескольких лет. Поэтому даже предположительно установить сроки метастазирования невозможно.
Рассматривая метастазирование в лимфосистеме, можно сказать, что метастазы являются признаком перехода рака на вторую стадию развития.
Если появилось гематогенное распространение злокачественных клеток, то речь идет о переходе онкопатологии на 4 стадию. В среднем метастазы образуются на 3-4 стадии рака. Т. е. фактически, появление метастатических процессов определяет стадию раковой опухоли.
Видео о том, как происходит метастазирование раковых опухолей:
Как метастазируют различные виды рака?
Обычно метастазы выявляются в легочных структурах, печени и лимфоузлах. Гораздо реже метастатические очаги обнаруживаются в сердце и мышцах скелета, селезенке и поджелудочной железе.
Специалисты определили некоторую закономерность метастазирования рака различной локализации:
Чем опасны?
Летальный исход при онкопатологиях чаще наступает именно из-за активного метастазирования, нежели из-за наличия первичной опухоли. Поэтому метастазы очень опасны.
- Они нарушают деятельность жизненно важных систем и органов;
- Если появились метастазы, то организм уже не может самостоятельно противостоять онкологии;
- Метастазирование отрицательно сказывается на течении онкопроцесса и состоянии пациента, ухудшая его.
Разновидности
Метастазирование имеет множество вариантов и разновидностей, существенно различающихся друг с другом.
Вирховский
Метастаз Вирхова локализуется в надключичной области на шее и возникает на фоне желудочного рака. Подобное расположение вторичного онкоочага обуславливается направлением лимфотока из брюшной полости.
Злокачественные клеточные структуры поднимаются по лимфатическим путям именно до шейного лимфоузла, дальше пройти они не могут, поэтому начинают формироваться во вторичную опухоль. Вирховский метастаз может возникнуть вследствие рака печени, поджелудочной и прочих брюшных структур.
Крукенбергский
Подобные метастазы также характеризуются лимфогенным происхождением и локализуются в яичниках. На долю подобных вторичных опухолей приходится порядка 35-40% от общего числа яичниковых метастазов.
Наблюдаются крукенбергские метастазы при злокачественных желудочных, молочножелезистых, кишечных или желчнопротоковых поражениях, мочепузырном или цервикальном раке.
Шницлеровский
Шницлеровскими метастазами называют распространение злокачественного процесса в клетчатку околопрямокишечной локализации и параректальные лимфоузлы.
Подобные метастатические образования прощупываются при ректальном пальцевом исследовании и представляют собой безболезненные уплотнения.
Чаще всего возникает на фоне рака желудка.
Остеобластический
Метастатические опухоли, образующиеся в костных тканях и способствующие активности остеобластов, называют остеобластическими. На фоне повышенной остеобластной активности происходит усиленное отложение кальция в костных тканях, что способствует их быстрому росту.
Возникают такие метастазные очаги на фоне молочножелезистого, щитовидного или простатического рака, саркомах и лимфомах. Прогнозы преимущественно неблагоприятные.
Солитарный
Метастазы солитарного типа представляют собой крупноузловые одиночные образования, локализующие в легочных, головномозговых и прочих тканях.
Остеолитический
Остеолитические вторичные образования тоже локализуются в костных структурах, однако, их воздействие на кости носит несколько иной характер. Они разрушают костную ткань и активируют остеокласты, что приводит к деструктивным изменениям костей.
Симптомы и признаки
Клиническая картина метастазирования зависит от его локализации и типа первичной опухоли. Обычно метастазы приводят к тяжелым дисфункциональным изменениям в структурах организма.
- При печеночном метастазировании у пациентов зудит кожа, появляется желтухи и недостаточность печени;
- Головномозговые метастатические процессы приводят к стремительной энцефалопатии;
- Легочное метастазирование вызывает бронхолегочные воспаления, нарушения дыхательной деятельности и пр.;
- Костные метастазы отличаются сильной болезненностью по всему телу.
На коже
Кожные метастазы возникают преимущественно на фоне злокачественных поражений яичников, легких и почек. Метастатические процессы на коже имеют лимфатическое или гематогенное происхождение. У мужчин такие метастазы локализуются на животе и шее, груди и голове, а у женщин на груди и животе.
Признаки кожных метастаз:
- Появление образований, похожих на родинки;
- Изменение цвета кожи на месте метастазов;
- Быстрое увеличение кожного образования;
- Астения;
- Обессиленность;
- Сонливость и слабость;
- Отсутствие работоспособности;
- Болезненные ощущения в области опухоли;
- Похудение и гипертермия.
На фото видно, как выглядит рак 4 стадии с метастазами на коже
Если метастаз образовался на коже головы, то он обычно имеет вид сального кистозного образования.
В ребрах
Первыми признаками реберных метастаз выступают интенсивные болезненные ощущения, приводящие к ограничению подвижности. На более поздних этапах вторичные опухолевые очаги могут приводить к переломам ребер, возникающим даже при незначительных нагрузках.
В ребра чаще всего метастазируют раковые опухоли щитовидки, груди, простаты и цервика, печени и легких, пищевода и пр. Для их обнаружения необходимо проведение сцинтиграфического исследования скелета.
Сердце
Сердечные опухоли вторичного характера обычно возникают вследствие плевральной мезотелиомы, карциномы, меланомы или пищеводного плоскоклеточного рака, почечной и щитовидной онкологии или лейкемии.
Признаками сердечных метастазов являются:
- Выпот перикарда;
- Непроходимость вен в миокарде;
- Угнетение сердечной деятельности;
- Аритмия, недостаточность миокарда.
Брюшине
Раковые клетки могут проникнуть в любую часть организма, в частности в брюшную полость. Злокачественные структуры оседают на поверхности внутренних органов и стенок брюшины. Довольно долгое время они накапливаются, постепенно образуя вторичную опухоль.
Подобные процессы в организме обычно сопровождаются асцитом, вызывающим увеличение живота. Если опухоль начала распадаться, то проявляются общие признаки интоксикации.При онкологии молочной железы
Метастатические очаги в молочной железе проявляются появлением уплотнений в груди, которые легко прощупываются при пальпации.
В молочную железу злокачественные клетки проникают с кровотоком или лимфогенно. Пациентка ощущает интенсивную болезненность в груди и прочие дискомфортные ощущения.
Отдаленные метастазы
Чем больше параметры первичного образования, тем раньше начнутся метастатические процессы. Обычно реальная угроза метастазирования возникает, когда опухоль превышает 3-сантиметровый диаметр.
Вместе с кровотоком злокачественные клетки распространяются в отдаленные ткани и органы, что указывает на поздние этапы опухолевого процесса.
- Если метастазы возникли в костной системе, то пациентки ощущают боль в костях, которая может серьезно снизить качество жизни.
- Если молочножелезистый рак метастазировал в легкие, то пациентку беспокоит одышка, кашель и грудные боли.
- При нервносистемном метастазировании появляются головокружения и головные боли, судороги и галлюцинации, слуховые и зрительные нарушения, координационные расстройства и пр.
Регионарные
Уже на ранних этапах онкологии в молочной железе могут возникнуть метастазы в регионарных лимфоузлах. Обычно это подмышечные лимфоузловые структуры.
Но если первичная опухоль образовалась ближе к центру грудной клетки, то метастазированию подвергаются грудинные лимфоузлы.
В дальнейшем раковый процесс распространяется в более отдаленные лимфоузлы.
В кишечнике
Метастазирование в кишечник сопровождается частыми поносами или запорами, примесями крови в каловых массах, болью в животе и вздутием.
Кроме того, продукты жизнедеятельности онкообразования вызывают общую интоксикацию организма, что проявляется диспепсическими нарушениями.
Почке
Основным признаком метастазирования в почках и надпочечниковых структурах является гематурия, которая характеризуется наличием крови в моче пациента.
Дополнительным признаком метастазирования в почках является болезненность в поясничной области, постоянная температура и слабость, повышенное АД и прогрессирующая анемия.
Селезенке
Метастазы в селезенке встречаются крайне редко, потому как сам орган способен производить вещества, уничтожающие злокачественные клетки.
Среди явных признаков метастазирования выделяют лихорадку, тромбопению, увеличение размеров органа, тяжесть и болезненность. С ростом вторичной опухоли состояние ухудшается, а организм истощается.
Плевре
Плевра выстилает грудную стенку и легкие с внутренней стороны. Она производит специальную смазку, облегчающую легочную работу в процессе дыхания. Метастазирование в плевральные ткани сопровождается кашлем, субфебрильной температурой и болезненностью в грудине.
Желудка
Метастазирование в желудке встречается достаточно редко, при этом опухоли распространяются сюда из матки, пищевода, молочной железы или легкого. Метастазирование сопровождается гипертермией и отсутствием аппетита, анемией и вкусовыми изменениями, болезненностью в желудке и пр.
Яичников
На начальных этапах метастазы яичников никак себя не проявляют. Некоторые онкопациентки наблюдают отсутствие аппетита и общую слабость, нарушения менструаций и гипертермию. Когда метастаз увеличивается, появляются болезненные ощущения и распирающее чувство в области низа живота.
Надпочечников
В надпочечники метастазируют многие опухоли, например, из легких, почек, молочных желез и пр.
Подобное распространение опухоли вызывает надпочечниковую недостаточность.
Крупные вторичные образования практически всегда сопровождаются некротическими процессами.
При онкологии матки
Метастазирование при маточном раке начинается на 3 стадии онкопроцесса. Распространение злокачественных клеток происходит лимфогенным путем, а гематогенное распространение возможно на последней стадии рака.
Пациентки жалуются на кровянистые выделения между месячными, поясничные боли и рези в нижней половине живота, особенно при нагрузках.
Мочевого пузыря
Метастатическое распространение злокачественных клеток в мочепузырные структуры происходит лимфогенным путем преимущественно из лоханок или мочеточников.
Поначалу появляются симптомы, наиболее характерные для цистита, беспокоят частые позывы, поясничные боли, болезненные мочеиспускания.
С развитием метастазирования состояние ухудшается, появляется постоянная гипертермия, кров в урине и пр.
Поджелудочной железы
Поджелудочножелезистое метастазирование характеризуется такими проявлениями, как резкое похудение и отсутствие аппетита, тошнотнорвотный синдром, эпигастральные боли и частая диарея.
Иногда метастазы в поджелудочной вызывают некоторое пожелтение кожных покровов и опоясывающую боль в животе.
Горла
Метастатические образования в горле появляются обычно из опухолей рта, органов дыхания и пищеварения. Чаще всего подобная локализация метастазов вызывает такие признаки:
- Ранки и язвочки в горле;
- Отек ротовых тканей;
- Проблемы при разговоре, дыхании, сглатывании;
- Увеличение лимфоузлов и пр.
Как определить в организме?
Выявление метастаз требует проведения тщательной диагностики, включающей:
- КТ;
- УЗИ;
- МРТ;
- Обзорную рентгенографию;
- ПЭТ;
- Радиоизотопную диагностику.
Подобные процедуры позволяют определить степень метастазирования, размеры вторичных опухолей, прорастание в другие ткани и наличие гнойных процессов либо распада, характер роста и пр.
Видны ли на УЗИ?
Ультразвуковая диагностика является одним из основных методов выявления метастатического распространения злокачественных процессов.
Подобное исследование считается достаточно информативным и широко применяется в современной диагностической практике.
Как вылечить?
Лечение онкопатологии с метастазированием обуславливается расположением, размерами и количеством вторичных очагов. Применяется несколько различных методик: хирургическое удаление, радиолечение и медикаментозная терапия.
Оперативное лечение
Изначально врачи стараются удалить первичное образование, которое в будущем может выступать в качестве источника метастазов.
Затем приступают непосредственно к удалению самих метастазных очагов. Для этого производят удаление лимфоузлов и прилегающей клетчатки.
При удалении вторичных образований хирург отсекает и часть здоровых тканей, на которых также могут находиться микрометастазы.
Радиочастотная абляция
Радиочастотная абляция сегодня успешно применяется в лечении метастазного распространения опухолевых процессов.
Подобный метод предполагает разрушение опухоли посредством высоких температур, которые создаются специальными электродами. Электромагнитные токи нагревают злокачественные ткани и разрушают их. Затем отмершие клетки ссыхаются, а на их месте формируется рубец.
Лекарства
Медикаментозное лечение метастазных опухолей предполагает применение таких способов, как химиотерапия, иммунотерапия, таргетная и гормональная терапия.
Химиотерапевтическое воздействие противоопухолевыми препаратами останавливает рост и распространение метастазов. Часто эту методику сочетают с облучением или радиочастотной абляцией.
Сколько живут с метастазами: прогноз
Обычно наличие метастазов в лимфоузловых и прочих органических структурах говорит о неблагоприятных прогнозах онкопатологии.
- Прогноз метастазов в брюшной полости. Летальный исход при подобном метастазировании на сегодня составляет 5%. Своевременное выявление брюшного метастазирования и обязательная химиотерапия с соответствующей реабилитацией намного повышает шансы пациента на благоприятный исход лечения онкологии.
- В надпочечники. Надпочечниковые метастазы обычно сочетаются с поражением других органов, поэтому прогноз зависит от конкретной клинической ситуации.
- Средостении. Подобное метастазирование при раннем выявлении может закончиться положительно, однако, при позднем выявлении прогнозы неблагоприятные.
- Кишечнике. При своевременном обращении к онкологу имеется тенденция к благополучному исходу заболевания. Излечение при своевременном хирургическом вмешательстве в сочетании с радиолечением и химиотерапией в среднем наступает у половины пациентов. На поздних этапах прогнозы неутешительные.
- Печени. Без лечения при метастазных поражениях печени выживаемость составляет 4 месяца. При получении необходимой помощи жизнь пациента продляется на полтора года, дополнительная химиотерапия способна подарить онкобольному еще около года жизни.
- Легких. Неблагоприятными факторами при легочном метастазировании является его появление раньше, чем через 12 месяцев после удаления первичного онкоочага, а также стремительное увеличение метастазных опухолей. Выживаемость в течение 5 лет при одиночном метастазировании и после проведения адекватного лечения составляет порядка 40%.
Практически все пациенты, страдающие раком, умирают в течение десятилетия вне зависимости от наличия метастатических процессов. А если они имеются, то продолжительность жизни существенно сокращается.
Если у пациента терминальная (четвертая)стадия онкологии и имеются метастазы, то продолжительность жизни исчисляется несколькими неделями, а иногда и днями, что зависит от вида опухоли.
Метастазы симптомы

На сегодняшний день раковые опухоли являются распространенным заболеванием. Такие опухоли характеризуются тем, что имеют злокачественный характер, а так же сопровождаются процессом метастазирования.
Что такое метастазы?
Раковая опухоль – это первичное новообразование, состоящее из мутировавших клеток. Такая опухоль характеризуется быстрыми темпами роста за счет процессов деления этих клеток. Метастазы – это последствия раковой опухоли. Они образуются из частей опухоли, отделившихся от общей ее массы и распространившихся по организму посредством лимфатической или кровеносной системы и закрепившихся на различных внутренних органах. Так рак кишечника часто сопровождается метастазами в печень.
Раковая опухоль и ее метастазы симптомы разного характера. Симптоматика во многом зависит от органа, в котором появилась опухоль или проросли метастазы.
Но есть общие симптомы метастаз, которыми характеризуются также, как и первичные опухоли:
– тошнота и рвота;– постоянное ухудшение общего самочувствия;
– кровотечения;
– повышение температуры тела;
– проблемы с кишечником;
– судороги;
– головокружение и головная боль;
– потеря аппетита и веса;
– сильные боли в каком-либо органе;
– увеличение лимфоузлов;
– большая подверженность организма различным простудным и инфекционным заболеваниям.
Среди причин возникновения раковых опухолей выделяют:
1. Неблагоприятные экологические условия, загрязнения атмосферы.2. Генетическую предрасположенность.
3. Характер работы человека – если работа связана с производством или обработкой токсичных веществ.
4. Радиационные облучения.
5. Вредные привычки.
Метастазы характерны для поздних стадий раковых опухолей. На последней стадии появляются метастазы в отдаленных органах, а на более ранних – в лимфоузлах. Но иногда процессом метастазирования сопровождаются и ранние этапы рака.
Для того чтобы предупредить процессы метастазирования, необходимо обнаружить рак на ранних стадиях. Ведь именно на ранних стадиях это заболевание поддается лечению.
Диагностика
Проблема с выявлением опухоли рака заключается в том, что на ранних стадиях данное заболевание себя никак не проявляет. Именно поэтому врачи рекомендуют проходить ежегодные медосмотры, сдавать анализы и проходить флюрографию.
Помимо того, существуют следующие меры диагностики рака:
– анализы крови и мочи;– биохимия крови;
– биопсия;
– рентген;
– УЗИ;
– компьютерная ;
– флюорография;
– анализы с применением онкомаркеров.
Итак, если обнаружен рак – что делать?
Конечно же, обращаться к специалисту! В настоящее время медицина развита настолько, что помогает излечить рак, за исключением тяжелых случаев на последней стадии. Но и для пациентов с последней стадией рака, отягощенной метастазами, специалисты тоже могут многое сделать. Например, с помощью лечения можно продлить срок жизни и уменьшить боль.
Лечение
Врачи не рекомендуют применять методы народной медицины при лечении раковых опухолей. Помимо того, что действие этих методов не доказано, Вы можете потерять драгоценное, в случае болезни раком, время.
Среди методов лечения на данный момент известны следующие:
– операция;– химиотерапия;
– лечение гормонами;
– иммунотерапия;
– лучевая терапия;
– криотерапия.
Если терапия направлена на уничтожение опухоли, то используется комбинация из вышеперечисленных методов. Если же терапевтические меры признаны поддержать состояние пациента на поздних стадиях, то обычно используется химиотерапия, а в некоторых случаях и операция.
При обнаружении у пациента раковой опухоли, его обычно отправляют в хоспис, где пациенту оказывается должное лечение и уход. Но в некоторых случаях, пациент может лечиться дома в условиях домашнего стационара.
Медицинские прогнозы при раке с метастазами
Если ранее считалось, что рак с метастазами свидетельствуют о скорой смерти пациента, то на сегодняшний момент современные методики лечения позволяют увеличить срок жизни пациента с таким заболеванием. Сроки жизни больного раком в последней стадии, даже при оказании должного лечения, во многом зависят от расположения опухоли. Если это печень – то срок жизни пациента может достигать полугода, мозг – до месяца, кости – до нескольких лет.
симптомы, признаки метастаз в легких, сколько живут с метастазами в легких
Метастатическим или вторичным раком легких называются опухоли, которым дают начало раковые клетки, попавшие в легочную ткань из других органов.
Лёгкие – излюбленная мишень для метастазирования опухолей
Статистика говорит о том, что у 30-55% онкологических больных обнаруживаются метастазы в легких. Злокачественные опухоли дают отсевы в лёгочную ткань: рак любого органа, саркомы, меланомы, заболевания кроветворной и лимфатической системы. Через лёгкие проходит вся кровь, и условия благоприятны для выживания бактерий, вирусов, грибов и опухолевых клеток.
Собирающий лимфу общий лимфатический проток несёт её в крупные вены, которые впадают в верхнюю полую вену. При посредстве правых отделов сердца венозная кровь, смешанная с лимфой, тоже проходит через лёгкие. Площадь структурных единиц, составляющих то, что мы называем лёгкими – лёгочных альвеол – более 150 квадратных метров. Достаточно места, изумительное полнокровие, прекрасные условия для размножения злокачественных клеток.
Иными словами, присутствуют благоприятные условия для распространения раковых клеток в легкие гематогенным (через кровь) и лимфогенным (через лимфатическую систему) путем.
Запись на консультацию круглосуточно
Какими бывают метастазы в лёгких
Метастатические узлы бывают очень разными, считают, что по плотности они полное отражение первичной опухоли. Если определять плотность на ощупь, то все опухоли тяготеют к каменистости или, по крайней мере, к костной плотности. Но плотность для очагов в лёгких понятие относительное, прощупать их можно только во время операции, которую в метастатической стадии делают чрезвычайно редко. Плотность определяют при рентгенологическом исследовании преимущественно для дифференциальной диагностики, то есть поиска признаков характерных отличий одного заболевания от другого.
Формально метастазы делят на лимфогенные и гематогенные, то есть занесенные в лёгочную ткань с лимфой или кровью, но в каждом конкретном случае разобрать, что принесло раковую клетку в альвеолу вряд ли можно, и практикующему онкологу совсем ненужно, ведь это уже ничего не изменит. Какие бы ни были метастазы по пути распространения, их надо лечить.
Метастазы в лёгких бывают разными по форме, ее определяют по рентгеновским снимкам:
- Очаговые метастазы, которые на рентгеновском снимке видны образования разного диаметра. Традиционно этот вариант метастазирования считается проявлением менее агрессивной злокачественной опухоли. При небольшом распространении более благоприятно протекают именно очаговые образования. Они как раз считаются преимущественно гематогенными, то есть занесёнными кровью.
- Инфильтративные метастазы, когда опухолевые клетки расползаются по эпителиальной выстилке альвеол, что на рентгенограмме проявляется в виде сетки или разной формы затемнений. Такой вариант традиционно считают вариантом более агрессивной опухоли – агрессивные по течению меланомы и саркомы дают преимущественно очаговые, а не инфильтративные метастазы в лёгких. Эти вторичные проявления относят к лимфогенным.
- Смешанные метастазы – сочетание очаговых и инфильтративных «теней» в лёгких – частое явление в клинической практике.
По числу метастазы могут быть:
- солитарными – один очаг;
- единичными – не более десяти;
- множественными.
Метастатические узлы бывают мелкими и крупными, а ещё сливающимися друг с другом, односторонними, когда поражено одно лёгкое и двухсторонними.
Вокруг метастазов тоже могут жить бактерии, всё-таки по бронхиальному дереву проходит нестерильный воздух, а опухоль меняет местный иммунитет, и возникает воспаление. Когда внутренняя часть опухоли не получает достаточного питания – она отмирает, и в центре образуется полость распада. Если такая полость соединится с бронхом, то в неё могут попасть бактерии, и полость заполнится гноем.
В чем разница между метастазами в легких и метастазами в плевре?
Плевра – пленка из соединительной ткани. Она состоит из двух листков: один покрывает снаружи легкие, а другой выстилает изнутри стенки грудной полости. Плевра интимно спаяна с лёгким. В ней тоже могут возникнуть метастазы, но намного реже. Опухоли из легких могут прорастать в плевру и наоборот. Зачастую в легких обнаруживаются метастазы, а плевра не поражена.
Диагностика
При подозрении на метастазы в легких прибегают к следующим методам диагностики:
- Рентгенография. Простой и быстрый, но не самый информативный метод диагностики. Обычно на снимках можно увидеть только опухоли размером более 1 см;
- Компьютерная томография. Позволяет обнаружить очаги менее 5 мм. Это недоступно для рентгенографии и МРТ;
- Биопсия легкого. Обычно проводится при помощи иглы. Получают небольшой фрагмент ткани опухоли для исследования;
- Бронхоскопия. Эндоскопическое исследование, во время которого специальный инструмент с источником света и видеокамерой – бронхоскоп – вводят в бронхиальное дерево. Во время процедуры можно провести биопсию.
Как правило, динамическое наблюдение за онкологическим пациентом после лечения первичной опухоли предполагает регулярную рентгенографию органов грудной клетки. При выявлении теней в лёгких, правильно будет сделать компьютерную томографию с введением контрастного вещества. КТ способна выявить очаги меньше 5 мм, что недоступно магнитно-резонансной томографии. В дальнейшем для контроля динамики процесса после лечения также необходимо будет делать КТ.
Бессмысленно перед лечением делать КТ, а после перейти на обычную рентгенографию лёгких, пытаясь сравнивать снимки, чтобы выявить отличие прошлого состояния лёгких с настоящим. КТ обнаружит более мелкие образования, рентген способен в лучшем варианте выявить очаги более 1 см, то есть опухоли меньше сантиметра «выпадают» из-под контроля, когда нет возможности сделать контрольное КТ-обследование. Нельзя оценивать эффект лечения по паре видимых крупных очагов. Некоторые опухоли от химиотерапии уменьшаются, какие-то увеличиваются, а другие месяцами стабильны.
Клиническая симптоматика
Клинические признаки метастазов в лёгких зависят от обширности поражения и присоединения воспалительных изменений.
Основные симптомы:
- боль в груди;
- упорный кашель;
- примесь крови в мокроте;
- ослабленное дыхание;
- хрипы;
- слабость;
- снижение веса.
При одиночных очагах округлой формы, небольшого размера никаких признаков поражения может и не быть, их часто случайно обнаруживают при контрольном обследовании. Площадь лёгких огромна, и несколько квадратных сантиметров опухолевого поражения альвеол не отразятся на газообмене и состоянии пациента. Множество теней, когда их уже не пересчитать, ухудшат самочувствие, провоцируя сухой кашель, плохо откликающийся на средства от кашля.
Инфильтративные метастазы раньше меняют самочувствие, поскольку к ним часто присоединяется воспаление окружающей опухоль ткани – пневмонит. Появляется кашель, может быть температура, слабость, почти как пневмония, но чуть-чуть полегче. Закупорка бронха опухолью приведёт к ателектазу – полной безвоздушности части лёгкого, присоединение инфекции существенно ухудшит состояние, повысится температура, появится одышка. Приём антибиотиков помогает снять воспаление и самочувствие улучшается, но ненадолго, потому что опухоль растёт, и безвоздушная часть лёгкого тоже увеличивается. И опять воспаляется, так и идёт по замкнутому кругу.
Лечение метастазов в лёгкие
Сегодня оперировать метастазы в лёгких стали чаще, чем раньше, но всё-таки операции делают довольно редко. Радикальное лечение метастазов в лёгкие – оперативное в принципе возможно при определённых условиях:
- не должно быть первичной опухоли или рецидива;
- не должно быть метастазов в других органах;
- метастаз в лёгком очаговый и единственный или не более 3 очагов;
- скорость прогрессирования опухолевого процесса должна быть невысокой, как правило, после радикального лечения первичной опухоли до появления метастаза должно пройти более года;
- со времени появления метастаза в лёгком в течение полугода не должно появиться других метастазов;
- состояние пациента должно позволять довольно сложное оперативное вмешательство, потому что во время операции реальная ситуация может оказаться значительно хуже, чем описывалась при компьютерной томографии, и придётся удалять больше запланированного.
Основное лечение метастазов в лёгких – химиотерапия, схема которой определяется первичной опухолью, при раке молочной железы ещё и гормональная терапия, естественно, при наличии чувствительности к ней.
Лучевая терапия множественных метастазов в лёгких проводилась в экспериментальных группах, результаты неудовлетворительные. При единственном довольно крупном очаге облучение возможно, но эффективность много хуже, чем при раке лёгкого. Наличие метастаза, где бы то ни было, показатель диссеминации – разброса злокачественных клеток, что не предполагает хорошего прогноза в отношении возможности полного излечения.
Каковы прогнозы выживаемости?
Метастазы в любом органе говорят о том, что защитные силы организма исчерпаны, опухолевые клетки успели распространиться по разным органам. Ремиссия в большинстве случаев невозможна. Но это не означает, что врач совсем ничего не может сделать. Паллиативное лечение поможет продлить жизнь, избавит от мучительных симптомов.
Паллиативная помощь при метастазах рака в легкие
Часть легкого, занятая опухолью, выключается из процесса дыхания. Поначалу оставшаяся здоровая ткань успешно справляется и работает за целое легкое. Но постепенно опухоль растет, перестает реагировать на химиотерапию и занимает все больше места.Наступает момент, когда оставшаяся здоровая ткань перестает справляться. Легкие больше не могут обеспечить организм нужным количеством кислорода, развивается дыхательная недостаточность. Кислородное голодание затрагивает все органы, в первую очередь — сердечно-сосудистую систему.
Симптомы дыхательной недостаточности нарастают постепенно:
- Поначалу возникает лишь одышка после ходьбы и физических нагрузок;
- Затем одышка начинает беспокоить при минимальных нагрузках, при любой движении;
- В тяжелых случаях человек задыхается постоянно, даже когда лежит в постели. Больного мучит постоянный кашель, слабость, на ногах появляются отеки, сердцебиение учащается. Стоит совершить небольшое движение, и все симптомы усиливаются на порядок.
Страдания больного может облегчить кислородотерапия. Но проводить ее нужно по 15 часов в день. Существуют специальные дыхательные маски, их можно приобрести, и все же проводить такое лечение в домашних условиях очень сложно.
Государственные онкологические клиники не госпитализируют таких пациентов в экстренном порядке. Помощь можно получить в отделении паллиативной медицины, но таких в Росии пока еще очень мало. В обычном стационаре практически ничем не помогут. Кислородотерапию можно получить в хосписе, но там практически нет симптоматической терапии. При тяжелой дыхательной недостаточности одной кислородотерапии недостаточно. Нужна дыхательная поддержка — искусственная вентиляция легких. В данном случае ИВЛ проводят через маску, интубацию трахеи не проводят.
Такое лечение не избавит от рака и не уничтожит метастазы, но оно способно сильно облегчить состояние больного:
- уменьшится одышка;
- отдохнуть дыхательные мышцы, которым в последнее время пришлось интенсивно работать;
- нормализуется состав крови, уменьшится кислородное голодание;
- уменьшатся даже воспалительные изменения в легких;
- в конце концов, человек перестанет задыхаться, улучшится качество жизни.
Помочь человеку с тяжелым нарушением дыхания в домашних условиях невозможно. Родные постоянно слышат, как он тяжело дышит, хрипит, кашляет, но помочь ничем не могут. Страдают все.
Врачи онкологи и реаниматологи Европейской онкологической клиники знают, как помочь пациенту с метастатическим раком легких в рамках паллиативной помощи. Грамотное лечение избавит от тяжелых симптомов, подарит драгоценное время.
Запись на консультацию круглосуточно
почему метастазы так сложно остановить?
Статья на конкурс «био/мол/текст»: Когда в организме случилось несчастье, и из 100 триллионов нормальных клеток хоть одна переродилась в раковую и не была уничтожена, срабатывает спусковой крючок, и запускается рост опухоли. Постепенно она приспосабливает к себе окружающие клетки, а также оказывает значительное влияние на весь организм. С развитием заболевания некоторые раковые клетки покидают опухоль и формируют метастазы — вторичные очаги опухолевого роста. Зачастую своевременное удаление первичной опухоли и послеоперационная терапия не способны вызвать ремиссию. Оказывается, что первичная опухоль способна «обучать» микроокружение в очагах развития будущих метастазов уже на ранних этапах своего роста. Кроме того, метастазные раковые клетки перепрограммируют экспрессию своих генов так, чтобы лучше прижиться в новом месте обитания. Знание того, как предотвратить эти процессы, а не только рост первичной опухоли, поможет спасти до 90% людей, умирающих от основных видов рака.

Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Усилия многих онкологов на протяжении последних десятилетий были направлены на установление деталей возникновения и развития рака — механизмов зарождения опухоли и регуляции ее активного роста, формирования благоприятного микроокружения из клеток стромы [2]. Эти знания несомненно привели к разработке новых подходов в терапии онкозаболеваний. Со временем стало понятно, что основная угроза рака заключена в способности к распространению по организму. Так, некоторые раковые клетки первичной опухоли (то есть развившейся изначально) отделяются от нее за счет эпителиально-мезенхимального перехода или других механизмов [3] и, попадая в кровоток или лимфоток, по маленьким капиллярам путешествуют в главные магистрали сосудистой системы. Они покидают ее за счет задержки в узких капиллярах органов, адгезии к их эндотелиальной стенке и выхода из просвета сосуда в строму органа (рис. 1). Лишь небольшой процент раковых клеток, покинувших первичную опухоль, преуспевает в этом процессе и выживает в новой среде. Эти клетки формируют будущие очаги роста опухоли в новых органах — метастазы.
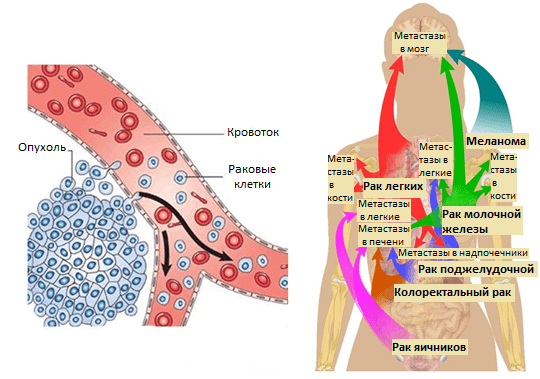
Рисунок 1. Метастазирование и пути рассеивания раковых клеток.
Процесс рассеивания раковых клеток по организму, названный метастазированием (от древнегреч. «менять, переносить»: meta — «через» + histanai — «устанавливать»), впервые описал еще в 1889 году Стивен Педжет [4], но механизм его развития оставался загадкой для ученого сообщества долгое время (рис. 2).
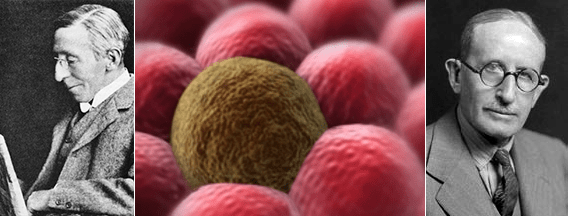
Рисунок 2. Основоположники учений о метастазировании: английский хирург Стивен Педжет (слева) и американский патолог Джеймс Юинг (справа).
Педжет провел аналогию такого распространения раковых клеток с прорастанием семян. Они тоже выживают и делятся на плодотворной «почве» — в подходящем микроокружении. В те времена невозможно было найти этому экспериментального подтверждения, и долго преобладала совсем иная теория — Джеймса Юинга (рис. 2). Он утверждал, что основную роль в распределении метастазов по организму играет динамика кровотока и устройство сосудистой системы.
Наконец в 1970-е годы в ходе нескольких экспериментов по инъекции радиоактивно меченных раковых клеток мышам Исаак Фидлер смог доказать, что результат метастазирования также зависит от природы раковых клеток. В этом случае клетки меланомы развивали метастазы только в легких, но не в печени, в сосудах которой они также задерживались, но позже не выживали [5].
Позднее было установлено еще больше фактов, подтверждающих, что раковые клетки разной природы метастазируют преимущественно в определенные органы и иногда даже в заданной последовательности. Например, клетки рака молочной железы — сначала в кости, печень, лимфатические узлы, легкие, а потом уже в мозг; клетки рака желудочно-кишечного тракта и яичников — в печень и легкие; рака простаты — в основном, в кости (рис. 1). Явление специфичного распределения метастазов по организму назвали органотропией метастазирования. Чаще всего метастазы встречаются в легких, печени и костях.
Несмотря на активные исследования, в онкологии все еще остается много вопросов без ответа. Отличаются ли метастазные раковые клетки от других клеток первичной опухоли? Что лежит в основе органотропии? Как метастазам удается выжить после удаления первичной опухоли и проведенной химиотерапии?
Генетическая информация лежит в основе программирования поведения клетки. Перерождение нормальных клеток организма в раковые (злокачественная трансформация) обусловлено мутациями в генах-драйверах, которые приводят к неконтролируемому клеточному делению. Помимо таких выгодных для опухолевых клеток мутаций, также происходят мутации в генах-пассажирах, то есть тех, что изначально не имеют влияния на рост опухоли. С каждым поколением, новым клоном внутри опухоли, накапливаются эти генетические изменения, и некоторые клоны преуспевают больше остальных, что стало основой для формирования представления об эволюции внутри опухоли. Одна из предложенных гипотез, почему некоторые клетки опухоли приобретают способность к метастазированию, основана на схожем со злокачественной трансформацией принципе. По всей видимости, у них тоже накапливаются мутации в генах-драйверах, которые запускают этот процесс. Однако экспериментального подтверждения она так и не нашла, ученые сходятся во мнении, что большинство клеток первичной опухоли способны метастазировать. А вот что происходит позже с геномами метастазных клеток?
В результате сравнения геномов клеток первичных опухолей молочных желез и их локальных (в ближайших лимфатических узлах) и отдаленных метастазов (в печени, легких, дальних лимфатических узлах) было установлено, что геномы метастазов продолжают эволюционировать в своих очагах роста независимо от первичной опухоли [6]. Интересно, что паттерн мутаций схож между метастазами в одном органе, но различен между метастазами в разных органах. Это означает, что раковые клетки на самом глубоком уровне адаптируются к новому микроокружению в зависимости от занятой ими ниши. Изучение генетических изменений при метастазировании рака поджелудочной железы выявило наличие разных субклонов (новых поколений клона), которые формируют метастазы. Однако различия между ними оказались не больше, чем между двумя случайно взятыми клетками одного организма [7].
Интересно, что обнаружили как минимум один ген, FBXW7, мутации в котором противодействуют метастазированию [8]. Происходит это за счет усиления провоспалительной реакции, пролиферации и активности T-лимфоцитов, которые стимулируют формирование адаптивного иммунитета к опухолевым клеткам. Таким образом, мутации в гене FBXW7 противодействуют опухолевой иммунносупрессии. Ее проявления, такие как уменьшение количества лимфатических сосудов и эффекторных T-лимфоцитов в первичной опухоли, связаны с лицензированием метастазирования [8].
Следующую ступень в регуляции экспрессии генов после непосредственных изменений в ДНК (мутаций, вариаций числа копий и т.д.) занимают эпигенетические изменения (метилирование гистонов, ДНК и др.) (рис. 3). По своей природе они более пластичны, более переменчивы по сравнению с генетическими изменениями и подвластны влиянию клеточной сигнализации, которая подстраивается под воздействие внешних факторов. Оказалось, что эпигенетический код значительно отличается в клетках метастазов по сравнению с первичной опухолью. При раке поджелудочной железы потеря большого количества меток неактивного хроматина (гетерохроматина) — метилирования гистонов (h4K9, h5K20) — и ослабление метилирования ДНК связаны с метастазированием. Эти модификации в раковых клетках переводят участки гетерохроматина в активное состояние, доступное для транскрипционных факторов, и в результате усиливают экспрессию генов онкогенеза, таких как регуляторы мезенхимального фенотипа, KRAS-сигнализации и метаболизма [9].
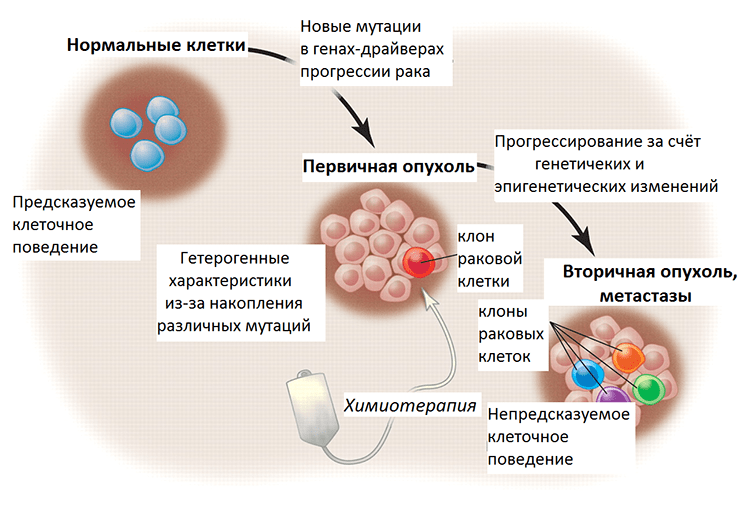
Рисунок 3. Злокачественная трансформация и прогрессирование рака в перспективе генетических и эпигенетических изменений. Нормальные клетки ткани имеют предсказуемое поведение — темпы пролиферации, срок жизни, характер взаимодействия с другими клетками. При злокачественной трансформации накапливаются мутации, и постепенно опухоль становится генетически гетерогенной (состоит из нескольких клонов, поколений раковых клеток). Химиотерапия уничтожает некоторые клоны, тогда как другие, с выгодными в новых условиях мутациями, выживают и создают новых клонов. Их поведение уже непредсказуемо, так как генетические и эпигенетические изменения этих раковых клеток привели к приобретению ими новых свойств.
Эпигенетическая регуляция является одним из важнейших механизмов программирования клеточного метаболизма. С ростом опухоли внутри нее образуются области с недостаточным снабжением кислородом (гипоксией), так как до них не доходят кровеносные сосуды. Это вызывает в раковых клетках активацию гена фактора, индуцируемого гипоксией (HIF-1α). Происходит это за счет эпигенетического освобождения, деметилирования промотора гена, который становится доступным для транскрипционных факторов. Усиленное образование и активность белка HIF-1α, в свою очередь, регулирует экспрессию генов множества метаболических ферментов и транспортеров, что приводит к комплексным изменениям метаболизма раковых клеток и поддерживает их потребности.
Клеточный метаболизм разделен на процессы расщепления с выделением энергии (катаболизм) и образования соединений с использованием энергии (анаболизм). Энергетический обмен клетки протекает за счет этапов клеточного дыхания — гликолиза, цикла трикарбоновых кислот и окислительного фосфорилирования. Раковые клетки по-своему приспосабливаются к сохранению продуктивности энергетического обмена в условиях недостатка кислорода. В первичной опухоли они, в основном, используют анаэробный гликолиз, а не окислительное фосфорилирование, как в нормальных клетках. Это усиленное поглощение глюкозы с преобразованием до лактата, выделяемого раковыми клетками, названо эффектом Варбурга. Он позволяет им выжить при гипоксии и активно пролиферировать за счет использования промежуточных соединений для биосинтеза и выделения энергии [10].
Преимущественный способ генерирования энергии у метастазов, однако, до сих пор мало изучен. Используя клетки рака молочной железы, обладающие широкой или специфической органотропией при метастазировании, ученые обнаружили различия в метаболизме первичной опухоли и метастазов. Раковые клетки, колонизировавшие кости и легкие, активировали использование окислительного фосфорилирования, колонизировавшие печень — гликолиз. Когда раковые клетки колонизировали все вышеперечисленные очаги, они активировали сразу оба метаболических пути (рис. 4) [11]. Похоже, что такая пластичность помогает раковым клеткам освоить новые ниши для колонизации. Например, в печени гликолитический фенотип поддерживается при росте метастазов за счет активности упомянутого ранее фактора HIF-1α, а также повышенной экспрессии белка PDK1. Это фермент, который ингибирует формирование соединения ацетил-КоА. И так как его поток на развилке с гликолитическим путем в цикл трикарбоновых кислот уменьшается, усиливается образование конечного продукта гликолиза — лактата [12].
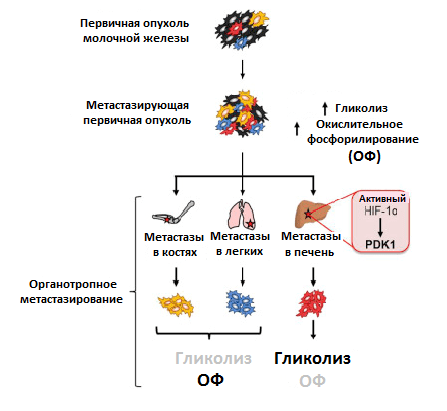
Рисунок 4. Различия в метаболизме первичной опухоли и метастазов в разных органах. Условные обозначения: ОФ — окислительное фосфорилирование; HIF-1α — индуцируемый гипоксией фактор 1; PDK1 — пируватдегидрогеназный комплекс 1.
Почему же для метастазов в одном органе выгоднее использовать преимущественно один вид метаболизма, чем другой? Ответ на этот вопрос и роль различных факторов в регуляции метаболической пластичности раковых клеток еще только предстоит узнать.
И все же метастазные раковые клетки не могут в одиночку справиться со столь непростой задачей — освоением совершенно незнакомого места обитания. Эксперименты группы Дэвида Лидена в 2005 году впервые показали, что первичная опухоль за счет продуцируемых факторов стимулирует формирование так называемых преметастазных ниш в различных органах. Ученые показали, что раковые клетки первичной опухоли за счет стимулирования рецептора фактора роста сосудов (VEGFR-1) на миелоидных клетках-предшественниках активируют их распространение из костного мозга в известные очаги развития метастазов [13]. Кроме того, в этих очагах запускается избыточная экспрессия фибробластами одного из компонентов внеклеточного матрикса (ВКМ) — фибронектина. Миелоидные клетки-предшественники, имея рецепторы клеточной адгезии (интегрины) к этому белку, активно «ловятся на удочку» и заселяют преметастазные ниши. Они секретируют воспалительные цитокины, факторы роста и проангиогенные факторы, стимулирующие формирование сосудов. Это способствует ремоделированию стромы и колонизации ее метастазами (рис. 5) [13].
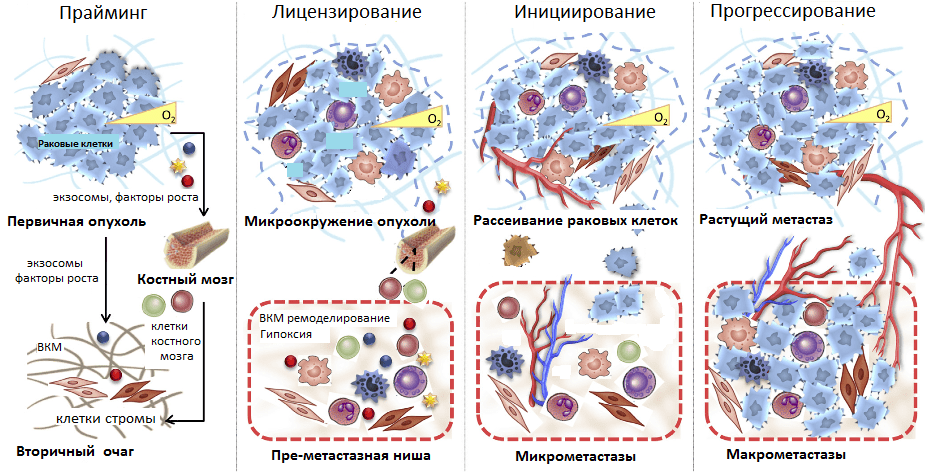
Рисунок 5. Стадии развития метастазов. Прайминг, или обучение, будущего вторичного очага роста первичной опухолью; лицензирование — иммуносупрессия первичной опухоли, создание благоприятного микроокружения в преметастазных нишах; инициирование — начало метастазирования и освоения преметастазной ниши; прогрессирование — рост метастазов во вторичном очаге.
Таким образом, в текущем представлении формирование метастазов происходит в несколько стадий. Начиная с раннего роста первичной опухоли происходит прайминг — обучение будущих ниш развития метастазов с помощью выделения различных факторов раковыми клетками, привлечения клеток из костного мозга. Затем клетки стромы первичной опухоли и преметастазных ниш (фибробласты, клетки миелоидного ряда, T-лимфоциты) формируют благоприятное микроокружение, лицензируя дальнейшее расселение метастазов. Фаза инициирования метастазирования заключается в росте сосудов, ангиогенезе, по которым метастазные клетки покидают первичную опухоль и приходят в преметастазные ниши. Прогрессирование — это финальный этап перехода микрометастазов в макрометастазы — вторичные сформированные опухоли. Он может занять от нескольких месяцев до нескольких лет (рис. 5).
Хотя для большинства органов характерна эта общая схема, существуют некоторые особенности в зависимости от места (органа) формирования ниши. Например, преметастазная ниша в печени и легких также формируется за счет привлечения нейтрофилов. Известно, что они могут помогать метастазирующим клеткам при интеграции в новую нишу за счет секретирования протеаз, цитокинов и непосредственного контакта с раковыми клетками при выходе из капилляров. Другой пример — клетки рака поджелудочной железы. Они выделяют экзосомы — липидные везикулы, которые переносят макрофаг-ингибирующий фактор (MIF). Их поглощают клетки Купфера в печени, и это запускает цепочку обучения ниши. Клетки Купфера синтезируют трансформирующий фактор роста β (TGF-β), клетки Ито активируются им и запускают перестраивание ВКМ, затем привлекая к нему макрофагов [15]. Их роль в микроокружении опухоли подробнее рассмотрена в статье «Одураченные макрофаги, или несколько слов о том, как злокачественные опухоли обманывают иммунитет» [16].
Метастазы в костях — одни из самых коварных, и их преметастазная ниша по-своему особенна. Например, оказалось, что при раке молочной железы только раковые клетки без рецепторов к эстрогену метастазируют в кости. Такие клетки первичной опухоли активно выделяют фермент лизилоксидазу. В костях он вызывает образование взрослых остеокластов и за счет этого стимулирует резорбцию кости. [17]. Именно эти «емкости» внутри кости метастазы занимают позднее. Другая и, пожалуй, основная функция лизилоксидазы — формирование поперечных связей между коллагеновыми волокнами ВКМ — также связана с образованием преметастазных ниш, но в легких. Преобразование коллагеновых волокон привлекает миелоидные клетки, а те позднее разрушают коллагеновые сети и дают путь раковым клеткам при заселении ткани легкого [18].
При некоторых типах рака, таких как меланома, для успешного метастазирования в лимфатические узлы и органы необходимо формирование новых лимфатических сосудов в их преметастазной нише. Недавно ученые установили, что такой лимфангиогенез начинается на ранних стадиях роста первичной опухоли, и медиатором его запуска является фактор роста мидкин, секретируемый клетками меланомы в составе экзосом или в свободном виде [19].
Безусловно, механизмы формирования преметастазных ниш в комплексе позволяют лучше понять развитие рака и не перестают удивлять своей сложностью.
Причины органотропии
Описанные различия в специфичных механизмах формирования ниш могут служить одним из объяснений органотропному метастазированию, но как раковые клетки, которые могут метастазировать сразу в несколько органов, выбирают только один из них?
Ключевой механизм, известный на данный момент, основан на обучении будущих очагов рассеивания метастазов с помощью специфичных к ним экзосом. Эти везикулы, ранее описанные в статье «Экзосома — механизм координации и взаимопомощи клеток организма» [20], представляют собой структуры с рецепторами на своей поверхности и генетическим и секретируемым материалом внутри. Ученые провели интересный эксперимент — выделили экзосомы от раковых клеток разного происхождения (рака груди, поджелудочной железы и пр.) и, внедрив их в кровоток мышей с отличным типом опухоли, показали, что с их помощью возможно перепрограммировать распределение метастазов по органам. Это обусловлено тем, что экзосомы разных типов рака преимущественно содержат на своей поверхности основные рецепторы адгезии, интегрины, специфичные к определенному белку ВКМ (к ламинину — α6β4 и α6β1; к фибронектину — αvβ5 и т.д.).
Именно они адресуют доставку экзосом в определенный орган, который преимущественно имеет этот специфический ВКМ-белок в составе стромы. Сливаясь с мембранами клеток стромы того или иного органа, экзосомы доставляют содержимое и запускают свою программу: в фибробластах легких — через экспрессию одних генов S100, в клетках Купфера в печени — через экспрессию других. Активность этих генов стимулирует клеточную сигнализацию и воспалительные реакции, которые занимаются обучением преметастазной ниши (рис. 6) [21].
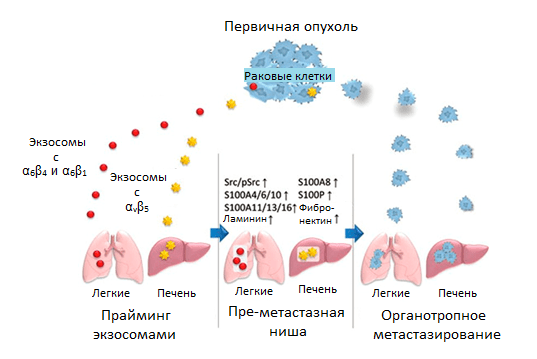
Рисунок 6. Регуляция органотропного метастазирования с помощью прайминга преметастазной ниши экзосомами со специфическими рецепторами интегринами. Условные обозначения: α6β4 и α6β1 — гетеродимеры интегринового рецептора; Src/pSrc — пропорция неактивной/активной форм киназы.
Подведем итог: описанные здесь механизмы, очевидно, усложняют картину течения онкозаболеваний и развития тактик их лечения. Важно подчеркнуть, что гетерогенность первичной опухоли и метастазов по ряду рассмотренных здесь признаков (генетическая, метаболическая, нишевая) дает понимание того, что следует использовать комбинированное и таргетное лечение на разных стадиях течения болезни. Как подтверждение тому — результаты одного из последних исследований, проведенных на материалах пациента с рецидивами между курсами длительной иммунотерапии. Сравнение популяций T-лимфоцитов из микроокружения разных метастазов показало, что они гетерогенны [22] и, следовательно, первичная, вторичные и т.д. опухоли по-разному отвечали на лечение.
Мы также знаем, что после химиотерапии зачастую выживают субклоны раковых клеток с полезными в новой среде мутациями. Под стрессом воздействия цитостатиков субклоны раковых клеток активируют секрецию факторов роста и запускают клеточную сигнализацию, препятствующую гибели (рис. 7). Кроме того, их выживанию помогает поддержка клеток стромы, заодно изменяющих свое поведение на «оборонительное» под эффектом терапии.
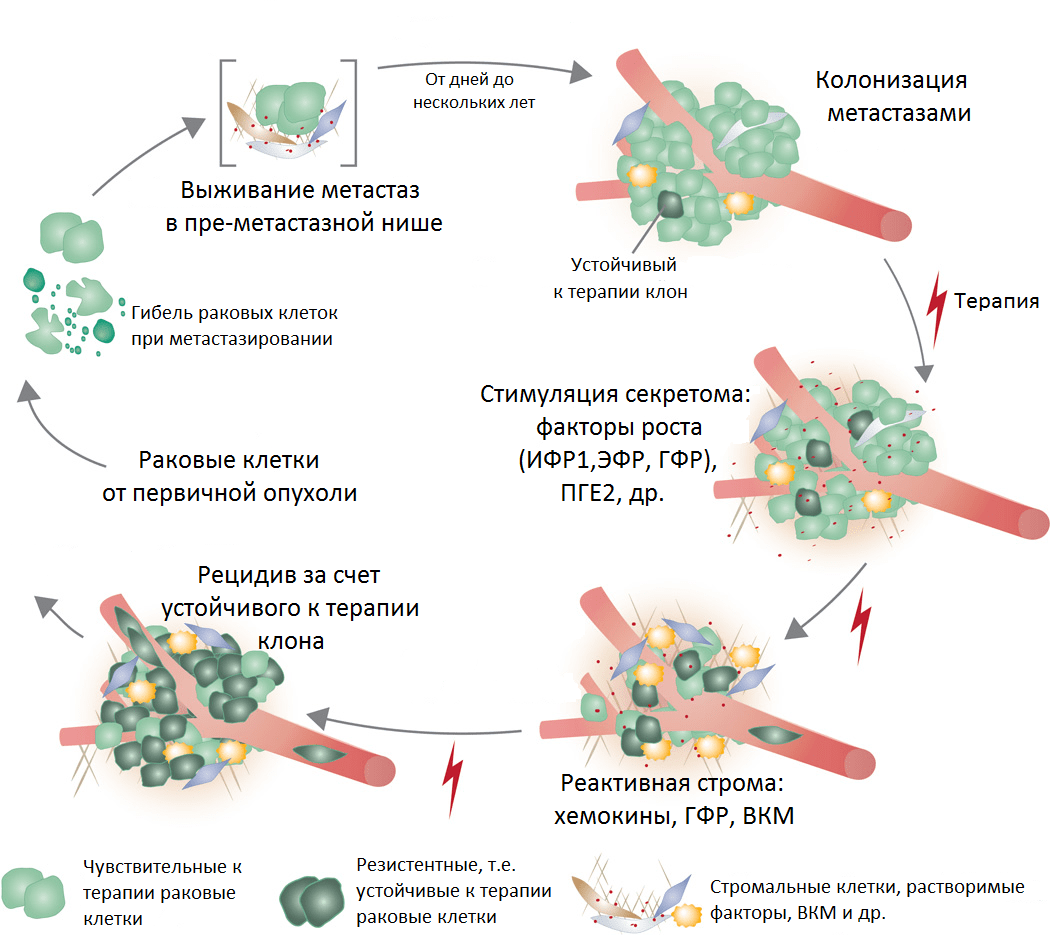
Рисунок 7. Реакция метастазов на терапию, образование резистентности и развитие рецидива. Условные обозначения: ИФР1 — инсулиноподобный фактор роста; ЭФР — эпидермальный фактор роста; ГФР — фактор роста гепатоцитов; ПГЕ2 — простагландин 2; ВКМ — внеклеточный матрикс.
Обнаружение преметастазных ниш и понимание их устройства предложили по-новому взглянуть на развитие подходов в терапии. Если бы стало возможным предотвратить формирование преметастазных ниш, то с большой вероятностью было бы остановлено метастазирование, а значит, и возможность ремиссии. Будем и дальше следить за прорывами в этой области.
- Shimpei I. Kubota, Kei Takahashi, Jun Nishida, Yasuyuki Morishita, Shogo Ehata, et. al.. (2017). Whole-Body Profiling of Cancer Metastasis with Single-Cell Resolution. Cell Reports. 20, 236-250;
- Опухолевые разговоры, или Роль микроокружения в развитии рака;
- Krakhmal N.V., Zavyalova M.V., Denisov E.V., Vtorushin S.V., Perelmuter V.M. (2015). Cancer invasion: patterns and mechanisms. Acta Naturae. 7, 17–28;
- Stephen Paget. (1889). THE DISTRIBUTION OF SECONDARY GROWTHS IN CANCER OF THE BREAST.. The Lancet. 133, 571-573;
- Fidler I.J. (1970). Metastasis: quantitative analysis of distribution and fate of tumor emboli labeled with 125 I-5-iodo-2’-deoxyuridine. J. Natl. Cancer Inst. 45, 773–782;
- Lucy R. Yates, Stian Knappskog, David Wedge, James H.R. Farmery, Santiago Gonzalez, et. al.. (2017). Genomic Evolution of Breast Cancer Metastasis and Relapse. Cancer Cell. 32, 169-184.e7;
- Alvin P Makohon-Moore, Ming Zhang, Johannes G Reiter, Ivana Bozic, Benjamin Allen, et. al.. (2017). Limited heterogeneity of known driver gene mutations among the metastases of individual patients with pancreatic cancer. Nat Genet. 49, 358-366;
- B. Mlecnik, G. Bindea, A. Kirilovsky, H. K. Angell, A. C. Obenauf, et. al.. (2016). The tumor microenvironment and Immunoscore are critical determinants of dissemination to distant metastasis. Science Translational Medicine. 8, 327ra26-327ra26;
- Oliver G McDonald, Xin Li, Tyler Saunders, Rakel Tryggvadottir, Samantha J Mentch, et. al.. (2017). Epigenomic reprogramming during pancreatic cancer progression links anabolic glucose metabolism to distant metastasis. Nat Genet. 49, 367-376;
- Вослед Варбургу — последние достижения в изучении биоэнергетики рака;
- J. M. Rosen, C. T. Jordan. (2009). The Increasing Complexity of the Cancer Stem Cell Paradigm. Science. 324, 1670-1673;
- Fanny Dupuy, Sébastien Tabariès, Sylvia Andrzejewski, Zhifeng Dong, Julianna Blagih, et. al.. (2015). PDK1-Dependent Metabolic Reprogramming Dictates Metastatic Potential in Breast Cancer. Cell Metabolism. 22, 577-589;
- Rosandra N. Kaplan, Rebecca D. Riba, Stergios Zacharoulis, Anna H. Bramley, Loïc Vincent, et. al.. (2005). VEGFR1-positive haematopoietic bone marrow progenitors initiate the pre-metastatic niche. Nature. 438, 820-827;
- Yang Liu, Xuetao Cao. (2016). Characteristics and Significance of the Pre-metastatic Niche. Cancer Cell. 30, 668-681;
- Bruno Costa-Silva, Nicole M. Aiello, Allyson J. Ocean, Swarnima Singh, Haiying Zhang, et. al.. (2015). Pancreatic cancer exosomes initiate pre-metastatic niche formation in the liver. Nat Cell Biol. 17, 816-826;
- Одураченные макрофаги, или Несколько слов о том, как злокачественные опухоли обманывают иммунитет;
- Thomas R. Cox, Robin M. H. Rumney, Erwin M. Schoof, Lara Perryman, Anette M. Høye, et. al.. (2015). The hypoxic cancer secretome induces pre-metastatic bone lesions through lysyl oxidase. Nature. 522, 106-110;
- Janine T. Erler, Kevin L. Bennewith, Thomas R. Cox, Georgina Lang, Demelza Bird, et. al.. (2009). Hypoxia-Induced Lysyl Oxidase Is a Critical Mediator of Bone Marrow Cell Recruitment to Form the Premetastatic Niche. Cancer Cell. 15, 35-44;
- David Olmeda, Daniela Cerezo-Wallis, Erica Riveiro-Falkenbach, Paula C. Pennacchi, Marta Contreras-Alcalde, et. al.. (2017). Whole-body imaging of lymphovascular niches identifies pre-metastatic roles of midkine. Nature. 546, 676-680;
- Экзосома — механизм координации и взаимопомощи клеток организма;
- Ayuko Hoshino, Bruno Costa-Silva, Tang-Long Shen, Goncalo Rodrigues, Ayako Hashimoto, et. al.. (2015). Tumour exosome integrins determine organotropic metastasis. Nature. 527, 329-335;
- Alejandro Jiménez-Sánchez, Danish Memon, Stephane Pourpe, Harini Veeraraghavan, Yanyun Li, et. al.. (2017). Heterogeneous Tumor-Immune Microenvironments among Differentially Growing Metastases in an Ovarian Cancer Patient. Cell. 170, 927-938.e20;
- Joan Massagué, Anna C. Obenauf. (2016). Metastatic colonization by circulating tumour cells. Nature. 529, 298-306.

