Метотрексат или арава что лучше – МЕТОТРЕКСАТ таблетки – инструкция по применению, отзывы, состав, аналоги, форма выпуска, побочные эффекты, противопоказания
(OFFLINE) Метотрексат vs Арава – Медикаментозная терапия
Lina (11.4.2012, 3:31) писал:
На сульфасалазине потеряла драгоценное время(1,5 года).
Lina, как я тебя понимаю, мне тоже безумно жалко года, который я просидела на сульфасалазине. Причем не просто не было эффекта от него – гораздо хуже, у меня в результате именно на нем случилось сильнейшее за весь мой анамнез обострение. Очень боюсь повторения этой истории.SagaanDara (11.4.2012, 3:57) писал:
я за Араву. Она мне хорошо подошла, от метотрексата много побочек было. Плаквенил без эффекта. Другое не использовала. Пью уже полгода.
SagaanDara, а плаквенил – что за зверь? Базис, цитостатик? Если не ошибаюсь, это устаревший препарат, сейчас его избегают назначать, или нет?Дрофа (11.4.2012, 8:03) писал:
Я не смогла вообще ее принимать. Дело закончилось приемом одной таблетки в пятницу на ночь, а в субботу рано утром супруг сдал меня в стационар (была на дневном) с жутким отеком и дикой рвотой. Больше Араву не принимала.
Елена2011 (11.4.2012, 13:52) писал:
Склоняюсь к араве, уже не так пугает процесс отмывания.
Елена2011, почитала еще раз про процедуру отмывания углем. Жесть, конечно. Оказывается, отмываться от аравы надо не только перед планируемой беременностью, но и в случае возникновения сильных побочек.Nadia_1 (11.4.2012, 22:53) писал:
мне мой ревматолог сказал, что методжект все-такие более эффективный преп.., в процентном соотношении большему числу людей помогает
Nadia_1, методжект – это коммерческое название метотрексата? Я так поняла, этих метотрексатов пруд пруди – сколько фармфирм, столько и метотрексатов.юла (11.4.2012, 23:49) писал:
в 2003 году мне назначили вместе араву и метотрексат. Тогда вобще было модно эти препараты именно вместе назначать. В итоге, не помогали они мне потом тоже вместе!))))
юла, было очень агрессивное течение РА? Странная мода.Метотрексат аналоги при ревматоидном артрите — Все про суставы
3318 0
 Чтобы с возрастом не превратиться в сгорбленную под тяжестью прожитых лет старушку и как можно дольше сохранять легкость во всем теле, позаботьтесь о своих суставах до того, как получите сигнал SOS.
Чтобы с возрастом не превратиться в сгорбленную под тяжестью прожитых лет старушку и как можно дольше сохранять легкость во всем теле, позаботьтесь о своих суставах до того, как получите сигнал SOS.
Как известно, скелет – основа структуры тела, а суставы — области, где сходятся кости, позволяя ему быть гибким. Постепенно, с возрастом кости утрачивают кальций и другие минералы.
Вместе с ними теряется плотность и масса костей. То же самое касается и позвоночника, со временем он искривляется и сжимается.
В процессе этих изменений суставы становятся твердыми. Жидкость в них может понижаться, и хрящи при трении друг о друга, разрушаются.
Такое же действие оказывает кальцификация из-за отложения солей в суставах. Существует целый ряд болезней костей и суставов, к которым склонны люди после 40 лет, и женщин среди них в 5 раз больше, чем мужчин.
Содержание статьи
Содержание статьи:
Ревматоидный артрит — болезнь опасная, но излечимая
Одним из этих неприятных заболеваний является ревматоидный артрит. Суставы припухают, становятся болезненными, отмечается повышение температуры. Подвижность суставов уменьшается, особенно это наблюдается утром.
Значительная выраженность артрита или его острая форма, могут сопровождаться общей слабостью, лейкоцитозом, лихорадочным состоянием.
Ревматоидный артрит может поражать внутренние органы. Если при отечности вас беспокоят покраснение и боль в суставах, посетите ортопеда и ревматолога.
Лечите болезнь правильно
Первым симптомом является боль в суставе, которая мешает спать, ходить, и, пытаясь избавиться от нее, люди готовы испробовать любое чудо-лекарство.
Но многие из широко используемых препаратов не избавляют от ревматоидного артрита, а лишь помогают комплексному лечению.
Попробуем разобраться, для чего используется то или иное лекарство.
Медикаментозная терапия — основа основ
Современные лекарственные методы борьбы с ревматоидным артритом делятся на несколько групп.
Нестероидные противовоспалительные препараты
Их традиционно применяют для устранения воспаления суставов и снятия боли. После ликвидации этими препаратами боли, можно перейти к физиотерапевтическим процедурам. НПВП действуют быстро, и зачастую из-за эффективности этого лечения больные в следующий раз снова пользуются ими.
Создается обманчивое впечатление, что эти препараты способствуют излечению, но НПВП лишь снимают симптомы болезни, а артрит тем временем продолжает прогрессировать.
Глюкокортикоидные препараты
С их помощью во многих случаях состояние пациента значительно облегчается. В больной сустав вводятся препараты кортикостероидных гормонов. Они хороши тем, что способствуют быстрому подавлению воспаления и болевых ощущений при отеке и припухании сустава. Однако, как и НПВП, их следует применять в комплексной терапии.
Следует знать: делать такие инъекции в один и тот же сустав крайне нежелательно чаще двух раз в месяц.
Введенное лекарство даст эффект не сразу, врач может зафиксировать результат процедуры спустя 10-12 дней.
Базисные препараты
 Они прицельно оказывают воздействие на базис – основу болезни. Эти средства способны прервать развитие заболевания. Но в отличие от НПВП и гормонов, базисные препараты не убирают симптомы заболевания в первые дни и недели их использования.
Они прицельно оказывают воздействие на базис – основу болезни. Эти средства способны прервать развитие заболевания. Но в отличие от НПВП и гормонов, базисные препараты не убирают симптомы заболевания в первые дни и недели их использования.
Их недостаток заключается в том, что оказываемое действие происходит примерно через месяц.
Базисные препараты приостанавливают развитие ревмотоидного артрита и в течение определенного промежутка времени дают улучшение.
Но предугадать результат не может даже опытный специалист, и итог зависит и от опыта врача, и от его интуиции.
Базисная терапия применяет препараты пяти групп:
- Антималярийные лекарства – результат применения можно ощутить через полгода — год при условии их непрерывного приема. Из всех базисных препаратов они наиболее слабые. Начинать с них базисную терапию можно в том случае, когда заболевание слабо выражено, и применять более сильные лекарства нет смысла. Достоинство антималярийных лекарств – неплохая переносимость и отсутствие побочных эффектов.
- Соли золота – помогают больным на начальной стадии ревматоидного артрита, с быстро прогрессирующим заболеванием: появившимися ревматоидными узелками, костными эрозиями, со значительными показателями в крови РФ — ревматоидного фактора. Если пациент не получает ожидаемую помощь от НПВП при сильных болях в суставах и утренней скованности, то применение препаратов золота может принести положительный результат.
- Д-пеницилламин – если лечение ревматоидного артрита Метотрексатом, фолиевой кислотой или солями золота не помогает
 пациенту, или эти препараты отменяют из-за их непереносимости организмом, тогда врач применяет Д-пеницилламин. И хотя это лекарство по результатам использования не уступает упомянутым препаратам, оно еще более токсично и чаще способствует осложнениям. Побочные явления при нем возникают в 30-40% случаев, поэтому лечение этим препаратом назначают только в самых крайних случаях, когда пациент крайне нуждается в неотложной помощи.
пациенту, или эти препараты отменяют из-за их непереносимости организмом, тогда врач применяет Д-пеницилламин. И хотя это лекарство по результатам использования не уступает упомянутым препаратам, оно еще более токсично и чаще способствует осложнениям. Побочные явления при нем возникают в 30-40% случаев, поэтому лечение этим препаратом назначают только в самых крайних случаях, когда пациент крайне нуждается в неотложной помощи. - Сульфаниламиды – антимикробные препараты по силе лечебного воздействия менее эффективны, чем препараты золота и метотрексат, но могут сравниться по результативности с Д-пеницилламином. Главное преимущество этих препаратов заключается в их хорошей переносимости. Антимикробные средства даже при длительном применении почти не дают побочных эффектов, а небольшие проявления не бывают тяжелыми. Недостаток сульфаниламидных препаратов – в их медленном действии на организм: улучшение состояния наступает после трех месяцев лечения.
- Цитостатики считаются наиболее эффективной группой базисных препаратов для лечения всех видов артрита. Их терапевтический результат является положительным для 70-80% больных ревматическим артритом. Побочные явления наблюдаются у каждого пятого-шестого пациента, но не отличаются тяжестью поражения.
Аллергические сыпи, небольшие нарушения мочеиспускания, расстройство стула, – все это проходит после отмены цитостатиков. Чтобы контролировать состояние пациента, следует во время приема препаратов исследовать мочу, кровь из пальца и вены.
Если пациент хорошо переносит цитостатическую терапию, то улучшение наступит через 2-4 недели.
В настоящее время ревматологи чаще всего используют для лечения ревматоидного артрита 3 цитостатических препарата:
- Ллефлуномид, или Арава;
- Инфликсимаб, или Ремикейд;
- Метотрексат.
Как применять Метотрексат: инструкция по применению
Метотрексат по праву считается лучшим базисным препаратом для лечения ревматоидного артрита – имеет формы внутреннего, подкожного или внутривенного введения.
Если у пациента есть проблемы с органами ЖКТ, то препарат назначается в инъекциях.
При его применении необходим постоянный врачебный контроль состояния крови, чтобы предупредить появление интоксикации.
Для лечения ревматоидного артрита лекарство получают всего лишь 1 раз (по 7.5 мг) в неделю, в пожилом возрасте или при почечной болезни – 5 мг.
На протяжении лечебного курса препарат принимают именно в конкретный день недели, начало базисной терапии. Эффект от лечения обычно выявляется через 30-40 дней от начала приема и достигает пика после 6-12 месяцев.
Метотрексат рекомендуется принимать до еды.
 Определив переносимость организма, через месяц врач может повысить дозу на 2,5-5,0 мг в неделю, максимум, до 25 мг в неделю. После достижения результата начинается снижение дозы до терапевтически эффективной.
Определив переносимость организма, через месяц врач может повысить дозу на 2,5-5,0 мг в неделю, максимум, до 25 мг в неделю. После достижения результата начинается снижение дозы до терапевтически эффективной.
Длительность терапевтического курса определяет врач по результатам лечения.
В день приема препарата ни в коем случае не стоит применять нестероидные противовоспалительные препараты. В остальные дни недели использование НПВП не возбраняется.
Ревматоидный артрит – очень сложное заболевание, но применение Метотрексата помогает держать недуг под контролем, а иногда и достичь на несколько лет стойкой ремиссии.
Сочетание с фолиевой кислотой — двойной удар по болезни
Фолиевая кислота применяется во время лечения ревматоидного артрита Метотрексатом, и оказывает благотворное влияние на терапию. Такое сочетание положительно влияет на результат лечения.
Фолиевую кислоту выписывают в комплексе с Метотрексатом, и ее прием предохраняет организм от побочных действий во время терапии.
Отдельного применения фолиевой кислоты нужно избегать, чтобы не получить нежелательных последствий.
Когда следует отказаться от такого лечения?
Любой лекарственный препарат – орудие обоюдоострое. Поэтому его применение может привести к всевозможным осложнениям и побочным реакциям.
Лечение следует прекратить, если у пациента наблюдается на лекарство следующая реакция:
- тяжелая печеночная и/или почечная недостаточность;
- непереносимость препарата;
- беременность;
- лактация;
- угнетение костномозгового кроветворения;
- иммунодефицит.
Или появились побочные эффекты, как то:
- нарушение функции почек или признаки цистита;
- зубная боль, тошнота или рвота, головокружение;
- снижение аппетита;
- сонливое состояние, головная боль;
- зуд, сыпь, лихорадка;
- выраженные нарушения зрения;
- цирроз печени.
Из практики больных
Отзывы пациентов о лечении Метотрексатом, в основном, однозначны: его применение привело к значительным улучшениям здоровья или полному излечению от ревматоидного артрита.
 Благодаря этим процедурам, многие из тех, кто страдает заболеванием суставов, признают, что держат заболевание под контролем.
Благодаря этим процедурам, многие из тех, кто страдает заболеванием суставов, признают, что держат заболевание под контролем.
Больные отмечают, что после лечения с помощью препарата стали реже сидеть «на больничном», ощутили легкость в ходьбе.
У некоторой части больных применение препарата вызвало побочные эффекты, например: появление сыпи, цистит, тошноту, снижение аппетита, боли в печени.
После этих проявлений доза препарата у них была сокращена, или лечение было пересмотрено. Особенно, такие жалобы на ухудшение здоровья отмечены у больных в старческом возрасте.
Лекарство дает улучшение при онкологических заболеваниях: раке костей и суставных хрящей.
Лечебная терапия с применением Метотрексата комплексная: она пытается вернуть не только подвижность суставам, но и облегчить страдания человека от боли. Опыт применения этого метода доказывает эффективность препарата и его безопасность при врачебном контроле.
Но, ни одно лекарство, и даже самый лучший врач не помогут, если больной сам не возьмется за свое здоровье: вовремя обратится к специалисту и не запустит свою болезнь, ведь лечение суставов – дело длительное.
Source: osteocure.ru
Читайте также
Что лучше при ревматоидном артрите метотрексат или арава
Многие годы пытаетесь вылечить СУСТАВЫ?
Глава Института лечения суставов: «Вы будете поражены, насколько просто можно вылечить суставы принимая каждый день…Читать далее »
В соответствии с рекомендациями Европейской антиревматической лиги сразу после установки диагноза назначают Метотрексат при ревматоидном артрите. Эксперты Американской коллегии ревматологов также предлагают применять в первую очередь «золотой стандарт» лечения системного заболевания. Лекарственный препарат отвечает принципам программы «Treat to Target — Т2Т» («Лечение до достижения цели»), которая была разработана в 2008 году представителями 25 стран Европы, Северной и Латинской Америки, Австралии и Японии. Она включает в себя стратегические терапевтические подходы, обеспечивающие наилучшие результаты в лечении патологии.
Описание препарата Метотрексат
Метотрексат является цитостатическим препаратом из группы антиметаболитов, антагонистов фолиевой кислоты. Цитостатиками называют противоопухолевые лекарственные средства, которые нарушают процессы роста и развития тканей, в том числе злокачественных. Они негативно влияют на механизм деления и восстановления клеток. Наиболее чувствительны к цитостатикам быстро делящиеся клетки, в том числе клетки костного мозга. Благодаря такому свойству цитостатические препараты применяются для лечения аутоиммунных заболеваний. Угнетая образование лейкоцитов в кроветворной ткани костного мозга, они подавляют иммунитет.
Иммуносупрессивная терапия является основой лечения ревматоидного артрита, поскольку заболевание является аутоиммунным. При аутоиммунных патологиях защитные силы организма начинают бороться со своими собственными клетками, разрушая здоровые суставы, ткани и органы. Иммуносупрессивная терапия приостанавливает развитие симптомов и затормаживает разрушительные процессы в сочленениях. Цитостатики сдерживают рост соединительной ткани в суставе, которая постепенно разрушает хрящи и субхондральные отделы костей (прилегающие к сочленению, покрытые хрящевой тканью).
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!
Для лечения суставов наши читатели успешно используют СустаЛайф. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Действие Метотрексата основано на блокировании дигидрофолатредуктазы (фермента, расщепляющего фолиевую кислоту). Препарат нарушает синтез тимидинмонофосфата из дизоксиуридинмонофосфата, блокируя образование ДНК, РНК и белков. Он не позволяет клеткам вступать в период S (фаза синтеза дочерней молекулы ДНК на матрице родительской молекулы ДНК).
Метотрексат относится к препаратам первого ряда, применяемым при базисной терапии ревматоидного артрита. Он подавляет выработку не только иммунокомпетентных клеток, но также синовиоцитов (клетки синовиальной мембраны) и фибробластов (основные клетки соединительных тканей). Угнетение процесса размножения этих клеток помогает предотвратить деформацию и воспаление сочленения. Метотрексат останавливает костные эрозии, которые возникают в результате атаки активно разрастающихся тканей синовиальной оболочки сустава.
Метотрексат при ревматоидном артрите позволяет добиться стойкой ремиссии. Клинический эффект сохраняется даже после его отмены.
Токсичность Метотрексата
Метотрексат является самым токсичным антагонистом фолиевой кислоты. Вследствие нарушения метилирования дезоксиуридинмонофосфата происходит его накопление и частичное превращение в дезоксиуридинтрифосфат. Дезоксиуридинтрифосфат концентрируется в клетке и встраивается в ДНК, вызывая синтез дефектной ДНК. В ней тимидин частично замещен уридином. В результате патологических процессов развивается мегалобластная анемия.
Мегалобластной анемией называют состояние, при котором в организме возникает дефицит витамина В12 и фолиевой кислоты. Фолиевая кислота (наряду с железом) принимает участие в синтезе эритроцитов. Эти клетки крови играют важную роль в кроветворении и функционировании всего организма.
При недостатке фолиевой кислоты образуются измененные по форме и размеру эрит
народные средства, признаки заболевания, признаки и лечение, причины
Противоревматический препарат Лефлуномид: инструкция, отзывы
Многие годы пытаетесь вылечить СУСТАВЫ?
Глава Института лечения суставов: «Вы будете поражены, насколько просто можно вылечить суставы принимая каждый день…Читать далее »
Лефлуномид — единственный препарат на рынке, эффективность и безопасность которого при ревматоидном артрите подтверждена с позиции доказательной медицины.
У пациентов наблюдается положительная динамика уже после первого месяца терапии.
Средство также эффективно применяется при псориатическом артрите.
Форма выпуска и состав
В составе средства следующие компоненты:
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!
Для лечения суставов наши читатели успешно используют СустаЛайф. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
- лефлуномид — основной компонент;
- гипролоза;
- гидрофосат дигитрат кальция;
- крахмал кукурузный;
- натрия кроскармелоза;
- магния стеарат;
- целлюлоза микрокристаллическая;
- селекоат;
- макрогол;
- титана диоксид.
Таблетки, покрытые пленочной оболочкой, выпуклые с двух сторон, помещены в блистер. В продажу поступают в картонных упаковках №30 по 10, 20 и 100 мг.
При поперечном рассечении сердцевина таблетки имеет белый или сероватый цвет.
Фармакологический профиль
Препарат оказывает следующее воздействие на организм:
- имуномоделирующее;
- антипролиферативное;
- противовоспалительное.
Средство затормаживает пролиферативный процесс и образование лимфоцитов (ДНК – Т). Метаболит (активный) производит разрушение фермента дегидрооротата до дегидрогеназы.
Препарат не влияет на всасывание пищи. Абсорбция Лефлуномида составляет примерно 85% после употребления таблетки.
Метаболизм происходит стремительно в печени и стенках кишечника от главного метаболита и второстепенного. Основной метаболит при употреблении одной дозы происходит в течение 24 часов. В крови препарат вступает в связь с альбумином.
Фракция несвязанного вида равна примерно 0,64%. Вывод основного метаболита при длительном приеме происходит медленно и период его полувыведения равен 14 дням.
Показания и противопоказания для применения
Лефл
Лефлуномид в лечении ревматоидного артрита | Мазуров В.И., Жугрова Е.С.
Ревматоидный артрит (РА) – одно из наиболее распространенных хронических воспалительных заболеваний человека, частота которого в популяции, согласно данным ВОЗ, составляет от 0,6 до 1,3%, а у близких родственников достигает 3–5%. Ежегодная частота возникновения новых случаев заболевания составляет около 0,02% [1,2].
РА приводит к снижению качества жизни пациентов и ранней инвалидизации. Так, почти 50% больных РА становятся инвалидами в течение 5 лет заболевания, а 10% – в течение первых 2 лет болезни. Продолжительность жизни больных РА, согласно данным проспективных исследований, уменьшается в связи с поражением различных органов и систем [1–3].Лечение РА основано на применении базисных противовоспалительных препаратов (БПВП). К БПВП относят группу различных по химической структуре лекарственных средств, объединяемых способностью «модифицировать» течение РА, приводя к стойкому уменьшению активности заболевания, замедлению темпов рентгенологического прогрессирования и достижению клинико–лабораторной ремиссии [1,2].
Основными базисными препаратами для лечения РА является лефлуномид и метотрексат. Различаются подходы к назначению этих препаратов. Согласно рекомендациям АСR, оба препарата являются препаратами 1-го выбора при стартовой терапии РА. В то же время разработанные EULAR рекомендации предлагают начинать терапию с назначения метотрексата, а при его непереносимости или неэффективности использовать лефлуномид.
Арава® (лефлуномид) принадлежит к классу базисных противоревматических препаратов и обладает антипролиферативными, иммуномодулирующими, иммуносупрессивными и противовоспалительными свойствами. Активный метаболит лефлуномида А771726 ингибирует фермент дегидрооротат дегидрогеназу и обладает антипролиферативной активностью. А771726 в условиях in vitro тормозит вызванную митогенами пролиферацию и синтез ДНК Т–лимфоцитов. Антипролиферативная активность А771726 проявляется, по–видимому, на уровне биосинтеза пиримидина, поскольку добавление в клеточную культуру уридина устраняет тормозящее действие метаболита А771726. С использованием радиоизотопных лигандов показано, что А771726 избирательно связывается с ферментом дегидрооротат дегидрогеназой, чем объясняется его свойство тормозить этот фермент и пролиферацию лимфоцитов на стадии G1. Пролиферация лимфоцитов является одним из ключевых этапов развития РА. Одновременно А771726 тормозит экспрессию рецепторов к интерлейкину–2 (СВ–25) и антигенов ядра Ki–67 и PCNA, связанных с клеточным циклом.
Терапевтическое действие лефлуномида было показано на нескольких экспериментальных моделях аутоиммунных заболеваний, включая РА. Лефлуномид (Арава®) уменьшает симптомы и замедляет прогрессирование поражения суставов при активной форме РА. Терапевтический эффект обычно проявляется через 4–6 нед. и может нарастать в дальнейшем на протяжении 4–6 мес. Лефлуномид быстро превращается в свой активный метаболит А771726 (первичный метаболизм в кишечной стенке и печени). В плазме, моче или кале были замечены лишь следовые количества неизмененного лефлуномида. Единственным определяемым метаболитом, ответственным за основные свойства препарата in vivo, является А771726. При приеме внутрь абсорбируется 82–95% препарата. Максимальные плазменные концентрации А771726 определяются в течение 1–24 ч после однократно принятой дозы. Лефлуномид может приниматься вместе с пищей.
Из–за очень длительного периода полувыведения А771726 (около 2 нед.) использовалась нагрузочная доза 100 мг в сут. в течение 3 дней. Это позволило быстро достигнуть равновесного состояния плазменной концентрации А771726. Без нагрузочной дозы для достижения равновесной концентрации потребовался бы 2–месячный прием препарата. В исследованиях с многократным назначением препарата фармакокинетические параметры А771726 были дозозависимыми в диапазоне доз от 5 до 25 мг. В этих исследованиях клинический эффект был тесно связан с плазменной концентрацией А771726 и суточной дозой лефлуномида. При дозе 20 мг в сут. средние плазменные концентрации А771726 при равновесном состоянии имели значение 35 мкг/мл. В плазме происходит быстрое связывание А771726 с альбуминами. Несвязанная фракция А771726 составляет примерно 0,62%. Связывание А771726 более вариабельно и несколько снижается у больных РА или пациентов с хронической почечной недостаточностью.
Надо отметить, что оригинальный препарат лефлуномида (Арава®) уже содержит некоторое количество активного метаболита, процентное содержание которого запатентовано. Доказательства клинической эффективности и безопасности получены именно в отношении оригинального препарата (Арава®). Основываясь на данном факте, можно предположить, что терапевтическая эффективность оригинального препарата лефлуномида может превосходить таковую генерика.
Лефлуномид метаболизируется до одного главного (А771726) и нескольких второстепенных метаболитов, включая 4–трифлюорометилаланин. Биотрансформация лефлуномида в А771726 и последующий метаболизм самого А771726 контролируются несколькими ферментами и происходят в микросомальных и других клеточных фракциях. Исследования взаимодействия с циметидином (неспецифическим ингибитором цитохрома Р450) и рифампицином (неспецифическим индуктором цитохрома Р450) показали, что in vivo СYP–энзимы вовлечены в метаболизм лефлуномида только в незначительной степени.
Выведение А771726 из организма медленное и характеризуется клиренсом 31 мл/ч. Лефлуномид выводится с фекалиями (вероятно, за счет билиарной экскреции) и мочой. Период полувыведения составляет около 2 нед.
Фармакокинетика А771726 у пациентов, находящихся на ХАПД, подобна таковой у здоровых добровольцев. Более быстрое выведение А771726 наблюдается у пациентов, находящихся на гемодиализе, что связано не с экстракцией препарата в диализат, а с вытеснением его из связи с белком. Хотя клиренс А771726 увеличивается приблизительно в 2 раза, конечный период полувыведения является подобным таковому у здоровых лиц, т. к. одновременно увеличивается объем распределения [3,4,13].
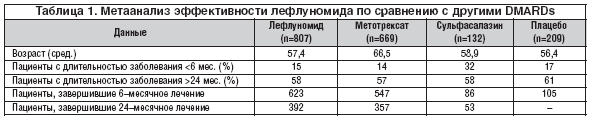
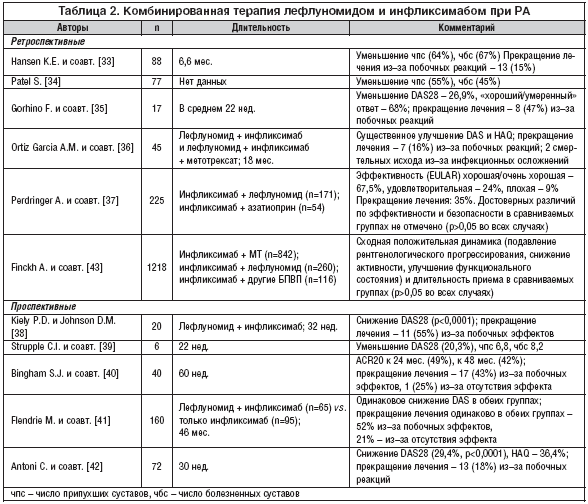
Данные метаанализа основных рандомизированных плацебо–контролируемых исследований (РПКИ), касающихся эффективности лефлуномида при РА, суммированы в таблицах 1 и 2 [5–11].
В исследование III фазы были включены 1817 пациентов с РА. Исходные демографические данные и число пациентов в исследовании приведены в таблице 1 [4–10]. По данным этих исследований была проанализирована сравнительная оценка эффективности лефлуномида в группе пациентов, получавших метотрексат и сульфасалазин. По результатам метаанализа опубликованных исследований по лефлуномиду, ACR–ответ был лучше в группе пациентов, получавших лефлуномид, чем в группе пациентов, получавших плацебо. На 6 мес. и 12 мес. соответственно ACR20 (20% улучшение в соответствии с критериями ACR) достигли 60 и 53% пациентов, получавших лефлуномид, и 27 и 26% пациентов из группы плацебо. Точно так же ACR50 (50% улучшение в соответствии с критериями ACR) было отмечено у 29 и 34% пациентов, получавших лефлуномид, и у 11 и 8% из группы плацебо в тех же точках.
В группе пациентов, получавших лефлуномид, наблюдалось значительное снижение индекса HAQ на 0,37 (95% доверительный интервал (ДИ) 0,33, 0,41) в течение 12 мес., а по сравнению с увеличением в группе плацебо – на 0,06 (95% ДИ 0,03, 0,16). Сопоставимые результаты терапии лефлуномидом наблюдались у пациентов, принимавших сульфасалазин и метотрексат в течение 2–летнего исследования, показали более значимое снижение индекса HAQ в группе пациентов, получавших лефлуномид. Также анализ индекса Sharp показал значительно меньшую радиологическую прогрессию в группе лефлуномида, чем в группе плацебо (лефлуномид по сравнению с плацебо: 6–месячное исследование, p=0,0004; 12–месячное исследование, р = 0,0007) [5–11].
В исследовании MN302 оценивались эффективность и безопасность применения лефлуномида и метотрексата у больных РА. В исследование было включено 999 пациентов с активным РА. Все рандомизированные пациенты были разделены на 2 группы: группа больных, получавших лефлуномид (n=501, 100 мг/сут. в течение 3 дней, затем 20 мг/сут.), и группа пациентов, получавших метотрексат (в дозе 10–15 мг/нед.) в течение 52 нед. Установлено, что эффективность лефлуномида, применяемого как 1–й базисный препарат, несколько выше, чем у больных, которым лефлуномид был назначен после приема метотрексата [17, 18].
Анализ исследования US301 (12 мес., двойное слепое рандомизированное контролируемое) показал клинические преимущества лефлуномида (20 мг/сут., нагрузочная доза 100 мг) по сравнению с метотрексатом. Безопасность и эффективность лефлуномида и метотрексата сохранялись в течение 2 лет наблюдения. Лефлуномид статистически значительно превосходит метотрексат в улучшении функционального состояния суставов в соответствии с индексом HAQ DI. Результаты исследования показывают, что лефлуномид является безопасным и эффективным в начальной терапии для активного РА, с клинически устойчивым эффектом в течение 2 лет лечения [19,20].
В другом открытом исследовании [19,20] у 30 больных с ранней стадией РА (длительность болезни менее 1 года) за 18 мес. лечения лефлуномидом в качестве 1–го БПВП ремиссия по критериям ACR была зарегистрирована у 43,3% больных, еще у 26,7% больных было достигнуто 70–процентное улучшение (ACR70), у 16,7% больных – 50–процентное улучшение (ACR50). То есть при назначении лефлуномида в 1–й год болезни развитие хорошего, очень хорошего эффекта и ремиссии зарегистрировано у 86,7% пациентов.
Результаты исследования RELIEF продемонстрировали, что комбинация лефлуномида и сульфасалазина позволяет увеличить эффективность терапии РА без ухудшения переносимости лечения. Получены данные о достоверно более выраженном эффекте комбинации лефлуномида (10–20 мг/сут.) и метотрексата (10–20 мг/нед.) по сравнению с эффектом монотерапии метотрексатом при удовлетворительной переносимости комбинации БПВП [6–8].
Особенный интерес представляет опыт использования лефлуномида в сочетании с биологическими агентами, в первую очередь с ингибиторами ФНО–α (табл. 2). Уже сообщалось, что комбинация лефлуномида и инфликсимаба эффективна. К настоящему времени отсутствуют проспективные рандомизированные исследования эффективности и переносимости этой комбинации. Имеется ряд открытых исследований – как проспективных, так и ретроспективных (табл. 2), в которых зафиксирован выраженный эффект применения инфликсимаба в комбинации с лефлуномидом. Ретроспективные исследования свидетельствуют и о приемлемой переносимости, тогда как в проспективных исследованиях данные о частоте побочных эффектов различны.
Было высказано мнение, что число аутоиммунных осложнений при комбинации лефлуномида и инфликсимаба (кожный васкулит, волчаночноподобный синдром, церебральный васкулит, синдром Стивена–Джонса) увеличивается у больных, имевших АНФ в сыворотке крови к началу терапии или при его появлении на этапах лечения. Авторы зарегистрировали наличие позитивности по АНФ к началу комбинированной терапии у 12% больных, а к концу – у 75%. Однако количество больных с позитивным АНФ на фоне лечения инфликсимабом увеличивается и при комбинации с метотрексатом.
На сегодняшний день показано, что от присутствия АНФ не зависят ни эффективность, ни переносимость комбинации инфликсимаба с метотрексатом или лефлуномидом. Сравнение эффективности комбинации инфликсимаба с лефлуномидом или другими БПВП показало их примерную равнозначность. Некоторое преимущество комбинации инфликсимаба именно с лефлуномидом заключается в длительности сохранения эффекта и даже увеличении числа больных с хорошим эффектом терапии через 18 и 24 мес. лечения.
Комбинация инфликсимаба и лефлуномида вызывает большее количество слабых побочных реакций за счет симптомов непереносимости со стороны кожи (кожные реакции являются самым часто возникающим симптомом непереносимости при монотерапии лефлуномидом). Выраженные побочные реакции в результате применения комбинации инфликсимаба с лефлуномидом встречаются не чаще, чем при использовании комбинации с другими БПВП, а тяжелые инфекции – даже реже.
Таким образом, можно заключить, что комбинация лефлуномида с инфликсимабом является эффективной; профиль безопасности схож с профилем безопасности применения лефлуномида в виде монотерапии; частые кожные реакции могут приводить к отмене терапии [15,16].
Подводя итог, можно сказать, что лефлуномид (Арава®) эффективен в лечении больных с любой длительностью заболевания. Однако на ранней стадии болезни наблюдаются более быстрое действие, высокая частота выраженного эффекта лечения и клинической ремиссии. Отмечается быстрое развитие эффекта препарата Арава® с достоверным снижением показателей суставного синдрома и лабораторных параметров активности воспаления через 1 мес. лечения, далее эффект лечения нарастает в течение 4–5 мес. Арава® демонстрирует базисную активность, достоверно уменьшая титр РФ, внесуставные проявления РА (в том числе и проявления васкулита), достоверно замедляя темп рентгенологического прогрессирования, а у большинства больных с хорошим и отличным эффектом – останавливая деструктивный процесс.
Литература
1. Мазуров В.И. Современные методы диагностики и лечения ревматических заболеваний // Медицинская иммунология. 2001. Т. 3. № 2. С. 187–193.
2. Scott D.L., Pugner K., Kaarela K. et al. The links between joint damage and disability in rheumatoid arthritis // Rheumatology (Oxford). 2000. Vol. 39. P. 122–132.
3. Cutolo M., Sulli A., Ghiorzo P. et.al Anti–inflammatory effects of leflunomide on cultured synovial macrophages from patients with rheumatoid arthritis. // Ann. Rheum. Dis. 2003. Vol. 62 (4). Р. 297–302.
4. Насонов Е.Л., Чичасова Н.В., Чижова К.А. Перспективы применения лефлуномида в ревматологии // РМЖ. 2004. № 12 (20). С. 1147–1151.
5. Strand V., Cohen S., Schiff M. et al. Treatment of active rheumatoid arthritis with leflunomide compared with placebo and methotrexate. Leflunomide Rheumatoid Arthritis Investigators Group // Arch Int Med. 1999. Vol. 159. Р. 2542–2550.
6. Smolen J.S., Kalden J.R., Scott D.L. et al. Efficacy and safety of leflunomide compared with placebo and sulfasalazine in active rheumatoid arthritis: a double blind, randomised, multicentre trial. European Leflunomide Study Group // Lancet. 1999. Vol. 353. Р. 259–266.
7. Emery P., Breedfeld C., Lemmel E.M. et al. and the multinational leflunomide study group. A comparison of the efficacy and safety of leflunomide and methotrexate for the treatment of rheumatoid arthritis // Rheumatology. 2000. Vol. 39. Р. 655–665.
8. Cohen S., Cannon G.W., Schiff M. et al. Two–year blinded randomized controlled treatment of active rheumatoid arthritis with leflunomide compared with methotrexate. Utilization of Leflunomide in theTreatment of Rheumatoid Arthritis Trial Investigator Group // Arthritis Rheum. 2001. Vol. 44. Р. 1984–1992.
9. Scott D.L., Smolen J.S., Kalden J.R. et al. Treatment of active rheumatoid arthritis with leflunomide: two year follow up of a double blind, placebo controlled trial versus sulfasalazine // Ann Rheum Dis. 2001. Vol. 60. Р. 913–923.
10. Kalden J.R., Schattenkirchner M., Sorensen H. et al. The efficacy and safety of leflunomide in patients with active rheumatoid arthritis: a five–year follow up study // Arthritis Rheum. 2003. Vol. 48. Р. 1513–1520.
11. Scott D.L., Strand V. The effects of disease–modifying anti–rheumatic drugs on the Health Assessment Questionnaire score. Lessons from the leflunomide clinical trials database // Rheumatology. 2002. Vol. 41. Р. 899–909.
12. Scott D.L., Smolen J.S., Kalden J.R. et al. Treatment of active rheumatoid ar–thritis with leflunomide: two year follow up of a double–blind, placebo–controlled trial versus sulfasalasine // Ann Rheum Dis. 2001. Vol. 60. Р. 913–923.
13. Cutolo M., Sulli A., Ghiorzo P. et Al. Anti–inflammatory effects of leflunomide on cultured synovial macrophages from patients with rheumatoid arthritis // Ann. Rheum. Dis. 2003. Vol. 62 (4). Р. 297–302.
14. Osiri M., She A.B., Robinson V. et al. Leflunomide for the treatment of rheumatoid arthritis: a systematic review and meta–analysis. // J. Rheum. 2003. Vol. 30. Р. 1182–1190.
15. Kalden J. R., Antoni C., Alvaro–Gracia J.M. et al. Use of combination of leflunomide with biological agents in treatment of rheumatoid arthritis // J. Rheum. 2005. Vol. 32. Р. 1620–1631.
16. Dougados M., Emery P., Lemmel E.M. et al. Maintenance rate of leflunomide in patients with rheumatoid arthritis: RELIEF 1–year data // Arthritis Rheum. 2001. Vol. 44. Р. 173.
17. Scott D.L., Smolen J.S., Kalden J.R. et al. Treatment of active rheumatoid ar–thritis with leflunomide: two year follow up of a double–blind, placebo–controlled trial versus sulfasalasine. // Ann Rheum Dis. 2001. Vol. 60. Р. 913–923.
18. Cohen S, Weaver A, Schiff M, Strand V. Two–year treatment of active RA with leflunomide compared with placebo or methotrexate // Arthritis Rheum. 2001. Vol. 44. Р. 1984–1992.
19. Yaremenko O.V., Mikitenko A.M. Comparative evaluation of effects of le–flunomide and methotrexate for early rheumatoid arthritis. In Leflunomide. A selection of communications presented at the annual congress of the European League Against Rheumatism. Netherlands, Amsterdam. June 21–24 2006. P. 22.
20. Karateev D., Luchikhina E.L., Nasonov E.L. High frequency of clinical remission in patients with early rheumatoid arthritis treated with le–flunomide. In Leflunomide. A selection of communications presented at the annual congress of the European League Against Rheumatism, Netherlands, Amsterdam. June 21–24 2006. P. 23.
АРАВА® — новый препарат для базисной терапии ревм

28-29 марта 2003 года в Институте кардиологии им. Н. Д. Стражеско АМН Украины была проведена ежегодная Украинская ревматологическая школа. В рамках Школы состоялся научно-практический семинар «Доказательная медицина:
Подготовил Дмитрий Решотько, г. Киев
 28-29 марта 2003 года в Институте кардиологии им. Н. Д. Стражеско АМН Украины была проведена ежегодная Украинская ревматологическая школа. В рамках Школы состоялся научно-практический семинар «Доказательная медицина: реальность новых возможностей базисной терапии ревматоидного артрита», где прозвучал доклад доцента кафедры госпитальной терапии №1 НМУ им. А. А. Богомольца, доктора медицинских наук Олега Борисовича Яременко «Базисная терапия ревматоидного артрита Аравой (лефлуномидом): анализ соотношения пользы и риска в широкомасштабных длительных наблюдениях».
28-29 марта 2003 года в Институте кардиологии им. Н. Д. Стражеско АМН Украины была проведена ежегодная Украинская ревматологическая школа. В рамках Школы состоялся научно-практический семинар «Доказательная медицина: реальность новых возможностей базисной терапии ревматоидного артрита», где прозвучал доклад доцента кафедры госпитальной терапии №1 НМУ им. А. А. Богомольца, доктора медицинских наук Олега Борисовича Яременко «Базисная терапия ревматоидного артрита Аравой (лефлуномидом): анализ соотношения пользы и риска в широкомасштабных длительных наблюдениях».
Докладчик отметил, что появление каждого нового базисного средства для лечения ревматоидного артрита (РА) является событием как в жизни ревматологов, так и в жизни больных. В первую очередь это обусловлено ограниченным числом имеющихся базисных средств для лечения этой патологии. В последнее время арсенал ревматологов обогатился несколькими препаратами — биологическими агентами и препаратом лефлуномид (Арава). Докладчик напомнил известные ревматологам данные проведенных клинических испытаний (два в Европе — MN301 и MN302 и одно в США — US301), в которых было показано, что Арава в сравнении с метотрексатом и сульфасалазином демонстрирует лучшую эффективность в терапии больных РА по ряду показателей. Кроме того, препарат отличается более быстрым началом действия, замедляет рентгенологическое прогрессирование заболевания в большей мере, чем метотрексат и сульфасалазин.
В докладе было отмечено, что на сегодняшний день не существует ни одного базисного препарата, при назначении которого на протяжении всего заболевания наблюдается положительная динамика. Ревматоидный артрит — это хроническое заболевание, и имеющиеся традиционные базисные препараты сохраняют свою эффективность, как правило, на протяжении только двух-трех лет лечения. Чтобы установить, как долго сохраняются преимущества нового препарата — Аравы, было проведено открытое дополнительное исследование, включавшее больных ревматоидным артритом, у которых был получен положительный эффект от применения Аравы на протяжении 4,6-5 лет в вышеупомянутых исследованиях и которые пожелали продолжать терапию лефлуномидом.
В исследование было включено 214 пациентов в возрасте до 60 лет. Средняя длительность наблюдения составила 4,6 года, при этом 182 пациента принимали Араву на протяжении 4 лет и более, 58 пациентов — 5 лет и более. Эффективность лечения оценивалась по критериям Американской коллегии ревматологов (ACR 20%, ACR50%, ACR 70%). Как показали результаты исследований, эффективность лечения не снижалась на протяжении всех пяти лет наблюдения. Улучшение по шкалам ACR 20%, ACR50% и ACR 70%, достигнутое через год после начала лечения лефлуномидом (соответственно 73%, 48% и 15%), сохранялось в течение всего периода исследования (соответственно 69%, 43% и 20% к концу исследования). Более того, количество пациентов, у которых наблюдалось резко выраженное улучшение, увеличивалось.
Золотым стандартом оценки эффективности базисных средств для лечения ревматоидного артрита является замедление рентгенологического прогрессирования заболевания. В упоминаемом в докладе исследовании этот показатель оценивался по улучшенной шкале Шарпа-ван дер Хейда (она включает оценку как суставных эрозий, так и сужения суставной щели, которые суммируются для получения общего балла). По результатам проведенных исследований у пациентов, получавших терапию Аравой, отмечалось достоверное замедление ежегодной скорости прогрессирования почти в 4 раза (до 1,9 единицы в год по сравнению с 7,9 единицы до начала лечения), а у трети пациентов по рентгенологическим данным наблюдалась стабилизация процесса. У 16 пациентов (12,5%) исходно не было признаков поражения суставов, связанного с ревматоидным артритом (общее число баллов — 0), и по прошествии пяти лет лечения лефлуномидом у 15 из них (11,7%) общее число баллов оставалось равным 0. Эти данные еще раз подтверждают тот тезис, что чем раньше начато базисное лечение ревматоидного артрита (до формирования паннуса, до появления первых эрозий и сужения суставной щели), тем лучше результаты лечения, и такой путь ведения больных ревматоидным артритом является оптимальным.
Далее О. Б. Яременко сравнил возможные побочные эффекты при терапии лефлуномидом с таковыми при лечении другими базисными средствами. Он отметил, что в последних Рекомендациях и Американского, и Европейского обществ ревматологов указано, что при применении метотрексата целесообразно использовать фолиевую кислоту для уменьшения частоты побочных эффектов. Однако эти рекомендации базировались на результатах очень небольшого количества исследований. Позже в ряде исследований было показано, что добавление фолиевой кислоты снижало эффективность лечения метотрексатом и увеличивало частоту некоторых побочных эффектов (стоматит, диарея, диспепсия). Не получил объяснения и тот факт, что снижение эффективности метотрексата при сочетании с фолиевой кислотой было особенно выраженным в группе больных с положительным ревматоидным фактором. Исходя из вышеизложенного, О. Б. Яременко сделал вывод, что, очевидно, следует занять выжидательную позицию, пока данный факт не получит подтверждения либо опровержения в дальнейших исследованиях, и фолиевую кислоту назначать по показаниям, например, больным, склонным к развитию побочных эффектов (по опыту назначения предыдущих базисных препаратов), или при наличии таковых.
Затем докладчик перешел к характеристике недавно закончившегося исследования RELIEF, целью которого было установить, является ли добавление сульфасалазина к лефлуномиду более эффективным, чем переход на сульфасалазин при отсутствии адекватного ответа на терапию лефлуномидом в течение 24 недель. Дизайн исследования был следующим: около 1000 больных ревматоидным артритом в течение полугода получали терапию Аравой. Пациенты, у которых наблюдался хороший или умеренный ответ на терапию лефлуномидом (в соответствии с критериями EULAR) продолжали его прием в течение последующих 24 недель. Пациентам, у которых не наблюдалось адекватного ответа на терапию лефлуномидом в течение 24 недель, был назначен либо сульфасалазин в комбинации с лефлуномидом, либо только сульфасалазин. В данном исследовании для оценки ответа на терапию применяли не критерии ACR, а критерии EULAR с использованием шкалы DAS 28. Она включает в себя примерно те же параметры, что и ACR (количество болезненных и отечных суставов, СОЭ, общую оценку состояния здоровья пациентом), однако учитывается не только динамика состояния по сравнению с исходным, но и абсолютные признаки активности заболевания. Это важно, поскольку цель лечения ревматоидного артрита — не только улучшить уровень ответа на терапию, но и достичь целевого уровня активности заболевания. Через 48 недель наблюдения на терапию Аравой ответили 71% больных, у 47% из них наблюдали умеренный ответ, у 24% — хороший, ремиссия достигнута у 13% больных (DAS
Интересная информация была представлена на очередном Европейском конгрессе ревматологов EULAR 2002 в Стокгольме по применению новых базисных препаратов в комбинации с метотрексатом для лечения больных, у которых не удавалось добиться эффекта при монотерапии метотрексатом. В частности, у 1300 пациентов были проанализированы результаты контролируемых плацебо исследований, в которых использовались антитуморнекротические препараты, лефлуномид или ингибиторы интерлейкина-1 в комбинации с метотрексатом. Оказалось, что эффективность антитуморнекротических препаратов в сочетании с метотрексатом была практически равной эффективности комбинации Аравы и метотрексата, а комбинация с антиинтерлейкиновыми препаратами достоверно уступала по эффективности последней. Учитывая существенную разницу в стоимости биологических агентов и Аравы, становится ясно, какому препарату отдаст предпочтение доктор при назначении.
Далее О. Б. Яременко привел данные о том, какие базисные препараты назначают ревматологи в США в практической работе с 1998 года. Метотрексат остается самым часто назначаемым базисным препаратом (85% больных) до настоящего времени, с такой же частотой назначается и преднизолон. Докладчик акцентировал внимание на том, что среднесуточная доза преднизолона в США для больных ревматоидным артритом составляет 5 мг. Метаанализ 16 исследований, в которых оценивалась эффективность различных доз преднизолона у больных ревматоидным артритом (в дозах от 2,5 до 15 мг/сут), показал, что достоверных различий в эффективности в этом диапазоне доз не наблюдается, однако имеется разница в частоте побочных эффектов. Поэтому общей тенденцией сейчас является снижение дозы преднизолона до минимально эффективных — 5-7,5 мг/сут. На втором месте по частоте назначения базисных препаратов в США находится Арава — каждый пятый больной получает этот препарат. Следующие препараты по частоте назначения — Плаквенил и биологические агенты. Существенно «сдал свои позиции» сульфасалазин, который назначается всего 4% больных. Комбинацию метотрексата с лефлуномидом назначают каждому десятому больному, только 9% больных не получают базисной терапии (в конечной стадии заболевания, когда базисная терапия, как правило, уже неэффективна).
Известно, что результаты многоцентровых клинических испытаний зачастую тяжело перенести в практическую деятельность. Это может быть связано, в частности с тем, что для таких испытаний группы больных подбираются очень тщательно с учетом множества критериев включения и исключения. Поэтому важное место в комплексной оценке любого, в том числе базисного препарата отводится так называемым постмаркетинговым исследованиям (в реальной клинической практике). На сегодняшний день в мире получают Араву более 300 тысяч пациентов, и уже можно сделать определенные заключения в плане эффективности и безопасности этого препарата. Для анализа переносимости Аравы была взята одна из крупнейших в мире баз данных Aetna-US Healthcare claims о 40 594 больных ревматоидным артритом, которые хотя бы один день получали какой-либо базисный препарат. Анализ вели по нескольким группам больных, которым назначали монотерапию лефлуномидом, монотерапию метотрексатом, комбинированную терапию с применением лефлуномида, комбинированную терапию с применением метотрексата, и лечение другими базисными препаратами (в качестве монотерапии или в комбинациях). Частота побочных явлений (на 100 пациенто-лет использования препарата) при монотерапии лефлуномидом была достоверно ниже, чем при приеме любых других базисных препаратов. Интересные данные получены в результате анализа частоты побочных эффектов при назначении комбинации лефлуномида с другими базисными препаратами. По данным многих исследований, токсичность комбинации двух или трех базисных препаратов оказывается примерно такой же, как и использование каждого базисного препарата в отдельности. На практике оказалось, что частота побочных эффектов при применении комбинированной базисной терапии ниже, чем в группах монотерапии. Очевидно, имеет место эффект, который зарубежные исследователи называют «индуцированной предвзятостью». Этот эффект объясняют тем, что при назначении больному комбинированной базисной терапии доктор сознательно или подсознательно отбирает пациентов, более «здоровых» для комбинированной терапии с целью максимального снижения риска осложнений. Частота побочных явлений при приеме лефлуномида в комбинации с другими препаратами достоверно ниже, чем при приеме метотрексата в комбинации с другими препаратами. Говоря о спектре побочных эффектов, О. Б. Яременко отметил, что по всем оцениваемым побочным эффектам (включая влияние на печеночные ферменты) Арава продемонстрировала их меньшую частоту как в сравнении с метотрексатом, так и с другими базисными препаратами. Особенно наглядно это проявилось по отношению к инфекционным осложнениям, они в 2 раза меньше, чем при комбинированной терапии с использованием метотрексата. Смертность на фоне лечения этими базисными препаратами составила для Аравы 0,4%, для метотрексата — 1,1%, для других базисных препаратов — 1,2%. Говоря о сроках возникновения побочных эффектов при терапии Аравой, докладчик подчеркнул, что по результатам исследования RELIEF и ряда других, они возникают в первые 6 месяцев лечения. В дальнейшем частота их возникновения стабилизируется, и больные успешно продолжают лечение.
Известно, что Арава противопоказана при беременности. Что же делать, если женщина во время лечения решила забеременеть или мужчина решил стать отцом? В этом случае рекомендации следующие: прекратить лечение препаратом и провести элиминацию холестирамином.
Для минимизации риска возникновения побочных эффектов данный препарат не следует принимать лицам с диффузным поражением печени, инфицированным вирусами гепатита В или С. Также следует избегать назначения лефлуномида в комбинации с потенциально гепатотоксичными препаратами.
В заключение доклада О. Б. Яременко рассказал о результатах совещания экспертов комитета FDA, прошедшего в марте 2003 года, о регистрации еще одного показания к назначению Аравы — улучшение физической функции больных ревматоидным артритом (во всех испытаниях Арава продемонстрировала более раннее и выраженное улучшение физического состояния больных). Кроме того, при рассмотрении профиля безопасности эта организация сделала вывод, что Арава имеет положительное соотношение преимущества/риск терапии и является безопасным и эффективным лекарственным средством из узкого круга препаратов, используемых для лечения ревматоидного артрита.
В рамках проведенного научно-практического семинара были продемонстрированы три интересных и показательных клинических случая применения Аравы в Киевском городском ревматологическом центре и в Институте кардиологии им. Н. Д. Стражеско АМН Украины.
Таким образом, на основании прозвучавших на семинаре данных и демонстрации клинических случаев применения Аравы можно сделать следующие выводы.
- Лефлуномид обладает высокой эффективностью в лечении ревматоидного артрита на протяжении длительного времени.
- Длительный прием лефлуномида эффективно замедляет прогрессирование ревматоидного артрита, что подтверждается данными рентгенологических исследований.
- Лефлуномид в комбинации с сульфасалазином хорошо переносится больными.
- Побочные эффекты возникают в ранние сроки терапии (в течение первых 24 недель) и поддаются контролю при условии проведения регулярного мониторинга.
- Частота побочных эффектов Аравы сопоставима или ниже, чем при приеме метотрексата и других базисных препаратов.
Лефлуномид занимает серьезное место среди базисных препаратов как для первой линии терапии ревматоидного артрита, так и после применения других базисных препаратов, оказавшихся неэффективными, и обладает благоприятным соотношением преимущество-переносимость терапии.
Читайте также


 пациенту, или эти препараты отменяют из-за их непереносимости организмом, тогда врач применяет Д-пеницилламин. И хотя это лекарство по результатам использования не уступает упомянутым препаратам, оно еще более токсично и чаще способствует осложнениям. Побочные явления при нем возникают в 30-40% случаев, поэтому лечение этим препаратом назначают только в самых крайних случаях, когда пациент крайне нуждается в неотложной помощи.
пациенту, или эти препараты отменяют из-за их непереносимости организмом, тогда врач применяет Д-пеницилламин. И хотя это лекарство по результатам использования не уступает упомянутым препаратам, оно еще более токсично и чаще способствует осложнениям. Побочные явления при нем возникают в 30-40% случаев, поэтому лечение этим препаратом назначают только в самых крайних случаях, когда пациент крайне нуждается в неотложной помощи.